protocolul COC in cancerul de San
acest document este un rezumat al rațiunii și unele dintre dovezile științifice actuale care susțin utilizarea medicamentelor Protocolului COC alături de tratamentele standard de îngrijire pentru cancerul de sân. Înțelegem că cancerul este o afecțiune foarte personală și fiecare pacient are un set unic de provocări. Pentru mai multe informații cu privire la propria situație personală, vă rugăm să luați legătura cu Clinica de oncologie Care la 800-392-1353 din Statele Unite sau vizitați site-ul web la https://careoncology.com.
Dacă sunteți nou să aibă grijă de oncologie vă rugăm să rețineți următoarele:
- nu aveți nevoie să călătorească. Vă puteți întâlni cu echipa noastră de oncologi și asistente medicale oncologice prin intermediul unui videoclip securizat pentru sprijin continuu.
- medicamentele Care Oncology adjuvant protocol sunt expediate direct la domiciliu de la farmaciile noastre partenere din SUA și pot fi utilizate alături de standardul dvs. de tratament de îngrijire.
- suntem incredibil de mândri să anunțăm că am trecut procesul de validare extrem de riguros al Institutului de validare de analiză a datelor, revendicări de rezultate și calcul al valorii. Am muncit din greu pentru a ajunge la acest punct. La început, am recunoscut valoarea extraordinară a unui program livrat în mod responsabil de medicamente refolosite oferite pacienților cu cancer, totuși, nu a fost oferit la scară largă. Acum patru ani, ne-am propus să schimbăm acest lucru știind că este un maraton, nu un sprint.
protocolul COC și cancerul de sân: puncte cheie
- cocprotocol este o combinație de patru medicamente prescrise în mod obișnuit(atorvastatină, metformină, mebendazol și doxiciclină) cu potențialul cancer de sân totarget și ajută la îmbunătățirea eficacității anticanceroterapiilor standard.
- un număr de studii observaționale au legat utilizarea metforminei sau a statinei de îmbunătățirea rezultatelor la pacienții cu cancer de sân.
- studiile de laborator asupra celulelor cancerului de sân cultivate în vase arată că metformina și statinele pot viza și deteriora direct celulele cancerului de sân – slăbindu-le și făcându-le mai vulnerabile la tratamentele standard.
- rezultatele din mica fereastră de oportunitate studiile clinice la pacienții cu cancer de sân operabil arată, în general, că administrarea de metformină sau statină pre-intervenție chirurgicală poate duce la modificări potențial pozitive ale markerilor moleculari ai cancerului, inclusiv cei care reglează creșterea și diviziunea celulelor cancerului de sân. Sunt în curs de desfășurare mai multe teste care investighează dacă metformina sau statinele pot afecta răspunsul la boală.
- Doxiciclinapoate bloca creșterea celulelor stem ale cancerului de sân HER2 pozitive și triple-negative incubate în vase în laborator și a contribuit la îmbunătățirea modificărilor legate de rezistență induse de paclitaxelul chimioterapic standard.
- doxiciclina tocmai a ajuns la studii clinice timpurii la pacienții cu cancer de sân. Rezultatele primului mic studiu arată că pacienții cu cancer de sân în stadiu incipient care au luat doxiciclină timp de doar 14 zile înainte de operație au redus nivelurile de markeri moleculari pentru prezența celulelor stem canceroase cu o medie de aproximativ 40%. Au fost observate efecte benefice pentru toți pacienții tratați, cu excepția unuia (8/9).
- Mebendazolepoate încetini creșterea și diviziunea celulelor canceroase de sân cultivate în laborator,inclusiv celulele canceroase de sân care sunt mai rezistente la chimioterapie. Mai multsunt necesare studii umane.
protocolul COC și cancerul de sân: Dovezi publicate
Protocolul cec este un regim combinat de patru medicamente prescrise în mod obișnuit,fiecare cu dovezi ale activității anticanceroase bazate pe metabolic și profiluri de siguranță bine înțelese. Aceste medicamente sunt: metformină,atorvastatină, doxiciclină și mebendazol. Unele dintre studiile care susțin utilizarea protocolului coc ca terapie adjuvantă alături de tratamentele standard actuale pentru cancerul de sân sunt prezentate mai jos. Aceste dovezi provin în principal din studii de laborator, studii epidemiologice mari (care investighează legăturile dintre administrarea medicamentelor și rezultatele cancerului de sân în grupuri de indivizi) și studii clinice timpurii.
puteți observa că multe dintre studiile de mai jos se concentrează doar pe medicamente individuale de protocol COC. Suntem primii care proiectăm o terapie adjuvantă care combină allfour. Noi credem că combinarea acestor medicamente va realiza cele mai mari rezultate, iar propriul nostru program de cercetare, numit METRICS, produce deja mai multe dovezi necesare pentru a arăta acest lucru. Puteți citi mai multe despre motivul pentru care credem că aceste medicamente lucrează împreună atât de bine pentru a ajuta la țintirea cancerului și despre programul theMETRICS în sine, în secțiunile ulterioare de mai jos.
Metformin și cancerul de sân
Metforminuse legate de potențialele beneficii ale cancerului de sân
multe studii observaționale oferă acum dovezi care susțin utilizarea metforminei în cancerul de sân. Metformina este autorizată pentru a trata diabetul de tip 2, iar studiile observaționale efectuate pe grupuri de pacienți cu diabet tind să arate că cei care iau metformină au șanse mai mari de a obține un rezultat îmbunătățit dacă dezvoltă cancer de sân (Aksoy și colab., 2013; El-Benhawy și El-Sheredy, 2014; Sonnenblick și colab., 2017).Utilizarea metforminei a fost legată de supraviețuirea îmbunătățită la pacienții cu cancer mamar (Kim și colab., 2015; Xuet al., 2015), răspuns îmbunătățit la tratamentul cancerului de sân (Jiralerspong și colab., 2009), și mai puține șanse de răspândire a cancerului de sân șirelapse (Chen și colab., 2017;Jacob și colab., 2016). este probabil că unele dintre efectele benefice ale metforminei găsite în aceste studii se datorează capacității metforminei de a îmbunătăți diabetul și/sau greutatea unui pacient prin reducerea nivelului de glucoză, ceea ce poate ajuta la reducerea riscului de apariție a cancerului de sân și la îmbunătățirea sănătății pacientului și a capacității de a aborda cancerul de sân dacă are (Hatoum și McGowan, 2015). Dar studiile de laborator arată, de asemenea, că metformina esteface mai mult decât atât. De fapt, metformina poate lucra în mod activ direct împotrivacelulele canceroase mamare, reducându-și capacitatea de a prelua și utiliza energie și blocând capacitatea lor de a crește, răspândi, supraviețui și recidiva (Alimova și colab., 2009;Hadad și colab., 2014; Orecchioni și colab., 2015).
diferiteTipurile de cancer mamar necesită tratamente diferite. Trastuzumab, de exemplu, este utilizat în mod special pentru a trata cancerul de sân pozitiv al receptorului factorului de creștere epidermal uman 2 (HER2). Tamoxifenul este eficient împotriva cancerului de sân pozitiv al receptorilor de estrogen (ER). Important, studiile de celule canceroase din laborator demonstreazăcă metformina are activitate anticancerigenă împotriva multor tipuri diferite de celule de cancer mamar, inclusiv ER pozitiv (Giles și colab.,2018), HER2 pozitiv (Chen și colab., 2013) și subtipuri potențial mai greu de tratat, cum ar fi celulele canceroase triple-negative (Deng și colab., 2012; Vazquez-Martin și colab., 2011; Wahdan-Alaswad și colab., 2014).Aceasta înseamnă că metformina are potențialul de a lucra eficient alături de tratamentele standard pentru cancerul de sân, indiferent de subtipul cancerului.
Metformintargets celulele stem ale cancerului de sân
s-a demonstrat, de asemenea, că metformina vizează celulele stem ale cancerului de sân (Bao și colab., 2014; Cufiet al., 2012; Hirsch și colab., 2009).Această activitate împotriva celulelor stem ale cancerului de sân, împreună cu capacitatea sa de aținta diferite subtipuri de cancer de sân, ajută la explicarea de ce studiile de laboratorcum poate funcționa în combinație cu o serie de tratamente standard, inclusivtrastuzumab (Cufi și colab.,2012), tamoxifen (Ma și colab., 2014) șiagenți chimioterapeutici standard (Iliopoulos și colab.,2011). Studiile pe animale și celule arată că metformina ambeleajută la îmbunătățirea eficacității tratamentelor standard (Bradford și Khan,2013; Liu și colab., 2012; Zhang și colab., 2014) șide asemenea, întârzie recidiva cancerelor care au fost tratate cu aceste terapii (Iliopoulos și colab.,2011). în plus, studiile de laborator arată, de asemenea, că metformina poate ajuta, de asemenea, la prevenirea rezistenței celulelor canceroase la sân la chimioterapie și la îmbunătățirea sensibilității celulelor canceroase deja rezistente la tratament (Davies și colab., 2017).
metformina îmbunătățește markerii cancerului de sân în studiile clinice timpurii
ca rezultat al cantității mari de date de susținere a metforminei în cancerul de sângenerate prin studii observaționale și de laborator, sunt în curs de desfășurare diferite studii clinice care investighează metformina în cancerul de sân (Camacho și colab., 2015).În general, analizele colective ale rezultatelor acestor studii în stadiu incipient (meta-analiză) încep să sugereze un efect general pozitiv atunci când metformina este adăugată la terapiile standard pentru cancer (Rahmani etal., 2019; Zhang și colab., 2019b).
Numărul de studii de oportunitate investighează dacă administrarea metforminf cu aproximativ două săptămâni înainte de operație poate ajuta la îmbunătățirea markerilor moleculari ai bolii la pacienții cu cancer mamar operabil în stadiu incipient. Rezultatele din aceste studii sugerează, în general, că administrarea metforminei poate duce la modificări potențiale pozitive ale markerilor moleculari ai cancerului, inclusiv cele care reglează creșterea și diviziunea celulelor cancerului de sân (Bonanni și colab., 2012;Cazzaniga și colab., 2013; Hadad și colab., 2011; Kalinsky și colab., 2014; Niraula etal., 2012), precum și îmbunătățirea potențială a reglementăriihormoni și alți factori pentru unii pacienți (Kalinsky și colab., 2014; Niraula și colab., 2012). Aceste studii ajută acum oamenii de știință să înțeleagă exact cum și când metformina ar putea ajutapacienții cu cancer de sân (Bonanni etal., 2012; deceni și colab., 2014, 2015; Rahmani și colab., 2019).
studiile de fază 2 ‘neoadjuvant’ sunt, în general, studii mai lungi și mai complexe care investighează metformina alături de cursuri de tratamente standard pentru a trata diferite tipuri de cancer de sân. Scopul acestor studii este de a stabili dacă metformina ajută într-adevăr la îmbunătățirea eficacității tratamentelor standard, sugerează studiile aslab (Kim și colab., 2014). Întrun studiu recent (studiul METTEN) (Martin-Castillo etal., 2018), la femeile cu cancer mamar în stadiu incipient HER2 pozitiv, mai mulți pacienți care au luat metformină au răspuns bine la chimioterapie/tratament vizat (65,5%) comparativ cu pacienții care nu au luat metformină (58,6%). Această diferență nu a fost semnificativă statistic; ceea ce înseamnă că acest rezultat ar fi putut fi atins din întâmplare. Cu toate acestea, studiile de fază 2 sunt, în general, insuficient dezvoltate pentru a atinge semnificația statistică în acest fel, iar cercetătorii au solicitat progresia către studii de fază 3 mai mari, care pot fi proiectate corespunzător pentru a determina cât de real este acest efect (Martin-Castillo etal., 2018). Rezultate potențial încurajatoare din alte faze 2, cum ar fi unul la persoanele supraponderale cu cancer de sân metastazatau fost, de asemenea, raportate (Yam și colab.,2019). De asemenea, este demn de remarcat faptul că, așa cum era de așteptat, nu toatestudiile de cancer cu metformină au raportat rezultate pozitive. De exemplu, alte studii de fază 2 au descoperit că metformina cu terapie standard nu a avut nicio diferență reală în comparație cu terapia standard singură în anumite circumstanțe (Mark și colab., 2019; Nanni și colab., 2019). Credem că metformina va fi cea mai eficientă în orice situație atunci când este administrată în combinație cu alte medicamente anti-metabolice.
sunt necesare studii mai mari pentru a ajuta la rezolvarea acestor probleme, iar un studiu de fază 3 este acum în curs de investigare a metforminei în cancerul de sân. Deși studiul nu estedatorită finalizării până în 2020, rezultatele inițiale din primele 6 luni ale studiului au arătat că pacienții care au început să ia metformină imediat după finalizarea intervenției chirurgicale și a ciclurilor standard de chimioterapie au avut modificări favorabile într-un marker molecular al cancerului de sân (Dowling și colab., 2018) șifactori metabolici îmbunătățiți (Goodwin și colab., 2015).
statinele și cancerul de sân
studiile observaționale leagă statinele de rezultatele mai bune ale cancerului de sân
statinele sunt de obicei administrate pentru a ajuta la gestionarea bolilor cardiovasculare. Cu toate acestea, studiile observaționale pe grupuri mari de persoane care iau statine au constatat, de asemenea, că persoanele cu cancer de sân care iau statine pot, de asemenea, să fi redus riscul recurenței cancerului după tratament, comparativ cu pacienții care nu iau statine (Ahern și colab., 2014;Manthravadi și colab., 2016). De exemplu, într-un studiu la aproape 2000 de supraviețuitori ai cancerului de sân, cei care au început să ia pete în termen de trei ani de la diagnostic au avut o șansă redusă de revenire a cancerului (Kwan și colab., 2008). Într-un alt studiu, doar 6 luni de utilizare a statinelor post-diagnostic au fost legate de rate îmbunătățite de recidivă (Chae și colab., 2011).
important,efectul benefic al statinelor în aceste studii și în alte studii a fost mai puternic legat de statinele lipofile mai solubile în grăsimi (cum ar fi atorvastatina). În unele studii de laborator, s‑a demonstrat, de asemenea, că statinele lipofile au efecte superioranticancer la nivel celular, comparativ cu statinele mai puțin solubile în grăsimi (Liu și colab., 2017).
studiile observaționale leagă, de asemenea, utilizarea statinei de răspunsul îmbunătățit al bolii la tratament și supraviețuire la pacienții cu cancer de sân, chiar și pentru pacienții cu tipuri de cancer de sân care pot fi mai agresivi (Manthravadi și colab., 2016; Murtola și colab., 2014; Zhong și colab., 2015). De exemplu, într-un studiu la pacienții cu cancer de sân inflamator, pacienții care au luat atorvastatină în timp ce erau tratați pentru cancer au avut o perioadă mai lungă de timp înainte ca boala lor să progreseze, comparativ cu cei care nu au luat o statină (Brewer și colab., 2013).
Statinstarget cancer de San celule
statine,în special liposolubile lipofile statine ca atorvastatina, reduce crestereași diviziunea celulelor cancerului de san si de a creste cancerul de San moartea celulelor instudii de laborator
German Diabetes Association”,”page”:”47-48″,”volume”:”111″,”issue”:”1″,”source”:”PubMed”,”abstract”:”theeffect de cinci statine, adică atorvastatina, fluvastatina, lovastatina, pravastatina și simvastatina au fost investigate cu privire la proliferarea liniei celulare de cancer mamar uman MCF-7. Toate statinele, cu excepția pravastatinei, au fost capabile să inhibe proliferarea celulelor până la 90% la o concentrație de 50 micro M. între statinele eficiente nu s-a observat nicio diferență semnificativă care să indice un efect specific aclass. Aceste date sugerează că statinele pot avea o semnificație clinică în prevenirea primară a cancerului de sân uman dincolo de efectul lor de scădere a colesterolului. Cu toate acestea, trebuie să se aștepte dovezi clinice înaintetragerea oricăror concluzii suplimentare.”, „DOI”:”10.1055/s-2003-37501″,”ISSN”:”0947-7349″,”notă”:”PMID: 12605351″,”journalAbbreviation”: „Exp. Clin. Endocrinol.Diabet”, „limbă”:”eng”,”autor”:,”emis”: {„date-părți”:]}}}],”schemă”:”https://github.com/citation-style-language/schema/raw/master/csl-citation.json”} (Alarcon Martinez etal., 2018; M., 2004; Seeger și colab., 2003).Studiile arată, de asemenea, că statinele pot bloca invazivitatea celulelor canceroase de sân în laborator, sugerând că pot ajuta, de asemenea, la încetinirea răspândirii cancerului în alte părți ale corpului (Kanugula și colab., 2014;Wolfe și colab., 2015). Într-un model de șoarece de cancer de sân metastatic, tratamentul cu stat a întârziat creșterea cancerului care se răspândise deja cu până la 80%,cu activitate benefică observată în decurs de o săptămână de la începerea tratamentului (Vintonenko și colab.,2012).
Otherstudies arată, de asemenea, că statinele pot ajuta la sensibilizarea celulelor cancerului de sân la tratamente standard de radioterapie ȘI chimioterapie (Kozar și colab., 2004; Van Wyhe și colab., 2017). Un studiu a constatsimvastatina ar putea sensibiliza celulele de cancer mamar triplu-negativ sau inflamator la radioterapie în laborator. Același studiu a continuat să observe la un pacientpopulație că femeile cu cancer de sân inflamator care au luat statine în timpul tratamentului lor au avut mai puține șanse ca cancerul lor să revină în termen de 3 ani (Lacerda și colab., 2014).
similar cu metformina, statinele pot produce aceste efecte anticanceroase în diferite tipuri de cancer de sân, inclusiv ER pozitiv, HER2 pozitiv și triplu-negativcancerul de sân. De fapt, unele studii de laborator arată că statinele sunt deosebit de eficienteîmpotriva celulelor triple-negative ale cancerului de sân (Campbell și colab., 2006;Yao și colab., 2017).
studiile clinice care investighează statinele în cancerul de sân sunt acum în curs de desfășurare
câteva studii clinice în stadiu incipient arată acum rezultate puternice pozitive în ceea ce privește statinele în cancerul de sân. Studiile de fază timpurie au investigat dacă statinele pre-chirurgicale timpurii pot ajuta la îmbunătățirea markerilor moleculari ai bolii la pacienții cu boală operabilă. Până în prezent,aceste studii arată profiluri moleculare îmbunătățite ale cancerului la pacienții cu tratament cu statine, sugerând că atorvastatina și alte statine în acest context pot avea efecte benefice asupra creșterii și divizării celulelor canceroase și a morții celulare, chiar și la femeile cu tumori mai agresive de grad înalt (Bjarnadottir și colab., 2013, 2015; Feldt și colab., 2015; Garwood și colab., 2010).
pe baza acestor rezultate promițătoare, un număr de studii de fază 2 care investighează statine adjuvante pentru o varietate de tipuri diferite de cancer de sân, inclusivtriple-negativ cancer de sân, sunt acum în curs de desfășurare. Aceste studii ar trebui să ajute la stabilirea modului în care statinele pot ajuta pacienții cu cancer de sân.
mebendazol și cancer de sân
interesul pentru mebendazolca un potențial tratament anticanceros se bazează în mare parte pe studii mecaniciste promițătoare și rapoarte convingătoare din studii de caz la pacienții cu cancer (Nygren și Larsson,2014; Pantziarka și colab., 2014).
Mebendazolese crede că ucide celulele canceroase parțial prin perturbarea structurilor speciale din interiorul celulei, numite microtubuli (Pantziarka și colab.,2014). Acesta funcționează într-un mod similar cu vincristina, medicament achemotherapy utilizat în prezent pentru tratamentul unor tipuri de cancer,inclusiv cancerul de sân în stadiu avansat (de Witt și colab., 2017).
studiile asupra celulelor canceroase de sân crescute în laborator arată că mebendazolul și medicamentele înrudite din aceeași clasă (numite benzimidazoli) pot încetini creșterea și diviziunea mai multor tipuri diferite de celule canceroase de sân, inclusiv celulele rezistente la chimoterapie (Coyne și colab., 2013;Hou și colab., 2015; Mukhopadhyay și colab., 2002). Într-un studiu, mebendazolul a redus puternic supraviețuirea celulelor canceroase de sân rezistente la chimioterapie cu până la 63,1% (Coyne și colab., 2013).Studiile au demonstrat, de asemenea, o activitate anticanceroasă robustă a benzimidazolelorîmpotriva cancerului de sân triplu negativ (Hou și colab., 2015; Zhang și colab., 2015). Important, într-un studiu a fost, de asemenea, demonstrat că benzimidazolul vizează direct celulele stem ale cancerului de sân (Hou și colab., 2015).
dovezile bazate pe laborator sugerează, de asemenea, că benzimidazolii pot spori activitatea tratamentelor standard pentru cancerul de sân, cum ar fi doxorubicina și fluorouracilul (Hou și colab., 2015). Întrun studiu de laborator, mebendazolul a crescut eficacitatea radioterapiei pecelulele canceroase de sân triplu-negative și a împiedicat rezistența la tratamentdezvoltarea (Zhang și colab., 2019a). În plus,o serie de studii utilizândcelulele canceroase pozitive rezistente la chimioterapie er/HER2 crescute în laborator,au arătat în mod constant că mebendazolul nu numai că a redus supraviețuirea celulelor canceroase, ci a contribuit, de asemenea, la completarea și îmbunătățirea activității formelor special dezvoltate de medicamente chimioterapice pentru cancerul de sân epirubicină și gemcitabină (Coyne și colab., 2014,2012, 2013).
doxiciclina și cancerul de sân
ca fiind un antibiotic eficient, doxiciclina posedă și alte proprietăți extrem de valoroase, inclusiv activitatea antiinflamatorie și anticanceroasă. Acest lucru oferă doxiciclinei un potențial terapeutic real în tratarea unei serii de alte boli, inclusiv a cancerului (Bahrami și colab., 2012).
studiile de laborator și studiile pe animale au arătat de mult că doxiciclina poate bloca creșterea, diviziunea și mișcarea celulelor canceroase la sân (Duivenvoorden și colab.,2002; Fife și Sledge, 1995, 1998).Studii mai recente arată, de asemenea, că doxiciclina poate opri celulele canceroase să-și refacă ADN-ul atunci când acesta devine deteriorat, de exemplu, prin chimioterapie (Peiris-Pag.,2015). Într-adevăr, studiile de laborator arată că doxiciclina poate ajutaîmbunătăți eficacitatea activității chimioterapice împotriva celulelor cancerului de sân (Foroodi și colab., 2009;Lamb și colab., 2015a).
cel mai recent, accentul a căzut pe înțelegerea modului în care doxiciclina poate bloca creșterea celulelor stem ale cancerului de sân (Ozsvari etal., 2017; Zhang și colab., 2017). Un studiu foarte recent asupra celulelor cultivate în laborator a arătat că doxiciclina poateblocați creșterea celulelor stem ale cancerului de sân HER2 pozitive și triple-negative și a contribuit la îmbunătățirea modificărilor legate de rezistență induse de standardchemoterapia paclitaxel (Lin și colab.,2018). Într-un studiu de laborator diferit, o abordare combinatoricăinclusiv doxiciclina a eradicat foarte eficient celulele stem ale cancerului de sân (Fiorillo etal., 2019).
doxiciclina tocmai a ajuns la studii clinice timpurii la pacienții cu cancer de sân. Rezultatele primului mic studiu, publicat în octombrie 2018, arată că pacienții cu cancer de sân în stadiu incipient care au luat doxiciclină timp de doar 14 zile înainte de operație au redus nivelurile de markeri moleculari pentru prezența celulelor stem canceroasecu o medie de aproximativ 40%. Au fost observate efecte benefice pentru toți, cu excepția unuia dintre pacienții tratați (8/9) (Scatena și colab., 2018).Studiile clinice mai mari sunt acum în curs de desfășurare.
propriile noastre dovezi: studiul METRICS
Ce este METRICS?
METRICS este propriul nostru program in-houseresearch. O mare parte este deja cunoscută despre siguranța șieficacitatea medicamentelor Protocolului COC în cancer. Dar este, de asemenea, responsabilitatea noastră să recunoaștem că nu avem toate răspunsurile și că West încă mai trebuie să genereze cercetări clinice de bună calitate care să investigheze Cocprotocolul la pacienții cu cancer, pentru a ne asigura că Protocolul COC este cât se poate de eficient și sigur.
pentru a ne permite să finanțăm această cercetare, am dezvoltat un sistem nou, accesibil, în care studiul nostru clinic, metricile, este în esență finanțat de pacienți. Fiecare pacient consimțit care intră în clinică esteînscris în valori, iar aceste taxe ajută la finanțarea studiului. Acesta este un nou model de cercetare clinică, care vizează reducerea decalajelor de finanțare și de date, care împiedică în prezent reutilizarea și dezvoltarea clinică ulterioară a medicamentelor deja autorizate.
METRICS first results
într-o primă formetrică de succes, rezultatele studiului nostru pilot inițial au fost publicate recent în revista științifică Frontiers in Pharmacology. Hârtia poate fi accesată gratuit online aici.
studiul pilot METRICS a fost un studiu retrospectiv observațional, ceea ce înseamnă că cercetătorii noștri au privit înapoi și au analizat înregistrările clinice ale pacienților pentru a afla ce s-a întâmplat. Ei au colectat date și au înregistrat rezultatele de la 95 de pacienți cu un tip avansat de cancer cerebral numit glioblastom care au participat la Clinica de oncologie Care și care au luat Protocolul complet COC alături de tratamentele standard obișnuite. Acest studiu nu a avut un grup de control, astfel încât cercetătorii noștri au comparat rezultatele din măsurători cu rezultatele publicate anterior din studiile anterioare la pacienți cu același tip de cancer și care au luat, de asemenea, tratamente standard de îngrijire.
rezultatele inițiale sugerează că pacienții care au participat la clinica noastră și au luat Protocolul COC ca parte a îngrijirii lor obișnuite au avut mult mai multe șanse să supraviețuiască cel puțin 2 ani (64.0% dintre pacienții din studiul nostru au supraviețuit cel puțin 2 ani, comparativ cu 27-29% pentru pacienții incluși în studiile publicate anterior) și au avut tendința de a avea o durată de supraviețuire mai lungă decât ar fi de așteptat în general pentru pacienții cu acest tip de cancer (pacienții au supraviețuit în medie 27 de luni în studiul nostru, comparativ cu 15-16 luni în studiile anterioare)(Agrawalet al., 2019).
aceste rezultate sunt extremepromițătoare, dar ele sunt, de asemenea, încă preliminare. Încă nu știm exact cum Protocolul COC ar fi putut afecta timpii de supraviețuire, de exemplu, sau cum alți factori, cum ar fi anumite caracteristici ale pacientului, ar fi putut influența, de asemenea, aceste rezultate. Dar această primă dovadă inițială este cu siguranță încurajatoare și ne sugerează că ne îndreptăm în direcția cea bună. Următorul nostru planificatetapa este de a efectua un studiu mai mare, bine conceput. Puteți afla mai multe despreplanuri de metrici viitoare căutând online sau contactând clinica.
mai multe despre protocolul COC
ce este protocolul COC?
protocolul COC este un regim de tratament combinat compus din medicamente autorizate, concepute în mod specific de Oncologie de îngrijire pentru utilizare adjuvantă alături de tratamentele obișnuite ale pacientului (adică standard de îngrijire).
cele patru medicamente incluse în regimul protocolului COC sunt: metformina, un medicament anti-diabet foarte comun; atorvastatina, un tip de statină utilizată pentru gestionarea afecțiunilor cardiovasculare; doxiciclina, un tip de antibioticadesea utilizat pentru tratarea infecțiilor cronice precum acneea; și mebendazolul, amedicina frecvent utilizată pentru tratarea infecțiilor parazitare la copii și adulți.
am ales aceste patru medicamente de la mii de potențiali candidați, în special pentru că se potrivesc criteriilor noastre de selecție prestabilite. Aceste criterii includ dovezi solide de eficacitate împotriva cancerului, un mecanism coerent de acțiune și, în mod important, un profil de siguranță bun. Aceste trei principii centrale ne-au modelatabordare de la bun început.
siguranța este primordială
cancerul este o boală complexă cu tratamente complexe și credem că adăugarea de terapii suplimentare alături de tratamentele standard ar trebui evaluată foarte atent. Nu doar din perspectiva eficacității, ci și, important, din punct de vedere al siguranței. Acesta este motivul pentru care întreaga noastră abordare se bazează pedovezi-studii științifice publicate în cea mai mare parte și, din ce în ce mai mult, date proprii.
multe medicamente diferite de pe piață au cel puțin unele dovezi publicate care susțin utilizarea lor relativ eficientă în cancer, dar puține dintre aceste medicamente au nivelul de dovezi atât de siguranță, cât și de eficacitate care au fost necesare pentru protocolul COC. Există deja cantități mari de date detaliate pentru fiecare dintre medicamentele de protocol, obținute din anii de utilizare în populația generală – și acest lucru ne-a ajutat să ne oferim un început crucial în timpul dezvoltării.
am căutat cu migală prin zeci de ani de date publicate despre fiecare dintre medicamentele Protocolului coc, explorând modul în care acestea funcționează în diferite populații de pacienți (inclusiv pacienți cu cancer) și pe modele celulare și animale din laborator. Aceste date, alături de propria noastră experiență clinică, ne ajută să ne asigurăm că avem o bună înțelegere a modului în care aceste medicamente se vor comporta la pacienți cu diferite stadii și tipuri de cancer, atât în combinație între ele, cât și în combinație cu numeroase alte terapii pentru cancer. Această cunoaștere esteparamumă, iar din studiile noastre, acest tip de dovezi nu există încă pentru mulți alți candidați la medicamente anticanceroase off‑label – mai ales atunci când li se administrează incombinație.
o terapie anti-metabolică care poate viza orice cancer
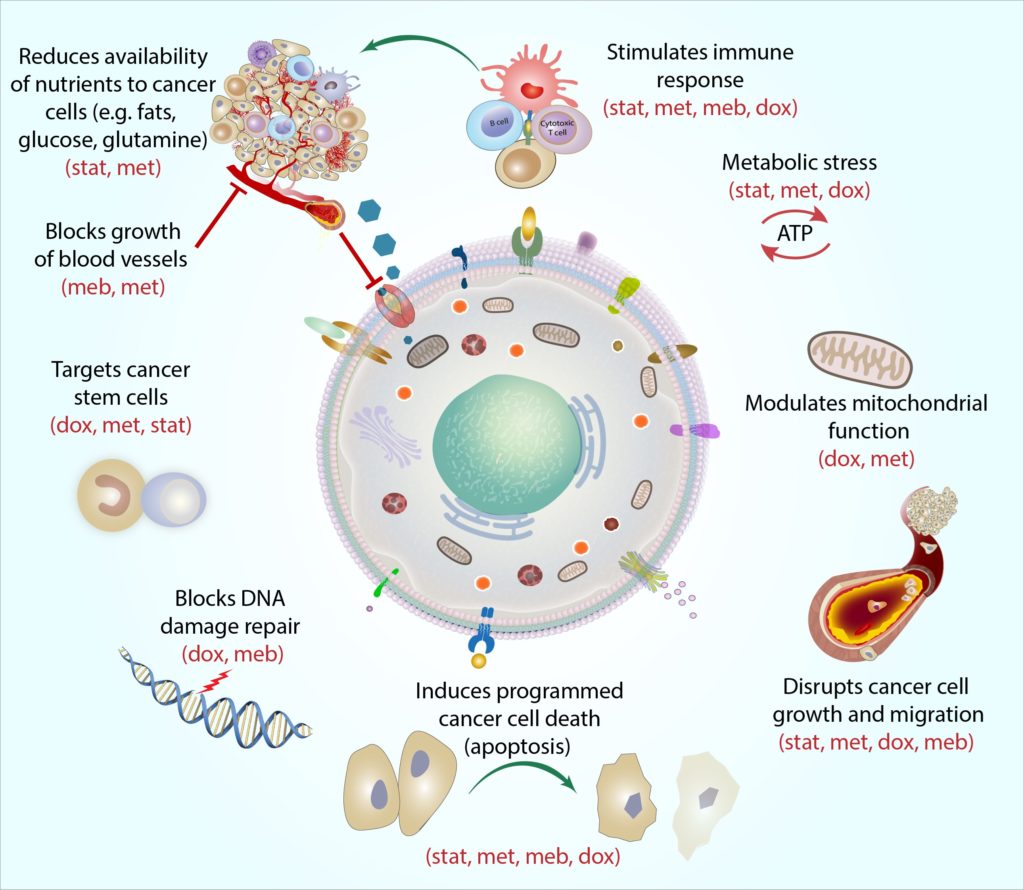
Protocolul Cecoc este conceput să funcționeze prin restricționarea capacității globale a celulelor canceroase de a prelua și utiliza (adică ‘metaboliza’) energie.
celulele canceroase au nevoie de cantități uriașe de energie pentru a supraviețui, iar marea majoritate a cancerelor utilizează un proces adaptiv numit glicoliză aerobă pentru a genera energia excesivă de care au nevoie (Kroemer andPouyssegur, 2008). Fiecare dintre medicamentele din protocol poate viza diverse procese metabolice moleculare implicate în și în jur aerobicglicoliza, iar acest lucru poate ajuta la scăderea ratei metabolice globale a canceruluicelulă (Jang și colab.,2013).
credem că medicamentele COCProtocol pot funcționa în combinație pentru a restricționa în mod constant furnizarea și utilizarea energiei, împiedicând simultan celulele canceroase să se adapteze și să utilizeze alte căi pentru a prelua energie (Jagust și colab.,2019). Ca urmare, celulele canceroase devin din ce în ce mai slabe și mai puțin capabile să ia și să utilizeze substanțele nutritive (de ex. cum ar fi glucoza și esențialăaminoacizi glutamină și arginină) au nevoie de împrejurimile lor (Andrzejewskiet al., 2018; Liu și colab., 2016).Acest lucru face mai dificil, în general, ca celulele canceroase să supraviețuiască, să crească și să se răspândească în organism. Treptat, celulele slăbite (inclusiv celulele mai rezistente și mai rezistente la tratament) devin mai vulnerabile la atacul de la alte terapii de cancer care ucid celulele, cum ar fi radioterapia,chimioterapia, terapia hormonală și terapiile vizate (Bradford andKhan, 2013; Chen și colab., 2012; Lacerda și colab., 2014; Lamb și colab., 2015a;Pantziarka și colab., 2014). prin orientarea mecanismelor metabolice adaptate, care sunt comune pentru majoritatea cancerelor (dar nu și pentru celulele sănătoase), credem că protocolul COC poate fi eficient și selectiv pentru aproape orice cancer,indiferent de tipul, stadiul sau localizarea specifică a cancerului. Studii epidemiologice și de laborator publicate din ce în ce mai multsprijină gama potențial largă a acestei terapii (Chae și colab., 2015, 2016; Iliopoulos și colab., 2011; Lamb și colab., 2015b; Pantziarka și colab.,2014).
coerența Mecanică în acțiune – puterea combinației
adevărata putere a Protocolului coc constă în combinația specifică de medicamente pe care le folosim. Am dezvoltat Protocolul nu doar ca un regim de patru tratamente individuale, fiecare cu activitate anticanceroasă, ci și pentru a funcționa ca un singur tratament combinat – cu potențialul de a produce efecte sinergice puternice (Mokhtari și colab., 2017).
fiecare medicament din Protocolul COC vizează metabolismul celulelor canceroase într-un mod distinct și complementar și am numit această acțiune ‘coerență mecanică’. Pur și simplu, coerența mecanicistă descrie modul în care fiecare medicament poate ataca celula canceroasă dintr-un unghi diferit. De exemplu, celulele stem canceroase sunt un tip de celule canceroase deosebit de rezistente și fiecare medicament vizează aceste celule într-un mod diferit: metformina vizează bateriile celulei (numite mitocondrie), făcând foarte dificil mitocondriilor să ruleze reacțiile moleculare de care au nevoie pentru a produce energie, doxiciclina blochează ADN-ul celular pe care mitocondriile trebuie să-l reproducă și să-l repare (Skoda și colab., 2019), statinepoate modifica expresia genei celulelor stem canceroase, făcând celulele mai sensibile la alte terapii împotriva cancerului (Kodach și colab., 2011), șimebendazolul poate întrerupe numeroase procese moleculare implicate în diviziunea celulară pentru a ajuta la blocarea creșterii celulelor stem canceroase (Hothi și colab., 2012; Hou și colab., 2015). prin combinarea tuturor celor patru agenți, protocolul COC poate lovi celulele stem canceroase (și alte celule canceroase) în mai multe puncte slabe și, ca un pumn unu-doi, acest lucru lasă celulele mai puțin capabile să se eschiveze și să se recupereze.
studiile de laborator încep să evidențieze eficacitatea acestei abordări folosind combinații de medicamente COCprotocol. Într-un studiu mecanicist, combinarea statinei și metforminei a scăzut foarte mult creșterea celulelor cancerului de prostată mai mult decâtfie agent singur (Wang și colab., 2017). Studiile observaționale au raportat, de asemenea, efecte potențial sinergice ale acestor medicamente împotriva diferitelor tipuri de cancer (Babcook etal., 2014; Danzig și colab., 2015; Lehman și colab., 2012; Nimako și colab., 2017). Un studiu clinic care investighează metformina și doxiciclina în cancerul de sân este nowunderway (NCT02874430), iar propriul nostru program de cercetare, METRICS, începe acum să producă date promițătoare.
o terapie adjuvantă pe termen lung
Protocolul COC este conceput în primul rând pentru a fi o terapie adjuvantă pe termen lung, pentru a ajuta la optimizarea tratamentelor standard. Cu toate acestea, deoarece tratamentul metabolic cu COCProtocol este destinat să se desfășoare pe termen lung, pacienții pot lua, de asemenea, protocolul ca regim de întreținere după terminarea tratamentului standard sau în timpul pauzelor de la tratamentul standard și ca parte a unei strategii pe termen lung de atenuare a riscului de recurență sau metastaze. Din acest motiv, este, de asemenea, de remarcat faptul căfiecare dintre medicamentele Protocolului COC a raportat, de asemenea, mecanisme benefice de acțiune în cancer care nu depind de administrarea concomitentă a terapiilor standard și care pot contribui în mod independent la reducerea riscului de recidivă și răspândire metastatică.
Modelul Oncologic de îngrijire
supravegherea medicală activă a fiecărui pacient
deși medicamentele COCProtocol au fost utilizate în siguranță în populația generală de mulți ani, fiecare pacient care vine la noi este unic. Acesta este motivul pentru care fiecare pacient care participă la Clinica de Oncologie de îngrijire este plasat sub îngrijirea directă a cliniciilorcu cunoștințe de specialitate privind prescrierea medicamentelor Protocolului COC în contextul cancerului. Clinicienii noștri evaluează individual beneficiile potențiale și riscurile implicate în luarea Protocolului COC cu fiecare pacient. Ei vor recomanda pacienților protocolul COC doar atunci când consideră că va fi sigur și benefic să facă acest lucru. Fiecare prescripție de protocol COC este adaptată nevoilor pacientului, iar dozele și regimurile sunt revizuite cu atenție și ajustate în funcție de modul în care progresează pacientul. prin urmare, este esențial ca pacienții să ia Protocolul COC numai în timp ce sunt monitorizați cu atenție la clinica noastră pe durata tratamentului.
*********************************************************************************
Notă importantă
Scopul acestui articol
Acest articol este o prezentare generală a unora dintre științifice și medicale publicateliteratura privind medicamentele care cuprind patentat de ingrijire Oncologyprotocol. S-a avut grijă să se selecteze articolele relevante care susțin utilizarea fără etichetă a acestor medicamente într-un cadru clinic pentru tratamentul adjuvant al cancerului. Acest articol nu se pretinde a fi o revizuire cuprinzătoare a tuturor dovezilor și nici nu surprinde toate efectele secundare potențiale ale unui astfel de tratament.
Acest articol are doar scop informativ și nu constituie sfaturi medicale. Medicamentele discutate aici sunt disponibile numai pe bază de rețetă și nu trebuie luate fără consultarea medicului dumneavoastră sau a altui furnizor profesionist de servicii medicale. Îngrijire medicii oncologi vor discuta despre adecvarea acestor medicamente cu dvs. și vor lua legătura cu medicul dumneavoastră sau oncologul pentru a discuta despre adecvarea lor pentru dumneavoastră.
nu trebuie să se bazeze pe informațiile din acest articol ca o alternativă la medicaladvice de la medicul dumneavoastră sau alt furnizor de servicii medicale profesionale. Dacă aveți orice întrebări specifice cu privire la orice problemă medicală, ar trebui să consultați medicul dumneavoastră sau alt furnizor de servicii medicale profesionale. Dacă credeți că este posibil să suferiți de orice afecțiune medicală, trebuie să solicitați asistență medicală imediată. Nu ar trebui să întârzieți niciodată să solicitați sfatul medicului, să nu luați în considerare sfatul medicului, saucontinuați tratamentul medical din cauza informațiilor conținute în acest articol.
Copyright
drepturile de autor din acest articol sunt deținute de Health Clinics LLC și de licențiatorii săi.
brevet
protocolul Care Oncology(„COC”) este protejat de brevetul SUA US9622982B2 și de diverse brevete internaționale suplimentare.
*********************************************************************************
Agrawal,S., Vamadevan, P., Mazibuko, N., Bannister, R., Swery, R., Wilson, S., andEdwards, S. (2019). O nouă metodă de generare a dovezilor etice și eficientepentru utilizarea medicamentelor Off-Label în oncologie (un studiu de caz în glioblastom). În față.Pharmacol. 10.Ahern, T. P., Lash, T. L., Damkier, P.,Christiansen, P. M. și Cronin-Fenton, D. P. (2014). Statinele și prognosticul cancerului de sân: dovezi și oportunități. Lancet Oncol. 15, e461-468.
Aksoy, S., Sendur, M. A. N. și Altundag, K. (2013).Caracteristicile demografice și clinico-patologice la pacienții cu invazivecancerul de sân care primește metformină. Med. Oncol. Northwood Lond. Engleză. 30, 590.
Alarcon Martinez, T., Zeybek, N. D., și m. Evaluarea efectelor citotoxice și Autofagice ale atorvastatinei asupracelulele canceroase mamare MCF-7. Sustrage. Med. J. 35, 256-262.
Alimova, I. N., Liu, B., Fan, Z., Edgerton, S. M.,Dillon, T., Lind, S. E. și Thor, A. D. (2009). Metformina inhibă cancerul de sâncreșterea celulelor, formarea coloniilor și induce oprirea ciclului celular in vitro. CellCycle 8, 909-915.
Andrzejewski, S., Siegel, P.M. și St-Pierre, J.(2018). Profiluri metabolice asociate cu eficacitatea metforminei în Cancer. În față.Endocrinol. 9.
Babcook, M. A., Shukla, S., Fu, P., Vazquez, E. J.,Puchowicz, M. A., Molter, J. P., stejar, C. Z., MacLennan, G. T., balon, C. A.,Lindner, D. J. și colab. (2014). Simvastatină sinergică și Metforminăchimoterapie pentru cancerul de prostată rezistent la castrare metastatică osoasă. Mol.Cancer Acolo. 13, 2288–2302.Bahrami, F., Morris, D. L. și Pourgholami,M. H. (2012). Tetracicline: medicamente cu potențial terapeutic imens. Mini Rev.Med.Chem. 12, 44–52.
Bao, B., Azmi, A. S., Ali, S., Zaiem, F. și Sarkar,F. H. (2014). Metformina poate funcționa ca agent anti-cancer prin țintirea celulelor canceroase: semnificația biologică potențială a miARN asociate tumorii în cancerele mamare și pancreatice. Ann. Trad. Med. 2.
Bjarnadottir, O., Romero, Q., Bendahl, P.-O.,Jirstr, K., Ryd, L., Loman, N., Uhl, M., Johannesson, H., Rose, C., Grabau, D., etal. (2013). Direcționarea HMG-CoA reductază cu statine într-o fereastră de oportunitate. Cancerul De Sân Res. Trata. 138, 499–508.
Bjarnadottir, O., Kimbung, S., Johansson, I.,Veerla, S., J, M., Bendahl, P.-O., Grabau, D., Hedenfalk, I. și Borgquist, S.(2015). Modificări transcripționale globale după tratamentul cu statină în cancerul de sân. Clin. Rac Res.Off. J. Am. Conf. Cancer Res. 21, 3402-3411.
Bonanni, B., Puntoni, M., Cazzaniga, M., Pruneri, G., Serrano, D., Guerrieri-Gonzaga, A., Gennari, A., Trabacca, M. S.,Galimberti, V., Veronesi, P. și colab. (2012). Efectul dublu al metforminei asupra cancerului de sânproliferarea într-un studiu randomizat presurgical. J. Clin. Oncol. Oprit. J. Am.Soc. Clin. Oncol. 30, 2593–2600.Bradford, S. A. și Khan, A. (2013). Individualizarechimoterapie folosind medicamentul antidiabetic, Metformin, ca un studiu Neexplorator de la Al-Qaida: Al-Qaida: Al-Qaida: Al-Qaida: Al-Qaida: Al-Qaida. J. Cancer Sci. Acolo. 5.
Brewer, T. M., Masuda, H., Liu, D. D., Shen, Y., Liu, P., Iwamoto, T., Kai, K., Barnett, C. M., Woodward, W. A., Reuben, J. M., și colab.(2013). Utilizarea statinei în cancerul de sân inflamator primar: un studiu de cohortă. Br.J. Cancer 109, 318-324.
Camacho, L., Dasgupta, A. și Jiralerspong, S.(2015). Metformin în cancerul de sân – un mister în evoluție. Cancer de sân Res. BCR 17, 88.
Campbell, M. J., Esserman, L. J., Zhou, Y., Cizmar,M., Lobo, M., Borman, E., Baehner, F., Kumar, A. S., Adduci, K., Marx, C., etal. (2006). Prevenirea creșterii cancerului de sân prin statine. Cancer Res. 66,8707-8714.
Cazzaniga, M., DeCensi, A., Pruneri, G., Puntoni, M., Bottiglieri, L., Varricchio, C., Guerrieri-Gonzaga, A., Gentilini, O. D., Pagani, G., Dell ‘ Orto, P. și colab. (2013). Efectul metforminei asupra apoptozeiîntr-un studiu pre-chirurgical al cancerului de sân. Br. J. Cancer 109, 2792-2797.
Chae, Y. K., Valsecchi, M. E., Kim, J., Bianchi, A. L.,Khemasuwan, D., Desai, A. și Tester, W. (2011). Reducerea riscului de cancer mamar la pacienții care utilizează inhibitori ECA, Bra și/sau statine. CancerInvest. 29, 585–593.
Chae, Y. K., Yousaf, M., Malecek, M.-K., Carneiro,B., Chandra, S., Kaplan, J., Kalyan, A., Sassano, A., Platanias, L. C. și Giles,F. (2015). Statinele ca terapie anti-cancer; Putem traduce datele preclinice și epidemiologice în beneficii clinice? Discov. Med. 20, 413–427.
Chae, Y. K., Arya, A., Malecek, M.-K., Shin, D. S.,Carneiro, B., Chandra, S., Kaplan, J., Kalyan, A., Altman, J. K., Platanias, L. și colab. (2016). Reutilizarea metforminei pentru tratamentul cancerului: studii clinice actuale. Oncotarget 7, 40767-40780.Chen, J., Lan, T., Hou, J., Zhang, J., An, Y., Tie, L., Pan, Y., Liu, J. și Li, X. (2012). Atorvastatina sensibilizează carcinoamele pulmonare cu celule mici humannon la carboplatină prin suprimarea activării AKT și reglarea în sus a TIMP-1. Int. J. Biochem. Biol Celular. 44, 759–769.Chen, L., Chubak, J., Boudreau, D. M., Barlow, W. E., Weiss, N. S. și Li, C. I. (2017). Tratamentele pentru diabet și riscurile de apariție a cancerului de sân în rândul pacienților cu cancer de sân în stadiu incipient: o analiză MEDICAREANALIZĂ SEER. Res. 77, 6033-6041.Chen, T., Liang, Y., Feng, D., Tao, L., Qi, K., Zhang, H., Wang, H., Lin, Q. și Kong, H. (2013). Metformina inhibă proliferarea și promovează apoptoza celulelor canceroase de sân HER2 pozitive prin reglarea în jos a hsp90. J. BUON Off. J. Balk. Uniunea Oncol. 18, 51–56.Coyne, C., Jones, T. și Bear, R. (2014).Citotoxicitatea Anti-neoplazică a gemcitabinei – (C4-amidă)-indual-combinație cu epirubicină – (C3-amidă)-împotriva adenocarcinomului mamar rezistent la chimioterapie (SKBr-3) și a efectului complementar al mebendazolului. J. Cancer Res. Oncol. 2.Coyne, C. P., Jones, T. și Bear, R. (2012). Influența inhibitorilor alternativi ai tubulinei asupra potenței aepirubicinei-Imunochimoterapeutic sintetizat cu un intermediar activat Ultra VioletLight. Cancer Clin. Oncol. 1, 49–80.Coyne, C. P., Jones, T. și Bear, R. (2013).Gemcitabine-(C4-amide)- Anti-Neoplastic Cytotoxicity in DualCombination with Mebendazole against Chemotherapeutic-Resistant MammaryAdenocarcinoma. J. Clin. Exp. Oncol. 2.
Cufi, S., Corominas-Faja, B., Vazquez-Martin, A.,Oliveras-Ferraros, C., Dorca, J., Bosch-Barrera, J., Martin-Castillo, B., andMenendez, J.A. (2012). Metformin-induced preferential killing of breast cancerinitiating CD44+CD24-/low cells is sufficient to overcome primary resistance totrastuzumab in HER2+ human breast cancer xenografts. Oncotarget 3, 395–398.
Danzig, M.R., Kotamarti, S., Ghandour, R.A., Rothberg, M. B., Dubow, B. P., Benson, M. C., Badani, K. K. și McKiernan, J. M. (2015).La bărbații cu diabet zaharat, riscul de apariție a prostatectomiei radicale poate fi modificat prin sinergie între metformină și statine în modificarea riscului de recidivă biochimică în urma prostatectomiei radicale la bărbații cu diabet zaharat. ProstateCancer Prostatic Dis. 18, 63–68.
Davies, G., Lobanova, L., Dawicki, W., Groot, G.,Gordon, J. R., Bowen, M., Harkness, T. și Arnason, T. (2017). Metformininhibă dezvoltarea și promovează resensibilizarea cancerului de sân rezistent la tratament. PLoS unu 12.de Witt, M., Gamble, A., Hanson, D., Markowitz, D., Powell, C., Al Dimassi, S., Atlas, M., Boockvar, J., Ruggieri, R. și Symons, M. (2017). Repurposing Mebendazol ca înlocuitor pentru vincristină pentrutratamentul tumorilor cerebrale. Mol. Med. 23, 50–56.
DeCensi, A., Puntoni, M., Gandini, S.,Guerrieri-Gonzaga, A., Johansson, H. A., Cazzaniga, M., Pruneri, G., Serrano,D., Schwab, M., Hofmann, U. și colab. (2014). Efectele diferențiale ale proliferării cancerului de sân metforminon în funcție de markerii rezistenței la insulină șitumor Subtip într-un studiu randomizat presurgical. Cancerul De Sân Res. Trata. 148,81–90.
DeCensi, A., Puntoni, M., Guerrieri-Gonzaga, A.,Cazzaniga, M., Serrano, D., Lazzeroni, M., Vingiani, A., Gentilini,O., Petrera, M., Viale, G. și colab. (2015). Efectul metforminei asupra proliferării Ductalcarcinomului mamar In Situ într-un studiu randomizat Presurgical. Cancer Prev.Res. Phila. Pa 8, 888-894.
Deng, X.-S., Wang, S., Deng, A., Liu, B., Edgerton,S. M., Lind, S. E., Wahdan-Alaswad, R. și Thor, A. D. (2012). Metformina ținteștetat3 pentru a inhiba creșterea celulară și a induce apoptoza în cancerul mamar triplu-negativ. Ciclul Celular Georget. Tex 11, 367-376.
Dowling, R. J., Parulekar, W. R., Gelmon, K. A., Shepherd, L. E., Virk, S., Ennis, M., Mao, F., Ligibel, J. A., Hershman,D. L., Rastogi, P. și colab. (2018). CA15-3 / MUC1 în CCTG MA-32 (NCT01101438): un RCT phaseIII al efectului metforminei față de placebo asupra bolii invazive libere și supraviețuirii permanente în cancerul de sân în stadiu incipient (BC). J. Clin. Oncol.
Duivenvoorden, W. C. M., Popovi, S. V., Lhot, S., Seidlitz,E., Hirte, H. W., Tozer, R. G., și Singh, G. (2002). Doxiciclina scade tumorulburări într-un model de metastază osoasă a cancerului de sân uman. Cancer Res. 62,1588-1591.
El-Benhawy, S. A. și el-Sheredy, H. G. (2014).Metformina și supraviețuirea la pacienții diabetici cu cancer de sân. J. Egipt.Sănătate Publică Conf. 89, 148–153.
Feldt, M., Bjarnadottir, O., Kimbung, S.,Jirstr, K., Bendahl, P.-O., Veerla, S., Grabau, D., Hedenfalk, I. și Borgquist, S.(2015). Efecte anti-proliferative induse de statină prin ciclina D1 și p27 în studiul cancerului de sân awindow-of-opportunity. J. Trad. Med. 13, 133.
Fife, R. S. și Sledge, G. W. (1995). Efectele doxiciclinei asupra creșterii in vitro, migrației și activității gelatinazei celulelor de cancer mamar. J. Lab. Clin. Med. 125, 407–411.
Fife, R. S., și Sledge, G. W. (1998). Efectele doxiciclinei asupra celulelor canceroase in vitro și in vivo. ADV. Dent. Res. 12, 94-96.
Fiorillo, M., T al zecelea, F., Sotgia, F. și Lisanti, M. P.(2019). Doxiciclina, Azitromicina și vitamina C (DAV) : o combinație potentăterapie pentru direcționarea mitocondriilor și eradicarea celulelor stem canceroase (CSC).Aging 11, 2202-2216.
Foroodi, F., Duivenvoorden, W. C. și Singh, G.(2009). Interacțiunile doxiciclinei cu agenții chimioterapeutici la om adenocarcinomul mamar MDA-MB-231 celule. Anticancer. Droguri 20, 115-122.
Garwood, E. R., Kumar, A. S., Baehner, F. L., Moore, D. H., Au, A., Hylton, N., flori, C. I., Garber, J., Lesnikoski, B.-A.,Hwang, E. S. și colab. (2010). Fluvastatina reduce proliferarea și creșteapoptoza la femeile cu grad ridicatcancerul mamar. Cancerul De Sân Res. Trata. 119, 137–144.
Giles, E. D., Jindal, S., Wellberg, E. A., Schedin, T.,Anderson, S. M., Thor, A. D., Edwards, D. P., MacLean, P. S. și Schedin, P.(2018). Metformina inhibă expresia aromatazei stromale și progresia tumoralăîntr-un model de rozătoare al cancerului de sân postmenopauzal. Cancerul de sân Res. BCR 20.
Goodwin, P. J., Parulekar, W. R., Gelmon, K. A., Shepherd, L. E., Ligibel, J. A., Hershman, D. L., Rastogi, P., Mayer,I. A., Hobday, T. J., Lemieux, J. și colab. (2015). Efectul metforminei față de placebo asupra factorilor metabolici și asupra MA NCIC CTG.32. J. Natl. Cancerul Inst. 107.
Hadad, S., Iwamoto, T., Iordania, L., Purdie, C., Bray,S., Baker, L., Jellema, G., Deharo, S., Hardie, D. G., Pusztai, L. și colab.(2011). Dovezi pentru efectele biologice ale metforminei în cancerul de sân operabil: un studiu preoperator, fereastră de oportunitate, randomizat. Cancerul De Sân Res. Trata. 128, 783–794.Hadad, S. M., Hardie, D. G., Appleyard, V., andThompson, A. M. (2014). Efectele metforminei asupra proliferării celulare a cancerului de sân, a căii AMPK și a ciclului celular. Clin. Trad. Oncol. Oprit.Publ. Fed. Span. Oncol. Soc. Natl. Cancerul Inst. Mex. 16, 746–752.
Hatoum, D. și McGowan, E. M. (2015). Progrese recenteîn utilizarea metforminei: tratarea diabetului poate preveni cancerul de sân? BioMedRes. Int. 2015, 548436.
Hirsch, H. A., Iliopoulos, D., Tsichlis, P. N., andStruhl, K. (2009). Metformina vizează selectiv celulele Stem canceroase și Acționeazăîmpreună cu chimioterapia pentru a bloca creșterea tumorii și a prelungi remisiunea. Cancer. 69, 7507–7511.
Hothi, P., Martins, T. J., Chen, L., Deleyrolle, L., Yoon, J.-G., Reynolds, B. și Foltz, G. (2012). Produse chimice de mare Tranzitatecranele identifică disulfiramul ca Inhibitor al celulelor Stem ale glioblastomului uman.Oncotarget 3, 1124-1136.
Hou, Z.-J., Luo, X., Zhang, W., Peng, F., Cui, B., Wu,S.-J., Zheng, F.-M., Xu, J., Xu, L.-Z., lung, Z.-J., și colab. (2015).Flubendazolul, antihelmintic aprobat de FDA, vizează celulele stem asemănătoare cancerului de sân.Oncotarget 6, 6326-6340.
Iliopoulos, D., Hirsch, H. A. și Struhl, K. (2011).Metformina scade doza de chimioterapie pentru prelungirea remisiunii tumorale înmouse xenogrefe care implică mai multe tipuri de celule canceroase. Cancer Res. 71,3196-3201.
Jacob, L., Kostev, K., Rathmann, W. și Kalder, M. (2016). Impactul metforminei asupra metastazelor la pacienții cu cancer de sân șidiabet de tip 2. J. Complicații Ale Diabetului 30, 1056-1059.
Jagust, P., De Lux-Delgado, B., Parejo-Alonso, B. și Sancho,P. (2019). Strategii Terapeutice Bazate Pe Metabolism Care Vizează Cancerulcelule Stem. În față. Pharmacol. 10.
Jang, M., Kim, S. S. și Lee, J. (2013). Cancer cellmetabolism: implicații pentru obiectivele terapeutice. Exp. Mol. Med. 45, e45.
Jiralerspong, S., Palla, S. L., Giordano,S. H., Meric-Bernstam, F., Liedtke, C., Barnett, C. M., Hsu, L., Hung,M.-C., Hortobagyi, G. N. și Gonzalez-Angulo, A. M. (2009). La pacienții diabetici cu cancer de sân, tratamentul cu metformină și Patologicărăspunsuri complete la chimioterapia neoadjuvantă la pacienții diabetici. J. Clin. Oncol. 27, 3297–3302.
Kalinsky, K., Crew, K. D., Refice, S., Xiao, T., Wang,A., Feldman, S. M., Taback, B., Ahmad, A., Cremers, S., Hibshoosh, H. și colab.(2014). Studiu pre-chirurgical al metforminei la pacienții supraponderali și obezi cucancerul de sân nou diagnosticat. Cancer Invest. 32, 150–157.
Kanugula, A. K., Gollavilli, P. N., Vasamsetti, S. B.,Karnewar, S., Gopoju, R., Ummanni, R. și Kotamraju, S. (2014). Indus de statininhibarea proliferării și invaziei cancerului de sân implică atenuarea transportului de fier: intermedierea oxidului nitric și a mecanismelor de apărare antioxidantă. Februarie J. 281, 3719-3738.
Kim, H. J., Kwon, H., Lee, J. W., Kim, H. J., Lee, S. B., Park, H. S., Sohn, G., Lee, Y., Koh, B. S., Yu, J. H. și colab. (2015). Metformincrește supraviețuirea în receptorii hormonali pozitivi, HER2-pozitivi cancer de sânpacienții cu diabet zaharat. Cancer de sân Res. BCR 17, 64.
Kim, J., Lim, W., Kim, E.-K., Kim, M.-K., Paik, N.-S.,Jeong, S.-S., Yoon, J.-H., Park, C. H., Ahn, S. H., Kim, L. S. și colab. (2014).Faza II studiu randomizat de metformin neoadjuvant plus letrozol versus placeboplus Letrozol pentru cancerul de sân postmenopauzal pozitiv al receptorului de estrogen (METEOR). Cancer BMC 14, 170.
Kodach, L. L., Jacobs, R. J., Voorneveld, P. W.,Wildenberg, M. E., Verspaget, H. W., van Wezel, T., Morreau, H., Hommes, D. W., Peppelenbosch, mp, van den Brink, G. R. și colab. (2011). Statinele sporesc hemosensibilitatea celulelor canceroase colorectale inducând reprogramarea epigenetică și reducând „tulpina” celulelor canceroase colorectale prin calea proteinei morfogenetice osoase. Intestin 60, 1544-1553.
Kozar, K., Kaminski, R., Legat, M., Kopec, M., Nowis,D., Skierski, J., Koronkiewicz, M., jak Unktibisiak, M. și Golab, J. (2004).Cerivastatina demonstrează o activitate antitumorală sporită împotriva liniilor celulare canceroase ale sânului uman atunci când este utilizată în asociere cu doxorubicină sau cisplatină. Int.J. Oncol.
Kroemer, G., și Pouyssegur, J. (2008). Tumoral CellMetabolism: călcâiul lui Ahile al cancerului. Celula Canceroasă 13, 472-482.Kwan, M. L., Habel, L. A., Flick, E. D., Quesenberry,C. P. și Caan, B. (2008). Utilizarea post-diagnostic a statinei și a cancerului de sânrecurența într-un studiu prospectiv de cohortă a cancerului de sân în stadiu incipient. Cancerul De Sân Res. Trata. 109, 573–579.
Lacerda, L., Reddy, J. P., Liu, D., Larson, R., Li, L.,Masuda, H., Brewer, T., Debeb, B. G., Xu, W., Hortob Unktigyi, G. N. și colab. (2014).Simvastatina radiosensibilizează liniile celulare diferențiate și asemănătoare tulpinilor și este asociată cu un control local îmbunătățit la pacienții cu cancer mamar inflamator tratați cu radiații postmastectomie. Celule Stem Transl. Med.3, 849–856.
Lamb, R., Fiorillo, M., Chadwick, A., Ozsvari, B.,Reeves, K. J., Smith, D. L., Clarke, R. B., Howell, S. J., Cappello, A. R.,Martinez-Outschoorn, U. E. și colab. (2015a). Doxiciclina reglează ADN-Pkși radiosensibilizează celulele de inițiere a tumorii: implicații pentru o terapie mai eficientă de radiație. Oncotarget 6, 14005-14025.
Lamb, R., Ozsvari, B., Lisanti, C. L., Tanowitz,H. B., Howell, A., Martinez-Outschoorn, U. E., Sotgia, F. și Lisanti, mp (2015b).Antibioticele care vizează mitocondriile eradică eficient celulele stem canceroase, în mai multe tipuri de tumori: tratarea cancerului ca o boală infecțioasă.Oncotarget 6, 4569-4584.
Lehman, D. M., Lorenzo, C., Hernandez, J. și Wang, C. (2012). Utilizarea statinei ca Moderator al efectului metforminei asupra riscului de cancer de prostată la pacienții cu diabet zaharat de tip 2. Îngrijirea Diabetului 35, 1002-1007.
Lin, C., Lo, M., Moody, R., Stevers, N., Tinsley, S. și Sun,D. (2018). Doxiciclina vizează cancerul de sân aldehidă dehidrogenază pozitivăcelulele stem. Oncol. Rep.
Liu, B., Yi, Z., Guan, X., Zeng, Y.-X. și Ma, F.(2017). Relația dintre statine și prognosticul cancerului de sân variază detipul de gelatină și timpul de expunere: o meta-analiză. Cancerul De Sân Res. Trata. 164,1–11.
Liu, H., Scholz, C., Zang, C., Schefe, J. H., Habbel,P., Regierer, A.-C., Schulz, C.-O., Possinger, K. și Eucker, J. (2012).Metformina și inhibitorul mTOR everolimus (RAD001) sensibilizează cancerul de sân la efectul citotoxic al medicamentelor chimioterapeutice in vitro. AnticancerRes. 32, 1627–1637.
Liu, X., Romero, I. L., Litchfield, L. M., Lengyel,E. și Locasale, J. W. (2016). Metformina vizează metabolismul central al carbonului șidezvăluie cerințele mitocondriale în cancerele umane. Metab Celulă. 24, 728–739.
Ma, J., Guo, Y., Chen, S., Zhong, C., Xue, Y., Zhang,Y., Lai, X., Wei, Y., Yu, S., Zhang, J. și colab. (2014). Metformina îmbunătățeșteinhibarea creșterii tumorale mediată de Tamoxifen în carcinomul mamar ER-pozitiv. BMCCancer 14, 172.
Manthravadi, S., Shrestha, A. și Madhusudhana, S.(2016). Impactul utilizării statinei asupra recurenței cancerului și a mortalității în cancerul de sân: o revizuire sistematică și meta-analiză. Int. J. Cancer 139, 1281-1288.
Mark, M., Klingbiel, D., Mey, U., Winterhalder, R.,Rothermundt, C., Gillessen, S., von Moos, R., Pollak, M., Manetsch, G.,Strebel, R. și colab. (2019). Impactul adăugării metforminei la abirateronă la pacienții cu cancer de prostată rezistenți la castrare metastatică cu Boalăprogresând în timpul tratamentului cu abirateronă (MetAb-Pro): studiu pilot de fază 2. Clin. Genitourin. Cancerul 17, e323-e328.
Martin-Castillo, B., Pernas, S., Dorca, J. A. S., A. S., A. S., A. S., A. S.,A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S. și colab. (2018). Un studiu de fază 2 de metformină neoadjuvantă în asociere cu trastuzumab și chimioterapie la femeicu cancer de sân HER2-pozitiv timpuriu: studiul METTEN. Oncotarget 9.35687-35704.Mokhtari, R. B., Homayouni, T. S., Baluch, N., Morgatskaya, E., Kumar, S., Das, B. și Yeger, H. (2017). Terapia combinată combaterea cancerului. Oncotarget 8, 38022-38043.M, A. O., Seeger, H. și Wallwiener, D. (2004).Efectul inhibitor al statinelor asupra proliferării cancerului de sân uman cells.Int J. Clin. Pharmacol. Acolo. 42, 695–700.Mukhopadhyay, T., Sasaki, J., Ramesh, R. și Roth, J. A. (2002). Mebendazolul provoacă un efect antitumoral puternic asupra celulelor canceroase umane, atât in Vitro, cât și in Vivo. Clin. Res.8, 2963-2969.
Murtola, T. J., Visvanathan, K., Artama, M.,Vainio, H. și Pukkala, E. (2014). Utilizarea statinei și supraviețuirea cancerului de sân: Un studiu la nivel naționalcohort din Finlanda. PloS Unul 9, e110231.
Nanni, O., Amadori, D., De Censi, A., Rocca,A., Freschi, A., Bologna, A., Gianni, L., Rosetti, F., Amaducci, L., Cavanna, L. și colab. (2019). Metformin plus chimioterapie versus chimioterapie singură în tratamentul de primă linie al cancerului de sân metastatic HER2-negativ. MYMErandomized, faza 2 studiu clinic. Cancerul De Sân Res. Trata. 174, 433–442.
Nimako, G. K., Wintrob, Z. A. P., Sulik, D. A., Donato,J. L. și Ceacăreanu, A. C. (2017). Beneficii sinergice ale statinei și Metformininei malignități gastro-intestinale. J. Pharm. Pract. 30, 185–194.
Niraula, S., Dowling, R. J. O., Ennis, M., Chang,M. C., terminat, S. J., Hood, N., Escallon, J., Leong, W. L., McCready, D. R., Reedijk, M. și colab. (2012). Metformina în cancerul de sân precoce: o fereastră prospectivă de oportunitate studiu neoadjuvant. Cancerul De Sân Res. Trata. 135, 821–830.Nygren, P. și Larsson, R. (2014). Repoziționarea medicamentuluide la bancă la noptieră:remiterea tumorii de către medicamentul antihelmintic mebendazolein cancer de colon metastatic refractar. Acta Oncol. 53, 427–428.Orecchioni, S., Reggiani, F., Talarico, G., Mancuso, P., Calleri, A., Gregato ,G., Labanca, V., Noonan, D. M., Dallaglio, K.,Albini, A. și colab. (2015). Biguanidele metformin și fenformin inhibăangiogeneza, creșterea locală și metastatică a cancerului de sân prin vizarea celulelor bothneoplastic și micromediu. Int. J. Cancer 136, E534-544.
Ozsvari, B., Sotgia, F. și Lisanti, M. P. (2017). O nouă abordare independentă de mutație a terapiei cancerului: inhibarea ras oncogenic șimyc, prin direcționarea biogenezei mitocondriale. Aging 9, 2098-2116.
Pantziarka, P., Bouche, G., Meheus, L., Sukhatme,V. și Sukhatme, V. P. (2014). Repurposing medicamente în oncologie (ReDO)—mebendazol Asan agent anti-cancer. Ecancermedicalscience 8.
Peiris-Pag, M., Sotgia, F. și Lisanti, M. P.(2015). Doxiciclina și direcționarea terapeutică a răspunsului la deteriorarea ADN-ului încelulele canceroase: medicament vechi, scop nou. Oncoscience 2, 696-699.
Rahmani, J., Manzari, N., Thompson, J., Gudi, S. K.,Chhabra, M., Naik, G., Mousavi, S. M., Varkaneh, H. K., Clark, C. și Zhang, Y.(2019). Efectul metforminei asupra biomarkerilor asociați cu cancerul de sân are loc: o revizuire sistematică, meta-analiză și răspuns la doză a studiilor clinice randomizate. Clin. Trad. Oncol.
Scatena, C., Roncella, M., Di Paolo, A., Aretini,P., Menicagli, M., Fanelli, G., Marini, C., Mazzanti, C. M., Ghilli, M., Sotgia,F. și colab. (2018). Doxiciclina,un Inhibitor al biogenezei mitocondriale, reduce în mod eficient celulele Stem canceroase (CSC) la pacienții cu Cancer de sân timpuriu: studiu Pilot Aclinic. În față. Oncol. 8.
Seeger, H., Wallwiener, D. și Mueck, A. O. (2003).Statinele pot inhiba proliferarea celulelor cancerului de sân uman in vitro. Exp.Clin. Endocrinol. Diabetul Oprit. J. Ger. Soc. Endocrinol. Ger. Diabet Conf.111, 47–48.
Skoda, J., Borankova, K., Jansson, P. J., Huang,M. L.-H., Veselska, R. și Richardson, D. R. (2019). Țintirea farmacologică a mitocondriilor în celulele stem canceroase: o organelă antică la intersecția terapiilor anti-cancer noi. Pharmacol. Rezoluția 139, 298-313.
Sonnenblick, A., Agbor-Tarh, D., Bradbury, I., DiCosimo, S., Azim, H. A., Fumagalli, D., Sarp, S., Wolff, A. C., Andersson, M.,Kroep, J. și colab. (2017). Impactul utilizării diabetului, insulinei și metforminei asupra rezultatului pacienților cu Receptor al factorului de creștere epidermică umană 2–cancer mamar primar pozitiv: analiză din studiul randomizat ALTTO de fază III. J. Clin. Oncol. 35, 1421–1429.Van Wyhe, R. D., Rahal, O. M., și Woodward, W. A. (2017). Efectul statinelor asupra recurenței și mortalității cancerului de sân: o revizuire.Cancerul De Sân Obiective Ther. 9, 559–565.
Vazquez-Martin, A., Oliveras-Ferraros, C., Cuff, S.,Del Barco, S., Martin-Castillo, B., Lopez-Bonet, E., și Menendez, J. A. (2011).Medicamentul antidiabetic metformin suprimă proteincd24 asociat metastazelor în celulele cancerului de sân triplu-negativ MDA-MB-468. Oncol. Rep. 25,135-140.
Vintonenko, N., Jais, J.-P., Kassis, N., Abdelkarim, M., Perret, G.-Y., Lecouvey, M., Crepin, M. și Di Benedetto, M. (2012).Analiza transcriptomului și activitatea in vivo a fluvastatinei versus zoledronicacid într-un model de metastază a cancerului de sân murin. Mol. Pharmacol. 82, 521–528.
Wahdan-Alaswad, R. S., Cochrane, D. R., Spoelstra,N. S., Howe, E. N., Edgerton, S. M., Anderson, S. M., Thor, A. D. și mai bogat, J. K.(2014). Uciderea indusă de metformină a celulelor cancerului de sân triplu negativ estemediată prin reducerea sintazei acidului gras prin miRNA-193b. Horm. Cancer 5.374-389.
Wang, Z.-S., Huang, H.-R., Zhang, L.-Y., Kim, S., El,Y., Li, D.-L., Farischon, C., Zhang, K., Zheng, X., Du, Z.-Y. și colab. (2017).Studiul mecanic al efectelor inhibitoare ale metforminei și atorvastatinei incombinate asupra celulelor cancerului de prostată in Vitro și in Vivo. Biol. Pharm. Taur.40, 1247–1254.
Wolfe, A. R., Debeb, B. G., Lacerda, L., Larson, R.,Bambhroliya, A., Huang, X., Bertucci, F., Finetti, P., Birnbaum, D., Van Laere,S. și colab. (2015). Simvastatina previne cancerul de sân triplu-negativmetastaza în modelele preclinice prin reglarea FOXO3a. cancer de sân. Trata. 154, 495–508.
Xu, H., Chen, K., Jia, X., Tian, Y., Dai, Y., Li, D.,Xie, J., Tao, M. și Mao, Y. (2015). Utilizarea metforminei este asociată cu o mai Bunăsupraviețuirea pacienților cu Cancer de sân cu diabet zaharat: o Meta-analiză. Teoncolog 20, 1236-1244.A. S., Ueno, N. T., Moulder, S. L., Hess, K. R., Shroff,G. S., Hodge, S., Koenig, K. H. și colab. (2019). Eficacitatea și siguranța combinației de metformină, everolimus și exemestan la pacienții supraponderali și obezi în postmenopauză cu cancer de sân metastatic,pozitiv la receptorul hormonal, HER2-negativ: un studiu de fază II.Investește. Medicamente Noi 37, 345-351.
Yao, H., He, G., Yan, S., Chen, C., Song, L., Rosol, T.J. și Deng, X. (2017). Cancer de sân triplu-negativ: există un tratamentpe orizont? Oncotarget 8, 1913-1924.
Zhang, L., Guo, M., Li, J., Zheng, Y., Zhang, S., Xie, T. și Liu, B. (2015). Descoperirea bazată pe biologia sistemelor a unui potențial Atg4Bagonist (Flubendazol) care induce autofagia în cancerul de sân. Mol. Biosyst.11, 2860–2866.
Zhang, L., Xu, L., Zhang, F. și Vlashi, E. (2017).Doxiciclina inhibă fenotipul celulelor stem canceroase și tranziția epitelială-mezenchimală în cancerul de sân. Ciclul Celular Georget. Tex16, 737-745.
Zhang, L., Bochkur Dratver, M., Yazal, T., Dong, K., Nguyen, A., Yu, G., Dao, A., Bochkur Dratver, M., Duhachek-Muggy, S., Bhat, K. și colab. (2019a). Mebendazolul potențează radioterapia în triplu-Negativcancerul de sân. Int. J. Radiat. Oncol. Biol. Fizică. 103, 195–207.Zhang, Y., Storr, S. J., Johnson, K., Green,A. R., Rakha, E. A., Ellis, I. O., Morgan, D. A. L. și Martin, S. G. (2014). Implicarea metforminei și AMPK în răspunsul radioactiv și prognosticul cancerului de sân luminal versusbasal tratat cu radioterapie. Oncotarget 5, 12936-12949.
Zhang, Z.-J., Yuan, J., Bi, Y., Wang, C., și Liu, Y.(2019b). Efectul metforminei asupra biomarkerilor și supraviețuitorilor pentru cancerul de sân-o revizuire sistematică și meta-analiză a studiilor clinice randomizate. Pharmacol.Res. 141, 551-555.
Zhong, S., Zhang, X., Chen, L., Ma, T., Tang, J., andZhao, J. (2015). Utilizarea statinei și mortalitatea la pacienții cu cancer: revizuire Sistematicăși meta-analiza studiilor observaționale. Tratamentul Cancerului. Rev. 41, 554-567.
