coc-Protokollen™ i Breast Cancer
dette dokumentet er et sammendrag av begrunnelsen og noen av de nåværende vitenskapelige bevisene som støtter bruk AV COC-Protokollmedikamenter sammen med standardbehandlingsbehandlinger for brystkreft. Vi forstår at kreft er en veldig personlig tilstand, og hver pasient har et unikt sett med utfordringer. For mer informasjon om din egen personlige situasjon, vennligst ta kontakt med Care Oncology Clinic på 800-392-1353 I Usa, eller besøk nettsiden på https://careoncology.com.
Hvis Du er ny Til Omsorg Onkologi vær oppmerksom på følgende:
- du trenger ikke å reise. Du kan møte med vårt team av onkologer og onkologi sykepleiere gjennom sikker video for kontinuerlig støtte.
- Care Oncology adjunct protocol medisiner sendes direkte hjem til deg fra VÅRE Amerikanske Partnerapotek og kan brukes sammen med din standardbehandling.
- Vi er utrolig stolte av å kunngjøre at vi har bestått Valideringsinstituttets ekstremt strenge valideringsprosess av dataanalyse, utfallskrav og verdiberegning. Vi har jobbet hardt for å komme til dette punktet. Tidlig anerkjente vi den enorme verdien et ansvarlig levert program med repurposed medisiner som tilbys til kreftpasienter, men det ble ikke tilbudt i stor skala. For fire år siden bestemte vi oss for å endre dette og visste at det var et maraton, ikke en sprint.
COC-Protokollen og brystkreft: Nøkkelpunkter
- DEN cocprotocol er en kombinasjon av fire vanlige foreskrevne medisiner(atorvastatin, metformin, mebendazol og doxycyklin) med potensial for å målrette brystkreft og bidra til å forbedre effektiviteten av standard anticancerterapier.
- et tall av observasjonsstudier har knyttet metformin eller statin bruk for å forbedreutfall hos pasienter med brystkreft.
- Laboratoriestudier på brystkreftceller dyrket i retter viser at metformin og statiner kan direkte målrette og skade brystkreftceller-svekke dem og gjøre dem mer utsatt for standardbehandlinger.resultater fra små ‘mulighetsvindu’ kliniske studier hos pasienter med operabel brystkreft viser generelt at det å ta metformin eller statin før kirurgi kan føre til potensielt positive endringer i molekylære markører for kreft, inkludert de som regulerer brystkreftcellevekst og deling. Flere forsøk undersøker om metformin eller statiner kan påvirke sykdomsrespons er i gang.
- Doxycyclinecan blokkere veksten AV BÅDE her2 positiv og trippel-negativ brystkreft stamceller inkubert i retter i laboratoriet, og bidro til å forbedre resistensrelaterte endringer indusert av standard kjemoterapi paclitaxel.
- Doxycyklinehar nettopp nådd tidlige kliniske studier hos brystkreftpasienter. Resultater fra den første lille studien viser at pasienter med tidlig stadium brystkreft som tok doxycyklin i bare 14 dager før kirurgi reduserte nivåene av molekylære markører for tilstedeværelse av kreftstamceller med et gjennomsnitt på rundt 40%. Gunstige effekter ble observert for alle unntatt en av pasientene som ble behandlet (8/9).
- Mebendazolekan bremse veksten og delingen av brystkreftceller dyrket i laboratoriet, inkludert brystkreftceller som er mer resistente mot kjemoterapi. Mermenneskelige studier er nødvendig.
COC-Protokollen og brystkreft: Publisert dokumentasjon
Icoc-Protokollen er et kombinasjonsregime med fire vanlige foreskrevne medisiner, hver med bevis på metabolisk-basert anticanceraktivitet og velforståtte sikkerhetsprofiler. Disse medisinene er: metformin, atorvastatin, doxycyklin og mebendazol. Noen av studiene som støtter bruk av theCOC-Protokollen som tilleggsbehandling sammen med dagens standardbehandling for brystkreft, er presentert nedenfor. Dette beviset kommer hovedsakelig fra laboratoriestudier, store epidemiologiske studier (som undersøker sammenhenger mellom å ta medisiner og brystkreftutfall i grupper av individer), og tidligstadie kliniske studier.Du kan legge merke Til at mange av studiene nedenfor bare fokuserer på individuelle COC-Protokollmedisiner. Vi er de første til å designe en tilleggsbehandling som kombinerer allfour. Vi tror at kombinering av disse medisinene vil oppnå de størsteresultatene, og vårt eget forskningsprogram, KALT METRICS, produserer allerede mer av bevisene som trengs for å vise dette. Du kan lese mer om hvorfor vi trordisse medisinene fungerer så godt sammen for å hjelpe til med å målrette kreft, og om metrics-programmet selv, i ytterligere seksjoner nedenfor.
Metformin og brystkreft
Metforminbruk knyttet til potensielle brystkreftfordeler
Mange Observasjonsstudier gir nå bevis for bruk av metformin inbrystkreft. Metformin er lisensiert til å behandle type 2 diabetes, ogobservasjonsstudier i grupper av pasienter med diabetes har en tendens til å vise detde som tar metformin har bedre sjanser for et bedre utfall hvis de utvikler brystkreft (Aksoy et al ., 2013; El-Benhawy og El-Sheredy, 2014; Sonnenblick et al., 2017).Metforminbruk har vært knyttet til forbedret overlevelse hos pasienter med brystkreft (Kim et al., 2015; Xuet al., 2015), forbedret respons på brystkreftbehandling (Jiralerspong et al.,2009), og mindre sjanse for brystkreft spredning andrelapse (Chen et al ., 2017; Jacob et al., 2016). det er usannsynlig at noen av de gunstige effektene av metformin som finnes i disse studiene skyldes metformins evne til å forbedre pasientens diabetes og / eller vekt ved å redusere glukosenivåer, noe som kan bidra til å redusere risikoen for å utvikle brystkreft, og forbedre pasientens helse og evne til å takle brystkreft hvis De har det (Hatoum og McGowan,2015). Men laboratoriestudier viser også at metformin ergjør mer enn dette. Faktisk kan metformin aktivt jobbe direkte motbrystkreftceller, redusere deres evne til å ta opp og bruke energi, og blokkerederes evne til å vokse, spre seg, overleve og tilbakefall (Alimova et al., 2009; Hadad et al., 2014; Orecchioni et al., 2015).
Forskjelligtyper brystkreft krever forskjellige behandlinger. Trastuzumab,for eksempel, er spesielt brukt til å behandle human epidermal vekstfaktorreseptor 2 (HER2)positiv brystkreft. Tamoxifen er effektiv mot østrogenreseptor (er) positiv brystkreft. Det er viktig at kreftcellestudier i laboratoriet viser at metformin har anticanceraktivitet mot mange forskjellige brystkreftcelletyper, inkludert er positive (Giles et al., 2018), HER2 positive (Ingeborg et al., 2013), ogpotensielt vanskeligere å behandle subtyper som trippel-negative kreftceller (Deng et al., 2012; Jørgen et al., 2011; Wahdan-Alaswad et al., 2014).Dette betyr at metformin har potensial til å fungere effektivt sammen med standardbehandlinger for brystkreft, uavhengig av kreftsubtype.
Metformintargets brystkreft stamceller
Metforminhar også vist seg å målrette brystkreft stamceller (Bao et al., 2014; Cufiet al., 2012; Hirsch et al., 2009).Denne aktiviteten mot brystkreftstamceller, sammen med evnen til å målrette ulike undertyper av brystkreft, bidrar til å forklare hvorfor laboratoriestudier kan fungere i kombinasjon med en rekke standardbehandlinger, inkludert trastuzumab (Cufi et al., 2012), jørgensen (et al., 2014), ogstandard kjemoterapi midler (Iliopoulos et al.,2011). Dyre-og cellestudier viser at metformin beggebidrar til å forbedre effektiviteten av standardbehandlinger (Bradford Og Khan, 2013; Liu Et al., 2012; Zhang et al., 2014) og forsinker også tilbakefall av kreft som har blitt behandlet med disse terapiene (Iliopoulos et al .,2011). I Tillegg viser laboratoriestudier også at metformin også kan bidra til å forhindre brystkreftceller fra å bli resistente mot kjemoterapi, og forbedre følsomheten av allerede resistente kreftceller til behandling (Davies et al., 2017).
Metforminforbedrer markører for brystkreft i tidlige kliniske studier
som et resultat av den store mengden støttende data for metformin i brystkreftgenerert ved observasjons-og laboratoriestudier, er ulike kliniske forsøk på å undersøke metformin i brystkreft nå i gang (Camacho et al., 2015).Samlet sett begynner kollektive analyser av resultatene av disse tidlige stadiene(meta-analyse) å foreslå en generelt positiv effekt nårmetformin legges til standard kreftbehandlinger (Rahmani etal., 2019; Zhang et al.( 2019b). Et Antall mulighetsvinduer undersøker om metforminfor rundt to uker før operasjonen kan bidra til å forbedre molekylære markører for sykdommen hos pasienter med operabel brystkreft i tidlig stadium. Resultater fra disse studiene tyder generelt på at metformin kan føre til potensieltpositive endringer i molekylære markører for kreft, inkludert de som regulerer brystkreft cellevekst og deling (Bonanni et al., 2012; Cazzaniga et al., 2013; Hadad et al., 2011; Kalinsky et al., 2014; Niraula etal., 2012), samt potensielt bedre reguleringen avhormoner og andre faktorer for noen pasienter (Kalinsky et al., 2014; Niraula et al., 2012). Disse studiene er nåhjelpe forskere å forstå nøyaktig hvordan og når metformin kan hjelpepasienter med brystkreft (Bonanni etal., 2012; DeCensi et al., 2014, 2015; Rahmani et al., 2019).Phase2′ neoadjuvant ‘ studier er generelt lengre og mer komplekse studier som undersøker metformin sammen med kurs av standard behandlinger for å behandle forskjellige typer brystkreft. Målet med disse forsøkene er å etablere ifmetformin virkelig bidrar til å forbedre effektiviteten av standardbehandlinger, foreslår aslab-studier (Kim Et al ., 2014). Inen nylig studie (METTEN-studien) (Martin-Castillo etal., 2018), hos kvinner MED HER2 positiv brystkreft i tidlig stadium, responderte flere pasienter som tok metformin godt på kjemoterapi/målrettet behandling (65,5%) sammenlignet med pasienter som ikke tok metformin (58,6%). Thisdifference var ikke statistisk signifikant; noe som betyr at dette resultatet kunne ha blitt nådd ved en tilfeldighet. Fase 2-forsøk er imidlertid generelt underpoweredfor å nå statistisk signifikans på denne måten ,og forskerne kalte for progresjon til større Fase 3-forsøk som kan utformes riktig for å bestemme hvor ekte denne effekten er (Martin-Castillo etal., 2018). Potensielt oppmuntrende resultater fra Andre Fase 2-forsøk, som en hos overvektige personer med metastatisk brystkrefthar også blitt rapportert (Yam et al.,2019). Det er også verdt å merke seg at som forventet, ikke allemetformin kreftforsøk har rapportert positive resultater. For eksempel har andre fase 2-studier funnet metformin med standardbehandling ikke hatt noen reell forskjell i forhold til standardbehandling alene under visse omstendigheter (Mark et al.,2019; Nanni et al., 2019). Vi tror thatmetformin vil være mest effektive i enhver setting når det gis i kombinasjon med andre anti-metabolske medisiner.Større Studier er nødvendig for å løse disse problemene, og En Fase 3-studie er nåundervei for å undersøke metformin i brystkreft. Selv om forsøket ikke er ferdig før 2020, viste de første resultatene fra de første 6 månedene av forsøket at pasienter som begynte å ta metformin umiddelbart etter ferdigstillelse av kirurgi og standard kjemoterapi sykluser, hadde gunstige endringer i en molekylær markør for brystkreft (Dowling et al., 2018), ogforbedret metabolske faktorer (Goodwin et al., 2015).
Statiner og brystkreft
Observasjonsstudier knytter statiner til bedre brystkreftutfall
Statiner blir vanligvis gitt for å håndtere kardiovaskulær sykdom. Men observasjonsstudier på store grupper av mennesker som tar statiner har også funnet atindivider med brystkreft som tar statiner kan også ha redusert risiko for deres kreft tilbakevendende etter behandling, sammenlignet med pasienter som ikke tar statiner (Ahern et al., 2014; Manthravadi et al., 2016). For eksempel, i enstudie i nesten 2000 overlevende av brystkreft, de som begynte å taflekker innen tre år etter diagnosen hadde redusert sjanse for at kreftkommer tilbake (Kwan et al., 2008). I en annen studie var bare 6 måneders statinbruk etter diagnose knyttet tilforbedrede tilbakefall (Chae et al ., 2011).Det Er Viktig at den gunstige effekten av statiner i disse og andre studier var sterkere knyttet til mer fettløselige ‘lipofile’ statiner (som atorvastatin). I somelaboratoriestudier har lipofile statiner også vist seg å ha superioranticancer-effekter på mobilnivå sammenlignet med mindre fettløselige statiner (Liu et al., 2017). Observasjonsstudier knytter også statinbruk til forbedret sykdomsrespons på behandling og overlevelse hos pasienter med brystkreft, selv for pasienter med brystkrefttyper som kan være mer aggressive (Manthravadi et al.,2016; Murtola et al., 2014; Zhong et al., 2015). For eksempel, i en studie hos pasienter med inflammatorisk brystkreft, pasienter som tok atorvastatin mens de ble behandlet for kreft, hadde en lengre periodefør sykdommen deres utviklet seg, sammenlignet med de som ikke tok statin (Brewer et al ., 2013).
Statinstarget brystkreftceller
Statiner,spesielt fettløselige lipofile statiner som atorvastatin, reduserer vekstog deling av brystkreftceller og øker brystkreftcelledød ilaboratoriestudier
tysk Diabetesforening»,»side»:»47-48″,»volum»:»111″,»utgave»:»1″,»kilde»:»PubMed»,»abstrakt»:»Effekten av fem statiner, dvs.atorvastatin, Fluvastatin, lovastatin, pravastatinog simvastatin ble undersøkt på spredning av human brystkreftcellelinje mcf-7. Alle statiner unntatt pravastatin var i stand til å hemme celleproliferasjon opp til 90 % ved en konsentrasjon på 50 mikro M. mellom de effektive statinene ble det ikke observert noen signifikant forskjell som indikerer aclassspesifikk effekt. Disse dataene tyder på at statiner kan ha kliniskbetydning i primær forebygging av brystkreft hos mennesker utover deres kolesterolsenkende effekt. Imidlertid må klinisk bevis ventes førtegne noen viderekonklusjoner.», «DOI»: «10.1055/s-2003-37501», «ISSN»:»0947-7349″,»notat»:»PMID: 12605351″,»journalforkortelse»: «Exp. Clin. Endokrinol.Diabetes», «språk»:»eng»,»forfatter»:,»utstedt»: {«dato-deler»:]}}}],»skjema»: «https://github.com/citation-style-language/schema/raw/master/csl-citation.json»} (Alarcon Martinez etal., 2018; Mü et al., 2004; Seeger et al., 2003).Studier viser også at statiner potensielt kan blokkere invasiviteten til brystkreftceller i laboratoriet, noe som tyder på at de også kan bidra til å redusere kreftspredningen til andre deler av kroppen (Kanugula et al., 2014; Wolfe et al., 2015). I en musemodell av metastatisk brystkreft forsinket statinbehandling veksten av kreft som allerede hadde spredt seg med opptil 80%, med gunstig aktivitet notert innen en uke etter behandlingsstart (Vintonenko et al.,2012). Andre Studier viser også at statiner kan bidra til å sensibilisere brystkreftceller tilstandard strålebehandling og kjemoterapi behandlinger (Kozar et al., 2004; Van Wyhe et al., 2017). En studie funnetsimvastatin kan sensibilisere trippel-negative eller inflammatoriske brystkreftceller til strålebehandling i laboratoriet. Den samme studien fortsatte å observere hos en pasientbefolkning at kvinner med inflammatorisk brystkreft som tok statiner under deres behandling hadde mindre sjanse for at kreften kom tilbake innen 3 år (Lacerda et al., 2014).Lignende Til metformin kan statiner produsere disse krefteffektene på tvers av ulike brystkrefttyper, inkludert ER-positiv, HER2-positiv og trippel-negativbrystkreft. Faktisk viser noen laboratoriestudier statiner er spesielt effektivemot trippel-negative brystkreftceller (Campbell et al., 2006; Yao et al., 2017).
Clinicaltrials undersøker statiner i brystkreft er nå i gang
et fåtidlig stadium kliniske studier viser nå robust positive resultater i form avstatiner i brystkreft. Tidlig fase ‘window of opportunity’ studier har undersøkt om tidlig, pre-kirurgiske statiner kan bidra til å forbedre molekylærmarkører av sykdommen hos pasienter med operabel sykdom. Så langt disse studienevis forbedret kreftmolekylære profiler hos pasienter med statinbehandling, noe som tyder på atorvastatin og andre statiner i denne sammenheng kan ha gunstige effekter på kreftcellevekst og deling og celledød, selv hos kvinner medhøyverdige mer aggressive svulster (Bjarnadottir et al.,2013, 2015; Feldt et al., 2015; Garwood et al., 2010).På disse lovende resultatene undersøker En rekke Fase 2-studier adjunktive statiner for en rekke forskjellige typer brystkreft, inkluderttrippel-negativ brystkreft, er nå i gang. Disse studiene skal hjelpeetablere hvordan statiner kan hjelpe pasienter med brystkreft.
Mebendazol og brystkreft
En potensiell kreftbehandling er for det meste basert på lovende mekanistiske studier og overbevisende rapporter fra case-studier hos kreftpasienter (Nygren Og Larsson,2014; Pantziarka et al., 2014). Mebendazol antas å drepe kreftceller delvis ved å forstyrre spesielle strukturer inni cellen, kalt mikrotubuli (Pantziarka et al.,2014). Det fungerer på samme måte som vinkristin, achemoterapi-legemiddel som for tiden brukes til behandling av enkelte typer kreft, inkludert avansert brystkreft (De Witt et al., 2017). Studier På brystkreftceller dyrket i laboratoriet viser at mebendazol og relaterte stofferfra samme klasse (kalt benzimidazoler) kan redusere veksten og delingen av flere forskjellige typer brystkreftceller, inkludert celler som er resistente motkjemoterapi (Coyne et al., 2013; Hou et al., 2015; Jørgen et al., 2002). Inone studie, mebendazol kraftig redusert overlevelse av kjemoterapi-resistantbrystkreftceller med så mye som 63,1% (Coyne et al., 2013).Studier har også vist robust anticancer aktivitet av benzimidazolermot trippel-negativ brystkreft (Hou et al., 2015; Zhang et al., 2015). Viktig, i en studie var også en benzimidazol vist å målrette brystkreft stamceller direkte (Hou et al., 2015).
Emerginglaboratory-baserte bevis tyder også på at benzimidazoler kan forbedre aktiviteten av standard brystkreftbehandlinger som doxorubicin ogfluorouracil (Hou et al., 2015). Inone lab studie, mebendazol økt effektiviteten av strålebehandling påtriple-negative brystkreftceller, og forhindret motstand mot behandlingutvikle (Zhang et al.(2019a). I tillegg har en rekke studier medkjemoterapi-resistente er/HER2 positive brystkreftceller vokst i laboratoriet, konsekvent viste at mebendazol ikke bare redusert overlevelse av kreftceller, det bidro også til å utfylle og forbedre aktiviteten til spesialutvikletmålrettede former for brystkreft kjemoterapi narkotika epirubicin og gemcitabin (Coyne et al ., 2014,2012, 2013).
Doxycyklin og brystkreft
Asidefra å være et effektivt antibiotikum har doxycyklin også andre ekstremtverdifulle egenskaper, inkludert antiinflammatorisk og anticanceraktivitet. Dette gir doxycyklin ekte terapeutisk potensial i behandling av en rekke andre sykdommer, inkludert kreft (Bahrami et al., 2012). Labstudier og dyrestudier har lenge vist at doxycyklin kan blokkere brystkreftcellevekst, divisjon og bevegelse (Duivenvoorden et al.(2002; Fife og Sledge, 1995, 1998).Nyere studier viser også at doxycyklin kan stoppe kreftceller frarepairing DERES DNA når det blir skadet, for eksempel ved kjemoterapi (Peiris-Pag@s et al .,2015). Faktisk viser laboratoriestudier at doxycyklin kan hjelpeforbedre effektiviteten av kjemoterapiaktivitet mot brystkreftceller (Foroodi et al., 2009; Lamb et al.( 2015a). For Det Meste har fokuset falt på å forstå hvordan doxycyklin kan blokkere brystkreftstamcellevekst (Ozsvari etal., 2017; Zhang et al., 2017). Avery nyere studie på celler dyrket i laboratoriet har vist at doksycyklin canblock vekst av BÅDE her2 positive og trippel-negative brystkreft stemcells, og bidro til å forbedre resistensrelaterte endringer indusert av standardkjemoterapi paclitaxel (Lin Et al .,2018). I en annen laboratoriestudie, en kombinatorisk tilnærminginkludert doxycyklin utryddet veldig effektivt brystkreft stamceller (Fiorillo etal., 2019).
Doxycyklinehar nettopp nådd tidlige kliniske studier hos brystkreftpasienter. Resultater fra den første lille studien, publisert i oktober 2018, viser at pasienter med tidlig stadium brystkreft som tok doxycyklin i bare 14 dager førkirurgi reduserte nivåer av molekylære markører for forekomst av kreftstamcellermed et gjennomsnitt på rundt 40%. Gunstige effekter ble notert for alle, men en av de behandlede pasientene (8/9) (Scatena et al., 2018).Større kliniske studier er nå i gang.
Våre egne bevis: METRICS Study
Hva ER METRICS?
METRICS er vår egen in-houseresearch program. Mye er allerede kjent om sikkerheten ogeffektiviteten AV COC-Protokollen medisiner i kreft. Men det er også vårt ansvar å erkjenne at vi ikke har alle svarene, og at vi fortsatt trenger å generere god kvalitet klinisk forskning som undersøker COCProtocol hos pasienter med kreft, for å sikre AT COC-Protokollen er så effektiv og trygg som den kan være. For å gjøre det mulig for oss å finansiere denne forskningen, har vi utviklet et nytt, rimelig system der vår kliniske studie, BEREGNINGER, i hovedsak er ‘pasientfinansiert’. Hver samtykkende pasient som går inn i klinikken er rullet inn I BEREGNINGER, og disse avgiftene bidrar til å finansiere studien. Dette er en ny modell for klinisk forskning, med sikte på å bygge bro over finansierings-og datagapsom for tiden hindrer gjenbruk og videre klinisk utvikling av allerede lisensierte medisiner. METRICS first results
i en første suksess forMETRICS ble resultatene fra vår første pilotstudie nylig publisert i thepeer-reviewed scientific journal Frontiers in Pharmacology. Den papercan nås fritt på nettet her.METRICS pilotstudien var anobservasjonell retrospektiv studie, noe som betyr at våre forskere så tilbake og analyserte pasientkliniske poster for å finne ut hva som skjedde. De samlet inn data og registrerte resultatene fra 95 pasienter med en avansert type hjernekreft kalt glioblastom som deltok På Care Oncology Clinic og som tok hele COC-Protokollen sammen med sine vanlige standardbehandlinger. Denne studien hadde ikke en kontrollgruppe, så våre forskere sammenlignet resultatene fra BEREGNINGER med tidligere publiserte resultater fra tidligere studier hos pasienter med samme type kreft,og som også tok standardbehandling. Innledende resultater tyder på atpasienter som deltok på vår klinikk og tok COC-Protokollen som en del av deresvanlig omsorg var mye mer sannsynlig å overleve minst 2 år(64 .0% av pasientene i vår studie overlevde minst 2 år, sammenlignet med 27-29% for pasienter inkludert i tidligere publiserte studier), og hadde en tendens til å ha lengre overlevelsestider totalt enn det som vanligvis forventes for pasienter med denne type kreft (pasientene overlevde i gjennomsnitt 27 måneder i vår studie, sammenlignet med 15 – 16 måneder i tidligere studier)(Agrawalet al., 2019).
disse resultatene er ekstremtlovende, men de er også fortsatt foreløpige. Vi vet ennå ikke nøyaktig hvordan COC-Protokollen kan ha påvirket overlevelsestider for eksempel, eller hvordan andre faktorer som visse pasientkarakteristikker også kan ha påvirket disse resultatene. Men dette første, første bevis er absolutt oppmuntrende, og detforeslår oss at vi er på vei i riktig retning. Vår neste planlagtscenen er å gjennomføre en større, godt designet studie. Du kan finne ut mer omfremtidige BEREGNINGER planer ved å se på nettet eller kontakte klinikken.
Mer om COC-Protokollen
Hva er COC-Protokollen?
COC-Protokollen er et kombinasjonsbehandlingsregime bestående av lisensierte medisiner, spesifikt utformet Av Care Oncology for tilleggsbruk sammen med pasientens vanlige behandlinger(dvs. standardbehandling). De Fire medisinene som inngår i COC-Protokollen er: metformin, avery common anti-diabetes drug; atorvastatin, en type statin som brukes til å administrere kardiovaskulære forhold; doxycyklin, en type antibiotika som ofte brukes til å behandle kroniske infeksjoner som akne; og mebendazol, amedicin som vanligvis brukes til å behandle parasittinfeksjoner hos barn og voksne.
vi valgte disse fourmedications fra tusenvis av potensielle kandidater spesielt fordi de passer våre forhåndsbestemte utvalgskriterier. Disse kriteriene omfatter solide bevis for effekt mot kreft, en sammenhengende virkningsmekanisme og viktig, en god sikkerhetsprofil. Disse tre sentrale prinsippene har formet vårtilnærming fra begynnelsen.
Sikkerhet er viktig
Kreft er en kompleks sykdom med komplekse behandlinger, og vi tror at tilleggetav ytterligere terapier sammen med standardbehandlinger bør være svært nøyevaluert. Ikke bare fra effektivitetsperspektivet, men også viktigere når det gjelder sikkerhet. Derfor er hele vår tilnærming basert påbevis-for det meste publiserte vitenskapelige studier, og også i økende grad våre egne data. Mange forskjellige medisiner på markedet har minst noen publiserte bevis som støtter deres relativt effektive bruk i kreft, men få av dissemedisiner har bevis på både sikkerhet og effektivitet som varkrever COC-Protokollen. Store mengder detaljerte data eksisterer allerede for hver av protokollmedisinene, oppnådd fra mange års bruk i den generelle befolkningen – og dette bidro til å gi oss en avgjørende start under utviklingen.
Vi har omhyggelig søkt gjennom flere tiår med publiserte data om hver av deecoc-Protokollmedisinene, og undersøkt hvordan de fungerer i ulike pasientpopulasjoner( inkludert pasienter med kreft), og på celle-og dyremodeller i laboratoriet. Disse dataene, sammen med vår egen kliniske erfaring, bidrar til å sikre at vi har en god forståelse av hvordan disse medisinene vil oppføre seg hos pasienter med ulike stadier og typer kreft, både i kombinasjon med hverandre og også i kombinasjon med en rekke andre kreftbehandlinger. Denne kunnskapen isparamount, og fra våre studier, denne typen bevis er bare ikke der ennå for mange andre off‑label anticancer narkotika kandidater – spesielt når gitt incombination.
ananti-metabolisk terapi som potensielt kan målrette mot kreft
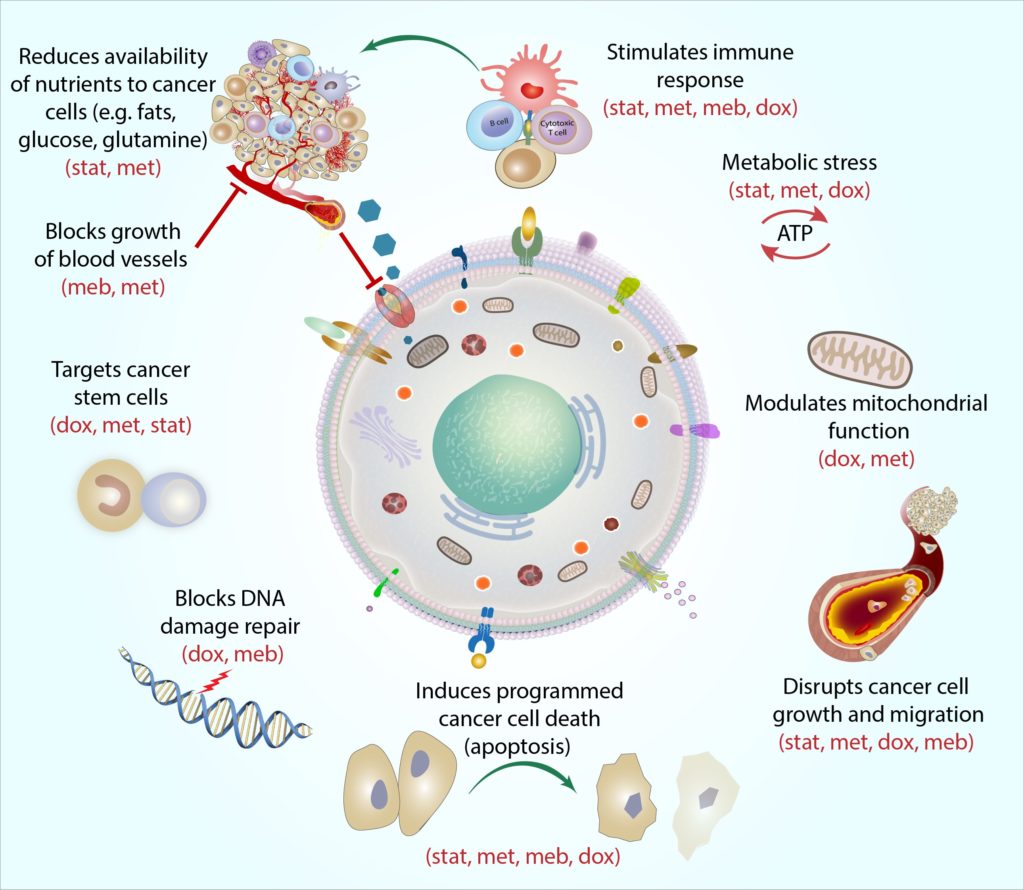
TheCOC-Protokollen er utformet for å fungere ved å begrense kreftcellers generelle evne til å ta opp og bruke (dvs.metabolisere) energi. Kreftceller trenger enorme mengder energi for å overleve, og de aller fleste kreftformer bruker en adaptiv prosess kalt aerob glykolyse for å generere den overdrevne energien de trenger (Kroemer andPouyssegur, 2008). Hver av medikamentene i protokollen kan målrette theulike molekylære metabolske prosesser som er involvert i og rundt aerobicglycolysis, og dette kan bidra til å senke den totale metabolic rate av kreftcellen (Jang et al.,2013). Vi tror At Cocprotocolmedisinene kan fungere i kombinasjon for konsekvent å begrense energiforsyning og bruk, samtidig som kreftceller ikke tilpasser seg og bruker andre veier for å ta opp energi (Jagust et al.,2019). Som et resultat blir kreftceller stadig svakere og mindre i stand til å ta inn og bruke næringsstoffene (f. eks. slik som glukose og essensielleaminosyrer glutamin og arginin) de trenger fra sine omgivelser (Andrzejewskiet al., 2018; Liu et al., 2016).Dette gjør det vanskeligere for kreftceller å overleve, vokse og spre seg i kroppen. Gradvis blir de svekkede cellene (inkludert mer motstandsdyktige ogtidligere behandlingsresistente celler)mer utsatt for angrep fraandre celledrepende kreftbehandlinger som strålebehandling, kjemoterapi, hormonbehandling og målrettede terapier (Bradford andKhan, 2013; Chen et al., 2012; Lacerda et al., 2014; Lamb et al., 2015a; Pantziarka et al., 2014). Ved Å Målrette de tilpassede metabolske mekanismene som er felles for de fleste kreftformer (men ikke vanligvis friske celler), tror VI AT COC-Protokollen kan være effektiv og selektiv for nesten hvilken som helst kreft uavhengig av spesifikk type, stadium eller plassering av kreft. Publiserte epidemiologiske og laboratoriestudier i økende gradstøtte det potensielt brede spekteret av denne terapien (Chae et al.,2015, 2016; Iliopoulos et al., 2011; Lamb et al., 2015b; Pantziarka et al.,2014).
Mechanistic coherence in action-the power of combination
den sanne kraften i theCOC-Protokollen ligger i den spesifikke kombinasjonen av medisiner vi bruker. Vi utviklet protokollen ikke bare som et regime av fire individuelle behandlinger hver med anticanceraktivitet, men også for å fungere som en enkelt kombinert behandling – med potensial til å produsere kraftige synergistiske effekter (Mokhtari et al ., 2017).
Hver Medisinering i COC-Protokollen retter seg mot kreftcellemetabolismen på en tydelig og utfyllende måte, og vi har kalt denne handlingen ‘mekanistisk sammenheng’. Mekanistisk sammenheng beskriver hvordan hver medisin kan angripe kreftcellen fra en annen vinkel. For eksempel er kreftstamceller apartikulært motstandsdyktig type kreftcelle, og hver medisin retter seg mot disse cellene på en annen måte: metformin retter seg mot cellens batterier (kalt mitokondrier) ved å gjøre det svært vanskelig for mitokondrier å kjøre molekylærreaksjonene de trenger for å produsere energi, blokkerer doxycyklin celle-DNAmachinery som mitokondrier trenger å replikere og reparere (Skoda et al., 2019), statinscan endre kreftstamcellegenuttrykk, noe som gjør cellene mer følsomme overfor andre kreftbehandlinger (Kodach et al., 2011), andmebendazole kan avbryte mange molekylære prosesser involvert i celldivision for å blokkere kreftstamcellevekst (Hothi et al., 2012; Hou et al., 2015). VED å kombinere alle fire agenter sammen, KAN COC-Protokollen slå kreftstamceller (og andre kreftceller) over flere ‘svake flekker’, og som en en-to slag, dette gjør at cellene er mindre i stand til å unnslippe og gjenopprette. Labstudier begynner å markere effektiviteten av denne tilnærmingen ved Hjelp Av COCprotocol medisineringskombinasjoner. I en mekanistisk studie, kombinere statinog metformin sterkt redusert veksten av prostatakreftceller mer ennenten agent alene (Wang et al., 2017). Observasjonsstudier har også rapportert potensielt synergistiske effekter av disse medisinene mot ulike kreftformer (Babcook etal., 2014; Danzig et al., 2015; Lehman et al., 2012; Nimako et al., 2017). Aklinisk studie som undersøker metformin og doxycyklin i brystkreft er nåunderway (NCT02874430), og vårt eget forskningsprogram, METRICS, begynner nå å produsere lovende data.
en langsiktig tilleggsbehandling
Ecoc-Protokollen er primært utviklet for å være en langsiktig tilleggsbehandling, for å optimalisere standardbehandlinger. Da metabolsk behandling med COCProtocol er ment å vare lenge, kan pasienter imidlertid også ta protokollen som et vedlikeholdsregime etter at standardbehandling er fullført eller under pausinger fra standardbehandling og som en del av en langsiktig strategi for å redusere risiko for tilbakefall eller metastaser. Av denne grunn er det også verdt å merke seg athver AV COC-Protokollmedisinene har også rapportert gunstige mekanismer for handling i kreft som ikke er avhengig av samtidig administrering av standardterapier, og som uavhengig kan bidra til å redusere risikoen for tilbakefall ogmetastatisk spredning.
Care Oncology model
Aktivt medisinsk tilsyn av hver pasient
Selv Om COCProtocol-medisinene har blitt brukt trygt i den generelle befolkningen i mangeår, er hver pasient som kommer til oss unik. Dette er grunnen til at hver pasient som deltar På Care Oncology Clinic er plassert under direkte omsorg for klinikeremed spesialkunnskap om forskrivning AV COC-Protokollen medisiner ikontekst av kreft. Våre klinikere vurderer individuelt de potensielle fordelene og risikoen ved å ta COC-Protokollen med hver pasient. DE vil bare anbefale COC-Protokollen til pasienter når de tror det vil være trygt og gunstig å gjøre det. Hver COC-protokoll resept er skreddersydd til pasientens behov, og doser og regimer blir nøye gjennomgått og justert basert på hvordan pasienten utvikler seg.
det er derfor viktig at pasientene bare tar COC-Protokollen mens de overvåkes nøye på vår klinikk i løpet av behandlingen.
*********************************************************************************
Viktig Merknad
Formålet med denne artikkelen
Denne Artikkelen er en oversikt over noen av de vitenskapelige og medisinske publisertlitteratur om medisiner som utgjør den patenterte Omsorg Oncologyprotocol. Det er tatt vare på å velge relevante artikler som støtter off-label bruk av disse legemidlene i en klinisk setting for tilleggsbehandling av kreft. Denne artikkelen gir seg ikke ut for å være en omfattende gjennomgang av alle bevisene, og den fanger heller ikke opp alle de potensielle bivirkningene av slik behandling.
Denne Artikkelen er kun til informasjonsformål, og den utgjør IKKE medicaladvice. Legemidlene som er omtalt her, er kun tilgjengelig på resept og bør ikke tas uten konsultasjon med legen din eller annen profesjonell helsepersonell. Care Oncology leger vil diskutere egnetheten til disse legemidlene med deg og vil snakke med legen din eller onkolog for å diskutere deres egnethet for deg.
Du Må ikke stole på informasjonen i denne artikkelen som et alternativ til medisinskråd fra legen din eller annen profesjonell helsepersonell. Hvis du har noen spesifikke spørsmål om noen medisinsk sak bør du rådføre deg med lege eller annen profesjonell helsepersonell. Hvis du tror du kan lide fra enhver medisinsk tilstand bør du søke øyeblikkelig legehjelp. Du bør aldri utsette å søke lege, se bort fra lege, eller fortsette medisinsk behandling på grunn av informasjonen i denne artikkelen.
Copyright
opphavsretten i denne artikkelen eies Av Health Clinics LLC og dets lisensgivere.
Patent
Care Oncology(«COC») Protokollen er beskyttet Av Usa patent US9622982B2 og byulike flere internasjonale patenter.
*********************************************************************************
Agrawal,S., Vamadevan, P., Mazibuko, N., Bannister, R., Swery, R., Wilson, S., andEdwards, S. (2019). En Ny Metode For Etisk Og Effektiv Evidensgenerering For Off-Label Medisinering Bruk I Onkologi(En Case Studie I Glioblastom). Front.Pharmacol. 10.Ahern, T. P., Lash, T. L., Damkier, P., Christiansen, P. M., Og Cronin-Fenton, D. P. (2014). Statiner og brystkreft prognose: bevis og muligheter. Lancet Oncol. 15, e461-468.Aksoy, S., Sendur, M. A. N., Og Altundag, K. (2013).Demografiske og klinisk-patologiske egenskaper hos pasienter med invasivbrystkreft som får metformin. Med. Oncol. Northwood Lond. Engl. 30, 590.
Alarcon Martinez, T., Zeybek, N. D., Og Müü, S.(2018). Evaluering Av Cytotoksiske Og Autofagiske Effekter Av Atorvastatin onMCF-7 Brystkreftceller. Balk. Med. J. 35, 256-262.alimova, I. N., Liu, B., Fan, Z., Edgerton, S. M., Dillon, T., Lind, S. E., Og Thor, A. D. (2009). Metformin hemmer brystkreftcellevekst, kolonidannelse og induserer cellesyklusstans in vitro. CellCycle 8, 909-915.Andrzejewski, S., Siegel, P. M., Og St-Pierre, J.(2018). Metabolske Profiler Assosiert Med Metformin Effekt Ved Kreft. Front.Endokrinol. 9.I Tillegg til Dette, er Det også en del av Det som er kjent for å være en del av Det som er kjent for å være en del av Det som er kjent for å være en del av Det som er kjent for å være en del av Det som er kjent for å være en del av Det som er kjent for å være en del av Det som er kjent for Å være en del av Det som er kjent for å være en del av Det som er kjent for Å være en del av Det som er kjent for å være en del av Det som er kjent for å være en del av Det som er kjent for Å være en del av Det som er kjent for Å være en del av Det som er kjent for å være en del av Det som er kjent for Å være en del av Det som er kjent for Å være en del av Det som er kjent for Å være en del av Det. (2014). Synergistisk Simvastatin Og Metformin Kombinasjonkjemoterapi ved Metastatisk Kastreringsresistent Prostatakreft I Benvev. Mol.Kreft Ther. 13, 2288–2302.Bahrami, F., Morris, D. L. og Pourgholami, M. H.(2012). Tetracykliner: legemidler med stort terapeutisk potensial. Mini Rev. Med.Chem. 12, 44–52.Bao, B., Azmi, A. S., Ali, S., Zaiem, F., Og Sarkar,F. H. (2014). Metformin kan fungere som anti-kreft middel via målretting cancerstem celler: den potensielle biologiske betydningen av tumorassosiert mirna inbreast og bukspyttkjertelkreft. Anne. Transl. Med. 2.
Bjarnadottir, O. Velg En Annen kategori for å velge en annen kategori, og velg En Annen kategori. (2013). Målretting HMG-CoA reduktase med statiner i et vindu-of-opportunitybrystkreft studie. Brystkreft Res. Behandle. 138, 499–508.
Bjarnadottir, O., Kimbung, S., Johansson, I., Veerla,S., Jö, M., Bendahl, P.-O., Grabau, D., Hedenfalk, I., Og Borgquist, S.(2015). Globale Transkripsjonelle Endringer Etter Statinbehandling I Brystkreft. Clin. Kreft Res. Av. J. Am. Assoc. Kreft Res. 21, 3402-3411.
Bonanni, B., Puntoni, M., Cazzaniga, M. I tillegg er det et stort utvalg av de mest brukte produktene. (2012). Dobbel effekt av metformin på brystkreftspredning i en randomisert presurgisk studie. J. Clin. Oncol. Ut. J. Am.Soc. Clin. Oncol. 30, 2593–2600.Bradford, S. A. Og Khan, A. (2013). Individualiseringkjemoterapi ved Bruk Av Antidiabetisk Legemiddel, Metformin, Som En ④adjuvantã ¢ â € â ○: Undersøkelsesstudie. J. Kreft Sci. Ther. 5.
Brewer, T. M., Masuda, H., Liu, D. D., Shen, Y., Liu, P., Iwamoto, T., Kai, K., Barnett, C. M., Woodward, W. A., Reuben, J. M., et al.(2013). Statin bruk i primær inflammatorisk brystkreft: en kohortstudie. Br.J. Kreft 109, 318-324.Camacho, L., Dasgupta, A., Og Jiralerspong, S. (2015). Metformin i brystkreft – et utviklende mysterium. Brystkreft Res. BCR 17, 88.I Tillegg til Dette har De også en rekke andre former for økonomisk vekst. (2006). Brystkreft vekst forebygging av statiner. Kreft Res. 66,8707-8714.
Cazzaniga, M., DeCensi, A., Pruneri, G., Puntoni,M., Bottiglieri, L., Varricchio, C., Guerrieri-Gonzaga, A., G., G., G., G., G., G., G., Et al. (2013). Effekten av metformin på apoptosei en brystkreft presurgical studie. Br. J. Kreft 109, 2792-2797.Chae, Yk, Valsecchi, Me, Kim, J., Bianchi, Al, Khemasuwan, D., Desai, A., Og Tester, W. (2011). Redusert Risiko For Brystkreft Hos Pasienter Som Bruker ACE-Hemmere, Arb og/eller Statiner. Kreftinvest. 29, 585–593.
Chae, Yk, Yousaf, M., Malecek, M.-K., Carneiro,B., Chandra, S., Kaplan, J., Kalyan, A., Sassano, A., Platanias, L. C.,Og Giles, F. (2015). Statiner som anti-kreft terapi; Kan vi oversette prekliniske ogepidemiologiske data til klinisk nytte? Discov. Med. 20, 413–427.A., A., A., A., A., A., A., A., A., A., A., A.,A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., Et al. (2016). Repurposing metformin for kreftbehandling: nåværende kliniske studier. Oncotarget 7, 40767-40780.Chen, J., Lan, T., Hou, J., Zhang, J., An, Y., Tie, L., Pan, Y., Liu, J. og Li, X. (2012). Atorvastatin sensibiliserer humannon – småcellet lungekarsinom til karboplatin via suppresjon AV akt-aktivering og oppregulering AV TIMP-1. Int. J. Biochem. Celle Biol. 44, 759–769.Chen, L., Chubak, J., Boudreau, D. M., Barlow, W. E., Weiss, N. S., Og Li, C. I. (2017). Diabetes Behandlinger og Risiko For AdverseBreast Cancer Utfall blant Tidlig Stadium Brystkreft Pasienter: En Seer-Medicareanalyse. Kreft Res. 77, 6033-6041.Chen, T., Liang, Y., Feng, D., Tao, L., Qi, K., Zhang, H., Wang, H., Lin, Q. og Kong, H. (2013). Metformin hemmer proliferasjon og fremmer apoptose AV HER2 positive brystkreftceller ved nedreguleringhsp90. J. BUON Av. J. Balk. Union Oncol. 18, 51–56.
Coyne, C., Jones, T., Og Bear, R. (2014).Antineoplastisk Cytotoksisitet Av Gemcitabin – (C4-amid)- inDual-kombinasjon Med Epirubicin-(C3-amid) – motkjemoterapeutisk Resistent Brystadenokarsinom (SKBr-3) ogkomplementær Effekt Av Mebendazol. J. Kreft Res. Ther. Oncol. 2.Coyne, C. P., Jones, T. og Bear, R. (2012). Influenceav Alternative Tubulinhemmere På Styrken av aEpirubicin-Immunokjemoterapeutisk Syntetisert Med Et Ultra VioletLight-Aktivert Mellomprodukt. Kreft Clin. Oncol. 1, 49–80.
Coyne, C. P., Jones, T., Og Bear, R. (2013).Gemcitabine-(C4-amide)- Anti-Neoplastic Cytotoxicity in DualCombination with Mebendazole against Chemotherapeutic-Resistant MammaryAdenocarcinoma. J. Clin. Exp. Oncol. 2.
Cufi, S., Corominas-Faja, B., Vazquez-Martin, A.,Oliveras-Ferraros, C., Dorca, J., Bosch-Barrera, J., Martin-Castillo, B., andMenendez, J.A. (2012). Metformin-induced preferential killing of breast cancerinitiating CD44+CD24-/low cells is sufficient to overcome primary resistance totrastuzumab in HER2+ human breast cancer xenografts. Oncotarget 3, 395–398.
Danzig, M.R., Kotamarti, S., Ghandour, R.A., Rothberg, M. B., Dubow, B. P., Benson, M. C., Badani, K. K., Og McKiernan ,J. M. (2015).Synergisme mellom metformin og statiner ved å modifisere risikoen for biokjemisk tilbakekomst etter radikal prostatektomi hos menn med diabetes. ProstateCancer Prostatic Dis. 18, 63–68.Davies, G., Lobanova, L., Dawicki, W., Groot,G., Gordon, Jr, Bowen, M., Harkness, T. og Arnason, T. (2017). Metforminhemmer utviklingen, og fremmer resensibilisering, avbehandlingsresistent brystkreft. PLoS ONE 12.
De Witt, M., Gamble, A., Hanson, D., Markowitz,D., Powell, C., Al Dimassi, S., Atlas, M., Boockvar, J., Ruggieri, R., Og Symons, M. (2017). Repurposing Mebendazol Som Erstatning For Vincristin forbehandling Av Hjernesvulster. Mol. Med. 23, 50–56.S., G., G., G., G., G.,G., G., G., G., G., G., G., G., G.,G., G., G., G., G., G., G., G., G., G., G., G., G., G., G., G., G., G., G., G., G., G., G., G., G., G., G., G., G., G., G., G., G., G., G., G., G., G., G., Et al. (2014). Differensielle effekter av metforminon brystkreftproliferasjon i henhold til markører for insulinresistens og tumorsubtype i en randomisert presurgisk studie. Brystkreft Res. Behandle. 148,81–90.
DeCensi, A., Puntoni, M., Guerrieri-Gonzaga, A.Serrano, M., Serrano, D., Lazzeroni, M., Vingiani, A., Gentilini, O., Petrera, M., Viale, G., et al. (2015). Effekt Av Metformin På Brystkanalkarsinom In Situ Proliferasjon i En Randomisert Presurgisk Studie. Kreft Forrige.Res. Phila. Pa 8, 888-894.
Deng, X.-S., Wang, S., Deng, A., Liu, B.,Edgerton, S. M., Lind, S. E., Wahdan-Alaswad, R. ,Og Thor, A. D. (2012). Metformin targetsStat3 for å hemme cellevekst og indusere apoptose i trippelnegative brystkreftmidler. Celle Syklus Georget. Tex 11, 367-376.
Dowling, R. J., Parulekar, W. R., Gelmon, K. A., Shepherd, L. E., Virk, S., Ennis, M., Mao, F., Ligibel, J. A., Hershman, D. L.,Rastogi, P., et al. (2018). CA15-3 / MUC1 I CCTG MA-32 (NCT01101438): en faseiii RCT av effekten av metformin vs. placebo på invasiv sykdomsfri ogoverall overlevelse i tidlig stadium brystkreft (BC). J. Clin. Oncol.
Duivenvoorden, W. C. M., Popović, S. V., Lhotá, S., Seidlitz, E., Hirte, H. W., Tozer, R. G., Og Singh, G. (2002). Doksycyklin reduserer tumorburden i en benmetastasemodell av human brystkreft. Kreft Res. 62,1588–1591.El-Benhawy, S. A. og El-Sheredy, H. G. (2014).Metformin og overlevelse hos diabetespasienter med brystkreft. J. Egypt.Public Health Assoc. 89, 148–153.
Feldt, M., Bjarnadottir, O., Kimbung, S., Jirströ, K., Bendahl, P.-O., Veerla, S., Grabau, D., Hedenfalk, I., Og Borgquist, S.(2015). Statininduserte antiproliferative effekter via cyclin D1 og p27 i awindow-of-opportunity brystkreft studie. J. Transl. Med. 13, 133.Fife, R. S. Og Sledge, G. W. (1995). Effekter av doksycyklin på in vitro vekst, migrasjon og gelatinaseaktivitet av brystkarsinomceller. J. Lab. Clin. Med. 125, 407–411.
Fife, R. S. Og Sledge, G. W. (1998). Effekter av doksycyklin på kreftceller in vitro og in vivo. Adv. Dent. Res. 12, 94-96.
Fiorillo, M., Tó, F., Sotgia, F. og Lisanti, M. P.(2019). Doxycyklin, Azitromycin og vitamin c (DAV): en potent kombinasjonsterapi for å målrette mitokondrier og utrydde kreftstamceller (CSCs).Aldring 11, 2202-2216.Foroodi, F., Duivenvoorden, W. C., Og Singh, G.(2009). Interaksjoner av doxycyklin med kjemoterapeutiske midler i menneskebryst adenokarsinom mda-MB-231 celler. Kreft. Narkotika 20, 115-122.
Garwood, E. R., Kumar, A. S., Baehner, F. L. I tillegg er det et stort antall av dem. (2010). Fluvastatin reduserer proliferasjon og økerapoptose hos kvinner med høy gradbrystkreft. Brystkreft Res. Behandle. 119, 137–144.Giles, Ed, Jindal, S., Wellberg, E. A., Schedin, T., Anderson, Smart, Thor, AD, Edwards, Dp, MacLean, PS, Og Schedin,P. (2018). Metformin hemmer stromal aromataseuttrykk og tumorprogresjoni en gnagermodell av postmenopausal brystkreft. Brystkreft Res. BCR 20.
Goodwin, P. J., Parulekar, W. R., Gelmon, K. A.,Shepherd, L. E. I. a., hershman, D. L., Rastogi, P., Mayer, I. A., Hobday, T. J., Lemieux, J., Et al. (2015). Effekt av metformin vs placebo på ogmetabolske faktorer I NCIC CTG MA.32. J. Natl. Kreft Ist. 107.
Hadad, S., Iwamoto, T., Jordan, L., Purdie, C., Bray,S., Baker, L., Jellema, G., Deharo, S., Hardie, D. G., Pusztai, L., Et al.(2011). Bevis for biologiske effekter av metformin i operabel brystkreft: en preoperativ, vindu-av-mulighet, randomisert studie. Brystkreft Res. Behandle. 128, 783–794.Hadad, S. M., Hardie, D. G., Appleyard, V., ogthompson, A. M. (2014). Effekter av metformin på brystkreftcellespredning, AMPK-banen og cellesyklusen. Clin. Transl. Oncol. Ut.Publ. Fed. Spenne. Oncol. Soc. Natl. Kreft Ist. Mex. 16, 746–752.
Hatoum, D., Og McGowan, E. M. (2015). Ved bruk av metformin: kan behandling av diabetes forebygge brystkreft? Biomedrene. Int. 2015, 548436.Hirsch, H. A., Iliopoulos, D., Tsichlis, P. N., andStruhl ,K. (2009). Metformin Målretter Selektivt Kreftstamceller, Og Virkersammen med Kjemoterapi For Å Blokkere Tumorvekst og Forlenge Remisjon. Kreft. 69, 7507–7511.
Hothi, P. I 2012 ble Det opprettet en egen organisasjon. Høy Gjennomstrømning Kjemiskskjermer Identifiserer Disulfiram som En Hemmer Av Humane Glioblastom Stamceller.Oncotarget 3, 1124-1136.
Hou, Z.-J., Luo, X., Zhang, W., Peng, F., Cui, B.,Wu, S.-J., Zheng, F.-M., Xu, J., Xu, L.-Z., Long, Z.-J., Et al. (2015).Flubendazole, FDA-godkjent anthelmintic, mål brystkreft stamlignende celler.Oncotarget 6, 6326-6340.Iliopoulos, D., Hirsch, H. A., Og Struhl, K. (2011).Metformin reduserer dosen av kjemoterapi for å forlenge tumor remisjon inmouse xenografts involverer flere kreftcelletyper. Kreft Res. 71,3196-3201.
Jacob, L., Kostev, K., Rathmann, W., Og Kalder, M.(2016). Effekt av metformin på metastaser hos pasienter med brystkreft ogtype 2 diabetes. J. Diabetes Komplikasjoner 30, 1056-1059.
Jagust, P., De Luxá-Delgado, B., Parejo-Alonso, B., Og Sancho, P. (2019). Metabolismebaserte Terapeutiske Strategier Rettet Mot Kreftstamme Celler. Front. Pharmacol. 10.
Jang, M., Kim, Ss, Og Lee, J. (2013). Kreftcellemetabolisme: implikasjoner for terapeutiske mål. Exp. Mol. Med. 45, e45.Jiralerspong, S., Palla, S. L., Giordano, S. H., Meric-Bernstam, F., Liedtke, C., Barnett, C. M., Hsu, L., Hung,M.-C., Hortobagyi, G. N., Og Gonzalez-Angulo, A. M. (2009). Metformin Og Patologiskfullstendig Respons På Neoadjuvant Kjemoterapi hos Diabetespasienter med Brystkreft. J. Clin. Oncol. 27, 3297–3302.
Kalinsky, K., Crew, K. D., Refice, S., Xiao, T.,Wang, A., Feldman, S. M., Taback, B., Ahmad, A., Cremers, S., Hibshoosh, H., Et al.(2014). Presurgical studie av metformin hos overvektige og overvektige pasienter medny diagnostisert brystkreft. Kreft Investere. 32, 150–157.Kanugula, A. K., Gollavilli, P. N., Vasamsetti, S. B.,Karnewar, S., Gopoju, R., Ummanni, R., Og Kotamraju, S. (2014). Statin-indusertinhibering av spredning av brystkreft og invasjon innebærer demping avjerntransport: intermediacy av nitrogenoksid og antioksidant forsvarmekanismer. FEBS J. 281, 3719-3738.
Kim, H. J., Kwon, H., Lee, J. W., Kim, H. J., Lee, S. B.,Park, H. S., Sohn, G., Lee, Y., Koh, B. S., Yu, J. H., et al. (2015). Metformin øker overlevelsen i hormonreseptor-positiv, HER2-positiv brystkreftpasienter med diabetes. Brystkreft Res. BCR 17, 64.
Kim, J., Lim, W., Kim, E.-K., Kim, M.-K., Paik,N.-S., Jeong, S.-S., Yoon, J.-H., Park, C. H., Ahn, S. H., Kim, L. S., Et al. (2014).Fase II randomisert studie av neoadjuvant metformin pluss letrozol versus placeboplus letrozol for østrogenreseptor positiv postmenopausal brystkreft (METEOR). BMC Kreft 14, 170.
Kodach, L. L., Jacobs, R. J., Voorneveld, P. W., Wildenberg, M. E., Verspaget, h. W., van Wezel, T., Morreau, H., Hommes, D. W.I. p., van Den Brink, G. R., et al. (2011). Statiner forsterker kjemosensitiviteten til kolorektale kreftceller som induserer epigenetisk omprogrammering og reduserer kolorektal kreftcelle «stemness» via benmorfogenetiskproteinveien. Gut 60, 1544-1553.Kozar, K., Kaminski, R., Legat, M., Kopec, M., Nowis,D., Skierski, J., Koronkiewicz, M., Jakó, M. og Golab, J. (2004).Cerivastatin viser økt antitumoraktivitet mot humane brystkreftcellelinjer når det brukes i kombinasjon med doksorubicin eller cisplatin. Int.J. Oncol.
Kroemer, G., Og Pouyssegur, J. (2008). Tumorcellemetabolisme: Kreftens Akilleshæl. Kreftcelle 13, 472-482.Kwan, M. L., Habel, L. A., Flick, E. D., Quesenberry, C. P., Og Caan ,b. (2008). Post-diagnose statin bruk og brystkreftforekomst i en prospektiv kohortstudie av tidlig stadium brystkreftovervivorer. Brystkreft Res. Behandle. 109, 573–579.
Lacerda, L., Reddy, J. P., Liu, D., Larson, R., Li, L., Masuda, H., Brewer, T., Debeb, B. G., Xu, W., Hortobá, G. N., Et al. (2014).Simvastatin radiosensibiliserer differensierte og stamlignende brystkreftcellelinjer og er forbundet med forbedret lokal kontroll hos inflammatoriske brystkreftpasienter behandlet med postmastektomistråling. Stamceller Transl. Med.3, 849–856.
Lamb, R., Fiorillo, M., Chadwick, A., Ozsvari,B., Reeves, K. J., Smith, D. L., Clarke, R. B., Howell, S. J., Cappello,A. R., Martinez-Outschoorn, U. e., Et al. (2015a). Doksycyklin nedregulerer DNA-Pkog radiosensitizes tumor initierende celler: Implikasjoner for mer effectiveradiation terapi. Oncotarget 6, 14005-14025.
Lam, R., Ozsvari, B., Lisanti, C. L., Tanowitz, H. B., Howell, A., Martinez-Outschoorn, U. E., Sotgia, F. ,Og Lisanti, M. P. (2015b).Antibiotika som retter seg mot mitokondrier effektivt utrydde kreftstamceller, på tvers av flere tumortyper: Behandling av kreft som en smittsom sykdom.Oncotarget 6, 4569-4584.Lehman, D. M., Lorenzo, C., Hernandez, J.,Og Wang, C. (2012). Statin Bruk Som Moderator Av Metformin Effekt På Risiko For ProstateCancer Blant Type 2 Diabetespasienter. Diabetes Care 35, 1002-1007.Lin, C., Lo, M., Moody, R., Stevers, N., Tinsley, S. og Sun, D. (2018). Doxycyklin mål aldehyd dehydrogenase-positiv brystkreftstamme celler. Oncol. Liu, B., Yi, Z., Guan, X., Zeng, Y.-X., Og Ma, F.(2017). Forholdet mellom statiner og brystkreft prognose varierer bystatin type og eksponeringstid: en meta-analyse. Brystkreft Res. Behandle. 164,1–11.Liu, H., Scholz, C., Zang, C., Schefe, J. H., Habbel, P., Regierer, A.-C., Schulz, C.-O., Possinger, K. og Eucker, J. (2012).Metformin og mtor-hemmeren everolimus (RAD001) sensibiliserer brystkreftceller for den cytotoksiske effekten av kjemoterapeutiske legemidler in vitro. AnticancerRes. 32, 1627–1637.Liu, X., Romero, I. L., Litchfield, L. M., Lengyel, E., Og Locasale, J. W. (2016). Metformin retter seg mot sentral karbonmetabolisme ogavslører mitokondrielle krav i humane kreftformer. Celle Metab. 24, 728–739.
A., J., Guo, Y., Chen, S., Zhong, C., Xue, Y.,Zhang, Y., Lai, X., Wei, Y., Yu, S., Zhang, J., Et al. (2014). Metformin forsterkertamoksifen-mediert tumorveksthemming ved er-positivt brystkarsinom. BMCCancer 14, 172.Manthravadi, S., Shrestha, A., Og Madhusudhana, S.(2016). Effekt av statinbruk på tilbakefall av kreft og dødelighet ved brystkreft: en systematisk oversikt og meta-analyse. Int. J. Kreft 139, 1281-1288.
Mark, M., Klingbiel, D., Mey, U., Winterhalder,R., Rothermundt, C., gillessen, s., von Moos, R., Pollak, M., Manetsch, G., Strebel, R., et al. (2019). Effekt Av Tillegg Av Metformin til Abirateron inmetastatisk Kastreringsresistent Prostatakreft Pasienter Med Sykdomsprogresjon Under Behandling Med Abirateron (MetAb-Pro): Fase 2 Pilotstudie. Clin. Genitourin. Kreft 17, e323-e328.
Martin-Castillo, B., Pernas, S., Dorca, J., A. s., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. s., a. s., a. s., a. s., a. s., a. s., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S. (2018). En fase 2-studie avneoadjuvant metformin i kombinasjon med trastuzumab og kjemoterapi hos kvinner med tidlig HER2-positiv brystkreft: METTEN-studien. Oncotarget 9.35687-35704.Mokhtari, R. B., Homayouni, T. S., Baluch,N., Morgatskaya, E., Kumar, S., Das, B., Og Yeger, H. (2017). Kombinasjonsterapi bekjemper kreft. Oncotarget 8, 38022-38043.Mü, Ao, Seeger, H. og Wallwiener, D. (2004).Hemmende effekt av statiner på spredning av human brystkreft cells.Int-J. Clin. Pharmacol. Ther. 42, 695–700.Mukhopadhyay, T., Sasaki, J., Ramesh, R.,Og Roth, J. A. (2002). Mebendazol Gir En Potent Antitumoreffekt på Humane Kreftcellelinjer både In Vitro og in Vivo. Clin. Kreft Res. 8, 2963-2969.Murtola, T. J., Visvanathan, K., Artama, M., Vainio, H. og Pukkala, E. (2014). Statin bruk og brystkreft overlevelse: en nationwidecohort studie Fra Finland. PloS One 9, e110231.
Nanni, O., Amadori, D., De Censi, A., Rocca ,A., Freschi, A., Bologna, A. I., c., C., C., C., C., C., C., C., C., C., Et al. (2019). Metformin pluss kjemoterapi versus kjemoterapi alene iførstelinjebehandling AV HER2-negativ metastatisk brystkreft. Den Mymerandomiserte, fase 2 kliniske studien. Brystkreft Res. Behandle. 174, 433–442.Nimako, Gk, Wintrob, Zap, Sulik, Da,Donato, Jl, Og Ceacareanu, Ac (2017). Synergistisk Nytte Av Statin Og Metforminin Gastrointestinale Maligniteter. J. Pharm. Pract. 30, 185–194.
Niraula, S., Dowling, R. J. O., Ennis, M., Chang, M. C., Done, S. J., Hood, N., Escallon, J., Leong, W. L., McCready, D. R., Reedijk,M., et al. (2012). Metformin i tidlig brystkreft: en prospektiv vindu ofopportunity neoadjuvant studie. Brystkreft Res. Behandle. 135, 821–830.
Nygren, P., Og Larsson, R. (2014). Drug repositioningfra benk til sengen: Tumor remisjon av antihelmintic narkotika mebendazolein ildfast metastatisk tykktarmskreft. Acta Oncol. 53, 427–428.Orecchioni, S., Reggiani, F., Talarico,G., Mancuso, P., Calleri, A., Gregato, G., Labanca, V., Noonan, D. M., Dallaglio, K.,Albini, A., Et al. (2015). Biguanidene metformin og phenformin inhibitangiogenese, lokal og metastatisk vekst av brystkreft ved å målrette både neoplastiske og mikromiljøceller. Int. J. Kreft 136, E534-544.Ozsvari, B., Sotgia, F. og Lisanti, M. P. (2017). Anew mutation-uavhengig tilnærming til kreftbehandling: Inhibering av onkogen RAS ogmyc, ved å målrette mitokondriell biogenese. Aldring 9, 2098-2116.Pantziarka, P., Bouche, G., Meheus, L., Sukhatme, V., Og Sukhatme, V. P. (2014). Repurposing Narkotika I Onkologi—ReDO)-mebendazole asan anti-kreft agent. Ecancermedicalscience 8.
Peiris-Sideè, M., Sotgia, F. og Lisanti, M. P. (2015). Doxycyklin og terapeutisk målretting AV DNA – skaderesponsen ikreftceller: gammelt stoff, nytt formål. Oncoscience 2, 696-699.Rahmani, J., Manzari, N., Thompson, J., Gudi, Sk, Chhabra, M., Naik, G., Mousavi, S. M., Varkaneh, H. K., Clark, C., Og Zhang, Y.(2019). Effekten av metformin på biomarkører assosiert med brystkreftutfall: en systematisk gjennomgang, meta-analyse og dose-respons av randomisertkliniske studier. Clin. Transl. Oncol.
Scatena, C., Roncella, M., Di Paolo, A., Aretini,P., Menicagli, M. I tillegg til dette, er det også en del av det som er viktig for oss. (2018). Doxycyklin,En Inhibitor Av Mitokondriell Biogenese, Reduserer Effektivt Kreftstamceller (CSCs) Hos Tidlige Brystkreftpasienter: Aklinisk Pilotstudie. Front. Oncol. 8.Seeger, H., Wallwiener, D. Og Mueck, A. O. (2003).Statiner kan hemme proliferasjon av humane brystkreftceller in vitro. Exp.Clin. Endokrinol. Diabetes Av. J. Ger. Soc. Endokrinol. Ger. Diabetes Assoc.111, 47–48.Skoda, J., Borankova, K., Jansson, P. J., Huang, M. L.-H., Veselska, R., Og Richardson, D. R. (2019). Farmakologisk målrettingav mitokondrier i kreftstamceller: en gammel organell ved krysset avroman anti-kreft terapi. Pharmacol. Res. 139, 298-313.Sonnenblick, A., Agbor-Tarh, D., Bradbury, I., DiCosimo, S., Azim, H. A., Fumagalli, D., Sarp, S., Wolff, A. C.,Andersson, M., Kroep, J., Et al. (2017). Effekt Av Bruk Av Diabetes, Insulin og Metformin påutfall Av Pasienter Med Human Epidermal Vekstfaktorreseptor 2-Positivprimær Brystkreft: Analyse Fra ALTTO Fase III Randomisert Studie. J. Clin. Oncol. 35, 1421–1429.
Van Wyhe, R. D., Rahal, O. M., Og Woodward, W. A. (2017). Effekt av statiner på brystkreft tilbakefall og dødelighet: en gjennomgang.Brystkreft Mål Ther. 9, 559–565.
Vazquez-Martin, A., Oliveras-Ferraros, C., Cufí, S., Del Barco, S., Martin-Castillo, B., Lopez-Bonet, E. ,Og Menendez, J. A. (2011).Det antidiabetiske legemidlet metformin undertrykker metastaseassosiert proteinCD24 i mda-MB-468 trippelnegative brystkreftceller. Oncol. Rep. 25,135–140.Vintonenko, N., Jais, J.-P., Kassis, N.,Abdelkarim, M., Perret, G.-Y., Lecouvey, M., Crepin, M., Og Di Benedetto, M. (2012).Transkriptomanalyse og in vivo-aktivitet av fluvastatin versus zoledronsyre i en murin metastasemodell for brystkreft. Mol. Pharmacol. 82, 521–528.Wahdan-Alaswad, R. S., Cochrane, D. R., Spoelstra,N. S., Howe, E. N., Edgerton, S. M., Anderson, S. M., Thor, A. D., Og Richer, J. K. (2014). Metformin-indusert drap av triple-negative brystkreftceller ermediert ved reduksjon av fettsyresyntase via miRNA-193b. Horm. Kreft 5,374-389.
Wang, Z.-S., Huang, H.-R., Zhang, L.-Y., Kim, S.,He, Y., Li, D.-L., Farischon, C., Zhang, K., Zheng, X., Du, Z.-Y., Et al. (2017).Mekanistisk Studie av Inhibitoriske Effekter Av Metformin og atorvastatin inkombinasjon på Prostatakreftceller in Vitro og in Vivo. Biol. Pharm. Bull.40, 1247–1254.I Tillegg til Å være en del av en rekke av disse, er Det også en del av En rekke av Disse. (2015). Simvastatin forhindrer trippelnegativ brystkreftmetastase i prekliniske modeller gjennom regulering Av FOXO3a. Behandle. 154, 495–508.xu, H., Chen, K., Jia, X., Tian, Y., Dai, Y., Li, D., Xie, J., Tao, M. og Mao, Y. (2015). Metforminbruk Er Assosiert Med Bedreoverlevelse Av Brystkreftpasienter Med Diabetes: En Meta-Analyse. TheOncologist 20, 1236-1244.Yam, C., Esteva, F. J., Patel, M. M., Raghavendra,A. S., Ueno, N. T., Moulder, S. L., Hess, K. R., Shroff, G. S., Hodge, S.,Koenig, K. H., Et al. (2019). Effekt og sikkerhet av kombinasjonen av metformin, everolimus og eksemestan hos overvektige og obese postmenopausale pasienter med metastatisk,hormonreseptor-positiv, HER2-negativ brystkreft: en fase II-studie.Investere. Nye Stoffer 37, 345-351.
Yao, H., Han, G., Yan, S., Chen, C., Song, L., Rosol, T.J., Og Deng, X. (2017). Trippel-negativ brystkreft: er det en behandlingpå horisonten? Oncotarget 8, 1913-1924.
Zhang, L., Guo, M., Li, J., Zheng, Y., Zhang, S., Xie, T., Og Liu, B. (2015). Systembiologibasert oppdagelse av en potensiell atg4bagonist (Flubendazol) som induserer autofagi ved brystkreft. Mol. Biosyst.11, 2860–2866.
Zhang, L., Xu, L., Zhang, F., Og Vlashi, E. (2017).Doxycyklin hemmer kreftstamcellefenotypen ogepitelial-til-mesenkymal overgang i brystkreft. Celle Syklus Georget. Tex16, 737-745.
Zhang, L., Bochkur Dratver, M. I tillegg til dette er det også en rekke andre former for fysisk aktivitet. (2019a). Mebendazol Forsterker Strålebehandling I Trippel-Negativbrystkreft. Int. J. Radiat. Oncol. Biol. Phys. 103, 195–207.Zhang, Y., Storr, Sj, Johnson, K., Green, A. R.,Rakha, E. A., Ellis, I. O., Morgan, D. A. l. og Martin, S. G. (2014). Involvering av metformin og AMPK i radioresponse og prognose av luminal versusbasal-lignende brystkreft behandlet med strålebehandling. Oncotarget 5, 12936-12949.
Zhang, Z.-J., Yuan, J., Bi, Y., Wang, C., Og Liu, Y.(2019b). Effekten av metformin på biomarkører og overlevende for brystkreft-en systematisk oversikt og meta-analyse av randomiserte kliniske studier. Pharmacol.Res. 141, 551-555.
Zhong, S., Zhang, X., Chen, L., Ma, T., Tang, j., andZhao ,J. (2015). Statinbruk og dødelighet hos kreftpasienter: Systematisk oversikt og meta-analyse av observasjonsstudier. Kreft Behandling. Åp 41, 554-567.
