A coc protokoll az emlőrákban
Ez a dokumentum összefoglalja az indoklást és a jelenlegi tudományos bizonyítékok egy részét, amelyek alátámasztják a COC protokoll gyógyszerek alkalmazását az emlőrák szokásos kezelési módjai mellett. Megértjük, hogy a rák nagyon személyes állapot, és minden betegnek egyedi kihívásai vannak. Személyes helyzetével kapcsolatos további információkért kérjük, vegye fel a kapcsolatot a Care Oncology Clinic telefonszámon 800-392-1353 az Egyesült Államokban, vagy látogasson el a https://careoncology.comweboldalra.
Ha még nem kezdte meg az onkológiai ellátást, kérjük, vegye figyelembe a következőket:
- nem kell utaznia. Az onkológusokból és onkológiai ápolókból álló csapatunkkal biztonságos videón keresztül találkozhat a folyamatos támogatás érdekében.
- A Care Oncology adjunct protocol gyógyszereket közvetlenül az Ön otthonába szállítjuk amerikai partner Gyógyszertárainkból, és az Ön szokásos ellátási kezelése mellett használhatók.
- Hihetetlenül büszkék vagyunk arra, hogy bejelenthetjük, hogy átmentünk a Validation Institute rendkívül szigorú érvényesítési folyamatán az adatok elemzésével, az eredménykövetelésekkel és az értékszámítással kapcsolatban. Keményen dolgoztunk, hogy idáig eljussunk. Korán felismertük azt a hatalmas értéket, amelyet a rákos betegeknek kínált, felelősségteljesen átadott gyógyszerprogram kínál, mégis, nem kínálták méretarányosan. Négy évvel ezelőtt elhatároztuk, hogy változtatunk ezen, tudva, hogy ez egy maraton, nem sprint.
A COC protokoll és a mellrák: kulcsfontosságú pontok
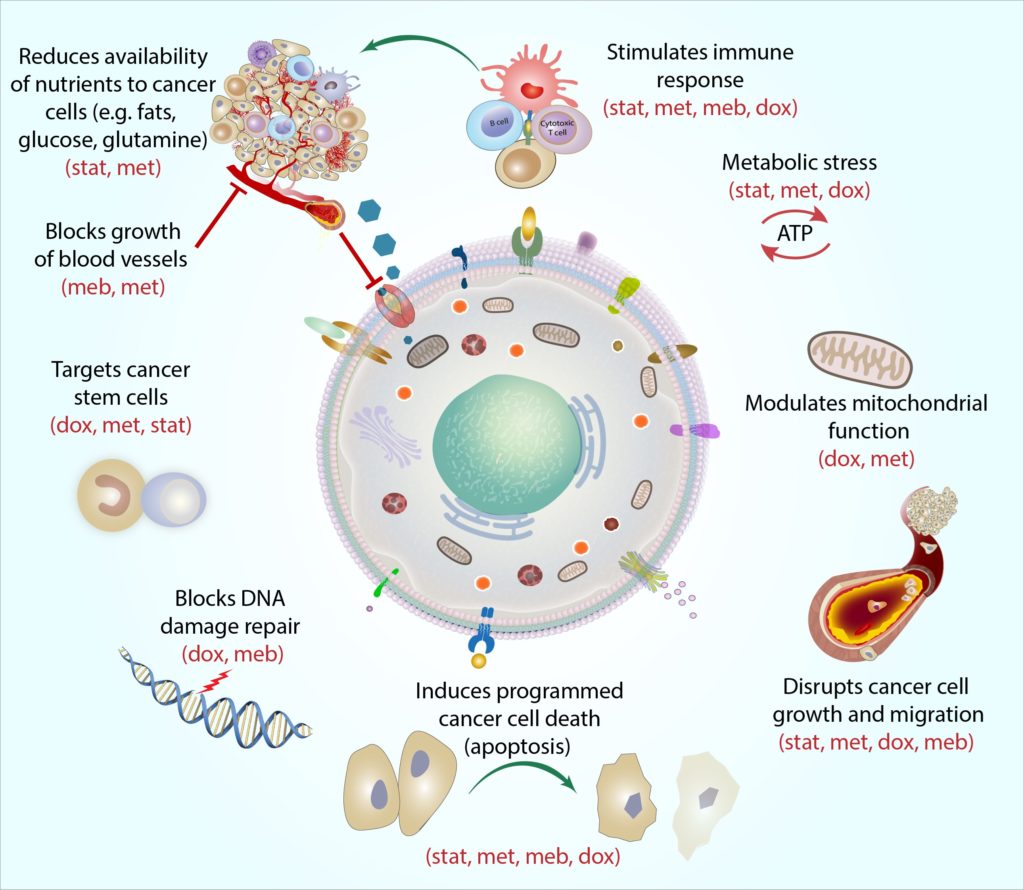
- A a cocprotocol négy általánosan felírt gyógyszer(atorvasztatin, metformin, mebendazol és doxiciklin) kombinációja, amelyek potenciálisan célozzák meg az emlőrákot, és segítenek javítani a standard rákellenes kezelések hatékonyságát.
- számos megfigyelési tanulmány összekapcsolta a metformin vagy a sztatin használatát az emlőrákos betegek jobb eredményeivel.
- laboratóriumi vizsgálatok emlőrákos sejtek nőtt ételek azt mutatják, hogy a metformin és a sztatinok közvetlenül megcélozni és károsítani emlőrákos sejtek – gyengíti őket, és makingthem sebezhetőbbé standard kezelések.
- a műthető emlőrákban szenvedő betegeken végzett kis ‘lehetőségek ablaka’ klinikai vizsgálatok eredményei általában azt mutatják, hogy a metformin vagy a sztatin műtét előtti alkalmazása potenciálisan pozitív változásokat eredményezhet a rák molekuláris markereiben, beleértve azokat is, amelyek szabályozzák az emlőrákos sejtek növekedését és osztódását. További vizsgálatok folyamatban vannak annak vizsgálata, hogy a metformin vagy a sztatinok befolyásolhatják-e a betegség válaszát.
- a doxiciklin képes blokkolni mind a HER2 pozitív, mind a tripla negatív emlőrákos őssejtek növekedését, amelyeket laboratóriumi edényekben inkubáltak, és segített javítani a standard kemoterápiás paklitaxel által kiváltott rezisztenciával kapcsolatos változásokat.
- Doxycyclinemcsak elérte a korai klinikai vizsgálatokat emlőrákos betegeknél. Az első kis vizsgálat eredményei azt mutatják, hogy a korai stádiumú emlőrákban szenvedő betegek, akik csak 14 napig szedték a doxiciklint a műtét előtt, átlagosan 40% – kal csökkentették a rákos őssejtek jelenlétének molekuláris markereit. A kezelt betegek egy kivételével mindegyikre kedvező hatást figyeltek meg (8/9).
- a mebendazolekán lelassíthatja a laboratóriumban termesztett emlőrákos sejtek növekedését és osztódását,beleértve a kemoterápiával szemben ellenállóbb emlőrákos sejteket is. Több emberi tanulmányokra van szükség.
A COC protokoll és a mellrák: Közzétett bizonyítékok
a COC protokoll négy általánosan felírt gyógyszer kombinációs rendszere, amelyek mindegyike bizonyítja a metabolikusan alapuló rákellenes aktivitást és a jól megértett biztonságossági profilokat. Ezek a gyógyszerek a következők: metformin, atorvasztatin, doxiciklin és mebendazol. Néhány olyan tanulmány, amely támogatja a theCOC protokoll kiegészítő terápiaként történő alkalmazását a mellrák jelenlegi szokásos kezelései mellett az alábbiakban mutatjuk be. Ez a bizonyíték elsősorban laboratóriumi vizsgálatokból, nagy epidemiológiai vizsgálatokból származik (amelyek a gyógyszerek szedése és az emlőrák kimenetele közötti összefüggéseket vizsgálják egyéncsoportokban), valamint korai klinikai vizsgálatokból.
észreveheti, hogy az alábbi tanulmányok közül sok csak az egyes COC Protokollgyógyszerekre összpontosít. Mi vagyunk az elsők, hogy tervezzen egy kiegészítő terápia, amely egyesíti allfour. Hisszük, hogy ezeknek a gyógyszereknek a kombinálása a legnagyobb eredményeket fogja elérni, és a saját kutatási programunk, a METRICS, már több bizonyítékot állít elő ennek bizonyítására. Az alábbiakban további részekben olvashat arról, hogy miért gondoljuk, hogy ezek a gyógyszerek olyan jól működnek együtt a rák megcélzásában, valamint magáról a metrics programról.
Metformin és emlőrák
metforminuse kapcsolódó potenciális emlőrák előnyök
Manyobservational vizsgálatok már alátámasztják a használatát metformin mellrák. A Metformin engedéllyel rendelkezik a 2-es típusú cukorbetegség kezelésére, ésmegfigyelési vizsgálatok cukorbetegek csoportjaiban általában azt mutatják, hogyA metformint szedőknek nagyobb esélyük van a jobb eredményre, ha mellrák alakul ki (Aksoy et al., 2013; El-Benhawy és El-Sheredy, 2014; Sonnenblick et al., 2017).A Metformin alkalmazását összefüggésbe hozták a mellrákos betegek jobb túlélésével (Kim et al., 2015; Xuet al., 2015), javított válasz az emlőrák kezelésére (Jiralerspong et al.,2009), és kevesebb esélye van a mellrák terjedésének andrelapse (Chen et al., 2017; Jacob et al., 2016).
valószínű, hogy a metformin jótékony hatása ezekben a tanulmányokban annak köszönhető, hogy a metformin képes javítani a beteg cukorbetegségét és/vagy súlyát a glükózszint csökkentésével,ami segíthet csökkenteni az emlőrák kialakulásának kockázatát, és javíthatja a beteg egészségét és képességét az emlőrák kezelésére, ha van (Hatoum and McGowan, 2015). De a laboratóriumi vizsgálatok azt is mutatják, hogy a metformintöbb, mint ez. Valójában a metformin aktívan képes közvetlenül fellépni az emlőrákos sejtek ellen, csökkentve az energia felvételére és felhasználására való képességüket, valamint blokkolva a növekedés, a terjedés, a túlélés és a visszaesés képességét (Alimova et al., 2009; Hadad et al., 2014; Orecchioni et al., 2015).
különbözőaz emlőrák típusai különböző kezeléseket igényelnek. A trasztuzumabot például kifejezetten a humán epidermális növekedési faktor receptor 2 (HER2)pozitív emlőrák kezelésére használják. A Tamoxifen hatékony az ösztrogénreceptor (ER)pozitív emlőrák ellen. Fontos, hogy a laboratóriumi rákos sejtvizsgálatok azt mutatják, hogy a metformin rákellenes aktivitással rendelkezik számos különböző emlőrákos sejttípus ellen, beleértve az ER pozitív (Giles et al., 2018), HER2 pozitív (Chen et al., 2013), éspotenciálisan nehezebben kezelhető altípusok, például hármas negatív rákos sejtek (Deng et al., 2012; Vazquez-Martin et al., 2011; Wahdan-Alaswad et al., 2014).Ez azt jelenti, hogy a metformin hatékonyan működhet az emlőrák standard kezelése mellett, függetlenül a rák altípusától.
Metformintargets mellrák őssejtek
Metforminazt is kimutatták, hogy az emlőrák őssejtjeit célozza meg (Bao et al., 2014; Cufiet al., 2012; Hirsch et al., 2009).Ez a tevékenység az emlőrák ellen őssejtek, valamint az a képessége, hogyaz emlőrák különböző altípusait célozza meg, segít megmagyarázni, miért laboratóriumi vizsgálatokhogyan működhet számos standard kezeléssel kombinálva, beleértvetrasztuzumab (Cufi et al., 2012), tamoxifen (Ma et al., 2014), ésstandard kemoterápiás szerek (Iliopoulos et al.,2011). Állat – és sejtvizsgálatok azt mutatják, hogy a metformin mindkettősegít a standard kezelések hatékonyságának javításában (Bradford and Khan, 2013; Liu et al., 2012; Zhang et al., 2014) ésés késlelteti az ilyen terápiákkal kezelt rákok visszaesését is (Iliopoulos et al.,2011).
ezenkívül a laboratóriumi vizsgálatok azt is mutatják, hogy a metformin segíthet megakadályozni, hogy az emlőrákos sejtek rezisztenssé váljanak a kemoterápiával szemben, és javítja a már rezisztens rákos sejtek érzékenységét a kezelésre (Davies et al., 2017).
A metformin javítja az emlőrák markereit a korai klinikai vizsgálatokban
a metformin emlőrákban való nagy mennyiségű szupportív adatának eredményekéntmegfigyelési és laboratóriumi vizsgálatok eredményekénta metformin emlőrákban történő vizsgálata jelenleg folyamatban van (Camacho et al., 2015).Összességében a korai stádiumú vizsgálatok eredményeinek kollektív elemzése (metaanalízis) általában pozitív hatásra utalnak, amikor a metformint hozzáadják a standard rákterápiákhoz (Rahmani etal., 2019; Zhang et al., 2019b).
a lehetőségek ablaka vizsgálatok azt vizsgálják, hogy a metforminfo szedése körülbelül két héttel a műtét előtt segíthet-e javítani a betegség molekuláris markereit operálható korai stádiumú emlőrákban szenvedő betegeknél. E vizsgálatok eredményei általában arra utalnak, hogy a metformin szedése potenciálisan pozitív változásokat eredményezhet a rák molekuláris markereiben, beleértve azokat is, amelyek szabályozzák az emlőrákos sejtek növekedését és osztódását (Bonanni et al., 2012; Cazzaniga et al., 2013; Hadad et al., 2011; Kalinsky et al., 2014; Niraula etal., 2012), valamint potenciálisan javítja a szabályozásthormonok és egyéb tényezők egyes betegeknél (Kalinsky et al., 2014; Niraula et al., 2012). Ezek a tanulmányok most segítenek a tudósoknak megérteni, hogy a metformin hogyan és mikor segíthet a mellrákos betegeknél (Bonanni etal., 2012; DeCensi et al., 2014, 2015; Rahmani et al., 2019).
a 2.fázisú neoadjuváns vizsgálatok általában hosszabb és összetettebb vizsgálatok, amelyek a metformint a különböző típusú emlőrák kezelésére szolgáló standard kezelések mellett vizsgálják. E vizsgálatok célja annak megállapítása, hogy a metformin valóban hozzájárul-e a standard kezelések hatékonyságának javításához, az aslab tanulmányok azt sugallják (Kim et al., 2014). Egy nemrégiben készült tanulmány (a METTEN-tanulmány) (Martin-Castillo etal., 2018), HER2 pozitív korai stádiumú emlőrákban szenvedő nőknél több metformint szedő beteg jól reagált a kemoterápiára/célzott kezelésre (65,5%), összehasonlítva a metformint nem szedő betegekkel (58,6%). Ez a különbség statisztikailag nem volt szignifikáns; ami azt jelenti, hogy ezt az eredményt véletlenül is el lehetett érni. A 2. fázisú kísérletek azonban általában alulteljesítenek a statisztikai szignifikancia ilyen módon történő elérése érdekében, és a kutatók felhívták a nagyobb 3.fázisú vizsgálatok előrehaladását, amelyek megfelelően megtervezhetők annak meghatározására, hogy ez a hatás mennyire valós (Martin-Castillo etal., 2018). Potenciálisan biztató eredmények más 2. fázisú vizsgálatokból, például túlsúlyos, metasztatikus emlőrákban szenvedő egyénekbőlrákról is beszámoltak (Yam et al.,2019). Érdemes megjegyezni, hogy a várakozásoknak megfelelően nem mindena metformin rákvizsgálatok pozitív eredményeket jelentettek. Például a otherPhase 2 vizsgálatok azt találták, hogy a metformin standard terápiával bizonyos körülmények között nem volt valódi különbség a standard terápiához képest (Mark et al.,2019; Nanni et al., 2019). Hisszük, hogy a metformin minden körülmények között a leghatékonyabb lesz, ha más anyagcsere-ellenes gyógyszerekkel kombinálva adják be.
nagyobb vizsgálatokra van szükség ezeknek a problémáknak a megoldásához, és a 3.fázisú vizsgálat jelenleg a metformin emlőrákban történő vizsgálatára szolgál. Bár a vizsgálat 2020-ig nem fejeződik be, a vizsgálat első 6 hónapjának kezdeti eredményei azt mutatták, hogy azok a betegek, akik a metformint azonnal elkezdték szedni a műtét befejezése és a szokásos kemoterápiás ciklusok kedvező változásokat mutattak az emlőrák molekuláris markerében (Dowling et al., 2018), ésjavult metabolikus tényezők (Goodwin et al., 2015).
sztatinok és emlőrák
Observationalstudies link sztatinok jobb mellrák eredmények
sztatinok általában adni, hogy segítsen kezelni a szív-és érrendszeri betegségek. A sztatinokat szedő emberek nagy csoportjainak megfigyelési tanulmányai azonban azt is megállapították, hogy a sztatinokat szedő emlőrákos egyének szintén csökkenthetik a kezelés után visszatérő rák kockázatát, összehasonlítva azokkal a betegekkel, akik nem sztatinokat szednek (Ahern et al., 2014; Manthravadi et al., 2016). Például, egy tanulmány közel 2000 túlélő emlőrák, azok, akik elkezdték szedésifoltok három éven belül a diagnózis után csökkent esélye a rák visszatér (Kwan et al., 2008). Egy másik tanulmányban mindössze 6 hónapos sztatinhasználat a diagnózis után kapcsolódott a relapszus javuló arányához (Chae et al., 2011).
fontos megjegyezni, hogy a sztatinok jótékony hatása ezekben és más vizsgálatokban erősebben kapcsolódott a zsírban oldódó ‘lipofil’ sztatinokhoz (mint az atorvasztatin). Néhánylaboratóriumi vizsgálatban a lipofil sztatinokról azt is kimutatták, hogy sejtszinten superioranticancer hatásúak a kevésbé zsírban oldódó sztatinokhoz képest (Liu et al., 2017).
megfigyelési vizsgálatoka sztatin használatát a kezelésre adott jobb betegségválaszhoz is kapcsolják éstúlélő emlőrákos betegeknél, még azoknál a betegeknél is emlőráktípusok, amelyek agresszívebbek lehetnek (Manthravadi et al.,2016; Murtola et al., 2014; Zhong et al., 2015). Például, egy gyulladásos emlőrákban szenvedő betegeken végzett vizsgálatban az atorvasztatint szedő, rákkezelés alatt álló betegeknek hosszabb ideje volt a betegségük előrehaladása előtt, összehasonlítva azokkal, akik nem szedtek sztatint (Brewer et al., 2013).
Statinstarget emlőrákos sejtek
a sztatinok,különösen a zsírban oldódó lipofil sztatinok, mint az atorvasztatin, csökkentik az emlőrákos sejtek növekedését és növelik az emlőrákos sejtek halálát laboratóriumi vizsgálatokban
német Diabetes Association”,”oldal”:”47-48″,”kötet”:”111″,”probléma”:”1″,”forrás”:”PubMed”,”absztrakt”:”öt sztatin hatása, az atorvasztatint, Fluvasztatint, lovasztatint, pravasztatint és szimvasztatint az MCF-7 humán emlőrákos sejtvonal proliferációjával vizsgálták. A pravasztatin kivételével az összes sztatin képes volt gátolnisejtproliferáció 90%-ig 50 mikro m koncentrációban. Ezek az adatok arra utalnak, hogy a sztatinok klinikai jelentőséggel bírhatnak az emberi emlőrák elsődleges megelőzésében a koleszterinszint-csökkentő hatásukon túl. A klinikai bizonyítékot azonban meg kell várniminden további következtetést levonni.”, “DOI”: “10.1055 / s-2003-37501″,”ISSN”:”0947-7349″,”megjegyzés”:”PMID:12605351″,”naplórövidítés”:”Felh. Clint. Endokrinol.Cukorbetegség”, “Nyelv”:”eng”,”szerző”:,”kiadott”: {“dátum-alkatrészek”:]}}}],”séma”:”https://github.com/citation-style-language/schema/raw/master/csl-citation.json”} (Alarcon Martinez etal., 2018; M .. C et al., 2004; Seeger et al., 2003).Tanulmányok azt is mutatják, hogy a sztatinok potenciálisan blokkolhatják az emlőrákos sejtek invazivitását a laboratóriumban, ami arra utal, hogy segíthetnek a rák lassú terjedésében a test más részein is (Kanugula et al., 2014; Wolfe et al., 2015). A metasztatikus emlőrák egérmodelljében a statintreatment késleltette a rák növekedését, amely már 80% – kal terjedt el,a kezelés megkezdésétől számított egy héten belül kedvező aktivitást észleltek (Vintonenko et al.,2012).
egyéb vizsgálatok azt is mutatják, hogy a sztatinok segíthetnek az emlőrákos sejtek szenzibilizálásában a szokásos sugárterápiában és kemoterápiás kezelésekben (Kozar et al., 2004; Van Wyhe et al., 2017). Egy tanulmány megállapította, hogy a szimvasztatin hármas-negatív vagy gyulladásos emlőrákos sejteket érzékenyítheta laboratóriumi sugárterápiára. Ugyanez a tanulmány folytatta a betegpopuláció megfigyelését, hogy a gyulladásos emlőrákban szenvedő nők, akik sztatinokat szedtek a kezelésük során, kevésbé voltak esélyük a rák visszatérésére 3 éven belül (Lacerda et al ., 2014).
a metforminhoz hasonlóan a sztatinok ezeket a rákellenes hatásokat különböző emlőráktípusokban, köztük ER pozitív, HER2 pozitív és hármas-negatív emlőrákban is előidézhetik. Valójában egyes laboratóriumi vizsgálatok azt mutatják, hogy a sztatinok különösen hatékonyak a hármas negatív emlőrákos sejtek ellen (Campbell et al., 2006; Yao et al., 2017).
az emlőrákban a sztatinokat vizsgáló klinikai vizsgálatok már folyamatban vannak
néhány súlyos stádiumú klinikai vizsgálat most határozottan pozitív eredményeket mutat az emlőrákban lévő statinok tekintetében. Korai fázisú ‘lehetőségek ablaka’ vizsgálatokat végeztek, ha korai, a műtét előtti sztatinok segíthetnek a betegség molekuláris markereinek javításában operálható betegségben szenvedő betegeknél. Eddig ezek a tanulmányok javították a rák molekuláris profilját a sztatin kezelésben részesülő betegeknél,ami arra utal, hogy az atorvasztatin és más sztatinok ebben az összefüggésben jótékony hatással lehetnek a rákos sejtek növekedésére és osztódására és a sejthalálra, még a magas fokú agresszívabb daganatokkal rendelkező nőknél is (Bjarnadottir et al.,2013, 2015; Feldt et al., 2015; Garwood et al., 2010).
Ezen ígéretes eredmények alapján SZÁMOS 2. fázisú tanulmány vizsgálja a kötő sztatinokat az emlőrák különféle típusaihoz, beleértve a háromszoros negatív mellrákot is, most folyamatban vannak. Ezeknek a vizsgálatoknak segíteniük kellhogy a sztatinok hogyan segíthetnek az emlőrákos betegeknek.
mebendazol és a mellrák
érdeklődés mebendazolpotenciálisan rákellenes kezelés többnyire alapul ígéretes mechanisztikus vizsgálatok és meggyőző jelentések esettanulmányok rákos betegek (Nygren and Larsson,2014; Pantziarka et al., 2014).
úgy gondolják, hogy a mebendazolez megöli a rákos sejteket részben azáltal, hogy megzavarja a sejten belüli speciális struktúrákat, amelyeket mikrotubulusoknak neveznek (Pantziarka et al.,2014). Hasonló módon működik, mint a vinkrisztin, az achemoterápiás gyógyszer, amelyet jelenleg bizonyos típusú rák kezelésére használnak, beleértve az előrehaladott stádiumú emlőrákot (De Witt et al., 2017).
a laborban termesztett emlőrákos sejtekről szóló tanulmányok azt mutatják, hogy a mebendazol és az azonos osztályba tartozó gyógyszerek (benzimidazolok) lassíthatják a mellrákos sejtek növekedését és osztódását, beleértve a kemoterápiával szemben rezisztens sejteket (Coyne et al., 2013; Hou et al., 2015; Mukhopadhyay et al., 2002). Egy vizsgálatban a mebendazol erőteljesen csökkentette a kemoterápiával szemben ellenálló emlőrákos sejtek túlélését akár 63,1% – kal (Coyne et al., 2013).Tanulmányok kimutatták a benzimidazolok robusztus rákellenes aktivitását is hármas negatív emlőrák ellen (Hou et al., 2015; Zhang et al., 2015). Fontos, hogy az egyik vizsgálatban benzimidazolt is mutattak közvetlenül megcélozni emlőrák őssejtek (Hou et al., 2015).
Emerginglaboratóriumi alapú bizonyítékok arra is utalnak, hogy a benzimidazolok fokozhatják a szokásos emlőrákkezelések, például a doxorubicin ésfluorouracil aktivitását (Hou et al., 2015). Egy laboratóriumi vizsgálatban a mebendazol növelte a sugárterápia hatékonyságát háromszoros negatív emlőrákos sejteken, és megakadályozta a kezeléssel szembeni rezisztencia kialakulását (Zhang et al.,2019a). Ezenkívül egy sor tanulmány, amely a laboratóriumban termesztett kemoterápiás rezisztens ER/HER2 pozitív emlőrákos sejteket alkalmazta, következetesen kimutatta,hogy a mebendazol nemcsak csökkentette a rákos sejtek túlélését, hanem segített kiegészíteni és fokozni a mellrák kemoterápiás gyógyszerek speciálisan kifejlesztett célzott formáinak aktivitását epirubicin és gemcitabin (Coyne et al., 2014,2012, 2013).
doxiciklin és emlőrák
mivel hatékony antibiotikum, a doxiciklin más rendkívül értékes tulajdonságokkal is rendelkezik, beleértve a gyulladáscsökkentő és rákellenes aktivitást. Ez a doxiciklin valódi terápiás potenciált biztosít számos más betegség kezelésében, beleértve a rákot is (Bahrami et al., 2012).
laboratóriumi vizsgálatok és állatkísérletek már régóta kimutatták, hogy a doxiciklin képes blokkolni az emlőrákos sejtek növekedését, osztódását és mozgását (Duivenvoorden et al., 2002; Fife and Sledge, 1995, 1998).Újabb tanulmányok azt is mutatják, hogy a doxiciklin képes megállítani a rákos sejteketa DNS javítása, amikor károsodik, például kemoterápiával (Peiris-Pag Xhams et al.,2015). Valójában a laboratóriumi vizsgálatok azt mutatják, hogy a doxiciklin segíthetjavítja a kemoterápiás aktivitás hatékonyságát az emlőrákos sejtek ellen (Foroodi et al., 2009; Lamb et al., 2015a).
a közelmúltban a hangsúly annak megértésére esett, hogy a doxiciklin hogyan képes blokkolni a mellrák őssejt növekedését (Ozsvari etal., 2017; Zhang et al., 2017). A laboratóriumban termesztett sejteken végzett Avery legújabb tanulmány kimutatta, hogy a doxiciklin képes blokkolni mind a HER2 pozitív, mind a hármas negatív emlőrák őssejtjeinek növekedését, és segített javítani a standard kemoterápiás paklitaxel által kiváltott rezisztenciával kapcsolatos változásokat (Lin et al.,2018). Egy másik laboratóriumi vizsgálatban kombinatorikus megközelítésbeleértve a doxiciklint is, nagyon hatékonyan felszámolták az emlőrák őssejtjeit (Fiorillo etal., 2019).
Doxiciklinemcsak elérte a korai klinikai vizsgálatokat emlőrákos betegeknél. Eredmények aaz első kis tanulmány, amelyet 2018 októberében tettek közzé, azt mutatják, hogy a korai stádiumú emlőrákban szenvedő betegek, akik csak 14 napig szedték a doxiciklinta műtét csökkentette a rákos őssejtek jelenlétének molekuláris markereinek szintjétátlagosan körülbelül 40% – kal. Kedvező hatásokat figyeltek meg a kezelt betegek kivételével (8/9) (Scatena et al., 2018).Nagyobb klinikai vizsgálatok folyamatban vannak.
saját bizonyítékunk: a metrika tanulmány
mi a metrika?
A METRICS a Saját házon belüli kutatási programunk. Már sokat tudunk a biztonságról ésa COC protokoll gyógyszereinek hatékonysága a rákban. De az is a mi felelősségünk, hogy elismerjük, hogy nincs minden válaszunk, és hogy még mindig jó minőségű klinikai kutatásokat kell készítenünk a cocprotocol rákos betegeknél, hogy a COC protokoll a lehető leghatékonyabb és legbiztonságosabb legyen.
annak érdekében, hogy finanszírozhassuk ezt a kutatást, kifejlesztettünk egy új, megfizethető rendszert, ahol klinikai tanulmányunk, a metrikák, lényegében ‘betegfinanszírozású’. Minden beleegyező beteg, aki belép a klinikára, be van jegyezve a mutatókba, és ezek a díjak segítik a tanulmány finanszírozását. Ez a klinikai kutatás új modellje, amelynek célja a finanszírozás és az adatrések áthidalása, amelyek jelenleg akadályozzák a már engedélyezett gyógyszerek újbóli felhasználását és további klinikai fejlődését.
METRICS első eredmények
az első siker forMETRICS, az első kísérleti tanulmányunk eredményeit nemrégiben tették közzé a Feer által áttekintett tudományos folyóiratban határok a farmakológiában. A papír szabadon elérhető online itt.
A METRICS kísérleti tanulmány anobservational retrospektív vizsgálat volt, ami azt jelenti, hogy kutatóink visszatekintettek és elemezték a betegek klinikai nyilvántartásait, hogy megtudják, mi történt. Összegyűjtötték az adatokat, és rögzítették a glioblastoma nevű előrehaladott agyrákban szenvedő 95 beteg eredményeit, akik részt vettek a Care onkológiai klinikán, és akik a szokásos szokásos kezeléseik mellett a teljes COC protokollt alkalmazták. Ennek a tanulmánynak nem volt kontrollcsoportja, ezért kutatóink összehasonlították a metrikák eredményeit az azonos típusú rákos betegeken végzett korábbi vizsgálatok korábban közzétett eredményeivel, akik szintén szokásos kezelést végeztek.
a kezdeti eredmények azt sugallják, hogy a klinikánkon részt vevő betegek, akik a COC protokollt a szokásos ellátásuk részeként vették igénybe, sokkal nagyobb valószínűséggel éltek túl legalább 2 évet (64.Vizsgálatunkban a betegek 0% – A élte túl legalább 2 évet, szemben a korábban publikált tanulmányokban szereplő betegek 27-29%-ával), és általában hosszabb túlélési idővel rendelkeztek, mint általában az ilyen típusú rákos betegeknél várható volt (a betegek átlagosan 27 hónapot éltek túl vizsgálatunkban, összehasonlítva a korábbi vizsgálatok 15-16 hónapjával)(Agrawalet al., 2019).
ezek az eredmények rendkívülígéretes, de még mindig előzetes. Még nem tudjuk pontosan, hogy a COC protokoll hogyan befolyásolhatta például a túlélési időket, vagy hogy más tényezők, például bizonyos betegjellemzők hogyan befolyásolhatták ezeket az eredményeket. De ez az első, kezdeti bizonyíték minden bizonnyal biztató, és azt sugallja nekünk, hogy jó irányba haladunk. A következő tervezett szakaszunk egy nagyobb, jól megtervezett tanulmány elvégzése. Többet megtudhatjövőbeli mutatók tervek online kereséssel vagy a klinikával való kapcsolatfelvétel útján.
További információ a COC protokollról
mi a COC protokoll?
a COC protokoll az engedélyezett gyógyszerekből álló kombinált kezelési rend, amelyet kifejezetten a Care Oncology tervezett kiegészítő használatra a beteg szokásos kezelése mellett (azaz a szokásos ellátás).
a COC protokollban szereplő négy gyógyszer a következő: metformin, rendkívül gyakori cukorbetegség elleni gyógyszer; atorvasztatin, a kardiovaszkuláris állapotok kezelésére használt sztatin; doxiciklin, egyfajta antibiotikum, amelyet gyakran használnak krónikus fertőzések, például pattanások kezelésére; és mebendazol, amedicine, amelyet általában gyermekek és felnőttek parazitafertőzéseinek kezelésére használnak.
ezt a négy gyógyszert több ezer potenciális jelölt közül választottuk, kifejezetten azért, mert megfelelnek az előre meghatározott kiválasztási kritériumoknak. E kritériumok közé tartozik a rák elleni hatékonyságra vonatkozó szilárd bizonyíték, a koherens hatásmechanizmus és a fontos biztonságossági profil. Ez a három központi tétel alakította a miétmegközelítés a kezdetektől fogva.
a biztonság a legfontosabb
a rák összetett betegség, komplex kezelésekkel, és úgy gondoljuk, hogy a standard kezelések mellett a további terápiák hozzáadását nagyon óvatosan kell értékelni. Nem csak a hatékonyság szempontjából,hanem a biztonság szempontjából is. Ez az oka annak, hogy az egész megközelítésünk bizonyítékokon alapul – többnyire publikált tudományos tanulmányokon, valamint egyre inkább a saját adatainkon.
sok különböző gyógyszer a piacon legalább néhány közzétett bizonyíték támasztja alá viszonylag hatékony alkalmazását a rákban, de ezek közül a gyógyszerek közül kevés rendelkezik olyan szintű bizonyítékokkal mind a biztonságosságról, mind a hatékonyságról, amelyek a COC protokollhoz szükségesek voltak. Nagy mennyiségű Részletes adat már létezik az egyes protokoll gyógyszerek, gyűjtött év használat a generalpopulation – és ez segített, hogy nekünk egy döntő előnyt a fejlesztés során.
alaposan átkutattuk a COC protokoll szerinti gyógyszerekre vonatkozó több évtizedes közzétett adatokat, feltárva, hogyan működnek a különböző betegpopulációkban (beleértve a rákos betegeket is), valamint a laboratóriumi sejt-és állatmodelleken. Ezek az adatok, saját klinikai tapasztalataink mellett, segítenek annak biztosításában, hogy jól megértsük, hogyan fognak viselkedni ezek a gyógyszerek a különböző stádiumú és típusú rákos betegeknél, mind egymással, mind számos más rákterápiával kombinálva. Ez a tudásparamount, és a mi vizsgálatok, ez a fajta bizonyíték csak nem létezik még sok más off‑label rákellenes gyógyszer jelöltek – különösen, ha adott inkombináció.
ananti-metabolikus terápia, amely potenciálisan megcélozhatja a rákot
a COC protokollt úgy tervezték, hogy korlátozza a ráksejtek általános képességét az energia felvételére és felhasználására (azaz metabolizálására).
a rákos sejteknek hatalmas mennyiségű energiára van szükségük a túléléshez, és a rákok túlnyomó többsége adaptív folyamatot, úgynevezett aerob glikolízist használ a szükséges túlzott energia előállításához (Kroemer andPouyssegur, 2008). A protokollban szereplő gyógyszerek mindegyike megcélozhatja a különböző molekuláris anyagcsere folyamatokat, amelyek részt vesznek az aerobicglycolysis-ben és környékén, és ez segíthet csökkenteni a ráksejt általános anyagcseréjét (Jang et al.,2013).
úgy gondoljuk, hogy a COCProtocol gyógyszerek kombinációban működhetnek, hogy következetesen korlátozzák az energiaellátást és a felhasználást, miközben megakadályozzák a rákos sejtek alkalmazkodását és más utakat használnak az energia felvételéhez (Jagust et al.,2019). Ennek eredményeként a rákos sejtek egyre gyengébbek és kevésbé képesek felvenni és felhasználni a tápanyagokat (pl. mint például a glükóz és az esszenciálisaminosavak glutamin és arginin), amelyekre szükségük van a környezetükből (Andrzejewskiet al., 2018; Liu et al., 2016).Ez megnehezíti a rákos sejtek túlélését, növekedését és terjedését a szervezetben. Fokozatosan, a legyengült sejtek (beleértve a rugalmasabb és a korábban kezelés-rezisztens sejtek) sebezhetőbbé válnak a támadás más sejtölő rák terápiák, mint a sugárkezelés,kemoterápia, hormonterápia, és célzott terápiák (Bradford andKhan, 2013; Chen et al., 2012; Lacerda et al., 2014; Lamb et al., 2015a; Pantziarka et al., 2014).
az adaptált metabolikus mechanizmusok megcélzásával, amelyek a legtöbb rák esetében közösek (de általában nem egészséges sejtek), úgy gondoljuk,hogy a COC protokoll hatékony és szelektív lehet gyakorlatilag bármilyen rákra, függetlenül a rák típusától, stádiumától vagy helyétől. A közzétett epidemiológiai és laboratóriumi vizsgálatok egyre inkább támogatják a terápia potenciálisan széles körét (Chae et al.,2015, 2016; Iliopoulos et al., 2011; Lamb et al., 2015b; Pantziarka et al.,2014).
mechanisztikus koherencia a cselekvésben – a kombináció ereje
a COC protokoll valódi ereje az általunk használt gyógyszerek specifikus kombinációjában rejlik. A protokollt nemcsak négy egyedi kezelésből álló kezelésként dolgoztuk ki, mindegyik rákellenes aktivitással, hanem egyetlen kombinált kezelésként is-az erőteljes szinergikus hatások előidézésének lehetőségével (Mokhtari et al., 2017).
a COC protokollban szereplő egyes gyógyszerek a rákos sejtek anyagcseréjét külön és kiegészítő módon célozzák meg, és ezt a műveletet ‘mechanisztikus koherenciának’neveztük. Egyszerűen, a mechanisztikus koherencia leírja, hogy az egyes gyógyszerek hogyan támadhatják meg a rákos sejteket más szögből. Például a rákos őssejtek a rákos sejtek egyik legrugalmasabb típusa, és minden gyógyszer más módon célozza meg ezeket a sejteket: a metformin a sejt ‘akkumulátorait’ (úgynevezett mitokondrium) célozza meg, mivel nagyon megnehezíti a mitokondriumok számára az energia előállításához szükséges molekuláris reakciók futtatását, a doxiciklin blokkolja a sejt-DNAmachinery-t, amelyet a mitokondriumoknak meg kell replikálniuk és javítaniuk kell (Skoda et al., 2019), a sztatinok megváltoztathatják a rák őssejt génexpresszióját, így a sejtek érzékenyebbek más rákterápiákra (Kodach et al., 2011), andmebendazole megszakíthatja a sejtosztódásban részt vevő számos molekuláris folyamatot, hogy segítsen blokkolni a rákos őssejtek növekedését (Hothi et al., 2012; Hou et al., 2015).
mind a négy ágens kombinálásával a COC protokoll a rákos őssejteket (és más rákos sejteket) több ‘gyenge ponton’ is elérheti, és mint egy-két ütés, ez a sejteket kevésbé képes elkerülni és helyreállítani.
a laboratóriumi vizsgálatok kezdik kiemelni ennek a megközelítésnek a hatékonyságát a COCprotocol gyógyszeres kombinációk alkalmazásával. Egy mechanisztikus vizsgálatban a sztatin kombinálásaés a metformin nagymértékben csökkentette a prosztatarák sejtjeinek növekedését több mintvagy önmagában (Wang et al., 2017). Megfigyelési tanulmányok is beszámoltak e gyógyszerek potenciálisan szinergikus hatásairól a különböző rákok ellen (Babcook etal., 2014; Danzig et al., 2015; Lehman et al., 2012; Nimako et al., 2017). Az emlőrákban a metformint és a doxiciklint vizsgáló aclinikai vizsgálat jelenleg (NCT02874430), és a saját kutatási programunk, a METRICS, most is ígéretes adatokat állít elő.
hosszú távú kiegészítő terápia
a COC protokollt elsősorban hosszú távú kiegészítő terápiának tervezték, amely segít a standard kezelések optimalizálásában. Mivel azonban a Cocprotocollal végzett anyagcsere-kezelés hosszú távra szól, a betegek a protokollt fenntartási rendszerként is alkalmazhatják a standard kezelés befejezése után vagy a szokásos kezelés szüneteiben, valamint a kiújulás vagy áttétek kockázatának enyhítésére irányuló hosszú távú stratégia részeként. Ezért azt is érdemes megjegyezni, hogy a COC protokoll mindegyik gyógyszere szintén beszámolt a rák kedvező hatásmechanizmusairól, amelyek nem függenek a standard terápiák együttes alkalmazásától, és amelyek önállóan segíthetnek a relapszus és a metasztatikus terjedés kockázatának csökkentésében.
A Care Oncology modell
az egyes betegek aktív orvosi felügyelete
bár a COCProtocol gyógyszereket sok éven át biztonságosan alkalmazták az általános populációban, minden hozzánk érkező beteg egyedi. Ez az oka annak, hogy minden beteg, aki részt vesz a Care onkológiai klinikán, a klinikusok közvetlen gondozása alá kerül, speciális ismeretekkel a COC protokoll gyógyszereinek felírásáról a rák környezetében. Klinikusaink egyénileg értékelik a lehetséges előnyöket és kockázatokat a COC protokoll minden betegnél történő alkalmazása során. Csak akkor ajánlják a COC protokollt a betegeknek, ha úgy vélik, hogy ez biztonságos és előnyös lesz. Minden COC protokoll előírása a beteg igényeihez igazodik, és az adagokat és kezelési módokat gondosan felülvizsgálják és kiigazítják a beteg előrehaladásának alapján.
ezért elengedhetetlen, hogy a betegek csak akkor vegyék be a COC protokollt, miközben klinikánkon gondosan figyelik őket a kezelésük időtartama alatt.
*********************************************************************************
fontos megjegyzés
A cikk célja
Ez a cikk áttekintést nyújt a szabadalmaztatott Care Oncologyprotocol-t tartalmazó gyógyszerekkel kapcsolatos tudományos és orvosi szakirodalomról. Ügyeltek arra, hogy kiválasszák azokat a releváns cikkeket, amelyek támogatják ezeknek a gyógyszereknek a címkén kívüli alkalmazását klinikai körülmények között a rák kiegészítő kezelésére. Ez a cikk nem az összes bizonyíték átfogó áttekintése, sem az ilyen kezelés összes lehetséges mellékhatását nem rögzíti.
Ez a cikk csak tájékoztató jellegű, és nem minősül medicaladvice-nak. Az itt tárgyalt gyógyszerek csak receptre kaphatók, és nem szabad orvosával vagy más szakmai egészségügyi szolgáltatóval folytatott konzultáció nélkül bevenni. Care onkológia az orvosok megvitatják Önnel ezen gyógyszerek alkalmasságát, és kapcsolatba lépnek orvosával vagy onkológusával, hogy megvitassák az Ön számára való alkalmasságukat.
nem szabad támaszkodnia az ebben a cikkben szereplő információkra az orvos vagy más professzionális egészségügyi szolgáltató orvosi tanácsadásának alternatívájaként. Ha bármilyen konkrét kérdése van bármilyen orvosi kérdéssel kapcsolatban, forduljon orvosához vagy más professzionális egészségügyi szolgáltatóhoz. Ha úgy gondolja, hogy bármilyen betegségben szenved, azonnal orvoshoz kell fordulnia. Soha ne késleltesse az orvosi tanács kérését, figyelmen kívül hagyja az orvosi tanácsot, vagyaz ebben a cikkben szereplő információk miatt folytassa az orvosi kezelést.
szerzői jog
a cikkben szereplő szerzői jog a Health Clinics LLC és licencadói tulajdonában van.
szabadalom
A Care Oncology(“COC”) protokollt az Egyesült Államok us9622982b2 szabadalma és számos további nemzetközi szabadalom védi.
*********************************************************************************
Agrawal, S., Vamadevan, P., Mazibuko, N., Bannister, R., Swery, R., Wilson, S., andEdwards, S. (2019). Új módszer az etikus és hatékony bizonyítékok előállítására az onkológiai gyógyszereken kívüli alkalmazásra (esettanulmány Glioblasztómában). Elöl.Pharmacol. 10.
Ahern, T. P., Lash, T. L., Damkier, P.,Christiansen, P. M., and Cronin-Fenton, D. P. (2014). Sztatinok és a mellrák prognózisa: bizonyítékok és lehetőségek. Lancet Oncol. 15, e461-468.
Aksoy, S., Sendur, M. A. N. és Altundag, K. (2013).Demográfiai és klinikai-patológiai jellemzők invazív betegeknélmellrák metformint kap. Med. Onkol. Northwood Lond. Engl. 30, 590.
Alarcon Martinez, T., Zeybek, N. D., és M.(2018). Az atorvasztatin citotoxikus és Autofágikus hatásainak értékelése az MCF-7 Emlőráksejtekre. Balk. Med. J. 35, 256-262.
Alimova, I. N., Liu, B., Fan, Z., Edgerton,S. M., Dillon, T., Lind, S. E. és Thor, A. D. (2009). A Metformin in vitro gátolja az emlőrák sejtnövekedését, kolóniaképződést és sejtciklus-leállást idéz elő. CellCycle 8, 909-915.Andrzejewski, S., Siegel, P. M. és St-Pierre, J.(2018). A metformin hatásosságával összefüggő metabolikus profilok rákbetegségben. Elöl.Endokrinol. 9.
Babcook, M. A., Shukla, S., Fu, P., Vazquez, E. J.,Puhowicz, M. A., Molter, J. P., Oak, C. Z., MacLennan, G. T., Flask,C. A., Lindner, D. J., et al. (2014). Szinergista szimvasztatin és Metformin Kombinációkemoterápia csontos metasztatikus kasztráció-rezisztens prosztatarák kezelésére. Mol.Rák. 13, 2288–2302.
Bahrami, F., Morris, D. L. és Pourgholami, M. H.(2012). Tetraciklinek: hatalmas terápiás potenciállal rendelkező gyógyszerek. Mini Rev. Med.Kémia. 12, 44–52.
Bao, B., Azmi, A. S., Ali, S., Zaiem,F. és Sarkar, F. H. (2014). A Metformin rákellenes szerként működhet a rákos sejtek megcélzásán keresztül: a tumorral összefüggő miRNS-ek potenciális biológiai jelentősége a mell-és hasnyálmirigyrákban. Ann. Ford. Med. 2.
Bjarnadottir, O., Romero, Q., Bendahl, P.-O.,Jirstr, K., Ryd, L., Loman, N., Uhl, M., Johannesson, H., Rose, C., Grabau, D., etal. (2013). Célzás HMG-CoA reduktáz sztatinokkal egy ablak-of-opportunity mellrák vizsgálat. A Mellrák Res. Kezelésére. 138, 499–508.
Bjarnadottir, O., Kimbung, S., Johansson, I., Veerla, S., J Kb Nsson, M., Bendahl, P.-O., Grabau, D., Hedenfalk, I. és Borgquist, S.(2015). Globális transzkripciós változások a sztatin kezelést követően a mellrákban. Clint. Rák Res. Ki. J. Am. Assoc. Rák Res. 21, 3402-3411.
Bonanni, B., Puntoni, M., Cazzaniga, M., Pruneri, G., Serrano, D., Guerrieri-Gonzaga, A., Gennari, A., Trabacca,M. S., Galimberti, V., Veronesi, P., et al. (2012). A metformin kettős hatása a mellrákraproliferáció egy randomizált elősebészeti vizsgálatban. J. Clin. Onkol. Ki. J. Am.Soc. Clint. Onkol. 30, 2593–2600.Bradford, S. A. és Khan, A. (2013). IndividualizingChemotherapy segítségével az antidiabetikus gyógyszer, Metformin, mint egy 6adjuváns GmbH: Anexploratory tanulmány. J. Rák Sci. Ott. 5.Brewer, T. M., Masuda, H., Liu, D. D., Shen, Y., Liu, P., Iwamoto, T., Kai, K., Barnett, C. M., Woodward, W. A., Reuben, J. M., et al.(2013). Sztatin alkalmazása elsődleges gyulladásos emlőrákban: kohorsz vizsgálat. Br.J. Rák 109, 318-324.
Camacho, L., Dasgupta, A. és Jiralerspong, S. (2015). Metformin a mellrákban-egy fejlődő rejtély. Mellrák res. BCR 17, 88.B. A., B. A., B. A., B. A., B. A., B. A., B. A.,B. A., B. A., B. A., B. A., A. A., A. A., A. A., A. A., A. A., A. A., A. A., A. A., A. A., A. A., A. A., A. A., A. A., A. A., A. A., A. A., A. A., A. A., A. A., A. (2006). A mellrák növekedésének megelőzése sztatinok által. Rák Res. 66,8707-8714.Cazzaniga, M., DeCensi, A., Pruneri, G., Puntoni, M., Bottiglieri, L., Varricchio, C., Guerrieri-Gonzaga, A., Gentilini, O. D., Pagani, G., Dell ‘ Orto, P., et al. (2013). A metformin hatása az apoptózisraegy emlőrák előtti vizsgálatban. Br. J. Rák 109, 2792-2797.
Chae, Y. K., Valsecchi, M. E., Kim, J., Bianchi,A. L., Khemasuwan, D., Desai, A., and Tester, W. (2011). Az emlőrák kockázatának csökkentéseace-gátlókat, ARB-ket és/vagy sztatinokat alkalmazó betegeknél. CancerInvest. 29, 585–593.Chae, Y. K., Yousaf, M., Malecek, M.-K., Carneiro, B.,Chandra, S., Kaplan, J., Kalyan, A., Sassano, A., Platanias, L. C. és Giles, F. (2015). Sztatinok mint rákellenes terápia; Le tudjuk fordítani a preklinikai ésepidemiológiai adatokat klinikai előnyökké? Discov. Med. 20, 413–427.
Chae, Y. K., Arya, A., Malecek, M.-K., Shin, D. S.,Carneiro, B., Chandra, S. Kaplan, J., Kalyan, A., Altman, J. K., Platanias, L.,et al. (2016). A metformin újbóli felhasználása a rák kezelésére: jelenlegi klinikai vizsgálatok. Oncotarget 7, 40767-40780.
Chen, J., Lan, T., Hou, J., Zhang, J., An, Y.,Tie, L., Pan, Y., Liu, J. és Li, X. (2012). Az atorvasztatin érzékenyíti a humannon-kissejtes tüdőkarcinómákat a karboplatinra az AKT aktiválásának és a TIMP-1 szabályozásának elnyomása révén. Int. J. Biochem. Sejt Biol. 44, 759–769.
Chen, L., Chubak, J., Boudreau, D. M., Barlow, W. E., Weiss, N. S. és Li, C. I. (2017). A cukorbetegség kezelése és az AdverseBreast Cancer kimenetelének kockázata a korai stádiumú emlőrákos betegek körében: látnok-MedicareAnalysis. Rák Res. 77, 6033-6041.
Chen, T., Liang, Y., Feng, D., Tao, L., Qi, K.,Zhang, H., Wang, H., Lin, Q. és Kong, H. (2013). A Metformin gátolja a proliferációt és elősegíti a HER2 pozitív emlőrákos sejtek apoptózisát azáltal, hogy csökkenti a hsp90 szabályozását. J. BUON vége. J. Balk. Union Oncol. 18, 51–56.Coyne, C., Jones, T. és Bear, R. (2014).A gemcitabin-(C4-amid)- indualis és Epirubicin-(C3-amid) kombináció daganatellenes citotoxicitása a kemoterápiás-rezisztens emlő adenokarcinóma (SKBr – 3) és a mebendazol kiegészítő hatása ellen. J. Rák Res. Ther. Onkol. 2.Coyne, C. P., Jones, T., and Bear, R. (2012). Az alternatív Tubulin inhibitorok hatása az aEpirubicin hatásosságára-Immunkemoterápiás szintetizált Ultra VioletLight-aktivált intermedier. Rák Clin. Onkol. 1, 49–80.Coyne, C. P., Jones, T., and Bear, R. (2013).Gemcitabine-(C4-amide)- Anti-Neoplastic Cytotoxicity in DualCombination with Mebendazole against Chemotherapeutic-Resistant MammaryAdenocarcinoma. J. Clin. Exp. Oncol. 2.
Cufi, S., Corominas-Faja, B., Vazquez-Martin, A.,Oliveras-Ferraros, C., Dorca, J., Bosch-Barrera, J., Martin-Castillo, B., andMenendez, J.A. (2012). Metformin-induced preferential killing of breast cancerinitiating CD44+CD24-/low cells is sufficient to overcome primary resistance totrastuzumab in HER2+ human breast cancer xenografts. Oncotarget 3, 395–398.
Danzig, M.R., Kotamarti, S., Ghandour, R.A.,Rothberg, M. B., Dubow, B. P., Benson, M. C., Badani, K. K. és McKiernan, J. M. (2015).A metformin és a sztatinok közötti szinergizmus a cukorbetegségben szenvedő férfiak radikális prosztatektómiáját követő biokémiai kockázat módosításában. ProstateCancer Prostatic Dis. 18, 63–68.
Davies, G., Lobanova, L., Dawicki, W., Groot, G., Gordon, J. R., Bowen, M., Harkness, T. és Arnason, T. (2017). A metformin gátolja a kezelés-rezisztens emlőrák kialakulását, és elősegíti a resenzitizációt. PLoS ONE 12.
De Witt, M., Gamble, A., Hanson, D., Markowitz, D., Powell, C., Al Dimassi, S., Atlas, M., Boockvar, J., Ruggieri, R. és Symons, M. (2017). A mebendazol újrafelhasználása a vinkrisztin helyettesítésére az agydaganatok kezelésére. Mol. Med. 23, 50–56.Gandini, S., Guerrieri-Gonzaga, A., Johansson, H. A., Cazzaniga, M., Pruneri,G., Serrano, D., Schwab, M., Hofmann, U., et al. (2014). A metforminon emlőrák proliferációjának differenciális hatásai az inzulinrezisztencia markerei éstumor altípus egy randomizált elősebészeti vizsgálatban. A Mellrák Res. Kezelésére. 148,81–90.DeCensi, A., Puntoni, M., Guerrieri-Gonzaga, A.,Cazzaniga, M., Serrano, D., Lazzeroni, M., Vingiani, A., Gentilini,O., Petrera, M., Viale, G., et al. (2015). A Metformin hatása az emlő DuctalCarcinoma In Situ proliferációjára egy randomizált Elősebészeti vizsgálatban. Rák Előző.Res. Phila. Apa 8, 888-894.
Deng, X.-S., Wang, S., Deng, A., Liu,B., Edgerton, S. M., Lind, S. E., Wahdan-Alaswad, R., and Thor, A. D. (2012). A Metformin a sejtnövekedés gátlására és apoptózis kiváltására irányul a tripla-negatív emlőrákban. Sejtciklus Georget. Tex 11, 367-376.Dowling, R. J., Parulekar, W. R., Gelmon, K. A., Shepherd, L. E., Virk, S., Ennis, M., Mao, F., Ligibel, J. A., Hershman, D. L., Rastogi, P., et al. (2018). CA15-3 / MUC1 a CCTG MA-32-ben (NCT01101438): a metformin vs.placebo invazív betegségmentes ésáltalános túlélés korai stádiumú emlőrákban (BC). J. Clin. Onkol.
Duivenvoorden, W. C. M., Popovi (2002), S. V., Lhot!, S.,Seidlitz, E., Hirte, H. W., Tozer, R. G., and Singh, G.). A doxiciklin csökkenti a tumorterhelést az emberi emlőrák csontmetasztázisos modelljében. Rák Res. 62,1588-1591.
El-Benhawy, S. A. és El-Sheredy, H. G. (2014).Metformin és túlélés diabéteszes emlőrákos betegeknél. J. Egyiptom.Közegészségügyi Assoc. 89, 148–153.
Feldt, M., Bjarnadottir, O., Kimbung, S.,Jirstr, K., Bendahl, P.-O., Veerla, S., Grabau, D., Hedenfalk, I. és Borgquist, S.(2015). Sztatin által indukált anti-proliferatív hatások a ciklin D1 és p27 segítségével az awindow-of-opportunity breast cancer vizsgálatban. J. Ford. Med. 13, 133.
Fife, R. S. és Sledge, G. W. (1995). A doxiciklin hatása a mellrák sejtek in vitro növekedésére, migrációjára és zselatináz aktivitására. J. Labor. Clint. Med. 125, 407–411.
Fife, R. S., és Sledge, G. W. (1998). A doxiciklin hatása a rákos sejtekre in vitro és in vivo. Dent ADV. Res. 12, 94-96.
Fiorillo, M., T!, F., Sotgia, F. és Lisanti, M. P.(2019). Doxiciklin, azitromicin és C-vitamin (DAV) : hatékony kombinációs terápia a mitokondriumok megcélzására és a rákos őssejtek felszámolására.Öregedés 11, 2202-2216.Foroodi, F., Duivenvoorden, W. C. És Singh, G.(2009). A doxiciklin kölcsönhatása kemoterápiás szerekkel emberbenmell adenokarcinóma MDA-MB-231 sejtek. Rákellenes. Drogok 20, 115-122.
Garwood, E. R., Kumar, A. S., Baehner, F. L., Moore, D. H., Au, A., Hylton, N., Virágok, C. I., Garber, J., Lesnikoski, B.-A., Hwang, E. S., et al. (2010). A fluvasztatin csökkenti a proliferációt és növekszikapoptózis magas fokú nőknélmellrák. A Mellrák Res. Kezelésére. 119, 137–144.
Giles, E. D., Jindal, S., Wellberg, E. A., Schedin, T., Anderson, S. M., Thor, A. D., Edwards, D. P., MacLean, P. S. és Schedin, P. (2018). A Metformin gátolja a stromális aromatáz expressziót és a tumor progresszióját a posztmenopauzális emlőrák rágcsáló modelljében. Mellrák res. BCR 20.
Goodwin, P. J., Parulekar, W. R., Gelmon, K. A., Shepherd, L. E., Ligibel, J. A., Hershman, D. L., Rastogi, P., Mayer, I. A., Hobday, T. J., Lemieux, J., et al. (2015). A metformin és a placebo hatása az andmetabolikus faktorokra az NCIC CTG MA – ban.32. J. Natl. Rák Inst. 107.L., L., Purdie, C., Bray, S., Baker, L., jellem, G., Deharo, S., Hardie, D. G., Pusztai, L., et al.(2011). Bizonyíték a metformin biológiai hatásaira operálható emlőrákban: műtét előtti, lehetőségablakos, randomizált vizsgálat. A Mellrák Res. Kezelésére. 128, 783–794.
Hadad, S. M., Hardie, D. G., Appleyard, V., andThompson, A. M. (2014). A metformin hatása az emlőrák sejtproliferációjára, az AMPK útvonalra és a sejtciklusra. Clint. Ford. Onkol. Ki.Publ. Szövetségi. Span. Onkol. Soc. NAT. Rák Inst. Mex. 16, 746–752.
Hatoum, D. és McGowan, E. M. (2015). Legutóbbi előrelépéseka metformin alkalmazásában: a cukorbetegség kezelése megakadályozhatja-e az emlőrákot? BioMedRes. Int. 2015, 548436.
Hirsch, H. A., Iliopoulos, D., Tsichlis, P. N., andStruhl, K. (2009). A Metformin szelektíven célozza meg a rákos őssejteket, és a kemoterápiával együtt gátolja a Tumor növekedését és meghosszabbítja a remissziót. CancerRes. 69, 7507–7511.
Hothi, P., Martins, T. J., Chen, L., Deleyrolle, L., Yoon, J.-G., Reynolds, B. és Foltz, G. (2012). Nagy áteresztőképességű vegyi anyagoka képernyők a diszulfiramot az emberi Glioblastoma őssejtek inhibitoraként azonosítják.Oncotarget 3, 1124-1136.
Hou, Z. J., Luo, X., Zhang, W., Peng, F., Cui, B., Wu,S. J., Zheng, F.-M., Xu, J., Xu, L.-Z., Hosszú, Z. J., et al. (2015).A flubendazol, az FDA által jóváhagyott féreghajtó, az emlőrák őssejtjeit célozza meg.Oncotarget 6, 6326-6340.
Iliopoulos, D., Hirsch, H. A. és Struhl, K. (2011).A Metformin csökkenti a kemoterápia dózisát a tumor remisszió meghosszabbításáhozegér xenograftok, amelyek több rákos sejttípust tartalmaznak. Rák Res. 71,3196-3201.
Jacob, L., Kostev, K., Rathmann, W. és Kalder, M.(2016). A metformin hatása a metasztázisokra emlőrákos betegeknél és2-es típusú cukorbetegség. J. Cukorbetegség Szövődményei 30, 1056-1059.
Jagust, P., De Lux, B., Parejo-Alonso, B. és Sancho, P. (2019). Anyagcsere – Alapú Terápiás Stratégiák, Amelyek A Rákot Célozzáktörzssejtek. Elöl. Pharmacol. 10.
Jang, M., Kim, S. S., and Lee, J. (2013). Rákos sejtanyagcsere: a terápiás célpontokra gyakorolt hatások. Felh. Mol. Med. 45, e45.jiralerspong, S., Palla, S. L., Giordano, S. H.,Meric-Bernstam, F., Liedtke, C., Barnett, C. M., Hsu, L., Hung,M.-C., Hortobágyi, G. N. és Gonzalez-Angulo, A. M. (2009). Metformin és a neoadjuváns kemoterápiára adott kórosan teljes válaszok diabéteszes, mellrákos betegeknél. J. Clin. Onkol. 27, 3297–3302.B. A., Wang,A., Feldman, S. M., Taback, B., Ahmad, A., Cremers, S., Hibshoosh, H., et al.(2014). A metformin prekurgiai vizsgálata túlsúlyos és elhízott betegeknélújra diagnosztizált emlőrák. Rák Invest. 32, 150–157.
Kanugula, A. K., Gollavilli, P. N., Vasamsetti, S. B.,Karnewar, S., Gopoju, R., Ummanni, R. és Kotamraju, S. (2014). Az emlőrák proliferációjának és inváziójának sztatin által indukált gátlása magában foglalja a vasszállítás csillapítását: a nitrogén-monoxid és az antioxidáns védelmi mechanizmusok intermedierje. FEBS J. 281, 3719-3738.Kim, H. J., Kwon, H., Lee, J. W., Kim, H. J., Lee,S. B., Park, H. S., Sohn, G., Lee, Y., Koh, B. S., Yu, J. H., et al. (2015). A metformin növeli a túlélést hormonreceptor-pozitív, HER2-pozitív emlőrákban cukorbetegek. Mellrák res. BCR 17, 64.
Kim, J., Lim, W., Kim, E.-K., Kim, M.-K., Paik, N.-S.,Jeong, S.-S., Yoon, J.-H., Park, C. H., Ahn, S. H., Kim, L. S., et al. (2014).Fázisú randomizált vizsgálat neoadjuváns metformin plusz letrozol versus placebo letrozol ösztrogénreceptor pozitív posztmenopauzális emlőrák(METEOR) esetén. BMC rák 14, 170.B. A., B. A., B. A., B. A., B. A., B. A.,B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., Peppelenbosch, M. P., van den Brink, G. R., et al. (2011). A sztatinok növelik a colorectalis rákos sejtek epigenetikus újraprogramozást indukáló kemoszenzitivitását, és csökkentik a colorectalis rákos sejtek “törzsét” a csont morfogenetikus fehérje útján. Gut 60, 1544-1553.
Kozar, K., Kaminski, R., Legat, M., Kopec, M., Nowis, D., Skierski, J., Koronkiewicz, M., jak ons, M. és Golab, J. (2004).A cerivasztatin fokozott daganatellenes aktivitást mutat az emberi emlőrákos sejtvonalakkal szemben, ha doxorubicinnel vagy ciszplatinnal kombinálva alkalmazzák. Int.J. Oncol.
Kroemer, G., és Pouyssegur, J. (2008). Tumorsejtek metabolizmusa: a rák Achilles-sarka. Rákos Sejt 13, 472-482.
Kwan, M. L., Habel, L. A., Flick, E. D., Quesenberry, C. P. és Caan, B. (2008). A korai stádiumú emlőrák túlélőinek prospektív kohorsz vizsgálatában. A Mellrák Res. Kezelésére. 109, 573–579.L., L., L., J. P., Liu, D., Larson, R., Li, L., Masuda, H., Brewer, T., Debeb, B. G., Xu, W., Hortob, G. N., et al. (2014).A szimvasztatin radioszenzibilizálja a differenciált és őssejtszerű emlőrákos sejtvonalakat, és a posztmastectomiás sugárzással kezelt gyulladásos emlőrákos betegeknél a lokális kontroll javulásával jár. Őssejtek Transzl. Med.3, 849–856.L. A., L. A., L. A., L. A., L. A., L. A., L. A., L. A.,L. A., L. A., L. A., L. A., L. A., L. A., L. A., L. A., L. A., L. A.,L. A., L. A., L. A., L. A., L. A., L. A., L. A., L. A., L. A., L. A., L. A., L. A., L. A., M. E., et al. (2015a). A doxiciklin lefelé szabályozza a DNS-Pk-tés radioszenzibilizálja a tumort kezdeményező sejteket: a hatékonyabb sugárzási terápia következményei. Oncotarget 6, 14005-14025.
Lamb, R., Ozsvari, B., Lisanti, C. L., Tanowitz, H. B., Howell, A., Martinez-Outschoorn, U. E., Sotgia, F. és Lisanti, M. P. (2015b).A mitokondriumokat megcélzó antibiotikumok hatékonyan felszámolják a rákos őssejteket, több tumortípuson keresztül:a rák kezelése fertőző betegségként.Oncotarget 6, 4569-4584.Lehman, D. M., Lorenzo, C., Hernandez, J. és Wang, C.(2012). A sztatin használata a metformin moderátoraként a prosztatarák kockázatára gyakorolt hatás a 2-es típusú cukorbetegek körében. Cukorbetegség Ellátás 35, 1002-1007.
Lin, C., Lo, M., Moody, R., Stevers, N., Tinsley,S. és Sun, D. (2018). A doxiciklin az aldehid‑dehidrogenáz-pozitív emlőrák-sejteket célozza meg. Onkol. REP.
Liu, B., Yi, Z., Guan, X., Zeng, Y.-X., és Ma, F.(2017). A sztatinok és az emlőrák prognózisa közötti kapcsolat a citatin típusától és az expozíciós időtől függ: metaanalízis. A Mellrák Res. Kezelésére. 164,1–11.
Liu, H., Schefe, C., Zang, C., Schefe, J. H.,Habbel, P., Regierer, A.-C., Schulz, C.-O., Possinger, K., és Eucker, J. (2012).A Metformin és az mTOR inhibitor everolimus (RAD001) in vitro érzékenyíti az emlőráksejteket a kemoterápiás gyógyszerek citotoxikus hatására. Rákellenes szerek. 32, 1627–1637.
Liu, X., Romero, I. L., Litchfield, L. M., Lengyel, E., and Locasale, J. W. (2016). A Metformin a központi szén-anyagcserét célozza megfeltárja a mitokondriális követelményeket az emberi rákokban. Sejt Metabolit. 24, 728–739.J. J., Gu, Y., Chen, S., Zhong, C., Xue, Y.,Zhang, Y., Lai, X., Wei, Y., Yu, S., Zhang, J., et al. (2014). A Metformin fokozzatamoxifen által közvetített tumor növekedés gátlása ER-pozitív emlőkarcinómában. BMCCancer 14, 172.
Manthravadi, S., Shrestha, A., and Madhusudhana, S.(2016). A sztatinhasználat hatása a rák kiújulására és mortalitására a mellrákban: szisztematikus áttekintés és metaanalízis. Int. J. Rák 139, 1281-1288.Mark, M., Klingbiel, D., Mey, U., Winterhalder, R., Rothermundt, C., Gillessen, S., von Moos, R., Pollak, M., Manetsch, G., Strebel, R., et al. (2019). A Metformin Abirateronhoz való hozzáadásának hatása a metasztatikus kasztrációval szemben rezisztens prosztatarákos betegek abirateron-kezelés alatt (Metabo-Pro): 2.fázisú kísérleti vizsgálat. Clint. Genitourin. Rák 17, e323-e328.
Martin-Castillo, B., Pernas, S., Dorca, J., A. S., A. S., A. S.,A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., A. S., et al. (2018). Trasztuzumabbal és kemoterápiával kombinált neoadjuváns metformin 2. fázisú vizsgálata korai HER2-pozitív emlőrákban szenvedő nőknél: a METTEN-vizsgálat. Oncotarget 9.35687–35704.Mokhtari, R. B., Homayouni, T. S., Baluch, N., Morgatskaya, E., Kumar, S., Das, B. és Yeger, H. (2017). Kombinált terápia a rák elleni küzdelemben. Oncotarget 8, 38022-38043.A. O., Seeger, H. és Wallwiener, D. (2004).A sztatinok gátló hatása az emberi emlőrák proliferációjára cells.Int J. Clin. Pharmacol. Ott. 42, 695–700.
Mukhopadhyay, T., Sasaki, J., Ramesh, R., and Roth, J. A. (2002). A mebendazol hatékony tumorellenes hatást vált ki az emberi rákos sejtvonalakra mind in Vitro, mind in Vivo. Clint. Rák Res. 8, 2963-2969.
Murtola, T. J., Visvanathan, K., Artama, M., Vainio, H. és Pukkala, E. (2014). Statin használata és a mellrák túlélése: országos kohort tanulmány Finnországból. PloS One 9, e110231.
Nanni, O., Amadori, D., De Censi, A., Rocca, A., Freschi, A., Bologna, A., Gianni, L., Rosetti, F., Amaducci, L., Cavanna,L., et al. (2019). Metformin plusz kemoterápia, szemben a kemoterápiával önmagában a HER2-negatív metasztatikus emlőrák első vonalbeli kezelésében. A Mymerandomizált, 2. fázisú klinikai vizsgálat. A Mellrák Res. Kezelésére. 174, 433–442.
Nimako, G. K., Wintrob, Z. A. P., Sulik, D. A., Donato, J. L. és Ceacareanu, A. C. (2017). Szinergikus előnye a sztatin és Metforminin gastrointestinalis malignus tumorok. J. Pharm. Pract. 30, 185–194.Niraula, S., Dowling, R. J. O., Ennis, M., Chang, M. C., Kész, S. J., Hood, N., Escallon, J., Leong, W. L., McCready, D. R., Reedijk, M., et al. (2012). Metformin korai emlőrákban: a neoadjuváns vizsgálat esélyes ablaka. A Mellrák Res. Kezelésére. 135, 821–830.
Nygren, P. és Larsson, R. (2014). A gyógyszer áthelyezése a padról az ágyra: tumor remisszió az antihelmintikus gyógyszer által mebendazolein refrakter metasztatikus vastagbélrák. Acta Oncol. 53, 427–428.E. A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A., A.. (2015). A biguanidok metformin és fenformin gátolják az emlőrák lokális és metasztatikus növekedését mind a neoplasztikus, mind a mikrokörnyezeti sejtek megcélzásával. Int. J. Rák 136, E534-544.
Ozsvari, B., Sotgia, F. és Lisanti, M. P. (2017). Új mutáció-független megközelítés a rákterápiában: az onkogén RAS Andmyc gátlása a mitokondriális biogenezis megcélzásával. Öregedés 9, 2098-2116.
Pantziarka, P., Bouche, G., Meheus, L., Sukhatme, V.,and Sukhatme, V. P. (2014). Repurposing gyógyszerek onkológiában (ReDO)—mebendazole asan rákellenes szer. Ecancermedicalscience 8.
Peiris-Pag Xhams, M., Sotgia, F. és Lisanti, M. P.(2015). Doxiciklin és a DNS-károsodás terápiás célzása ráksejtek: régi gyógyszer, új cél. Oncoscience 2, 696-699.Rahmani, J., Manzari, N., Thompson, J., Gudi, S. K., Chhabra, M., Naik, G., Mousavi, S. M., Varkaneh, H. K., Clark, C. és Zhang, Y.(2019). A metformin hatása az emlőrákkal kapcsolatos biomarkerekre: randomizált klinikai vizsgálatok szisztematikus áttekintése, metaanalízise és dózis-válasza. Clint. Ford. Onkol.Scatena, C., Roncella, M., Di Paolo, A., Aretini, P., Menicagli, M., Fanelli, G., Marini, C., Mazzanti, C. M., Ghilli, M., Sotgia, F., et al. (2018). A doxiciklin, a mitokondriális biogenezis inhibitora, hatékonyan csökkenti a rákos őssejteket (CSCs) korai emlőrákos betegeknél: aklinikai kísérleti vizsgálat. Elöl. Onkol. 8.Seeger, H., Wallwiener, D. és Mueck, A. O. (2003).A sztatinok in vitro gátolhatják az emberi emlőrákos sejtek proliferációját. Felh.Clint. Endokrinol. Cukorbetegség Ki. J. Ger. Soc. Endokrinol. Ger. Diabetes Assoc.111, 47–48.Skoda, J., Borankova, K., Jansson, P. J., Huang, M. L.-H., Veselska, R. és Richardson, D. R. (2019). A mitokondriumok farmakológiai célzása a rákos őssejtekben: egy ősi organella a rákellenes terápiák kereszteződésében. Pharmacol. Res. 139, 298-313.Sonnenblick, A., Agbor-Tarh, D., Bradbury, I., DiCosimo, S., Azim, H. A., Fumagalli, D., Sarp, S., Wolff, A. C., Andersson, M., Kroep, J., et al. (2017). A cukorbetegség, az inzulin és a Metformin alkalmazásának hatása a humán epidermális növekedési faktor Receptor 2-pozitív elsődleges emlőrákban szenvedő betegek kimenetelére: elemzés az ALTTO III. fázisú randomizált vizsgálatból. J. Clin. Onkol. 35, 1421–1429.
Van Wyhe, R. D., Rahal, O. M., és Woodward, W. A.(2017). A sztatinok hatása az emlőrák kiújulására és mortalitására: áttekintés.A Mellrák Célok Ther. 9, 559–565.
Vazquez-Martin, A., Oliveras-Ferraros, C., CUF,S., Del Barco, S., Martin-Castillo, B., Lopez-Bonet, E. és Menendez, J. A. (2011).Az antidiabetikus gyógyszer metformin elnyomja a metasztázishoz kapcsolódó proteinCD24 – et az MDA-MB-468 hármas negatív emlőrákos sejtekben. Onkol. REP. 25,135–140.B. A., B. A., B. A., B. A., B. A., B. A., B. A.,B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A., B. A. (2012).A fluvasztatin és a zoledronicacid transzkriptom analízise és in vivo aktivitása egér emlőrák metasztázis modelljében. Mol. Pharmacol. 82, 521–528.Wahdan-Alaswad, R. S., Cochrane, D. R., Spoelstra, N. S., Howe, E. N., Edgerton, S. M., Anderson, S. M., Thor, A. D. és Richer, J. K. (2014). A metformin által kiváltott hármas negatív emlőrákos sejtek elpusztításaa zsírsav-szintáz miRNS-193b-n keresztül történő csökkentésével. Rák 5,374-389.Wang, Z.-S., Huang, H.-R., Zhang, L.-Y., Kim, S.,ő, Y., Li, D.-L., Farischon, C., Zhang, K., Zheng, X., Du, Z.-Y., et al. (2017).A Metformin és az atorvasztatin inkombinációjának prosztatarákos sejtekre gyakorolt gátló hatásainak mechanisztikus vizsgálata in Vitro és in Vivo. Biol. Pharm. Baromság.40, 1247–1254.Bertucci, P., Birnbaum, D., Van Laere, S. et al. (2015). A szimvasztatin a FOXO3a szabályozásával megakadályozza a hármas negatív emlőrákmetasztázisát A preklinikai modellekben. mellrák. Treat. 154, 495–508.
Xu, H., Chen, K., Jia, X., Tian, Y., Dai, Y., Li, D., Xie, J., Tao, M. és Mao, Y. (2015). A Metformin használata jobba cukorbetegségben szenvedő emlőrákos betegek túlélése: metaanalízis. Teonológus 20, 1236-1244.G. A., G. A., G. A., G. A., G. A., G. A., G. A., G. A.,G. A., G. A., G. A., G. A., G. A., G. A., G. A., G. A., G. A., G. A., G. A., G. A.,G. A., G. A., G. A., G. A., G. A., G. A., G. A., G. A., G. A., G. A., G. A., G. A., G. A. (2019). Metformin, everolimus és exemestane kombinációjának hatékonysága és biztonságossága túlsúlyos és elhízott posztmenopauzás betegeknél metasztatikus,hormonreceptor-pozitív, HER2-negatív emlőrákban: fázis II vizsgálat.Fektessen be. Új Gyógyszerek 37, 345-351.
Yao, H., ő, G., Yan, S., Chen, C., Song, L., Rosol, T.J. és Deng, X. (2017). Hármas negatív emlőrák: van-e kezelésa horizonton? Oncotarget 8, 1913-1924.
Zhang, L., Guo, M., Li, J., Zheng, Y., Zhang, S.,Xie, T. és Liu, B. (2015). A potenciális Atg4bagonista (Flubendazol) rendszerbiológián alapuló felfedezése, amely autofágiát indukál az emlőrákban. Mol. Biosziszt.11, 2860–2866.
Zhang, L., Xu, L., Zhang, F. és Vlashi, E. (2017).A doxiciklin gátolja a rák őssejt fenotípusát ésepithelialis-mesenchymalis átmenet emlőrákban. Sejtciklus Georget. Tex16, 737-745.
Zhang, L., Bochkur Dratver, M., Yazal, T., Dong, K., Nguyen, A., Yu, G., Dao, A., Bochkur Dratver, M., Duhachek-Muggy, S., Bhat,K., et al. (2019a). A mebendazol fokozza a sugárterápiát hármas Negatívbanmellrák. Int. J. Sugárzik. Onkol. Biol. Phys. 103, 195–207.
Zhang, Y., Storr, S. J., Johnson, K., Green, A. R.,Rakha, E. A., Ellis, I. O., Morgan, D. A. L. és Martin, S. G. (2014). A metformin és az AMPK bevonása a radioterápiával kezelt luminalis versusbasal-szerű emlőrák radioreálválaszába és prognózisába. Oncotarget 5, 12936-12949.
Zhang, Z.-J., Yuan, J., Bi, Y., Wang, C., és Liu, Y.(2019b). A metformin hatása az emlőrák biomarkereire és túlélésére-randomizált klinikai vizsgálatok szisztematikus áttekintése és metaanalízise. Pharmacol.Res. 141, 551-555.
Zhong, S., Zhang, X., Chen, L., Ma, T., Tang, J., andZhao, J. (2015). Sztatinhasználat és mortalitás daganatos betegeknél: megfigyelési vizsgálatok szisztematikus áttekintése és meta-analízise. Rák Kezelésére. Rev. 41, 554-567.
