
Anek Suwannaphoom
Les raffineries utilisent d’énormes quantités d’énergie thermique pour traiter le pétrole brut.
La plupart des chimistes industriels passent leurs journées à séparer les composants de grandes quantités de mélanges chimiques sous des formes pures ou plus pures. Les procédés impliqués, tels que la distillation, représentent 10 à 15 % de la consommation mondiale d’énergie1,2.
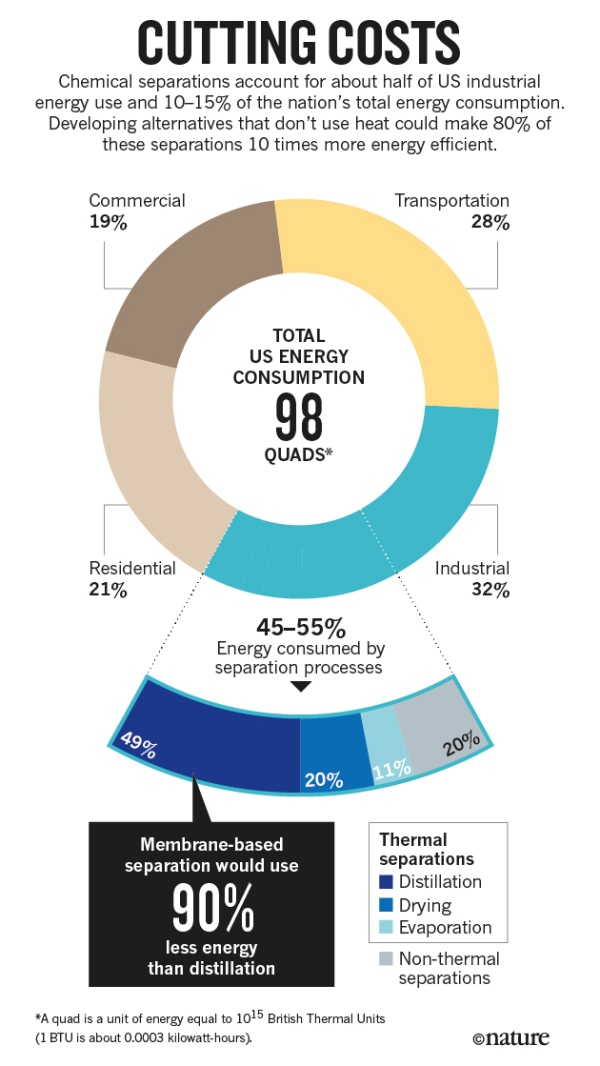
Les méthodes de purification des produits chimiques plus économes en énergie pourraient, si elles étaient appliquées aux seuls secteurs américains de la fabrication du pétrole, des produits chimiques et du papier, économiser 100 millions de tonnes d’émissions de dioxyde de carbone et 4 milliards de dollars de coûts énergétiques par an3 (voir « Réduction des coûts »). D’autres méthodes permettraient d’exploiter de nouvelles sources de matériaux, par exemple en extrayant des métaux de l’eau de mer.
Malheureusement, les alternatives à la distillation, telles que la séparation des molécules en fonction de leurs propriétés chimiques ou de leur taille, sont sous-développées ou coûteuses à mettre à l’échelle. Les ingénieurs de l’industrie et du milieu universitaire doivent développer des membranes meilleures et moins chères et d’autres moyens de séparer les mélanges de produits chimiques qui ne dépendent pas de la chaleur.
Ici, nous mettons en évidence sept processus de séparation chimique qui, s’ils étaient améliorés, récolteraient de grands avantages mondiaux. Notre liste n’est pas exhaustive; presque tous les produits chimiques commerciaux proviennent d’un processus de séparation qui pourrait être amélioré.
Sept séparations
Hydrocarbures du pétrole brut. Les principaux ingrédients de la fabrication des combustibles fossiles, des plastiques et des polymères sont les hydrocarbures. Chaque jour, les raffineries du monde entier traitent environ 90 millions de barils de pétrole brut, soit environ 2 litres par personne sur la planète. La plupart le font par distillation atmosphérique, qui consomme environ 230 gigawatts (GW) dans le monde3, soit l’équivalent de la consommation totale d’énergie du Royaume-Uni en 2014, soit environ la moitié de celle du Texas. Dans une raffinerie typique, 200 000 barils de pétrole brut par jour sont chauffés dans des colonnes de 50 mètres de haut pour libérer des milliers de composés en fonction de leurs points d’ébullition. Des gaz légers émergent au sommet frais (autour de 20 °C); des fluides progressivement plus lourds partent aux points les plus bas et les plus chauds (jusqu’à 400 °C).
Source: Données de la Réf. /EIE des États-Unis
Il est difficile de trouver une alternative à la distillation car le pétrole brut contient de nombreuses molécules complexes, dont certaines ont une viscosité élevée, et une myriade de contaminants, y compris des composés soufrés et des métaux tels que le mercure et le nickel. Il est possible en principe de séparer les hydrocarbures en fonction de leurs propriétés moléculaires, telles que l’affinité chimique ou la taille moléculaire. Les méthodes de séparation à membrane, ou d’autres méthodes non thermiques, peuvent être d’un ordre de grandeur plus économes en énergie que les séparations à entraînement thermique qui utilisent la distillation. Mais peu de recherches ont été faites.
Les chercheurs doivent trouver des matériaux capables de séparer plusieurs familles de molécules en même temps, et qui fonctionnent aux températures élevées nécessaires pour maintenir la circulation des huiles lourdes sans être bloqués par les contaminants.
Uranium de l’eau de mer. L’énergie nucléaire sera cruciale pour la production future d’énergie à faible émission de carbone. Bien que la trajectoire de l’industrie nucléaire soit incertaine, aux taux de consommation actuels, les réserves géologiques connues d’uranium (4,5 millions de tonnes) peuvent durer un siècle4. Plus de 4 milliards de tonnes d’uranium se trouvent dans l’eau de mer à des niveaux de partie par milliard.
Les scientifiques ont cherché des moyens de séparer l’uranium de l’eau de mer4 pendant des décennies. Il existe des matériaux capables de capturer l’uranium, tels que des polymères poreux contenant des groupes amidoxime. Mais ces « cages » moléculaires capturent également d’autres métaux, notamment le vanadium, le cobalt et le nickel.
Les chimistes doivent mettre au point des procédés pour éliminer ces métaux tout en purifiant et en concentrant l’uranium de l’eau de mer. En 1999-2001, des équipes japonaises ont capturé environ 350 grammes d’uranium à l’aide d’un tissu adsorbant4. Le démarrage d’une nouvelle centrale nucléaire nécessite des centaines de tonnes de combustible d’uranium, de sorte que l’échelle de ces processus devrait être considérablement augmentée. En particulier, des efforts pour réduire les coûts des matériaux adsorbants sont nécessaires.
Des technologies similaires pourraient capturer d’autres métaux valeurs4, tels que le lithium, qui est utilisé dans les batteries. La quantité de lithium dissoute dans les océans est dix fois supérieure à celle des ressources terrestres connues; la taille limitée de ces dernières peut devenir un obstacle à long terme au stockage de l’énergie.
Alcènes à partir d’alcanes. La fabrication de plastiques tels que le polyéthène et le polypropène nécessite des alcènes-hydrocarbures tels que l’éthène et le propène, également appelés oléfines. La production annuelle mondiale d’éthène et de propène dépasse les 200 millions de tonnes, soit environ 30 kilogrammes par personne sur la planète. La séparation industrielle de l’éthène de l’éthane repose généralement sur une distillation cryogénique à haute pression à des températures aussi basses que -160 ° C. La purification du propène et de l’éthène représente à elle seule 0,3% de la consommation énergétique mondiale, soit à peu près l’équivalent de la consommation énergétique annuelle de Singapour.
Comme pour le pétrole brut, trouver des systèmes de séparation qui ne nécessitent pas de changements d’une phase à l’autre pourrait réduire d’un facteur dix l’intensité énergétique du processus (énergie utilisée par unité de volume ou de poids de produit) et compenser les émissions de carbone d’une quantité similaire5. Par example, on développe des membranes carbonées poreuses capables de séparer les alcènes gazeux et les alcanes (également appelés paraffines) à température ambiante et à des pressions douces (inférieures à 10 bars)6. Mais ceux-ci ne peuvent pas encore produire les alcènes purs à plus de 99,9% nécessaires à la fabrication de produits chimiques.
À court terme, des techniques de séparation « hybrides » pourraient aider — des membranes peuvent être utilisées pour la séparation en vrac et la distillation cryogénique pour le « polissage » du produit. De telles approches réduiraient l’intensité énergétique de la production d’alcènes d’un facteur 2 ou 3, jusqu’à ce que les membranes deviennent suffisamment bonnes pour remplacer entièrement la distillation. Un obstacle majeur est la mise à l’échelle des membranes — l’industrie pourrait nécessiter des surfaces allant jusqu’à 1 million de mètres carrés. Le déploiement à cette échelle nécessitera de nouvelles méthodes de fabrication ainsi que des progrès dans les propriétés des matériaux.
Gaz à effet de serre provenant des émissions diluées. Les émissions anthropiques de CO2 et d’autres hydrocarbures, tels que le méthane libéré par les raffineries et les puits, sont des facteurs clés du changement climatique mondial. Il est coûteux et techniquement difficile de capturer ces gaz à partir de sources diluées telles que les centrales électriques, les gaz d’échappement des raffineries et l’air.
Les liquides tels que la monoéthanolamine réagissent facilement avec le CO2, mais comme il faut appliquer de la chaleur pour éliminer le CO2 du liquide résultant, le procédé n’est pas économiquement viable pour les centrales électriques. Si cette approche était appliquée à toutes les centrales électriques des États-Unis, la capture du CO2 pourrait coûter 30 % de la croissance du produit intérieur brut du pays chaque année7. Des méthodes moins coûteuses pour capturer les émissions de CO2 et d’hydrocarbures avec des coûts énergétiques minimes doivent être développées.
Un facteur de complication est de décider quoi faire avec le produit purifié. Le CO2 pourrait être utilisé dans une méthode de production de pétrole brut connue sous le nom de récupération assistée du pétrole, ou dans l’agriculture verticale et comme matières premières chimiques et de bioraffinerie. Mais les activités humaines émettent tellement de gaz8 qu’en pratique, une grande partie de ce gaz devra être stocké à long terme dans des réservoirs souterrains, ce qui soulève d’autres problèmes.

ORNL
Les polymères à haute capacité (HiCap) peuvent séparer des métaux tels que l’uranium de la solution.
Métaux des terres rares provenant des minerais. Les 15 métaux lanthanides, ou éléments de terres rares, sont utilisés dans les aimants, dans les technologies d’énergie renouvelable et comme catalyseurs dans le raffinage du pétrole. Les lampes fluorescentes compactes utilisent de l’europium et du terbium, par exemple, et les convertisseurs catalytiques reposent sur le cérium. La production économique de terres rares est un problème de séparation, pas de disponibilité. Malgré leur nom, la plupart des éléments sont beaucoup plus abondants dans la croûte terrestre que l’or, l’argent, le platine et le mercure. Malheureusement, les terres rares se trouvent à l’état de traces dans les minerais et sont souvent mélangées parce qu’elles sont chimiquement similaires.
La séparation des terres rares des minerais nécessite des approches mécaniques (telles que la séparation magnétique et électrostatique) et un traitement chimique (tel que la flottation de mousse). Ceux-ci sont inefficaces: ils doivent composer avec les compositions complexes des minerais extraits, utiliser de grands volumes de produits chimiques et produire beaucoup de déchets et de sous-produits radioactifs. Des améliorations sont cruellement nécessaires.
Le recyclage des terres rares à partir de produits mis au rebut augmente. Des procédés sur mesure pourraient être conçus car les compositions chimiques et physiques des produits sont bien définies. Diverses méthodes d’extraction métallurgique et en phase gazeuse ont été explorées, mais les terres rares recyclées ne font pas encore partie de la plupart des chaînes d’approvisionnement9,10. Des recherches sont nécessaires pour réduire l’impact écologique des éléments clés contenant des terres rares sur l’ensemble de leur cycle de vie.
Dérivés benzéniques les uns des autres. Les chaînes d’approvisionnement de nombreux polymères, plastiques, fibres, solvants et additifs pour carburants dépendent du benzène, un hydrocarbure cyclique, ainsi que de ses dérivés tels que le toluène, l’éthylbenzène et les isomères du xylène. Ces molécules sont séparées dans des colonnes de distillation, avec des coûts énergétiques globaux combinés d’environ 50 GW, suffisants pour alimenter environ 40 millions de foyers.
Les isomères du xylène sont des molécules présentant de légères différences structurelles les unes des autres qui conduisent à des propriétés chimiques différentes. Un isomère, le para-xylène (ou p-xylène), est le plus souhaitable pour la production de polymères tels que le polyéthylène téréphtalate (PET) et le polyester; plus de 8 kilogrammes de p-xylène sont produits par habitant chaque année aux États-Unis. La taille et les points d’ébullition similaires des différents isomères du xylène les rendent difficiles à séparer par des méthodes classiques telles que la distillation.
Les progrès réalisés dans les membranes ou les sorbants pourraient réduire l’intensité énergétique de ces processus. Comme pour d’autres procédés chimiques à l’échelle industrielle, la mise en œuvre de technologies alternatives de séparation des dérivés du benzène nécessitera que leur viabilité soit prouvée à des échelles successivement plus grandes avant leur mise en œuvre commerciale. La construction d’une usine chimique peut coûter 1 milliard de dollars ou plus, les investisseurs veulent donc être sûrs qu’une technologie fonctionnera avant de construire de nouvelles infrastructures.
« Un obstacle majeur est la mise à l’échelle des membranes. »
Trace les contaminants de l’eau. Le dessalement — que ce soit par distillation ou filtration membranaire – nécessite beaucoup d’énergie et de capital, ce qui le rend irréalisable dans de nombreuses zones sèches. La distillation n’est pas la solution: la thermodynamique définit la quantité minimale d’énergie nécessaire pour générer de l’eau potable à partir de l’eau de mer, et la distillation utilise 50 fois plus d’énergie que cette limite fondamentale.
La filtration par osmose inverse, un procédé qui applique une pression à travers une membrane à de l’eau salée pour produire de l’eau pure, ne nécessite que 25% d’énergie en plus que la limite thermodynamique5. Mais les membranes à osmose inverse traitent l’eau à des débits limités, nécessitant de grandes installations coûteuses pour produire un débit suffisant. L’osmose inverse de l’eau de mer se fait déjà à l’échelle commerciale au Moyen-Orient et en Australie. Mais les difficultés pratiques liées à la manipulation d’eau plus polluée – y compris la corrosion, la formation de biofilms, l’entartrage et le dépôt de particules — signifient que des systèmes de prétraitement coûteux sont également nécessaires.
Développer des membranes plus productives et plus résistantes à l’encrassement réduirait les coûts d’exploitation et d’investissement des systèmes de dessalement au point que la technique est commercialement viable même pour des sources d’eau très polluées.
Prochaines étapes
Les chercheurs universitaires et les décideurs politiques devraient se concentrer sur les questions suivantes.
Tout d’abord, les chercheurs et les ingénieurs doivent envisager des mélanges chimiques réalistes. La plupart des études universitaires se concentrent sur des produits chimiques uniques et déduisent le comportement des mélanges à l’aide de ces informations. Cette approche risque de manquer des phénomènes qui ne se produisent que dans les mélanges chimiques et ignore le rôle des contaminants à l’état de traces. Les universitaires et les chefs de file de la recherche et du développement industriels devraient établir des mélanges substitutifs pour les séparations communes qui incluent les principaux composants chimiques et les contaminants communs.
Deuxièmement, l’économie et la durabilité de toute technologie de séparation doivent être évaluées dans le contexte d’un processus chimique complet. Des paramètres de performance tels que le coût par kilogramme de produit et la consommation d’énergie par kilogramme devraient être utilisés. La durée de vie et les coûts de remplacement des composants tels que les modules membranaires ou les matériaux sorbants doivent être pris en compte.
Troisièmement, il faut sérieusement tenir compte, dès le début du développement technologique, de l’échelle à laquelle le déploiement est nécessaire. Des infrastructures physiques telles que des bancs d’essai universitaires et industriels seront nécessaires pour faire passer les nouvelles technologies du laboratoire à des échelles pilotes afin de réduire tout risque perçu. Pour gérer cela, il faudra que les universités, les organismes gouvernementaux et les partenaires de l’industrie collaborent.
Quatrièmement, la formation actuelle des ingénieurs chimistes et des chimistes dans les séparations met souvent l’accent sur la distillation. L’exposition à d’autres opérations — telles que l’adsorption, la cristallisation et les membranes – est cruciale pour développer une main-d’œuvre capable de mettre en œuvre toute la gamme de technologies de séparation dont l’avenir aura besoin.
