Science des chélants
Un chélant, parfois appelé séquestrant ou constructeur, est une molécule spécialisée conçue pour se lier à des ions métalliques chargés positivement, le plus souvent du calcium et du magnésium, en solution et empêcher ainsi ces ions de former des précipités insolubles avec d’autres ions pouvant être présents. Il existe deux types de chélants de base, désignés comme durs et mous:
- Les chélants durs, par exemple l’EDTA (acide éthylènediamine tétra acétique) et le NTA (acide Nitrilo triacétique), forment des complexes très stables avec un 1:1 stœchiométrie. C’est-à-dire qu’une molécule d’EDTA réagit avec un seul ion métallique.
- Les chélants mous, par exemple les polymères de l’acrylique et de l’acide maléique, forment des complexes moins stables et fonctionnent en empêchant la croissance des cristaux plutôt que par une véritable chélation.
Les ions calcium et magnésium forment des précipités insolubles très stables avec l’ion carbonate. Le bicarbonate est omniprésent dans les eaux de surface. Il est déprotoné pour donner du carbonate par le pH élevé de la plupart des formulations nettoyantes. Les précipités insolubles sont difficiles à éliminer sans l’utilisation d’un nettoyant acide. Ces dépôts difficiles à éliminer sont appelés tartre d’eau dure, et donc l’eau contenant des ions calcium et magnésium est appelée eau dure. Il existe deux méthodes courantes pour traiter l’eau dure. La première consiste à utiliser de l’eau adoucie. L’eau ramollie élimine les ions calcium et magnésium. Ceci est souvent accompli par l’utilisation d’un adoucisseur d’eau qui échange les ions sodium contre les ions calcium et magnésium en solution. La deuxième méthode consiste à utiliser des chélateurs dans la formulation du produit de nettoyage. La chélation des ions calcium et magnésium en solution empêche également efficacement la formation de ces dépôts.
Les ions calcium et magnésium forment également des précipités insolubles avec de nombreux tensioactifs anioniques, notamment les carboxylates d’acides gras (savon). La formation de complexes de savon calcique est si efficace que la concentration de tensioactif libre disponible pour le nettoyage est réduite à zéro jusqu’à ce que tout le calcium ait été éliminé de la solution, soit par chélation, soit par formation de l’adduit de savon insoluble. Sans le chélant présent dans un produit de nettoyage, il faudrait plus de tensioactif pour s’assurer qu’une concentration efficace de tensioactif libre soit disponible pour le nettoyage. En d’autres termes, le consommateur devrait utiliser davantage de produit de nettoyage pour obtenir le résultat souhaité. De plus, l’adduit de savon de calcium insoluble précipiterait de la solution sur la surface à nettoyer, ce qui donnerait un aspect terne et une sensation de raideur sur le tissu lavé. Ainsi, les chélateurs utilisés à ces fins sont parfois appelés « constructeurs » car ils aident à renforcer les performances du tensioactif.
En plus d’adoucir l’eau de la solution de nettoyage, les chélants sont également efficaces pour éliminer certaines taches, en particulier celles qui ont une forte concentration de calcium comme les taches de fromage. Les taches ont une structure moléculaire complexe et variée et beaucoup comprennent des ions métalliques qui réticulent et stabilisent la structure des taches. Les chélants présents dans la solution de nettoyage vont se lier à ces différents ions métalliques en aidant à les éliminer de la tache, affaiblissant ainsi la structure de la tache et facilitant son élimination.
Au-delà du calcium et du magnésium, les chélants se lient à tous les ions métalliques polyvalents en solution. Le fer et le manganèse, bien que moins répandus, peuvent également entraîner des problèmes de nettoyage importants, notamment la formation de précipités insolubles tels que l’oxyde de fer, la rouille et le dioxyde de manganèse. Par conséquent, les nettoyants spécialisés sont souvent formulés avec des chélateurs de fer très efficaces pour se lier à ces ions, éliminant à nouveau les problèmes qu’ils pourraient autrement causeror ou en aidant à éliminer les taches de rouille et de fer qui se sont déjà formées.
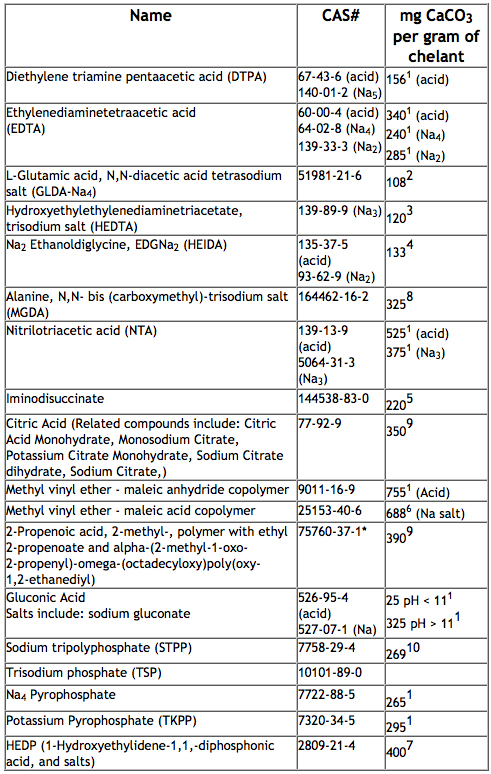
Le tableau ci-dessous présente de nombreux exemples d’agents chélatants utilisés dans des produits formulés et leur capacité théorique à se lier ou à séquestrer le calcium de l’eau pour améliorer les performances de nettoyage :