Was ist die Dichte der Zellen?
Lesemodus
Die Dichte des biologischen Materials ist für das Absetzen der Zellen auf dem Boden unserer Laborröhrchen und Multi-Well-Platten verantwortlich und dient als Grundlage für das routinemäßige Zentrifugieren, das zum täglichen Leben so vieler Biologen gehört. Dieselben Dichteunterschiede zwischen Zellen und ihrem wässrigen Äußeren sind auch die Grundlage für den Kontrast, den wir in phasenmikroskopischen Bildern beobachten. Diese Unterschiede sind auch außerhalb des Labors wichtig. Zum Beispiel muss Plankton mit diesem Dichteunterschied kämpfen, um in einer Tiefe im Ozean zu bleiben, in der Sonnenlicht reichlich vorhanden ist, anstatt in die geschwärzten Tiefen zu sinken. Angesichts der Tatsache, dass die meisten Biologen und Biochemiker täglich die Trennung nach Dichte anwenden, erscheint es überraschend, wie selten Dichten wie die in Tabelle 1 gesammelten tatsächlich diskutiert werden.
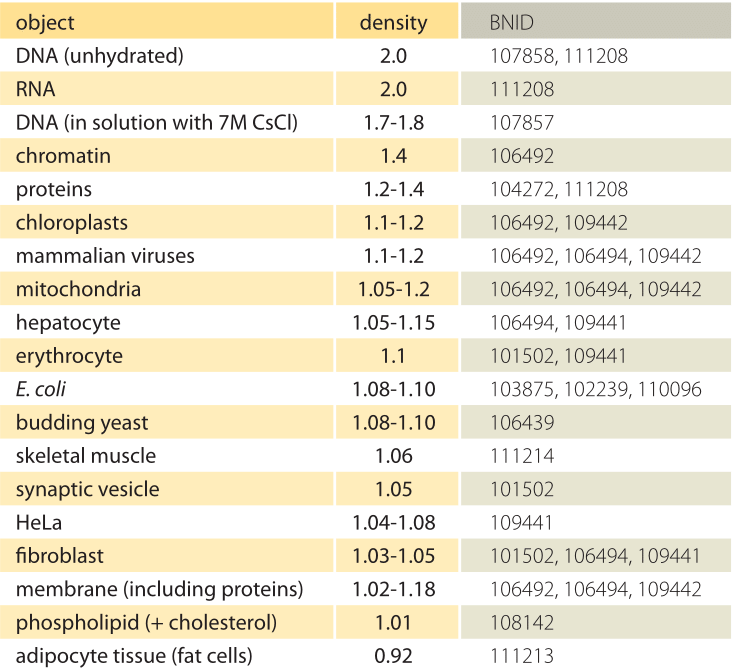
Tabelle 1: Dichten biologischer Objekte relativ zu Wasser. Dies entspricht fast der Angabe in Einheiten von g / ml oder 1000 kg/ m3. Die Werte werden in absteigender Reihenfolge sortiert. Sofern nicht anders angegeben, wurden die Werte in Saccharose oder Ficoll-Lösung gemessen.
Was ist die Grundlage für die unterschiedlichen Dichten verschiedener Organellen und Zelltypen? Diese Unterschiede sind zu einem großen Teil auf das Verhältnis zwischen Wassergehalt und Trockenmasse zurückzuführen. Proteine haben eine Dichte von ≈1,3-1,4 (BNID 104272, 101502) relativ zu Wasser (oder fast äquivalent in Einheiten von g / ml oder 1000 kg / m3). Bei dem Richtwert 1 für die Dichte von Wasser ergibt sich ein Spektrum von Zwischenwerten für die Zelldichte zwischen 1 und 1.3 werden basierend auf der relativen Häufigkeit von Proteinen und Wasser erhalten. Lipide befinden sich am unteren Ende neben Wasser mit einer Dichte von etwa 1 (BNID 108142). Im anderen Extremfall können Stärkekörnchen mit einer Dichte von ≈1,5 (BNID 103206) und Nukleotiden bei ≈1,7 die Gesamtmassebilanz in die entgegengesetzte Richtung verschieben.Die Kenntnis der Dichte basiert häufig auf dem Ort, an dem sich eine bestimmte biologische Komponente absetzt, wenn sie in einer Zentrifuge gesponnen wird, die einen Konzentrationsgradienten enthält, der häufig durch Saccharose oder im Fall von DNA Cäsiumchlorid erzeugt wird. Die Dichte spiegelt die Masse geteilt durch das Volumen wider, aber für geladene Verbindungen in Lösung wird die Dichte auch durch Schalen von sogenanntem gebundenem Wasser beeinflusst. Die Dichte wird dabei zu einer durch das gebundene Wasser verminderten effektiven Dichte und damit etwas abhängig von der Salzkonzentration (BNID 107858).
Die Sedimentationsrate, wie sie in einer Zentrifuge auftritt, wird in Einheiten von Svedberg quantifiziert, was der Ursprung der Namen 70S, 23S usw. ist. für das Ribosom und seine rRNA-Untereinheiten. Eine 23S-rRNA sedimentiert bei normaler Schwerkraft mit einer Geschwindigkeit von 23 × 10-12 m / s. In einer Ultrazentrifuge, die eine Beschleunigung von einer Million g erzeugt, skaliert die Geschwindigkeit proportional auf 23 × 10-6 m / s oder etwa 1 mm / min. Die Sedimentationsrate hängt von der Dichte, Größe und Form des Moleküls ab. Bei ähnlichen Formen und Dichten skaliert die Sedimentationsrate als Quadratwurzel der Molekülmasse. In solchen Fällen ist die Molekülmasse das Quadrat der Sedimentationsrate, so dass die 23S- und 16S-Untereinheiten des Ribosoms eine Molekülmasse mit einem Verhältnis von ungefähr (23/16) 2 oder ungefähr 2 aufweisen, was eng mit Messungen von 0,9 und 0 übereinstimmt.5 MDa jeweils (BNID 110972, 110967). In der Klinik wird routinemäßig die Sedimentationsrate von Erythrozyten (roten Blutkörperchen) zur Messung von Entzündungen verwendet. Raten, die viel höher als 10 mm / Stunde sind, weisen normalerweise auf das Vorhandensein des Pro-Sedimentationsfaktors Fibrinogen hin, der ein allgemeiner Indikator für einen entzündlichen Zustand ist.
Es ist bekannt, dass Wasser die am häufigsten vorkommende molekulare Fraktion von Zellen ist, aber wie reichlich genau? Wenn wir Gewebe von mehrzelligen Organismen untersuchen, ist das Ermitteln des Wassergehalts eine einfache Aufgabe, um die Masse des Gewebes vor und nach dem Trocknen zu messen. Aber wie kann man solche Messungen für Zellen durchführen? Wenn wir eine Masse von Zellen vor und nach dem Trocknen wiegen, wie messen wir dann nur die Zellen ohne Wasser um sie herum? Selbst nach der Zentrifugation verbleibt Wasser im Zellpellet, was zu Unklarheiten über die Trockenmasse selbst führt.
Wieder einmal kommt die Radioisotopenmarkierung zur Rettung (Cayley et al 1991). Zuerst wird markiertes Wasser (unter Verwendung von Tritium, 3H) in einem Zellpellet gemessen. Dies gibt die Summe des Wassers innerhalb und außerhalb der Zellen an. Dann misst eine andere lösliche Verbindung, die markiert ist, aber nicht in die Zelle gelangen kann, wie 14C-Inulin oder 3H-PEG, das Wasservolumen außerhalb der Zellen in einem zentrifugierten Pellet (beispielsweise in E. coli etwa 25-35% des Pelletvolumens (BNID)). Der Unterschied gibt den Wassergehalt in den Zellen an. Derartige Verfahren führen zu typischen Werten im Bereich von ≈60-65 Massen-% für knospende Hefen und rote Blutkörperchen über ≈70% für E. coli und die Amöbe D. discoideum bis hin zu ≈80% für Rattenmuskel- und Schweineherzgewebe (BNID 105938, 103689). Da der Trockensubstanzbeitrag von Bestandteilen der Dichte ≈1,3 (d.h. Proteinen) dominiert wird, führt dies zu der charakteristischen Gesamtdichte von ≈1,1 (BNID 103875, 106439, 101502). Aus diesen charakteristischen Anteilen kann auf eine Trockenmasse pro Volumen von etwa 300-500 mg/ml (BNID 108131, 108135, 108136) geschlossen werden, bei langsamem Wachstum können die Werte jedoch höher sein. Niedrige Dichten sind bei trockenen Samen und Unterwasserpflanzen üblich, die schwimmende Teile mit einer Dichte von weniger als dem umgebenden Wasser haben, wodurch sie schwimmen können. Dichten, die niedriger sind als die von Wasser, können entweder durch Gas wie in Seetang und einigen Bakterien oder durch Verwendung von gelösten Stoffen mit einem Molekulargewicht (MW) erreicht werden, das niedriger ist als das umgebende Medium (z. B. Ersetzen von Natrium durch MW≈23 durch Ammonium durch MW≈18) wie in den kleinen Krebstieren, antarktische Copepoden.Menschen bestehen zu etwa 60% aus Wasser (40% in Zellen, 15% in interstitieller Flüssigkeit und 5% im Blutplasma, BNID 110743) und die meisten von uns haben die starken Auswirkungen der Dehydration erlebt, nachdem sie vergessen haben, auch nur ein paar Gläser zu trinken. Einige Zellen können jedoch überraschend robust gegenüber einer Abnahme ihres Wassergehalts sein. Zum Beispiel wurde die Rate des Glukosestoffwechsels in Rattenleberzellen nicht durch einen 25% igen Verlust an intrazellulärem Wasser beeinflusst. Eine solche Abnahme kann durch Osmose erreicht werden – Änderung der Tonizität (gelöste Konzentration) der extrazellulären Flüssigkeit. Ein extremes Beispiel ist das der bemerkenswerten Salzgarnelen. Leben in Umgebungen, in denen die äußere Salzkonzentration schwanken und sehr hoch sein kann, es wurde gezeigt, dass Zysten, die auf nur ausgetrocknet werden können 2% Wasser ohne irreversible Schäden und bei Flüssigkeitszufuhr von mehr als 37% (nur etwa die Hälfte seines vollständig hydratisierten Zustands) Ihre Physiologie verhält sich normal. Diese Robustheit angesichts des Wasserverlustes könnte mit einer Unterscheidung zusammenhängen, die manchmal zwischen zwei Formen von Wasser im Zellinneren gemacht wird. Normales „Schüttwasser“, das besser dispensierbar ist, und „gebundenes Wasser“, das mit den zellulären Komponenten assoziiert ist und als Lösungsmittel dient, das für das reibungslose Funktionieren unerlässlich ist.





