Die Verwendung einer konsistenten Terminologie innerhalb und zwischen Studien ist entscheidend für einen effizienten Studienprozess. CDISC-Standards wie CDASH, SDTM, SEND und ADaM standardisieren die Strukturen, die beim Sammeln und Übermitteln von Daten verwendet werden, aber was ist mit den Datenwerten selbst?Dieser Beitrag gibt einen Überblick über die standardisierte kontrollierte Terminologie von CDISC und wie sie verwendet werden sollte, um Daten so zu sammeln und einzureichen, dass Studien beschleunigt und studienübergreifende Analysen ermöglicht werden.
Wenn Sie mehr über CDISC-Standards erfahren möchten, lesen Sie unsere Blogs Alles, was Sie über SDTM und Einführung in CDISC-Standards wissen müssen.
CDISC arbeitet mit NCI zusammen, um standardisierte Terminologie zu definieren
CDISC hat sich mit dem National Cancer Institute (NCI) zusammengetan, um die Terminologie in klinischen Studien einheitlicher zu gestalten. Durch diese Zusammenarbeit wurde ein Standardsatz an Terminologie definiert, der vierteljährlich aktualisiert wird, um semantische Konsistenz in allen Studien zu gewährleisten. Mit dieser Terminologie wird dieselbe Information in allen Studien auf die gleiche Weise dargestellt.
Nehmen wir ein einfaches Beispiel – Geschlecht:
- Sollte Männlich durch „Männlich“, „MÄNNLICH“, „M“ oder „1“ dargestellt werden?
- Wie soll jemand, der intersexuell ist, erfasst werden?
In früheren Zeiten wurden diese Informationen möglicherweise für jede Studie auf unterschiedliche Weise gesammelt. Der CDISC NCI-Terminologiestandard definiert jetzt, dass die einzigen zulässigen Optionen „F“ sind, „M“, „U“ und „UNDIFFERENZIERT“, und dass eine Person, die intersexuell ist, als „UNDIFFERENZIERT“ erfasst werden sollte. Sie können sehen, wie dieses sehr einfache Beispiel es bereits viel einfacher macht, die zugrunde liegenden Daten zu verstehen und für verschiedene Populationen über Studien hinweg leicht zu segmentieren.
![]() Hinweis
Hinweis
Der Datenstandardkatalog der FDA schreibt nun vor, dass die standardisierte NCI-Terminologie für alle neuen Studien verwendet wird. Dies erleichtert das Leben eines Reviewers erheblich, da er weiß, wie die Daten zu interpretieren sind.

Wie ist die CDISC-NCI-Terminologie definiert?
Die folgende Tabelle zeigt, wie die Standard-Sexterminologie definiert ist.
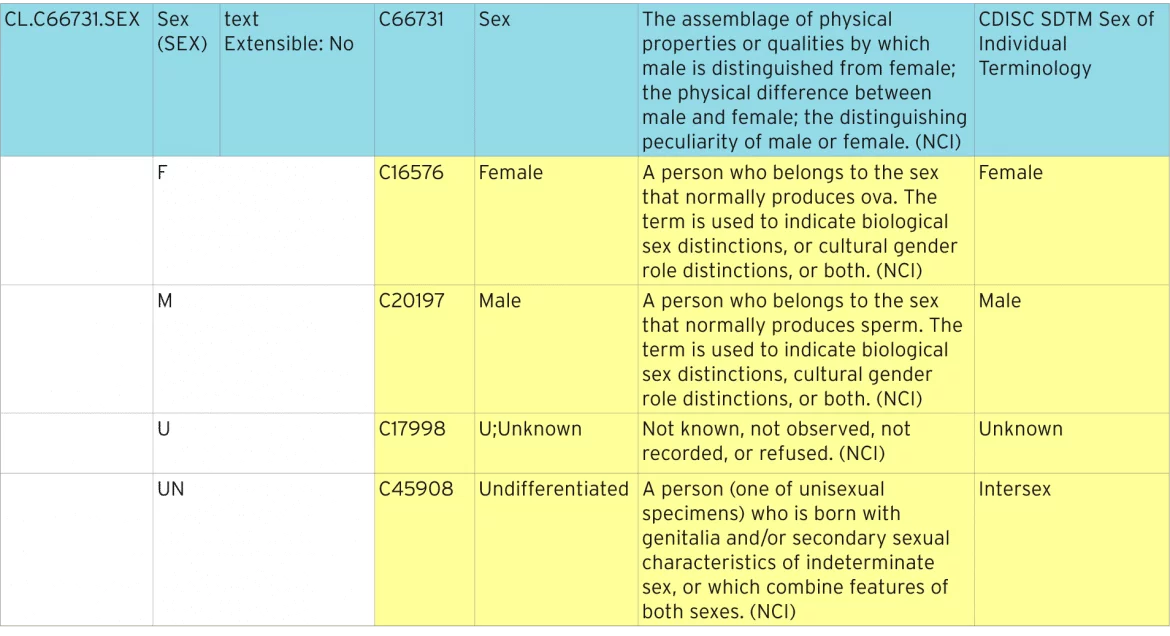
Identifizierung standardisierter Terminologie
Die blaue Linie stellt die Codeliste dar, die alle einzelnen Codes enthält. Die Codeliste hat einen Standard „C-Code“ von „C66731“. Jeder der einzelnen Codes hat einen eigenen C-Code, z.B. „C16576“. Diese C-Codes werden in ODM- und Define-XML-Metadaten verwendet, um Codelisten als NCI-Standardterminologie zu identifizieren.
Erweiterbarkeit
Diese Codeliste ist als nicht erweiterbar definiert, was bedeutet, dass sie überall dort, wo die Codeliste verwendet wird, keine Begriffe enthalten darf, die hier nicht aufgeführt sind. Für Codelisten, die erweiterbar sind, können zusätzliche Begriffe hinzugefügt werden. Diese zusätzlichen Begriffe müssen in Define-XML als erweiterte Begriffe beschrieben werden und dürfen nicht dupliziert oder Synonyme bestehender Begriffe sein.
Einreichungswert, Synonyme und bevorzugter Begriff
Der Einreichungswert ist das, was einer Regulierungsbehörde vorgelegt werden muss. Der tatsächlich in einem Formular angezeigte Wert kann unterschiedlich sein und möglicherweise eines der Synonyme oder der bevorzugte Begriff.
In vielen Farben erhältlich
Die NCI-Terminologiestandards sind in einer Reihe von Formaten für unterschiedliche Anforderungen erhältlich, darunter Excel, ODM, HTML und RDF. Das obige Beispiel stammt aus der Excel-Version.
Gruppiert in Teilmengen für CDASH, SDTM, ADaM und mehr
Der Einfachheit halber ist die NCI-Terminologie in eine Reihe von Teilmengen gruppiert.
- SDTM-Terminologie enthält Begriffe zur Verwendung in einer SDTM-basierten Einreichung
- CDASH-Terminologie enthält Begriffe zur Verwendung in einer CDASH-basierten Datenerfassung
- ADaM-Terminologie enthält Begriffe zur Verwendung in ADaM-Datensätzen
- SEND-Terminologie enthält Begriffe zur Verwendung in einer SEND-basierten Einreichung
- Protokollterminologie enthält Begriffe zur Verwendung mit dem Protocol Representation Model (PRM) und Clinical Trial Registry XML (CTR-XML)
Verwendung der CDISC NCI-Terminologie in einer Studie
Bei der Definition von Einreichungsmetadaten in Define-XML werden Codelisten verwendet, um feste Listen zu definieren von Werten für bestimmte Variablen. Gemäß der aktuellen FDA-Verordnung müssen diese Codelisten der standardisierten CDISC NCI-Terminologie entsprechen, sofern eine solche Terminologie vorhanden ist. Sie werden mit der standardisierten Terminologie verknüpft, indem den C-Codes Aliase hinzugefügt werden, z. B.:
<Alias Name="C66731" Context="nci:ExtCodeID"/>
Wenn Sie Metadaten zur Datenerfassung in ODM definieren, ist es nicht erforderlich, die standardisierte Terminologie zu verwenden. Dadurch entfällt jedoch die Notwendigkeit, Begriffe aus Ihren gesammelten Daten Ihren übermittelten Daten zuzuordnen. Dies vereinfacht Ihren End-to-End-Studienprozess erheblich und erhöht die Konsistenz zwischen den Studien.
Verwaltung von Aktualisierungen
Die Verwaltung von Terminologieupdates kann einen erheblichen Arbeitsaufwand darstellen, insbesondere wenn die Standards so regelmäßig aktualisiert werden. Woher wissen Sie, welche Studien oder Organisationsstandards von der neuen Terminologie betroffen sein könnten? Wie führen Sie dann die erforderlichen Updates effizient und zuverlässig durch?
Der einfachste Weg, dies zu verwalten, ist die Verwendung eines CDISC-fähigen Metadaten-Repositorys, mit dem Sie Organisationsstandards definieren können, die auf der standardisierten Terminologie basieren, und Ihre Studien aus diesen Standards erstellen können. Da das Repository die Beziehungen zwischen allen Standards und Ihren Studien versteht, kann es den Prozess der Aktualisierung auf neue Versionen der CDISC NCI-Terminologiestandards vereinfachen.
