Dringende Nachricht: Wenn ein relativ junger Patient mit Brustschmerzen in die Notaufnahme kommt, kann es eine „typische“ Ursache geben oder auch nicht. Eine schnelle Bewertung und genaue Bewertung der Risikofaktoren sind für eine effiziente Versorgung und häufig für das Überleben des Patienten von entscheidender Bedeutung.
Max Palatnik, MD
Fallpräsentation
Ein 35-jähriger Mann präsentierte um 21:59 Uhr eine Hauptbeschwerde über Brustschmerzen; Um 22:03 Uhr stellten wir Folgendes fest:
Temp: 98,9
Puls: 103
Resp: 16
Syst: 122
Diast: 69
O2Sat: 99%
Geschichte der gegenwärtigen Krankheit (22:47) (Wörtlich)
Pt. 38-jähriger Mann mit einer PMH von Myokarditis und Perikarditis in den Jahren 1983 und 1991, der um 6:30 Uhr zu Abend aß und anfing, Druck auf seine vordere Brust zu spüren, während er um 7:30 Uhr fernsah. – es fühlte sich an, als ob „jemand auf meiner Brust saß“. Assoziiertes Schluchzen und Strahlung in seine Schulter und linke Hand „Kribbeln“. Er hatte Sodbrennen, aber das fühlte sich anders an. Nahm Backpulver (das er normalerweise für sein Sodbrennen nimmt) und das half nicht. Keine Synkope, Übelkeit, Erbrechen, Fieber, RUQ-Schmerzen oder Nahrungsmittelunverträglichkeiten in der Vorgeschichte. Er hatte vor 2 Wochen einige virale Symptome (unproduktiver Husten, Nasennebenhöhlenentzündung und PND, die alle behoben sind.) Keine orthopnoe, PND, beziehung von schmerzen zu übung, brust trauma, pleuritic komponente
Vergangenheit Medizinische Geschichte/Triage
Medikamente, gemeinsame allergien: Keine
PMH: Myokarditis/Perikarditis
PSH: Keine
SocHx: nichtraucher
FamHx: Positive für CAD mit 52 jahre alte geschwister mit MI, vater CABG bei 53
Prüfung (22:52)
Allgemeine: Gut aussehende; gut aussehende genährt; in keiner offensichtlichen Not.
Kopf: Normozephal; atraumatisch.
Augen: PERLA; EOM intakt
HNO: TM ist normal; normale Nase; keine Rhinorrhoe, Der Hals ist rot und milde Exsudate.. Feuchte Schleimhäute.
Hals: Geschmeidig; nontender; keine zervikale Lymphadenopathie. Keine meningealen Zeichen
Kardiovaskulär: Normal S1, S2; kein Murmeln, Reiben oder Galoppieren. Keine reproduzierbare Brustwandempfindlichkeit
Atmung: Normale Brustexkursion mit Atmung; Atem klingt klar und gleich bilateral; kein Keuchen, Rhonchi oder Rasseln.
Bauch: Normale Darmgeräusche; nicht aufgebläht; nicht zart; keine tastbare Organomegalie.
Extremitäten: Normales ROM in allen vier Extremitäten; nicht palpationsempfindlich; distale Impulse sind normal und gleich.
Haut: Normal für Alter und Rasse; warm; trocken; guter Turgor; keine offensichtlichen Läsionen oder Exsudat
Fortschrittsnotizen (23:12)
Er erhielt 2 Baby Aspirin und SL NTG mit Linderung von Brustbeschwerden. Er hatte dann 1 Zoll Nitropaste platziert. Um 00:44 Uhr kehrte sein Schmerz zurück und sein EKG wurde wiederholt. Er erhielt 15mg Maalox ohne Verbesserung, dann ½ Zoll mehr NTP, was die Beschwerden linderte.
Ergebnisse
EKG 1: Abgeflachte T-Wellen inferior und in V2-V6.
EKG 2: Keine Änderungen
Labs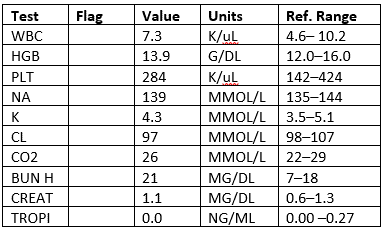
CXR: Negativ
Diagnose (01:57)
Brustschmerzen, Myokarditis in der Anamnese
Disposition (02:02)
Der Patient wurde telemetrisch ins Krankenhaus eingeliefert.
Krankenhaus-Kurs
Pt. unterzog serielle EKG und wiederholen EKG am Morgen. Er schloss für MI aus und wurde freigelassen. Ein nachfolgendes STRESSECHO war nach 12,5-minütigem Training ohne Brustbeschwerden oder EKG-Veränderungen negativ.
Zweiter Besuch
- Der Patient verfolgte sein PCP, wurde mit GERD diagnostiziert und mit einem PPI begonnen.
- Der Patient kehrte 6 Wochen später mit Engegefühl in der Brust und Dyspnoe im Rahmen einer Mahlzeit zur ED zurück. Seine Symptome wurden durch Anstrengung verschlimmert, treten in Ruhe auf und werden durch aufrechte Positionierung sowie mit Prilosec verbessert.
- Kein assoziiertes Fieber, Husten, Bestrahlung, Diaphorese, Wadenschmerzen, peripheres Ödem.
- Der Patient hat normale Vitalfunktionen mit einer unauffälligen, angemessenen Untersuchung.
- EKG zeigt TWI in aVL sowie neue Q-Wellen in V1-V2 und NSST-Änderungen.
- CXR ist negativ.
- Labore zeigen ein Troponin, das >das 20-fache der oberen Grenze des Normalwerts beträgt.
- Der Patient erhält Aspirin, Heparin, Plavix, Nitroglycerin und wird für das akute Koronarsyndrom zugelassen.
- Der Patient wird einer perkutanen Koronarintervention (PCI) mit erfolgreicher Stentplatzierung unterzogen und anschließend in gutem Zustand entlassen.
Diskussion
Brustschmerzen sind die Hauptbeschwerde für mehr als 5% der Patienten in Notaufnahmen (EDs) in den Vereinigten Staaten. Die Beurteilung des Patienten mit Brustschmerzen ist eine enorme Herausforderung, vor allem aufgrund der breiten Differentialdiagnose, aber auch wegen des mit Fehldiagnosen verbundenen Risikos. Zu den am schnellsten tödlichen Zuständen in der Notfallmedizin — von denen viele zunächst dringend behandelt werden müssen — gehören akutes Koronarsyndrom (Myokardischämie und Infarkt), Aortendissektion, Lungenembolie, Perikarditis mit Herztamponade, Myokarditis, Spannungspneumothorax und Ösophagusruptur. Alle diese Zustände neigen dazu, sich mit Brustschmerzen zu manifestieren, und sie alle sollten frühzeitig bei der Beurteilung des Patienten mit Brustschmerzen berücksichtigt werden.
Es liegt in der Verantwortung des Arztes, diese Patienten mit der Liste potenzieller Lebensbedrohungen an der Spitze der Differentialdiagnose zu bewerten. Eine detaillierte Anamnese, eine körperliche Untersuchung (mit Schwerpunkt auf Herz-, Lungen- und Gefäßuntersuchungen) und grundlegende Testinformationen (z. B. Elektrokardiogramm, Röntgenaufnahme des Brustkorbs) können diese Lebensbedrohungen häufig schnell mit angemessener Genauigkeit ausschließen. In Fällen, in denen diese erste schnelle Beurteilung eine der tödlichen Diagnosen nicht ausschließt, kann eine weitere Aufarbeitung in einer Umgebung mit höherer Schärfe gerechtfertigt sein.Obwohl typische Symptome von ACS als allmähliches Einsetzen von Schmerzen oder Druckschmerzen in der Brust mit Bestrahlung des linken Arms, Halses oder Kiefers beschrieben werden, können die atypischen Symptome in Wahrheit eher „typisch“ sein.“ In einer großen Datensynthese waren die hilfreichsten historischen Merkmale, die die Wahrscheinlichkeit eines akuten Myokardinfarkts erhöhten, Bestrahlung des rechten Arms oder der Schulter, Bestrahlung beider Arme, Schmerzen, die sich bei Anstrengung verschlechterten, Diaphorese und Übelkeit oder Erbrechen.1 Bestimmte Untergruppen, einschließlich Frauen, Diabetiker und ältere Menschen, haben häufiger Angina-Symptome, die durch Dyspnoe, Erbrechen, Diaphorese und generalisierte Schwäche dargestellt werden.2 Selbst bei Patienten mit atypischen Symptomen wie pleuritischem Schmerz oder tastbarer Empfindlichkeit in der Brustwand ist die Posttest-Wahrscheinlichkeit nur bei Patienten mit bereits geringem Risiko ausreichend gesenkt.1 Die Aufzählung der historischen kardialen Risikofaktorbelastung ist insbesondere bei Patienten, die älter als 40 Jahre sind, von geringem prognostischen Wert.3
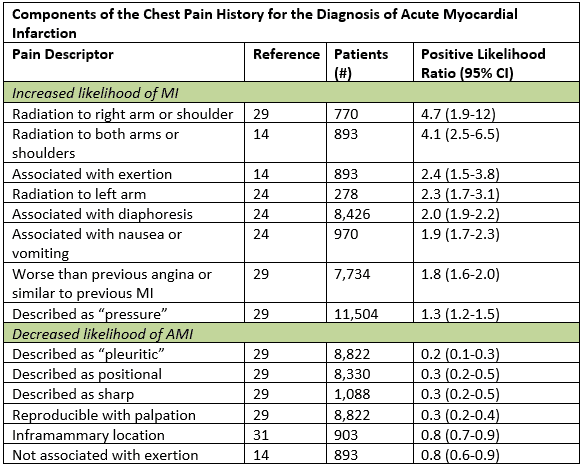
Angepasst von Swap CJ, et al. JAMA. 2005;294:2623-2629.
Junge Patienten (<45 Jahre alt) stellen eine Gruppe mit hohem Risiko für eine Fehldiagnose von ACS dar, vor allem aufgrund einer Tendenz von Ärzten, das kardiale Risiko zu unterschätzen. Bis zu 10% der Myokardinfarkte in den USA treten bei Patienten <im Alter von 45 Jahren auf, von denen die meisten mit atherosklerotischen Herzerkrankungen zusammenhängen. Atherosklerotische Erkrankungen wurden bei 17% der Jugendlichen in einer Studie festgestellt,4 und Multigefäßerkrankungen bei 20% der jungen Erwachsenen (Durchschnittsalter: 26 Jahre) in einer Autopsiestudie von Opfern innerstädtischer Gewalt.5 Eine kürzlich durchgeführte ED-Studie ergab, dass 5,4% der Patienten im Alter von 24 bis 39 Jahren mit Brustschmerzen innerhalb von 30 Tagen für ACS ausgeschlossen wurden und 2,2% ein unerwünschtes kardiales Ereignis (dh Tod, MI, Notwendigkeit einer perkutanen Koronarintervention oder einer Herzbypassoperation) hatten.6 Obwohl die Gesamtinzidenz von ACS bei jungen Patienten geringer ist, sollten Ärzte einen bestimmten HPI nicht nur aufgrund des Alters eines Patienten ausschließen.
Diabetes mellitus (DM) stellt eine weitere Hochrisikoerkrankung in Bezug auf das Potenzial für eine Fehldiagnose von ACS dar. Patienten mit DM sind anfällig für schmerzlose Präsentationen, wenn sie Herzischämie haben. Atypische Präsentationen (z. B. Dyspnoe, Verwirrtheit, Erbrechen, Müdigkeit) treten in bis zu 40% der Fälle auf. Diabetiker haben auch häufiger unerwünschte Ergebnisse von ACS.7 Die behandelnden Ärzte dürfen sich daher weder auf typische Herzbeschwerden verlassen, um eine Herzuntersuchung bei Diabetikern einzuleiten, noch sollten sie sich auf positive kardiale Biomarker verlassen, um bei diesen Patienten einen aggressiven Behandlungsansatz zu veranlassen.
Der Kokainkonsum muss als zusätzlicher unabhängiger Risikofaktor für atherosklerotische Herzerkrankungen und MI angesehen werden, insbesondere bei jungen Patienten. Einige Autoren schätzen, dass Kokain bis zu 25% der akuten MIs bei Patienten <45 Jahre ausmacht.7 Akuter Kokainkonsum kann eine koronare Vasokonstriktion, eine erhöhte Thrombozytenaggregation und / oder eine adrenerge Stimulation hervorrufen, die zu Herzrhythmusstörungen und Ischämie führt. Chronischer Kokainkonsum ist auch mit MI verbunden, was zu einer deutlich beschleunigten Atherogenese und einem anschließenden frühen MI führt. Insgesamt haben Kokainkonsumenten ein siebenfach erhöhtes Risiko für MI.8
Systemischer Lupus erythematodes (SLE) ist ein signifikanter, aber unterschätzter Risikofaktor für frühe Atherosklerose und Myokardinfarkt. Junge Patienten mit SLE haben schätzungsweise ein neunfach erhöhtes Risiko für einen frühen MI.9 Frauen <Insbesondere 45 Jahre sind einem erhöhten Risiko ausgesetzt, wobei Schätzungen zufolge das Risiko für einen frühen MI bis zum Fünfzigfachen erhöht ist.10 Die Ursache für vorzeitige Atherosklerose bei SLE ist wahrscheinlich multifaktoriell, hängt jedoch weitgehend mit koexistierenden systemischen Entzündungen und Dyslipidämien zusammen.Die Infektion mit dem humanen Immundefizienzvirus (HIV) wurde ebenfalls als unabhängiger Risikofaktor für vorzeitige Atherosklerose identifiziert. Es gibt Hinweise darauf, dass eine HIV-Infektion eine endotheliale Verletzung der Herzkranzgefäße verursacht und eine Entzündungskaskade auslöst, die zu atherosklerotischen Läsionen führt.11 Der Befund einer vorzeitigen Atherosklerose ist besonders ausgeprägt bei Patienten mit späteren Stadien einer HIV-Infektion (CD4-Anzahl <200).12 Die Medikationsschemata, die derzeit zur Behandlung von HIV (Proteasehemmer) angewendet werden, erhöhen auch das Risiko einer frühen Atherosklerose. Insgesamt sind HIV-Patienten mit ACS in einem Alter von mehr als 10 Jahren jünger als Nicht-HIV-Patienten.13
Die chronische Nierenerkrankung (CRD) wurde kürzlich auch als unabhängiger Risikofaktor für eine beschleunigte Atherosklerose identifiziert. CRD ist mit chronischer Entzündung verbunden14 und erhöhte Thrombozytenaggregation.15 Diese Faktoren führen in Kombination mit einer erhöhten Prävalenz konventioneller Risikofaktoren zu einem unverhältnismäßig hohen Risiko für kardiale Ereignisse bei diesen Patienten.14
Obwohl es innerhalb von 10 Minuten nach der Präsentation bezüglich der kardialen Ischämie erhalten und ausgewertet werden sollte, sollte das EKG nicht verwendet werden, um ACS auszuschließen. Bis zu 50% der Patienten mit Herzischämie oder Infarkt haben ein unspezifisches oder normales EKG.16 Serielle EKGs können die diagnostische Ausbeute bei der Bestätigung des Vorhandenseins von ACS bei Patienten mit anhaltenden Symptomen erhöhen.Ähnlich wie das EKG sind kardiale Biomarker nützlich, wenn sie positiv sind, aber nur begrenzt nützlich, wenn sie normal sind. Serielle Biomarker-Tests über einen Zeitraum von 3─ 6 Stunden sind in vielen EDs zu einem Routineprotokoll geworden und weisen eine hervorragende Empfindlichkeit beim Nachweis von MI auf. Auf Biomarker kann man sich jedoch nicht verlassen, um eine kardiale Ischämie auszuschließen. Die prospektive Validierung des „HERZ“ -Scores hat Praktikern die Möglichkeit gegeben, eine Untergruppe von Patienten mit geringem Risiko zuverlässig zu unterscheiden, die wahrscheinlich nicht von zusätzlichen Tests profitieren würden.17
Stresstests und Koronarangiographie werden häufiger früh in der Bewertung von Patienten mit Brustschmerzen verwendet, um in ACS zu regieren. Obwohl ein negativer Stresstest oder ein Angiogramm mit einem geringeren Risiko für eine zugrunde liegende CAD verbunden ist, kann keiner der Tests ACS oder das Vorhandensein signifikanter zugrunde liegender Koronarthrombosen definitiv ausschließen. Die Mehrheit der Stresstestmodalitäten erkennt Hinweise auf signifikante Koronarläsionen mit nur 85% bis 95% Empfindlichkeit.18-19 Koronarangiographie ist auch ein unvollkommener Test; falsch negative Angiographieinterpretationen sind nicht ungewöhnlich bei diffusen Erkrankungen, exzentrischen Plaques, „bündigen“ Verschlüssen, Ast-Ostialläsionen, überlappenden Seitenästen und sogar bei Läsionen innerhalb der linken Hauptkranzarterie.20 Eine weitere Beeinträchtigung der Zuverlässigkeit dieser Tests sind Daten, die darauf hindeuten, dass die Mehrheit der MIs von Verschlüssen innerhalb von Arterien herrührt, die zuvor <50% verstopft waren, bevor der Infarkt auftrat.21-23
Diese Arten von Läsionen sind normalerweise mit negativen Stresstests oder „nicht signifikanten“ Angiogrammen verbunden, wenn die Tests vor dem Infarkt durchgeführt werden. Aufgrund ihrer Art der Erkennung einer festen Koronarstenose sind Stresstests nicht in der Lage, gefährdete Koronarplaques zu bewerten oder vorherzusagen, bei denen das Risiko besteht, dass sie sich lösen, was zu einem akuten Koronarereignis führt. In einer Studie mit Patienten, die auf ACS untersucht wurden und in den letzten 3 Jahren einen negativen Stresstest hatten, erreichten über 20% den zusammengesetzten Index aus AMI, positivem Stresstest, CABG oder Katheterisierung mit Intervention, wobei die überwiegende Mehrheit der negativen Tests innerhalb von 1 Jahr nach der Präsentation auftrat.24 In ähnlicher Weise hatten bei noch invasiveren Tests Männer und Frauen mit normaler oder „minimaler“ CAD bei Herzkatheterisierung (1,2% bzw. 3,3%) entweder AMI oder Tod innerhalb von 1 Jahr nach der Nachuntersuchung.25 Es ist wichtig, dass sich der Arzt nicht auf vorherige objektive Tests angesichts eines Patienten mit Anzeichen und Symptomen stützt, die auf ACS hindeuten.
Zusammenfassung
Die Bewertung von Brustschmerzen und möglichem ACS ist ein Hochrisiko-Unterfangen. Die Entscheidung für eine „vollständige Herzuntersuchung“ sollte in erster Linie auf einem gründlichen HPI beruhen. Ärzte sollten sich der Häufigkeit atypischer Präsentationen bewusst sein, insbesondere bei Frauen, älteren Menschen und Diabetikern. Auch junge Patienten verdienen besondere Beachtung, da ihr Risiko oft unterschätzt wird. Zusätzliche nichttraditionelle kardiale Risikofaktoren, einschließlich Kokain, systemischer Lupus erythematodes, humanes Immunschwächevirus und chronische Nierenerkrankung, erfordern zusätzliche Aufmerksamkeit. Diagnostische Tests bestehen aus Elektrokardiographie (hilfreich, um ACS auszuschließen, aber nicht um die Diagnose auszuschließen) und kardialen Biomarker-Tests, die auch in erster Linie nützlich sind, wenn sie positiv sind. Wichtig ist, dass der negative Stresstest oder das Angiogramm sehr hilfreich ist, um Patienten auf ein geringes Risiko für ACS und CAD zu stratifizieren, aber sie schließen die Diagnose nicht definitiv aus.
Zitat: Palatnik M. Ein 38-jähriger Mann mit Brustschmerzen. In: J Urgent Care Med. März 2018. Verfügbar unter: https://www.jucm.com/a-38-year-old-man-with-chest-pain/.
- Tauschen CJ, Nagurney JT. Wert und Grenzen der Brustschmerzgeschichte bei der Beurteilung von Patienten mit Verdacht auf akute Koronarsyndrome. JAMA. 2005;294:2623-2629.
- El-Menyar A, Zubaid M, Sulaiman K. Atypische Darstellung des akuten Koronarsyndroms: Ein signifikanter unabhängiger Prädiktor für die Mortalität im Krankenhaus. In: J Cardiol. 2011;57;165-171.
- Han JH, Lindsell CJ, Storrow AB, et al. Die Rolle der kardialen Risikofaktorbelastung bei der Diagnose akuter Koronarsyndrome in der Notaufnahme. In: Ann Emerg Med. 2007;49;145-152.
- Tuzcu EM, Kapadia SR, Tutar E, et al. Hohe Prävalenz der koronaren Atherosklerose bei asymptomatischen Jugendlichen und jungen Erwachsenen: Evidenz aus intravaskulärem Ultraschall. Durchblutung. 2001;103:2705-2710.
- Joseph A, Ackerman D, Talley JD, et al. Manifestationen der koronaren Atherosklerose bei jungen Traumaopfern – eine Autopsiestudie. J Am Coll Cardiol. 1993;222:459-467.
- Marsan RJ Jr., Shaver KJ, Sease KL, et al. Evaluation einer klinischen Entscheidungsregel für junge erwachsene Patienten mit Brustschmerzen. In: Acad Emerg Med. 2005;12:26-32.
- Fergus TS, Fazel R, Fang J, et al. Präsentation, Management und Ergebnisse von Diabetikern im Vergleich zu Nicht-Diabetikern, die wegen akuter Koronarsyndrome aufgenommen wurden. Herzen. 2004;90:1051-1052.
- Qureshi AI, Suri MF, Guterman LR, et al. Kokainkonsum und die Wahrscheinlichkeit eines nicht tödlichen Myokardinfarkts und Schlaganfalls: Daten aus der dritten National Health and Nutrition Examination Survey. Durchblutung. 2001;103:502-506.
- D’Agate DJ, Kokolis S, Belilos E, et al. Vorzeitige koronare Herzkrankheit bei systemischem Lupus erythematodes mit ausgedehnter Reokklusion nach Bypass-Operation der Koronararterien. In: J Invasive Cardiol. 2003;15:157-163.
- Manzi S, Meilahn EN, Rairie JE, et al. Altersspezifische Inzidenzraten von Myokardinfarkt und Angina bei Frauen mit systemischem Lupus erythematodes: Vergleich mit der Framingham-Studie. Am J Epidemiol. 1997;145:408-415.
- Varriale P, Saravi G, Hernandez E, et al. Akuter Myokardinfarkt bei Patienten, die mit dem humanen Immunschwächevirus infiziert sind. Am Herz J. 2004;147:55-59.
- Hsue PY, Lo JC, Franklin A, et al. Progression der Atherosklerose nach Carotis Intima-Media-Dicke bei Patienten mit HIV-Infektion. Durchblutung. 2004;109:1603-1608.
- Hsue PY, Giri K, Erickson S, et al. Klinische Merkmale des akuten Koronarsyndroms bei Patienten mit einer Infektion mit dem humanen Immundefizienzvirus. Durchblutung. 2004;109:316-319.
- Yerkey MW, Kernis SJ, Franklin BA, et al. Nierenfunktionsstörung und Beschleunigung der Koronarerkrankung. Herzen. 2004;90:961-966.
- Aggarwal A, Kabbani SS, Rimmer JM, et al. Biphasische Effekte der Hämodialyse auf die Thrombozytenreaktivität bei Patienten mit Niereninsuffizienz im Endstadium: ein potenzieller Beitrag zum kardiovaskulären Risiko. Bin J Niere Dis. 2002;40:315-322.
- Brady WJ, Aufderheide TP, Chan T, et al. Elektrokardiographische Diagnose eines akuten Myokardinfarkts. Emerg Med Clin Norden Am. 2001;19:295-320.
- Backus BE, Sechs AJ, Kelder JC, et al. Eine prospektive Validierung des Herzwerts für Brustschmerzpatienten in der Notaufnahme. In: Int J Cardiology. 2013;168;2153-2158.
- Ioannidis JPA, Salem D, Kauen PW, et al. Genauigkeit von Bildgebungstechnologien bei der Diagnose einer akuten Herzischämie in der Notaufnahme: eine Metaanalyse. In: Ann Emerg Med. 2001;37:471-477.
- Lateef F, Gibler WB. Provokative Tests für Brustschmerzen. In: Am J Emerg Med. 2000;18:793-801.
- Schwartz L, Gourassa MG. Bewertung von Patienten mit Brustschmerzen und normalen Koronarangiogrammen. Arch Int Med. 2001;161:1825-1833.
- Giroud D, Li JM, Urban P, et al. Beziehung der Stelle des akuten Myokardinfarkts zur schwersten Koronararterienstenose bei vorheriger Angiographie. In: Am J Cardiol. 1992;69:729-732.
- Hackett D, Davies G, Maseri A. Vorbestehende Koronarstenosen bei Patienten mit erstem Myokardinfarkt sind nicht unbedingt schwerwiegend. Eur. J. 1988;9:1317-23.
- Hackett D, Verwilghen J, Davies G, et al. Koronarstenosen vor und nach akutem Myokardinfarkt. In: Am J Cardiol. 1989;63:1517-1518.
- Walker J, Galuska M, Vega D. Koronare Erkrankung bei Patienten mit Brustschmerzen in der Notaufnahme mit kürzlich durchgeführten negativen Stresstests. In: West J Emerg Med. 2010;11;384-388.
- Hemingway H, McCallum A, Shipley M, et al. JAMA 2006;295;1404-1411.
