Der erste Ansatz zur Entwicklung von Cannabinoidantagonisten in den späten 1980er Jahren bestand darin, die Struktur von THC zu modifizieren, aber die Ergebnisse waren enttäuschend. In den frühen 1990er Jahren wurde eine neue Familie von Cannabinoid-Agonisten aus dem NSAID (nicht-steroidale entzündungshemmende) Medikament Pravadolin entdeckt, die zur Entdeckung von Aminoalkyl-Indol-Antagonisten mit einigen, aber begrenzten Erfolg führte. Da die Suche nach der Struktur der Agonisten enttäuschend war, war es keine Überraschung, dass der erste potente und selektive Cannabinoid-Antagonist zu einer völlig neuen chemischen Familie gehörte. 1994 wurde der erste selektive Cannabinoid-Antagonist, SR141716 (Rimonabant), von Sanofi eingeführt, der zu einer Familie von 1,5-Diarylpyrazolen gehört.
RimonabantEdit
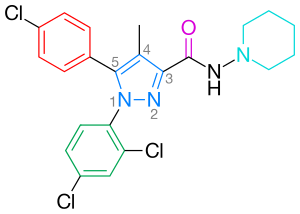
Rimonabant, auch unter dem systematischen Namen bekannt , ist ein 1,5-Diarylpyrazol-CB1-Rezeptorantagonist (Abbildung 2). Rimonabant ist nicht nur ein starker und in hohem Grade selektiver Ligand des Empfängers CB1, aber es ist auch mündlich aktiv und antagonisiert die meisten Effekte von Cannabinoidagonisten, wie THC, in vitro und in vivo. Rimonabant hat klare klinische Wirksamkeit für die Behandlung der Korpulenz gezeigt.
BindingEdit
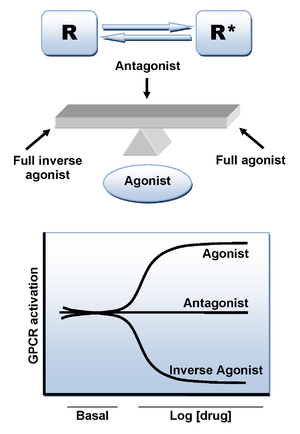
Die Bindung eines Agonistenliganden an den CB1-Rezeptor provoziert eine Konformationsänderung und führt zum aktiven Zustand des Rezeptors, der für die Signaltransduktion verantwortlich ist. Es gibt jedoch einen zusätzlichen Mechanismus, der in Abwesenheit von Liganden zum aktiven Zustand führen kann. Wie zahlreiche andere GPCRs, CB1-Rezeptor zeigt ein hohes Maß an konstitutiver Aktivität und somit kann es spontan einen aktiven Konformationszustand in Abwesenheit von Agonistenbindung annehmen, Halten erhöhte Basalspiegel der intrazellulären Signalgebung. Dies kann durch das Zwei-Zustands-Modell der Rezeptoraktivierung erklärt werden, bei dem sich Rezeptoren im Gleichgewicht zwischen zwei Zuständen befinden, aktiv und inaktiv (R * und R). Ein Agonist stabilisiert den aktiven Zustand, der zur Aktivierung führt, ein neutraler Antagonist bindet gleichermaßen an aktive und inaktive Zustände, während ein inverser Agonist den inaktiven Zustand bevorzugt stabilisiert (Abbildung 3).
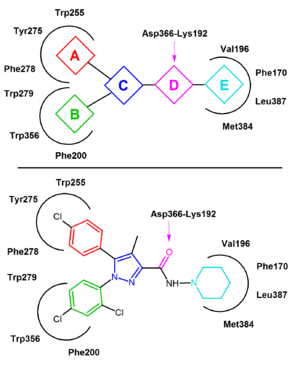
Es wurde in vielen Fällen berichtet, dass sich Rimonabant eher als inverser Agonist als als neutraler Antagonist verhält, und es ist wahrscheinlich, dass es bevorzugt an den inaktiven Zustand des CB1 bindet, wodurch die Aktivierung des Signalwegs verringert wird. Die Schlüsselbindungsinteraktion ist eine Wasserstoffbindung, die zwischen der Carbonylgruppe von Rimonabant und dem Lys192-Rest des CB1-Rezeptors gebildet wird. Diese Bindung stabilisiert die Lys192-Asp366-Salzbrücke des intrazellulären Endes der Transmembranhelices 3 und 6 (Abbildung 4). Diese spezifische Salzbrücke ist im inaktiven Zustand des Rezeptors vorhanden, fehlt jedoch im aktiven Zustand.
Im inaktiven Zustand von CB1 bindet Rimonabant innerhalb der Transmembran-3-4-5-6 aromatische Mikrodomäne. Die Bindung von Rimonabant beinhaltet direkte aromatische Stapelwechselwirkungen zwischen seinem 2,4-Dichlorphenylring und den Trp279 / Phe200 / Trp356-Resten auf der einen Seite und dem Para-Chlorphenylring und den Tyr275 / Trp255 / Phe278-Resten auf der anderen Seite. Der lipophile Piperidinylteil passt gut in einen Hohlraum, der durch die Aminosäurereste Val196 / Phe170 / Leu387 und Met384 gebildet wird (Abbildung 4).
PharmakophoreEdit
Die meisten bisher berichteten CB1-Antagonisten sind enge Analoga oder Isosterone von Rimonabant. Ein allgemeines CB1-Pharmakophormodell für inverse Agonisten kann aus den gemeinsamen Merkmalen dieser Analoga, Diarylpyrazolen, extrahiert werden (Abbildung 4). Dieser Pharmakophor enthält einen cyclischen Kern C (z. B. Pyrazol in Rimonabant), der durch zwei aromatische Reste A und B substituiert ist. Eine Wasserstoffbrückenakzeptoreinheit D verbindet C mit einem cyclischen lipophilen Teil E. In einigen Fällen verbindet sich Einheit E direkt mit C. In Abbildung 4 wird Rimonabant als Beispiel verwendet. Einheit A steht für eine 4-Chlorphenylgruppe und Einheit B für einen 2,4-Dichlorphenylring. Einheit C ist der zentrale Pyrazolring und Einheit D stellt die Carbonylgruppe dar, die als Wasserstoffbindungsakzeptor dient. Die Einheit E steht für einen lipophilen Aminopiperidinylrest.
Struktur-Wirkungs-Beziehungenbearbeiten
Für eine optimale Bindung am CB1-Rezeptor ist ein parasubstituierter Phenylring an der Pyrazol-5-Position erforderlich. Der 5-Substituent des Pyrazols ist an der Rezeptorerkennung und dem Antagonismus beteiligt. Der Parasubstituent des Phenylrings könnte Chlor, Brom oder Jod sein, es hat sich jedoch gezeigt, dass auch eine Alkylkette toleriert werden könnte. Die Nummerierung des zentralen Pyrazolrings ist in Abbildung 2 dargestellt.
Ein 2,4-Dichlor-substituierter Phenylring an der Pyrazol-1-Position ist sowohl für die Affinität als auch für die Aktivität bevorzugt. Es wurde gezeigt, dass zusätzliche Halogene an diesem Phenylring die Affinität verringern.
Günstig ist auch eine Ringsubstitution an der 3-Carbonsäureamidgruppe, wie der 1-Piperidinylgruppe in Rimonabant. Der Ersatz des Aminoperidinylsubstituenten durch Alkylamide, Ether, Ketone, Alkohole oder Alkane führte meist zu einer verminderten Affinität. Der Austausch des Piperidinyl durch Pentyl oder eine Heptylkette verlieh den Verbindungen agonistische Eigenschaften. Basierend auf diesen Ergebnissen wurde der Schluss gezogen, dass die Pyrazol-3-Position am Agonismus beteiligt zu sein scheint, während die 1-,4-,5-Positionen am Antagonismus beteiligt zu sein scheinen.
Untersuchungen haben gezeigt, dass die Abwesenheit des Carboxamid-Sauerstoffs zu einer verminderten Affinität führt. Darüber hinaus trägt die Anwesenheit von Carboxamidsauerstoff dazu bei, die inversen agonistischen Eigenschaften zu verleihen, während Analoga, denen dieser Sauerstoff fehlt, neutrale Antagonisten sind. Diese Ergebnisse stützen die Hypothese, dass der Carboxamidsauerstoff eine Wasserstoffbindung mit dem Lys192-Rest am CB1-Rezeptor bildet.
Diarylpyrazole derivativesEdit
SR141716 (rimonabant) Analoga wurden kürzlich von mehreren Gruppen beschrieben, was zu einem guten Verständnis der Struktur-Aktivitäts-Beziehung (SAR) innerhalb dieser chemischen Gruppe führte. Während die meisten beschriebenen Verbindungen weniger wirksam sind als SR141716, sind zwei von ihnen erwähnenswert, SR147778 und AM251, obwohl beide auch an Mu-Opioidrezeptoren wirken können.SR147778 (Surinabant), ein Antagonist der zweiten Generation, hat eine längere Wirkdauer als Rimonabant und eine verbesserte orale Aktivität. Diese verlängerte Wirkungsdauer ist wahrscheinlich auf das Vorhandensein der metabolisch stabileren Ethylgruppe an der 4-Position ihres Pyrazolrings zurückzuführen. Eine weitere Änderung ist der Ersatz des 5-Phenylchlorsubstituenten durch Brom.
Es wurde das Diarylpyrazolderivat AM251 beschrieben, bei dem der Chlorsubstituent in Para-Position des 5-Phenylrings durch Jod ersetzt wurde. Dieses Derivat schien wirksamer und selektiver zu sein als Rimonabant.
Es wurden 21 Analoga synthetisiert, die entweder ein Alkylamid oder ein Alkylhydrazid unterschiedlicher Länge in Position 3 besitzen. Es wurde beobachtet, dass die Affinität mit zunehmender Kohlenstoffkettenlänge bis zu fünf Kohlenstoffatomen zunimmt. Auch die Amidanaloga zeigten eine höhere Affinität als Hydrazid-Analoga. Keines dieser Analoga besaß jedoch eine signifikant größere Affinität als Rimonabant, aber dennoch waren sie für den CB1-Rezeptor gegenüber dem CB2-Rezeptor etwas selektiver als Rimonabant.
Es wurden mehrere Versuche unternommen, die Affinität der Diarylpyrazolderivate durch Versteifung der Struktur von Rimonabant zu erhöhen. Im Sinne des allgemeinen Pharmakophorenmodells sind die Einheiten A, B und/oder C durch zusätzliche Bindungen verbunden, die zu starren Molekülen führen. Zum Beispiel zeigte das kondensierte polycyclische Pyrazol NESS-0327 eine 5000-mal höhere Affinität zum CB1-Rezeptor als Rimonabant. Diese Verbindung besitzt jedoch eine schlechte zentrale Bioverfügbarkeit.Eine andere Verbindung, das Indazolderivat O-1248, kann als Analogon von Rimonabant angesehen werden, wobei seine 5-Arylgruppe mit dem Pyrazolteil kondensiert ist. Diese strukturelle Modifikation führte jedoch zu einer 67-fachen Abnahme der CB1-Rezeptoraffinität.
Diese Diarylpyrazol-Derivate von Rimonabant sind in Tabelle 1 zusammengefasst.
 |
 |
| SR147778 | AM251 |
 |
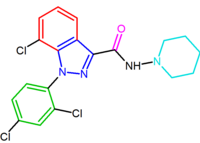 |
| NESS-0327 | O-1248 |
Other derivativesEdit
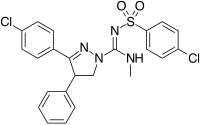
Structurally different from the 1,5-diarylpyrazoles are the chemical series of the 3,4-diarylpyrazolines. Innerhalb dieser Serie befindet sich SLV-319 (Ibipinabant), ein potenter CB1-Antagonist, der im Vergleich zu CB2 etwa 1000-fach selektiver für CB1 ist und eine ähnliche In-vivo-Aktivität wie Rimonabant aufweist.Ein anderer Ansatz zur Entwicklung von Analoga von Rimonabant bestand darin, den zentralen Pyrazolring durch einen anderen Heterocyclus zu ersetzen. Ein Beispiel für diesen Ansatz sind 4,5-diarylimidazole und 1,5-diarylpyrrol-3-carbonsäureamide.
Eine große Anzahl von kondensierten bicyclischen Derivaten von Diarylpyrazol und Imidazolen wurde berichtet. Ein Beispiel hierfür ist ein Purinderivat, bei dem ein Pyrimidinring mit einem Imidazolring kondensiert ist. Otenabant (CP-945,598) ist ein Beispiel für ein kondensiertes bicyclisches Derivat, das von Pfizer entwickelt wurde.
Mehrere Forschungsgruppen haben Sechsringpyrazol-Bioisosterone untersucht. Zum Beispiel wurde gezeigt, dass ein 2,3-Diarylpyridinderivat ein potenter und selektiver CB1-Inverse-Agonist ist. Die Struktur dieser Verbindung zeigt die Möglichkeit, dass die Amideinheit von Rimonabant in eine lipophile (Benzyloxy) und eine polare (Nitril) Funktionalität gespalten werden könnte. Weitere Sechsringanaloga sind beispielsweise Pyrimidine und Pyrazine.
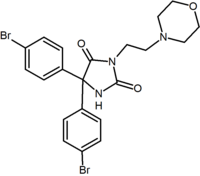
Neben den Fünf- und Sechsringanaloga gibt es weitere cyclische Derivate wie die Azetidine. Ein Beispiel ist das Methylsulfonamid-Azetidin-Derivat, das eine 1,1-Diarylgruppe aufweist, die den 1,5-Diarylteil der Diarylpyrazole nachahmt. Die Sulfonylgruppe dient als Wasserstoffbindungsakzeptor. Die 1,1-Diarylgruppe ist auch in Derivaten wie den Benzodioxolen und Hydantoinen vorhanden.
Azyklische Analoga wurden ebenfalls berichtet. Diese Analoga enthalten ein 1,2-Diarylmotiv, das den 1,5-Diarylsubstituenten von Rimonabant entspricht. Ein Beispiel für ein acyclisches Analogon ist Taranabant (MK-0364), das von Merck entwickelt wurde.
Vertreter dieser Analoga sind in Tabelle 2 zusammengefasst.
 |
 |
 |
|
| Type of derivative |
3,4-Diarylpyrazoline (Ibipinabant) | 4,5-Diarylimidazole | 1,5-Diarylpyrrole-3-carboxamides |
 |
 |
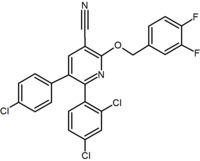 |
|
| Type of derivative |
Purine (pyrimidine ring fused to an imidazole ring) |
Purine derivative (Otenabant) | 2,3-Diarylpyridine |
 |
 |
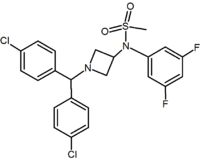 |
|
| Type of derivative |
Pyrimidine | Pyrazine | Methylsulfonamide azetidine |
 |
 |
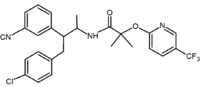 |
|
| Art des Derivats |
Benzodioxol | Hydantoin | Acyclisches Derivat (Taranabant) |
CB1
Antikörper gegen den CB1-Rezeptor wurden in Russland entwickelt und in die klinische Anwendung gebracht. Dazu gehören brizantin (russisch: Бризантин®) und dietressa (Russisch: Диетресса®). Brizantin ist zur Behandlung von Nikotinentzug und Raucherentwöhnung indiziert und Dietressa ist zur Gewichtsreduktion indiziert. Dietressa ist in Russland rezeptfrei erhältlich.
