Einführung
Zell- oder Gewebeerneuerung und -regeneration sind die beiden Hauptentwicklungsanforderungen erwachsener Organismen. Beide Prozesse haben als Ausgangspunkt eine Population von Stammzellen, die sich normalerweise in einer spezifischen Umgebung befindet, die als „Nische“ bezeichnet wird und ihnen die erforderlichen Signale liefert, um die Stammeigenschaften zu erhalten oder sich zu den erforderlichen verschiedenen Zelltypen zu differenzieren (Abbildung 1). Die Proliferation und Differenzierung der Stammzellen muss mit dem Tod der zu ersetzenden Zellen koordiniert werden. Darüber hinaus sind Prozesse wie Zellmigration, Epigenetik und zelluläre Kommunikation für eine ordnungsgemäße Zellerneuerung erforderlich . Schnelle Erneuerunggewebe können durch eine höhere mitotische Aktivität erkannt werden. Umgekehrt enthalten Gewebe mit langsamer Erneuerung weniger Mitose und können nicht leicht von nicht erneuernden Bereichen erkannt werden, die auch eine Mitose aufweisen können. Die Schicksalsentscheidungen von Stammzellen während der proliferationdirekt beeinflussen Gewebeerneuerung und Homöostase. Daher ist es wichtig, die regulatorischen Mechanismen zu verstehen, die eine ausgewogene Zellteilung und -differenzierung aufrechterhalten. Extrazelluläre Signale (z. B. Gewebemikroumgebung, intrazelluläres ROS und Zytokine) sowie intrazelluläre Faktoren (z. B. epigenetische Maschinen, Transkriptionsfaktoren und DNA-Schadensreaktion) sind für die Regulation der Stammzellteilung verantwortlich.
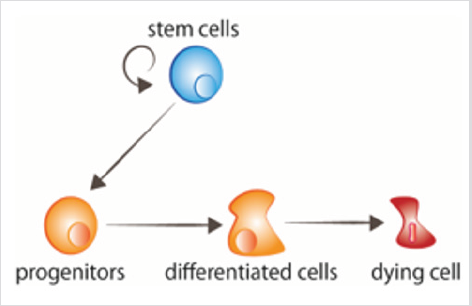
Abbildung 1: Zellumsatz Stammzellen vermehren sich, wodurch Vorläuferzellen entstehen, die danach die Signale zur Differenzierung erhalten. Gealterte Zellen erhalten Signale zum Absterben.
Stammzellen zeigen drei mögliche Teilungsoptionen: asymmetrische Teilung, bei der eine Stammzelle und eine festgeschriebene Tochterzelle entstehen; symmetrische Bindung, die zwei festgeschriebene Tochterzellen hervorbringt; und symmetrische Teilung, die zwei Tochterzellen ergibt, die die Stammzelleigenschaften beibehalten Abbildung 2. Obwohl vorhergesagt werden konnte, dass die asymmetrische Teilung der einzige Mechanismus ist, der die Aufrechterhaltung einer stabilen Stammzellpopulation ermöglicht, zeigten die aktuellen Daten aus Lineagetracingexperimenten, dass in den meisten Geweben das Gleichgewicht zwischen der Stammzellproliferation und der Erzeugung differenzierter Nachkommen auf der Ebene der gesamten Stammzellpopulation erreicht wird.Der Verlust von Stammzellen durch Differenzierung oder Zellschädigung induziertsymmetrische Teilung, um diese Lücke zu füllen . Nach der Stammzellteilung durchlaufen die Zellen, die dem Differenzierungsprozess folgen, verschiedene Stadien, die durch eine Kombination von Transkriptionsfaktoren definiert werden, die die Aktivität des entsprechenden Genrepertoires steuern und deren Bindung und terminale Differenzierung ermöglichen. Für jede Zelllinie ist das Endprodukt der Entscheidungssequenz ein spezifischer differenzierter Zelltyp Abbildung 3a. Unter den meisten Umständen ist die zelluläre Identität – das Produkt der normalen Differenzierung – im Gewebe stabil, und ihre Aufrechterhaltung ist für eine normale Gewebefunktion von entscheidender Bedeutung. Eine solche Stabilität wird durch epigenetische Regulation – z. B. Histondemethylierung und Acetylierung – erreicht, die zu erblichen Mustern der gewebespezifischen Genexpression führt .
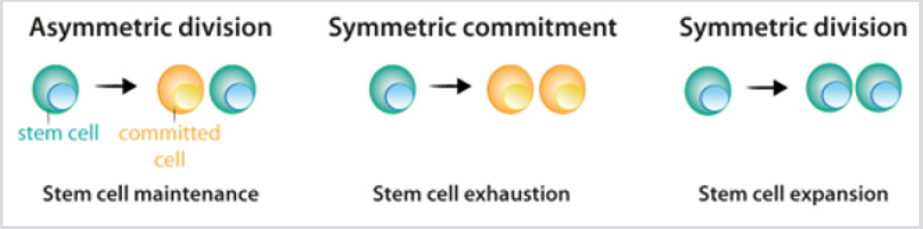
Abbildung 2: Teilungsmuster von Stammzellen.
a) Während der asymmetrischen Teilung führen Stammzellen zu einer Stammzelle, die die Stammzellpopulation aufrechterhält, und einer Zelledas wird zur Differenzierung verpflichtet.
b) Während der symmetrischen Bindung führt die Stammzellteilung zu zwei Tochterzellen, die sich der Differenzierung verschrieben haben.
c) Während der symmetrischen Teilung entstehen durch die Stammzellteilung zwei Stammzellen. Wie im Text erläutert, aktuelle Experimentelledaten zeigen an, dass die drei Teilungsmodi unter Beibehaltung der Stammzellpopulation auftreten können.
Es kann jedoch zu einem Verlust der Zellidentität kommen. In der Tat sind Zellen aus der Drosophila-Bandscheibe in der Lage, nach der Transplantation ein neues Schicksal für Erwachsene zu bestimmen und zu erwerben . In dieser Situation scheinen extrazelluläre Signale einige Vorläufer- oder differenzierte Zellen neu zu programmieren, um Eigenschaften entweder eines mehr Stammzustands oder eines neuen differenzierten Zustands zu erhalten. Es gibt zwei Mechanismen, durch die eine Zelle ihre Identität ändern kann: Dedifferenzierung Undtransdifferenzierung. Dedifferenzierung bezieht sich auf den Prozess, durch den eine differenzierte oder gebundene Zelle Eigenschaften einer weniger reifen Zelle erhält Abbildung 3b. Das dramatischste Beispiel für Dedifferenzierung ist die In-vitro-Umwandlung terminaldifferenzierter Zellen in pluripotente Zellen (induzierte pluripotente Stammzellen, iPSCs) durch Überexpression einer begrenzten Anzahl von Transkriptionsfaktoren . Transdifferenzierung hingegen tritt auf, wenn eine differenzierte Zelle ihr Transkriptionsprogramm ändert und sich in einen anderen differenzierten Zelltyp umwandelt. Der Prozess canoccur durch einen Zwischenstufe der Dedifferenzierung in Richtung aless reifen Stadium vor der Umwandlung in die neue differenzierte Zelle, oder direkt, ohne die Zwischenstufe Abbildung 3c-d.Die direkte Umwandlung von Fibroblasten in Myoblasten durch die ektopische Expression von MyoD ist ein Beispiel für den zweiten Prozess .
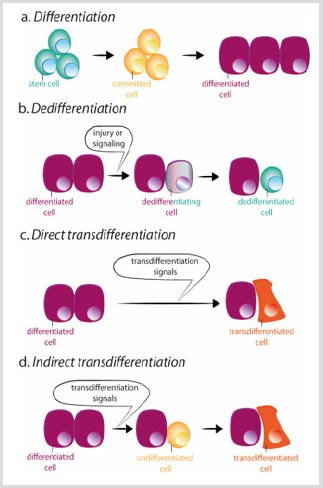
Abbildung 3: Schemata der Differenzierung, Dedifferenzierung und Transdifferenzierung.
a) Während der normalen Differenzierung entstehen aus Stammzellen Committed-Zellen, die sich wiederum in verschiedene Zelltypen differenzieren.
b) Dedifferenzierung besteht aus dem Erwerb von Stammzelleigenschaften durch eine differenzierte Zelle. Trans-Differenzierung kann auftretenauf direkte oder indirekte Weise.
c) Während der direkten Transdifferenzierung erhält eine differenzierte Zelle das Transkriptionsprogramm eines anderen Zelltyps, der normalerweise eng verwandt ist, wie zum Beispiel exokrin mit endokrinen Pankreaszellen, und wird zu einer anderen differenzierten Zelle.
d) Während der indirekten Transdifferenzierung dedifferenziert sich eine differenzierte Zelle, bevor sie das neue Transkriptionsprogramm des anderen Zelltyps übernimmt.
Dedifferenzierung und Transdifferenzierung treten auch aufeine natürliche Weise als Reaktion auf eine Verletzung oder Gewebeverlust .Dedifferenzierung, zum Beispiel, tritt natürlich während der limbregeneration in den Urodele Amphibien. Nach Gliedmaßenamputation, Zellen neben der Wunde dedifferenzieren, Bilden ein Blastem, das aus undifferenzierten Zellen besteht, die sich vermehren und schließlich in denselben Zelltyp umdifferenzieren, um alle Komponenten des verlorenen Gliedes zu erzeugen. Die natürliche Transdifferenzierung erfolgt indirekt: Zuerst wird die Zelle dedifferenziert; und dann wird das natürliche Entwicklungsprogramm aktiviert, wodurch sich die Zelle in die neue Linie differenzieren kann. Tsonis und Mitarbeiter beschrieben eine natürlichemechanismus der Transdifferenzierung in einem Newt. Sie fanden heraus, dass, wennlinsen entfernt werden, pigmentierte Epithelzellen aus der dorsalen Iris transdifferenzieren und regenerieren das fehlende Gewebe. Um dies zu erreichen, müssen pigmentierte Epithelzellen zuerst dedifferenzieren und proliferieren, um neue Linsenzellen zu erzeugen, und dann in sie differenzierenreife Zellen der Linse . In beiden Situationen – Dedifferenzierung und Redifferenzierung in den gleichen Zelltyp oder Transdifferenzierung in einen neuen Zelltyp – kann ein komplexes Netzwerk von Signalwegen das Transkriptionsprogramm steuern, das von jeder Zelle im perfekten Zeitpunkt erfasst wird.hus, die raum-zeitliche Kontrolle der Genexpression iscontinuously während der Tierhomöostase erforderlich, und während aregenerative Prozess. Während der Regeneration müssen sich die Zellen jedoch an die neue Situation anpassen, was fundiertere Entscheidungen auf zellulärer Ebene erfordert, häufig einschließlich der Prozesse Derdifferenzierung und Transdifferenzierung, die während der Homöostase selten sind.
- Clevers H, Loh KM, Nusse R (2014) Stammzellsignalisierung. Eine integralprogram für tissue erneuerung und regeneration Wnt signaling und stemcell control. Wissenschaft 346 (6205): 1-9.
- Leblond CP, Walker B(1956) Erneuerung der Zellpopulation 36(2): 255-276.
- Roostaee A, Benoit YD, Boudjadi S, Beaulieu JF (2016) Epigenetik bei der Erneuerung von Darmepithelzellen. J Cell Physiol 231(11): 2361-2367.
- Ito K, Ito K (2016) Metabolismus und die Kontrolle des Zellschicksals Entscheidungen Undstammzellerneuerung. Annu Rev Zelle Dev Biol 32: 399-409.
- Simons BD, Clevers H (2011) Strategien zur Selbsterneuerung homöostatischer Stammzellen in adulten Geweben. Zelle 145(6): 851-862.
- Yang Y, Akinci E, Dutton JR., Banga A, Slack JMW, et al. (2013) Stagespecific reprogramming of mouse embryo liver cells to a beta cell-likephenotype. Mech Dev 130(11-12): 602-612.
- Merrell AJ, Stanger BZ (2016) Adulte Zellplastizität in vivo: Dedifferenzierung und Transdifferenzierung sind wieder in Mode. Nat Rev MolCell Biol 17(7): 413-425.
- Worley MI, Setiawan L, Hariharan IK (2012) Regeneration und Transdetermination in Drosophila imaginal discs. Annu Rev Genet 46:289-310.
- Raff M (2003) Adulte Stammzellplastizität: Fakt oder Artefakt? Annu Rev CellDev Biol 19: 1-22.
- Takahashi K, Yamanaka S (2006) Induction of Pluripotent Stem Cellsfrom Mouse Embryonic and Adult Fibroblast Cultures by DefinedFactors. Zelle 126 (4): 663-676.
- S.Tapscotr, R. Davis, M. Thayer, P. Cheng, H. Weintraub, et al. (1988) MyoDi: Ein nukleares Phosphoprotein, das eine Myc-Homologieregion benötigt, um Fibroblasten in Myoblasten umzuwandeln. Wissenschaft 242 (4877): 405-411.
- Jopling C, Boue S, Izpisua Belmonte JC (2011) Dedifferenzierung, Transdifferenzierung und Reprogrammierung: drei Wege zur Regeneration.Nat Rev Mol Zelle Biol 12(2): 79-89.
- Tsonis PA, Madhavan M, Tancous EE, Del Rio-Tsonis K (2004) Del Rio-Tsonis, K. Eine Molchaugenansicht der Linsenregeneration. Int J Dev Biol 48 (8-9):975-980.
