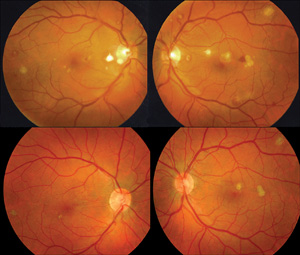
Abbildung 1. Farbfundusfoto beider Augen bei einem IV-Drogenabhängigen vor der sequentiellen bilateralen Vitrektomie (obere Reihe) und nach der Vitrektomie (untere Reihe). Vor der Vitrektomie gab es eine leichte Vitritis und einige Glaskörpertrübungen bilateral. Bereiche der hämorrhagischen Retinochoroiditis sind vorhanden. Nach Vitrektomie und fünf seriellen Amphotericin-B-Injektionen in beide Augen zweimal wöchentlich können retinochoroidale Narben mit Auflösung der Netzhautblutung und Glaskörpertrübung beobachtet werden. Dieser Patient erhielt auch einen Monat orales Ketoconazol. Endogene Endophthalmitis ist eine seltene, aber potenziell verheerende intraokulare Infektion, bei der Krankheitserreger über den Blutkreislauf in das Auge gelangen. Endogene Endophthalmitis ist seltener als exogene Endophthalmitis und macht in verschiedenen Studien 2 bis 8 Prozent aller Endophthalmitis-Fälle aus.1,2 Pädiatrische endogene Endophthalmitis ist noch seltener und macht 0,1 bis 4 Prozent aller endogenen Endophthalmitis-Fälle aus.2,3
Prädisponierende Bedingungen sind wichtig für die Bestimmung des Risikos eines Patienten für endogene Endophthalmitis. Bei Patienten mit akuter oder chronischer Panuveitis unklarer Herkunft können invasive diagnostische Verfahren, am häufigsten Pars plana Vitrektomie, notwendig sein, um die Diagnose zu stellen. Zu den identifizierten Risikofaktoren für eine endogene Endophthalmitis gehören: chronische Krankheiten (z. B. Diabetes mellitus, Nierenversagen, Malignome und erworbenes Immunschwächesyndrom); immunsuppressive Behandlung; jüngste invasive Chirurgie; intravenöser Drogenmissbrauch; Verweilkatheter; Endokarditis; infektionen der Leber- und Gallenwege; Organtransplantation; Schwangerschaft oder Entbindung; urogenitale Operationen; oder zahnärztliche Eingriffe.4 Das Auslösen einer Vorgeschichte von intravenösem Drogenmissbrauch ist besonders wichtig und angesichts der Zurückhaltung der Patienten, dieses Problem zu diskutieren, oft schwierig. Eine positive Vorgeschichte von Grunderkrankungen wie Diabetes, Herzerkrankungen und Malignität wurde bei 90 Prozent der Patienten in einem Bericht von Annabelle A. Okada und Kollegen im Jahr 1994 berichtet.5 In einer großen Übersicht über endogene Endophthalmitis-Patienten wurden in 56 bis 68 Prozent der Fälle Grunderkrankungen gemeldet, die für eine Augeninfektion prädisponieren.6 Zenith H. Wu und Kollegen berichteten über die Identifizierung eines bereits bestehenden prädisponierenden Zustands bei 90,9 Prozent der Patienten, und der häufigste systemische Zustand war Diabetes mellitus (50 Prozent).7
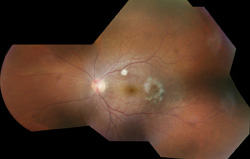
Abbildung 2. Farbfundusfoto des linken Auges eines Patienten mit endogener Candida-Endophthalmitis nach Vitrektomie und Behandlung mit fünf intravitrealen Injektionen von Amphotericin-B zweimal wöchentlich mit weißen retinochoroidalen Läsionen in der Makula sowie einem exzentrischen Makulaloch als Folge einer Pilzendophthalmitis. Die Sehschärfe betrug 20/30. Dieser Patient erhielt auch einen Monat orales Ketoconazol.
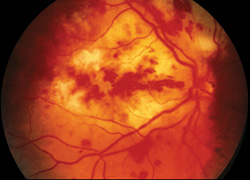
Abbildung 3. Farbfundusfoto des rechten Auges eines Patienten mit endogener Endophthalmitis durch Aspergillus. Der Patient hatte in der Vorgeschichte intravenösen Drogenmissbrauchs und wurde mit intravitrealem und systemischem Amphotericin B behandelt, hatte jedoch ein schlechtes visuelles Ergebnis.
Endogene Endopthalmitis wird am häufigsten durch Bakterien oder Pilze verursacht. Erreger variieren geografisch. Eine Studie des Bascom Palmer Eye Institute berichtete über Pilze als häufigere Ursache als Bakterien (62 Prozent Pilze vs. 38 Prozent Bakterien)8, während eine Studie in Hongkong Bakterien als häufigere Ursache für endogene Endophthalmitis (72,7 Prozent Bakterien vs. 27,3 Prozent Pilze) berichtete.7 Literatur aus Ostasien berichtet, dass gramnegative Organismen die häufigste Ursache (70 Prozent) und Klebsiella der häufigste Erreger (60 Prozent) sind.9 Daten aus Nordamerika und Europa zeigten einen steigenden Prozentsatz gramnegativer Organismen von 32 Prozent im Jahr 1986 auf 52 Prozent im Jahr 2003.6 Hefen sind eine häufigere Ursache und mit besseren visuellen Ergebnissen im Vergleich zu Schimmelpilzen bei endogener Endophthalmitis verbunden.10,11 Candida ist der häufigste Organismus, der für die endogene Endophthalmitis von Pilzen verantwortlich ist.8,11,12 Bei immunsupprimierten Patienten wie AIDS-Patienten müssen atypische Organismen wie Cryptococcus, Mycobacterium avium, Nocardia und Pneumocystis jiroveci in Betracht gezogen werden.
Das betroffene Auge kann Schmerzen, Rötungen, Floater oder Sehstörungen haben. Die Diagnose verzögert sich in der pädiatrischen Bevölkerung durch die Unfähigkeit, Symptome frühzeitig zu melden. Bilaterale Präsentation wird in 14 bis 25 Prozent der Fälle und häufiger mit Pilzen und Bakterien wie Meningokokken, Escherichia coli und Klebsiella berichtet.6 Die endogene Endophthalmitis kann zunächst einseitig sein und sich anschließend im rechten Auge entwickeln. Bakterielle oder Pilzinfektionen können Irismikroabszesse, Hypopyonen, unterschiedliche Grade von Glaskörperschleier, diskrete Netzhautknoten, perivaskuläre Netzhautblutungen, Arteriolenembolien oder nekrotische Netzhaut aufweisen. Schwere Fälle können zu Panophthalmitis führen. Das Vorhandensein von schokoladenbraunem Exsudat in der Vorderkammer deutet auf Bazillus als verantwortlichen Organismus hin, während Listerien durch braune Hypopyonen und Serratien durch eine rote Hypopyone gekennzeichnet sind.
Pilz endogene Endophthalmitis mit Candida kann flauschige Kugeln im Glaskörper, Chorioretinitis, Hypopyon, Perivaskulitis, Optikusneuritis oder chorioretinale Läsionen (cremig, tief und gut umschrieben) haben. Die Infektion mit Schimmelpilzen wie Aspergillus ist fulminanter, typischerweise auf den subretinalen Raum beschränkt und kann chorioretinale Läsionen (konfluent mit undeutlichen Rändern), intraretinale Blutungen, Gefäßverschluss oder Netzhautnekrose voller Dicke aufweisen. Positive Glaskörper-Aspiratkulturen sind schwieriger aus Schimmelpilzen zu gewinnen als Hefen, vielleicht weil Schimmelpilze den Glaskörper nicht so häufig betreffen wie Hefen.13
Endogene Endophthalmitis kann Konjunktivitis, nichtinfektiöse Uveitis anterior, Iritis, akutes Glaukom, Cellulitis, Katarakt und insbesondere Retinoblastom bei Kindern nachahmen. Eine Fehldiagnose bei der Erstpräsentation wurde in 16 bis 63 Prozent der Fälle gemeldet, wodurch die Diagnose und das ordnungsgemäße Management verzögert wurden.6,12
Die Diagnose einer endogenen Endophthalmitis wird typischerweise nach mikrobiologischem Nachweis einer Infektion aus einer intraokularen Probe (wässrig oder Glaskörper) gestellt. Positive Kulturen aus Blut, Zerebrospinalflüssigkeit oder einer extraokularen Stelle können sehr suggestiv sein. Die Positivitätsrate der Blutkultur variiert stark zwischen 33 und 94 Prozent der Fälle.6,8 In Ermangelung von lokalisierenden Symptomen wird berichtet, dass die diagnostische Ausbeute aus Blut bei endogener Aspergillus-Endophthalmitis sehr gering ist.14 Kulturen sollten sowohl mit aerobem als auch mit anaerobem Medium (Schokoladen-Agar, Schafsblut-Agar und Sabouraud-Agar) aufgestellt und bis zu zwei Wochen inkubiert werden. Gram-Färbung wird häufig verwendet, um Bakterien zu beurteilen. Pilzwachstum kann durch Geimsa oder Calcorfluor weiße Flecken bestätigt werden. Die Polymerase-Kettenreaktionsstudie der Gewebeprobe ist eine schnelle Methode, um verantwortliche Organismen zu identifizieren, hat jedoch den Nachteil, dass sie nicht zur Beurteilung der Empfindlichkeit gegenüber Antibiotika oder Antimykotika verwendet werden kann.
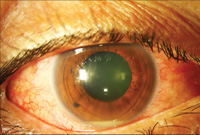
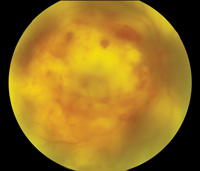
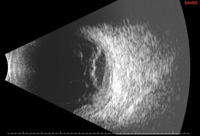
Abbildung 4. Nocardia endogene Endophthalmitis. Die anfängliche Glaskörperbiopsie war negativ und nur die subretinale Biopsie ergab positive Kulturen. Das obere Bild (4a) zeigt Hypopyon bei der Präsentation. Das mittlere Bild (4b) zeigt Fundusbefunde, einschließlich eines großen submakulären Abszesses. Die B-Scan-Sonographie (4c) zeigt eine neurosensorische Ablösung und eine submakuläre Masse.
Der Ultraschall-B-Scan des Auges ist wichtig für die Bestimmung des Ausmaßes und der Art der Glaskörperexsudate, der Skleradicke, des Aderhautabszesses und des Vorhandenseins einer Netzhautablösung. Computertomographie-Scans der Umlaufbahn helfen, orbitale Beteiligung zu identifizieren. Andere Untersuchungen wie Röntgenaufnahmen des Brustkorbs, Ultraschall-Abdomen, CT-Abdomen, Echokardiographie und Gallium-67-Scans können bei der Identifizierung eines systemischen Infektionsherds hilfreich sein.
Behandlung
* Bakterielle endogene Endophthalmitis. Soon-Phaik Chee und Kollegen berichteten, dass systemische Antibiotika aufgrund der gestörten Blut-Augenschranke therapeutische Spiegel im Auge erreichen können.1 Dennoch werden systemische Mittel am häufigsten mit intravitrealen antimikrobiellen Mitteln und Vitrektomie ergänzt, insbesondere bei prominenter Glaskörperbeteiligung. Vancomycin (1 mg / 0,1 ml) und Ceftazidim (2,25 mg / 0,1 ml) bleiben die intravitrealen Antibiotika der Wahl. Laut einer Übersichtsstudie behalten Augen, die sich einer Pars Plana-Vitrektomie unterziehen, dreimal häufiger ein nützliches Sehvermögen als diejenigen, die sich keiner Vitrektomie unterzogen haben.6 Auch diese Augen benötigen dreimal weniger Ausweidung oder Enukleation. Systemische Breitbandantibiotika wie Vancomycin, Ciprofloxacin, Aminoglykoside oder Cephalosporine der dritten Generation bildeten bisher die Hauptstütze der Behandlung, werden aber jetzt zusätzlich zur lokalen Therapie eingesetzt. Empfohlene Antibiotika sind Breitbandantibiotika, die die meisten grampositiven und negativen Organismen abdecken. Systemische Antibiotika werden in der Regel für mindestens drei bis vier Wochen oder als die extraokulare Infektion des Patienten diktiert fortgesetzt.
* Pilz endogene Endophthalmitis. Die Behandlung hängt vom Ausmaß der Augenbeteiligung ab. Systemische Therapie allein ist ausreichend, wenn die Infektion auf die Netzhaut und Aderhaut isoliert ist. Vitrektomie und intravitreale antimykotische Injektionen zusammen mit systemischer Therapie werden in Fällen empfohlen, in denen Glaskörper beteiligt ist.15
Intravenöses Amphotericin-B war klassisch das Medikament der Wahl, muss jedoch im Hinblick auf seine systemische Toxizität sorgfältig überwacht werden. Orales Voriconozol oder Fluconazol in Verbindung mit lokaler Therapie werden zunehmend verwendet. Intravitreale Injektion von entweder Voriconazol (100 µg/0.1 ml) oder Amphotericin-B (5 bis 10 µg / 0,1 ml) sorgt für sofortige, ausreichende Mengen an Antimykotikum im hinteren Segment. Voriconazol kann eine bessere Abdeckung für Aspergillus-Arten und einige Candida-Arten (wie C.glabrata und C.krusei) aufweisen, bei denen Fluconazol oder Amphotericin-B unwirksam sind. Neuere Antimykotika wie Posaconazol, Echinocandine, Micafungin, Caspofungin und Anidulafungin haben eine schlechte okuläre Penetration und werden nicht zur Anwendung bei Endophthalmitis empfohlen.16 Die Vitrektomie hilft bei der Verringerung der Infektionslast und der besseren Zugänglichkeit von Antimykotika zu intraokularen Strukturen. Die Notwendigkeit wiederholter intravitrealer Injektionen sollte auf der klinischen Verbesserung, dem Status des Auges (vitrektomisiert vs. nicht vitrektomisiert) und der Pharmakokinetik des Antimykotikums beruhen. Lokale oder systemische Kortikosteroide werden im Allgemeinen bei Pilz-Endophthalmitis vermieden,10 obwohl ihre Verwendung umstritten bleibt.14,15
Ergebnis
Endogene Endophthalmitis-Fälle haben normalerweise ein schlechtes visuelles Ergebnis. Die Sehschärfe des Zählens von Fingern oder mehr wird in 22 berichtet.2 bis 41 Prozent der Fälle.17,18 Verlust des Sehvermögens durch Erblindung, Ausweiden oder Enukleation wird in 55 bis 69 Prozent der Fälle berichtet.6 Die visuellen Ergebnisse nach der Behandlung sind bei endogener Aspergillus-Endophthalmitis im Vergleich zu Candida-Fällen schlechter und könnten auf eine frühere Erkennung einer Candida-Infektion zurückzuführen sein, was zu einer rechtzeitigeren Einleitung der Behandlung führt.15
Patienten mit extraokularen bakteriellen Infektionsherden haben eine gemeldete Mortalitätsrate von 5,6 bis 32 Prozent.19 Faktoren wie Infektion mit virulenten Organismen, schlechte Wirtsabwehr, Fehldiagnosen, die zu einer verzögerten Behandlung führen, unzureichende Behandlung, Einsatz ungeeigneter Antibiotika, Panophthalmitis werden als mit einer schlechten Prognose verbunden angesehen. Pilzinfektion hat eine hohe Mortalität, mit einer 7-prozentigen Mortalitätsrate bei systemischer Candida-Infektion.20
Endogene Endophthalmitis ist eine potenziell verheerende Augeninfektion und muss umgehend diagnostiziert und behandelt werden. Die Verwendung von kombinierten okulären und systemischen Antibiotika ist üblich. Eine systemische Koinfektion ist häufig und mit einer hohen Mortalitätsrate verbunden.
Dr. Relhan ist wissenschaftlicher Mitarbeiter für vireoretinale Erkrankungen und Uveitis am Bascom Palmer Eye Institute. Zuvor war sie Junior Consultant für vitreoretinale Chirurgie am LV Prasad Eye Institute in Hyderabad, Indien. Dr. Albini ist Associate Professor für klinische Augenheilkunde, spezialisiert auf vitreoretinale Erkrankungen und Uveitis am Bascom Palmer Eye Institute. Dr. Flynn ist Professor für Augenheilkunde, spezialisiert auf vitreoretinale Chirurgie bei Bascom Palmer. Anfragen richten Sie bitte an Dr. Albini unter [email protected] .
1. Chee SP, Jap A. Endogene Endophthalmitis. Curr Opin Ophthalmol 2001;12(6):464-70.
2. Rachitskaya AV, Flynn HW, Davis JL. Endogene Endophthalmitis durch Salmonellen Serotyp B bei einem immunkompetenten 12-jährigen Kind. Arch Ophthalmol 2012;130(6):802-4. doi: 10.1001/archophthalmol.2011.1862.
3. Chaudhry IA, Shamsi FA, Al-Dhibi H, Khan AO. Pädiatrische endogene bakterielle Endophthalmitis: Fallbericht und Überprüfung der Literatur. J AAPOS 2006;10(5):491-3. Epub 2006 September 7.
4. Flynn HW Jr. Die klinische Herausforderung der endogenen Endophthalmitis. Retina 2001;21(6):572-4.
5. Okada AA, Johnson RP, Liles WC, D’Amico DJ, Bäcker ALS. Endogene bakterielle Endophthalmitis – Bericht einer zehnjährigen retrospektiven Studie. Augenheilkunde 1994;101: 832-8.
6. Jackson TL, Eykyn SJ, Graham EM, Stanford MR (2003). Endogene bakterielle Endophthalmitis: Eine 17-jährige prospektive Serie und Überprüfung von 267 gemeldeten Fällen. Surv Ophthalmol 2003;48(4):403-23.
7. Wu ZH, Chan RP, Luk FO, Liu DT, Chan CK, Lam DS, Lai TY. Überprüfung der klinischen Merkmale, des mikrobiologischen Spektrums und der Behandlungsergebnisse der endogenen Endophthalmitis über einen Zeitraum von 8 Jahren. J Ophthalmol 2012:265078. doi: 10.1155/2012/265078. Epub 2012 Februar 23.
8. Schiedler V, Scott IU, Flynn HW Jr, Davis JL, Benz MS, Miller D. Kulturerprobte endogene Endophthalmitis: Klinische Merkmale und Ergebnisse der Sehschärfe. Am J Ophthalmol 2004;137:725-31.
9. Wong JS, Chan TK, Lee HM, Chee SP. Endogene bakterielle Endophthalmitis: eine ostasiatische Erfahrung und eine Neubewertung einer schweren Augenerkrankung. Augenheilkunde 2000;107:1483-91.
10. Lingappan A, Wykoff CC, Albini TA, Miller D, Pathengay A, Davis JL, Flynn HW Jr. Endogene Pilz-Endophthalmitis: Erreger, Managementstrategien und Ergebnisse der Sehschärfe. Am J Ophthalmol 2012;153:162-6.e1. geburtsdatum: 10.1016/j.ajo.2011.06.020. Epub 2011 September 13.
11. Sridhar J, Flynn HW Jr, Kuriyan AE, Miller D, Albini T. Endogene Pilz-Endophthalmitis: Risikofaktoren, klinische Merkmale und Behandlungsergebnisse bei Schimmel- und Hefeinfektionen. J Ophthalmic Inflamm Infizieren 2013;September 20;3(1):60. doi: 10.1186/1869-5760-3-60.
12. Binder MI, Chua J, Kaiser PK, Procop GW, Isada CM. Endogene Endophthalmitis: Eine 18-Jahres-Überprüfung kulturpositiver Fälle in einem Tertiärzentrum. Medizin (Baltimore) 2003;82(2):97-105.
13. Rao NA, Hidayat AA. Endogene mykotische Endophthalmitis: Variationen der klinischen und histopathologischen Veränderungen der Candidiasis im Vergleich zur Aspergillose. Am J Ophthalmol 2001;132(2):244-51.
14. Weishaar PD1, Flynn HW Jr, Murray TG, Davis JL, Barr CC, Gross JG, Mein CE, McLean WC Jr., Killian JH. Endogene Aspergillus-Endophthalmitis. Klinische Merkmale und Behandlungsergebnisse. Augenheilkunde 1998;105: 57-65.
15. Brod RD, Flynn HW, Miller D. Endogene Pilz-Endophthalmitis. In: Zeitschrift für Augenheilkunde. Hagerstown: Harper und Reihe; 2004. CD- ROM. ch 11
16. Bouza E1, Cobo-Soriano R, Rodríguez-Créixems M, Muñoz P, Suárez-Leoz M, Cortés C. Eine prospektive Suche nach Augenläsionen bei Krankenhauspatienten mit signifikanter Bakteriämie. Clin Infizieren Dis 2000;30(2): 306-12.
17. Riddell J 4th1, Comer GM, Kauffman CA. Behandlung der endogenen Pilzendophthalmitis: Fokus auf neue Antimykotika. Clin Infizieren Dis 2011;52(5): 648-53. ursprungsbezeichnung: 10.1093/cid/ciq204. Epub 2011 Januar 16.
18. Greenwald MJ, Wohl LG, Verkaufen CH. Metastatische bakterielle Endophthalmitis: Eine zeitgenössische Neubewertung. Surv Ophthalmol 1986;31(2):81-101.
19. Zhang YJ1, Zhang HK, Zhang Wu, Zhang ML, Zhang HH, Zhang CC, Zhang CH. Ein 10-Jahres-Vergleich der endogenen Endophthalmitis Ergebnisse: Eine ostasiatische Erfahrung mit Klebsiella pneumoniae Infektion. Retina 2004;24(3):383-90.
20. Menezes AV1, Sigesmund DA, Demajo WA, Devenyi RG. Mortalität von Krankenhauspatienten mit Candida-Endophthalmitis. Arch Intern Med 1994;154(18):2093-7.
