Angiotensin II orsakar ökningar av blodtrycket genom åtgärder på olika ställen:
- binjurar: Angiotensin II ökar frisättningen av steroidhormonet aldosteron, som verkar lokalt för att öka natriumretention och kaliumsekretion från njurarna. Nettoeffekten av detta är vattenretention, vilket återställer vätskebalansen.
- njurar: Angiotensin II ökar också natriumretentionen via direkta åtgärder på renala proximala tubuler, samt påverkar glomerulär filtreringshastighet och njurblodflöde.
- kardiovaskulärt System: Angiotensin II är en potent endogen vasokonstriktor som orsakar resistensartärer och vener att förtränga, vilket höjer blodtrycket. Dessutom i både blodkärlen och hjärtat uppmuntrar långvariga ökningar av Angiotensin II celltillväxt och resulterande hypertrofi.
- centrala nervsystemet: I hjärnan verkar Angiotensin II på den bakre hypofysen, stimulerande frisättning av antidiuretiskt hormon (ADH, även känt som arginin Vasopressin (AVP)). ADH ökar vattenreabsorptionen i njuruppsamlingskanalerna. Angiotensin II verkar också på det subforniska organet i hjärnan för att orsaka ökad törst och uppmuntra vattenintag.
kronisk aktivering av RAAS-systemet kan leda till skadlig ombyggnad och ökad inflammation i hjärtat, vaskulaturen och njurarna, liksom hypertoni och kronisk njursjukdom.
Neural kontroll av det kardiovaskulära systemet
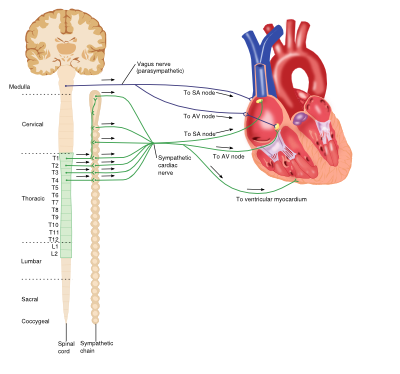
interaktion mellan det sympatiska och parasympatiska nervsystemet och hjärtat
sympatiska (adrenerga) nervsystemet
det adrenerga nervsystemet är en viktig del av många processer i hela kroppen, inklusive hjärt-kärlsystemet. Cirkulerande katekolaminer (t.ex. adrenalin och noradrenalin) binder till och aktiverar adrenerga receptorer på cellmembran. Adrenerga receptorer är en klass av G-proteinkopplade receptorer som framkallar en mängd vävnadsspecifika effekter och finns i flera subtyper.
kärl
den dominerande receptorsubtypen som finns i blodkärlen är a1-adrenerg receptor, vars aktivering genom katekolaminbindning orsakar aktivering av fosfolipas-C (PLC), inositoltrifosfat (IP3), diacylglycerol (dag) intracellulär signalväg. Detta resulterar i slutändan i myocytkontraktion, vasokonstriktion och därmed ökningar av systemiskt blodtryck.
hjärta
även om hjärtat är myogent, det vill säga drivkraften för sammandragning är självinitierad, påverkas hjärtets utgång av centrala nervsystemet. Nettoeffekten av det sympatiska systemet på hjärtat är att öka hjärtutgången. De adrenerga receptorerna som finns i hjärtat hör till subfamiljen av receptorreceptorer och inkluderar receptorreceptorer av typ 1 och 3. Katekolaminbindning till receptorreceptorer i hjärtat, som leder till ökad hjärtminutvolym via ett antal mekanismer: positiva kronotropa effekter, positiva inotropa effekter ökade automatik och ledning i både ventrikulära myocyter och den atrioventrikulära (AV) noden. Men aktivering av receptorreceptorn motverkar dessa åtgärder, vilket ger en negativ inotrop effekt och ger ett inbyggt styrsystem i hjärtat.
förlängd ökning av katekolaminnivåerna i cirkulationen (t.ex. när de utsöndras från binjurstumörer eller tider av stress) kan leda till kroniska kardiovaskulära problem som hypertoni och arytmier.
parasympatiskt nervsystem
det parasympatiska systemet är beroende av bindningen av neurotransmittorn acetylkolin (Ach) till muskarinreceptorer och har olika roller i hela kroppen.
vaskulatur
även om blodkärl uttrycker muskarinreceptorer, får de inte kolinerg innervation; men applicering av exogen Ach resulterar i en snabb och djup vasodilation.
hjärta
aktivering av muskarinreceptorer (m2-subtyp) i hjärtat av Ach som frigörs från vagusnerven orsakar en minskning av hjärtutgången via motsatta effekter mot adrenerg stimulering: negativa kronotropa effekter och minskningar av av-nodledning samt minskning av kraften i atriella sammandragningar.
trombocyt / koagulationssystem
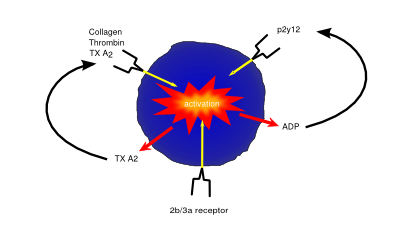
trombocytaktivering och hämning verkar genom ytreceptorer på blodplättar. Återkopplingsslingor förbättrar trombocytaktivering (t. ex. ADP som frigörs av blodplättar ökar trombocytaktiveringen genom ADP-receptorn)
blodplättar (även kända som trombocyter) är små celler som saknar kärnor som är ansvariga för hemostas eller blodkoagulering. Skada eller skada som leder till blodförlust och exponering av extracellulära kollagenfibrer detekteras, vilket aktiverar blodplättar. När de väl är aktiverade blir blodplättar klibbiga och fastnar på både den skadade kärlväggen och varandra och bildar en klump av celler eller ’koagulera’, vilket hjälper till att dämpa kärlläckan. De börjar sedan utsöndra cytokiner som uppmuntrar invasion av fibroblaster närvarande i den omgivande vävnaden som bildar en mer permanent lapp, antingen genom att skapa frisk vävnad eller deponera extracellulär matris för att bilda ett ärr.
det finns flera tillstånd där onormal koagulering kan skada kroppen; överskott av koagulering kan leda till vaskulär blockering och ischemi eller stroke; mindre vanligt kan bristande koagulering leda till överskott av blodförlust, till exempel vid hemofili. För att bekämpa dessa sjukdomar finns det läkemedel som modulerar koagulationsprocessen.
antikoagulantia
läkemedel som förhindrar koagulering (antikoagulantia) är viktiga för dem med ökad risk för koagulationsmedierad skada såsom stroke eller ischemi.förutom att vara ett smärtstillande och anti-pyretiskt medel är Aspirin ett antitrombotiskt medel som ges i låga doser till dem som riskerar skador från koagulering (t.ex. efter hjärtinfarkt). Aspirins antikoagulerande åtgärder kommer från dess undertryckande av viktiga Pro-koagulationsfaktorer såsom prostaglanding och tromboxaner via irreversibel inaktivering av ptgs-cyklooxygenasenzym. Denna undertryckning av faktorer som tromboxan A2 minskar trombocytaggregationen och förhindrar därmed koagulationsbildning.
P2Y12-hämmare såsom klopidogrel utövar sin antikoagulerande effekt via hämning av P2Y12-subtypen av trombocyt-ADP-receptorn. Genom att blockera P2Y12 förhindrar dessa läkemedel aktivering av blodplättar och bildandet av fibrinnätet som behövs för koagulering.
läkemedel som abciximab och tirofiban förhindrar koagulering via hämning av glykoprotein IIb/IIIa-receptorn som förhindrar både trombocytaktivering och aggregering.
farmakokinetik
vid administrering av läkemedel till en patient är det viktigt att känna till flera fakta om läkemedlet för att maximera effekten och minimera biverkningar/toxicitet. Dessa inkluderar information om vilken dos som är effektiv, hur länge läkemedlet förblir aktivt i kroppen, hur snabbt det bryts ner/tas bort från kroppen och hur lätt kroppen kan absorbera/använda det läkemedlet. Följande tabell beskriver dessa farmakokinetiska egenskaper och hur de beräknas:
| egenskap | beskrivning | standardenheter (förkortning) | formel |
|---|---|---|---|
| dos | mängd aktivt läkemedel som ges till patienten | mg (d) | läkemedelsspecifikt (från kliniska studier) |
| koncentration | mängd läkemedel i en given plasmavolym | usci/ml (C) | = d / VD |
| EC50 | koncentrationen av läkemedel som behövs för att framkalla ett svar halvvägs mellan noll och maximal respons. | augl/ml (EC50) | y = botten + (topp-botten)/(1+ Hill-koefficient) |
| distributionsvolym | den teoretiska volymen som läkemedlet skulle uppta om det fördelas jämnt i vävnaderna för att framkalla den aktuella plasmakoncentrationen. | L (Vd) | D/C |
| Elimineringskonstant (hastighet) | den hastighet med vilken läkemedlet avlägsnas från kroppen. | h-1 (Ke) | ln(2)/T1 / 2 eller CL/Vd |
| biotillgänglighet | hur mycket av den administrerade dosen är tillgänglig för faktisk användning av kroppen. | inga enheter som uttrycker en fraktion (f) | 100 AUC (AUC (po) CZD d (iv))/(AUC (iv) CZD d (po))
AUC = area under kurvan po = oral administrering iv = intravenös administrering |
| Cmax eller Cmin | maximal (Cmax) / minsta (Cmin) plasmakoncentration uppnådd efter läkemedelsadministrering | identifieras via direkt mätning av plasma C | |
| Tmax | den tid det tar för ett läkemedel att nå Cmax efter administrering | h (tmax) | identifieras via direkt mätning av plasma C över tid |
| halveringstid | den tid det tar för ett läkemedel att nå hälften av sin ursprungliga koncentration | h (t1/2) | ln(2) / Ke |
| Läkemedelsclearance | volymen av plasma som rensas av läkemedlet under en viss tid | l/h (CL) | vd x ke eller d / area under curve |
vanliga läkemedelsinteraktioner
det är viktigt att vara medveten om de interaktioner som kan uppstå mellan samtidigt administrerade läkemedel, eftersom de kan påverka effekt och/eller toxicitet eller ge negativa biverkningar biverkningar. Sådana interaktioner kan till exempel påverka läkemedelsabsorption, läkemedelsbiotillgänglighet eller effekt, eller kombinera för att producera oönskade metaboliter, samt eventuellt ha effekter på kliniska analyser. Om en kombination av två läkemedel minskar effekten av en eller båda av dem, kallas interaktionen en antagonistisk effekt; men om omvänt en kombination av två läkemedel ökar effekten av en eller båda av dem, kallas interaktionen en synergistisk effekt. Läkemedel som verkar på hjärt-kärlsystemet har hög interaktivitet, vilket är ett problem eftersom kardiovaskulära patienter normalt får mer än ett läkemedel. Några vanliga läkemedelsinteraktioner relaterade till kardiovaskulära läkemedel listas nedan:
| Drug | Drugs that drug action | Drugs that ↓ drug action |
|---|---|---|
| Digoxin |
|
|
| Warfarin |
|
|
| klopidogrel |
|
|
| Furosemide |
|
|
| ACE Inhibitors |
|
|
| ß-blockers |
|
|
| statiner |
|
|
det finns flera mekanismer genom vilka läkemedel bryts ner av kroppen, vanligtvis via nedbrytning av enzymer. En vanlig familj av enzymer som är involverade i läkemedelsmetabolismär familjen cytokrom P450 (CYP); en stor, mångfaldig grupp av enzymer som uppmuntrar oxidation av en mängd olika substrat, båda endogena (t. ex. steroidhormoner) och exogena (t.ex. toxiner och droger). CYP-enzymer står för upp till 75% av läkemedelsmetabolismen, vilket hjälper vissa läkemedel att bilda sina aktiva föreningar men mestadels deaktiverar läkemedel till inaktiva metaboliter som ska utsöndras. CYP-enzymer kan påverka läkemedelsverkan på flera sätt; de kan öka läkemedelsmetabolismen (antingen ökande verkan via bildning av den aktiva biprodukten eller minskande verkan genom metabolism av det aktiva läkemedlet) eller deras verkan kan hämmas av läkemedel som konkurrerar om tillgång till CYP-enzymets aktiva plats, vilket förhindrar normal interaktion mellan läkemedel och enzym. Många droger utövar sina interaktioner med andra droger viainterferens med CYP-systemet. Till exempel, om läkemedel a metaboliseras av CYP och läkemedel B hämmar CYP-aktivitet, kommer samtidig administrering att resultera i en minskad biotillgänglighet av läkemedel A. hos människor finns det 18 familjer och 43 underfamiljer av CYP-gruppen av enzymer, som riktar sig mot olika substrat. Vissa CYP-enzymer som är viktiga inom kardiovaskulär medicin, deras kardiovaskulära läkemedelssubstrat och några av deras interaktioner visas i tabellen nedan:
| enzym | substrat (t. ex.) | hämmare (t. ex.) | inducerare (t. ex.) |
|---|---|---|---|
| C2 P2C19 |
|
|
|
| CP li > statiner (atorvastatin)
|
|||
|
|
||
| CYP2D6 |
|
|
|
förutom läkemedelsinteraktioner påverkas också många läkemedels åtgärder av mat eller dryck. Till exempel bör man vara försiktig med alkoholkonsumtion med många typer av droger, eftersom det kan sätta stress på levern som redan arbetar hårt för att metabolisera droger i kroppen. Grapefruktjuice kan också orsaka problem, eftersom det är känt att hämma CYP3a. för mer information om interaktioner mellan läkemedel och mat/dryck se den här guiden: Allmän användning av läkemedel
- McMurray JJ, Adamopoulos S, Anker SD, Auricchio A, B, C, Dickstein K, Falk V, Filippatos G, Fonseca C, Gomez-Sanchez MA, Jaarsma T, K, C, L, Lip gy, Maggioni AP, Parkhomenko a, Pieske BM, Popescu BA, r p, stepinska j, Trindade pt, voors AA, Zannad f, zeiher A och Esc-Utskottet för övningsriktlinjer.. Esc riktlinjer för diagnos och behandling av akut och kronisk hjärtsvikt 2012: Arbetsgruppen för diagnos och behandling av akut och kronisk hjärtsvikt 2012 European Society of Cardiology. Utvecklad i samarbete med Heart Failure Association (HFA) av ESC. Eur Hjärta J. 2012 Juli; 33 (14): 1787-847. DOI: 10.1093/eurheartj | ehs104 / PubMed ID:22611136
- Ryd Ostergren J, Tuomilehto J, Thrainsdottir I, Vanhorebeek I, Stramba-Badiale M, Lindgren P, Qiao Q, Priori SG, Blanc JJ, budaj a, Camm j, Dean v, Deckers J, Dickstein K, Lekakis J, McGregor K, metra m, Morais J, Osterspey a, Tamargo J, Zamorano Jl, Deckers jw, Bertrand m, Charbonnel B, Erdmann e, Ferrannini e, Flyvbjerg a, Gohlke h, Juanatey Jr, Graham i, Monteiro PF, Parhofer K, Pyjamasjjjjjjjjjj, Bertrand m, Charbonnel B, Erdmann e, Ferrannini e, Flyvbjerg a, Gohlke h, Juanatey Jr, Graham i, Monteiro PF, Parhofer K, Pyjamasjjjjj, raz i, Schernthaner g, Volpe m, Trä d, arbetsgrupp på Diabetes och hjärt-kärlsjukdomar i European Society of Cardiology (ESC). och European Association for the Study of Diabetes (EASD).. Riktlinjer för diabetes, pre-diabetes och hjärt-kärlsjukdomar: sammanfattning. Arbetsgruppen för Diabetes och hjärt-kärlsjukdomar i European Society of Cardiology (ESC) och European Association for the Study of Diabetes (EASD). Eur Hjärta J. 2007 Januari; 28 (1): 88-136. DOI: 10.1093/eurheartj | ehl260 / PubMed ID:17220161
- Perk J, De Backer G, Gohlke H, Graham I, Reiner Z, Verschuren M, Albus C, Benlian P, Boysen G, Cifkova R, Deaton C, Ebrahim S, Fisher M, Germano G, Hobbs R, hackor A, Karadeniz S, Mezzani A, Prescott E, Ryden L, Scherer M, syv, trä d, Zamorano Jl, zannad f, Europeisk förening för kardiovaskulär förebyggande & rehabilitering (Eacpr). och ESC Committee for Practice Guidelines (CPG).. Europeiska riktlinjer för förebyggande av hjärt-kärlsjukdomar i klinisk praxis (version 2012). Den femte gemensamma arbetsgruppen för European Society of Cardiology and Other Societies on Cardiovascular Disease Prevention in Clinical Practice (bestående av företrädare för nio samhällen och av inbjudna experter). Eur Hjärta J. 2012 Juli; 33 (13): 1635-701. DOI: 10.1093/eurheartj | ehs092/PubMed ID:22555213
- arbetsgrupp för hantering av ST-segmenthöjning akut hjärtinfarkt av European Society of Cardiology (ESC)., Steg PG, James SK, Atar D, Badano LP, Blömstrom-Lundqvist C, Borger MA, Di Mario C, Dickstein K, Ducrocq G, Fernandez-Aviles F, Gershlick AH, Giannuzzi P, Halvorsen S, Huber K, Juni-P, Kastrati En, Knuuti J, Lenzens MJ, Mahaffey KW, Valgimigli M, van ’t Hof, A, Widimsky P, och Zahger D. ESC Riktlinjer för behandling av akut hjärtinfarkt i patienter som kommer in med ST-segmentet höjd. Eur Hjärta J. 2012 Oktober; 33 (20):2569-619. DOI: 10.1093 / eurheartj / ehs215 / PubMed ID:22922416
- Blomstru-Lundqvist C, Scheinman MM, Aliot EM, Alpert JS, Calkins H, Camm aj, Campbell WB, Haines de, Kuck KH, Lerman BB, Miller DD, Shaeffer CW Jr, Stevenson WG, Tomaselli GF, Antman EM, Smith SC Jr, Alpert JS, Faxon DP, Fuster V, Gibbons RJ, Gregoratos G, JJ, Budaj a, Burgos Ef, Cowie m, Deckers jw, Garcia ma, Klein WW, LEKAKIS J, Lindahl B, Mazzotta g, Morais JC, Oto a, Smiseth O, Trappe hj, American College of Cardiology., American Heart Association task Force om riktlinjer för Praxis. och European Society of Cardiology Committee for Practice riktlinjer. Skrivutskott för att utveckla riktlinjer för hantering av patienter med supraventrikulära arytmier.. ACC/AHA / ESC-riktlinjer för hantering av patienter med supraventrikulära arytmier-sammanfattning: en rapport från American College of Cardiology/American Heart Association task Force on Practice Guidelines och European Society of Cardiology Committee for Practice Guidelines (Writing Committee för att utveckla riktlinjer för hantering av patienter med supraventrikulära arytmier). Omsättning. 2003 Oktober 14; 108 (15): 1871-909. DOI: 10.1161 / 01.CIR.0000091380.04100.84 / PubMed ID:14557344
- European Association for Cardiovascular Prevention & rehabilitering., Reiner Z, Catapano AL, De Backer G, Graham I, Taskinen MR, Wiklund O, Agewall S, Alegria E, Chapman MJ, Durrington P, Erdine S, Halcox J, Hobbs R, Kjekshus J, Filardi PP, Riccardi G, Storey RF, Wood D och Esc Committee for Practice Guidelines (CPG) 2008-2010 och 2010-2012 utskott.. Esc / EAS riktlinjer för hantering av dyslipidemi: arbetsgruppen för hantering av dyslipidaemier från European Society of Cardiology (ESC) och European Atherosclerosis Society (EAS). Eur Hjärta J. 2011 Juli; 32 (14): 1769-818. DOI: 10.1093/eurheartj / ehr158 / PubMed ID:21712404
alla Medline abstracts: PubMed
