Urgent meddelande: när en relativt ung patient presenterar akutvård med bröstsmärta, kan det vara en ”typisk” orsak. Snabb utvärdering och noggrann bedömning av riskfaktorer är avgörande för effektiv vård och ofta patientens överlevnad.
Max Palatnik, MD
Fallpresentation
En 35-årig man presenterad vid 21:59 med ett huvudklagomål om bröstsmärta; vid 22:03 noterade vi följande:
Temp: 98.9
puls: 103
Resp: 16
Syst: 122
Diast: 69
O2Sat: 99%
historia av nuvarande sjukdom (22:47) (ordagrant)
Pt. 38-årig man med en PMH av myokardit och perikardit 1983 och 1991, som åt middag klockan 6:30 och började känna tryck över hans främre bröst medan han tittade på TV klockan 7:30. – det kändes som”några satt på mitt bröst”. Tillhörande snyfta och strålning i axeln och vänster hand ”stickningar”. Han har haft halsbränna men det kändes annorlunda. Tog bakpulver (som han normalt tar för sin halsbränna) och det hjälpte inte. Inget synkope, illamående, kräkningar, feber, RUQ-smärta eller historia av matintoleranser. Han hade några virala symtom för 2 veckor sedan (icke-produktiv hosta, sinus HA och PND som alla har löst sig. Brösttrauma, pleuritisk komponent
tidigare medicinsk historia / Triage
medicinering, vanliga allergier: ingen
PMH:myokardit / perikardit
PSH: ingen
SocHx: icke-rökare
FamHx: positivt för CAD med 52 år gammalt syskon med MI, far CABG vid 53
Examen (22:52)
allmänt: väl uppträdande; välnärd; i ingen uppenbar nöd.
Huvud: Normocephalic; atraumatisk.
Ögon: PERLA; EOM intakt
ENT: TM: S normala; normal näsa; ingen rhinorrhea; halsen är röd och milda utsöndringar.. Fuktiga slemhinnor.
hals: smidig; nontender; ingen cervikal lymfadenopati. Inga meningeal tecken
kardiovaskulär: Normal S1, S2; inga mumlar, gnuggar eller galoppar. Ingen reproducerbar bröstvägg ömhet
respiratorisk: Normal bröstutflykt med andning; andning låter klart och lika bilateralt; inga wheezes, rhonchi eller rales.
buken: normala tarmljud; icke-distended; nontender; ingen palpabel organomegali.
extremiteter: Normal ROM i alla fyra extremiteterna; nontender till palpation; distala pulser är normala och lika.
Hud: Normal för ålder och ras; varm; torr; bra turgor; inga uppenbara skador eller exsudat
Progress Notes (23:12)
han fick 2 baby aspirin och SL NTG med lindring av obehag i bröstet. Han hade sedan 1 tum Nitropaste placerad. Klockan 00: 44 återvände hans smärta och hans EKG upprepades. Han fick 15mg Maalox utan förbättring sedan 6 tum mer NTP som gjorde lindra obehag.
resultat
EKG 1: platta T-vågor sämre och i V2-V6.
EKG 2: inga ändringar
Labs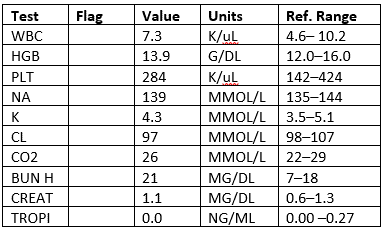
CXR: negativ
diagnos (01:57)
bröstsmärta, historia av myokardit
Disposition (02: 02)
patienten togs in på sjukhuset under telemetri.
Sjukhuskurs
Pt. genomgick seriella enzymer och upprepa EKG på morgonen. Han uteslutte för MI och släpptes. Ett efterföljande stresseko var negativt efter träning i 12,5 minuter utan obehag i bröstet eller EKG-förändringar.
andra besök
- patienten följde upp med sin PCP, diagnostiserades med GERD och startades på en PPI.
- patienten återvände till ED 6 veckor senare med brösttäthet och andfåddhet vid en måltid. Hans symtom förvärrades av ansträngning, uppträder i vila och förbättras genom upprätt positionering såväl som med Prilosec.
- ingen associerad feber, hosta, strålning, diafores, kalvsmärta, perifert ödem.
- patienten har normala vitala tecken, med en obotlig, lämplig undersökning.
- EKG avslöjar TWI i aVL, liksom nya q-vågor i V1-V2 och nsst-förändringar.
- CXR är negativt.
- Labs visar ett troponin som är >20 gånger den övre gränsen för normal.
- patienten får aspirin, heparin, Plavix, nitroglycerin och är tillåtet för akut koronarsyndrom.
- patienten genomgår perkutan koronarintervention (PCI) med framgångsrik stentplacering och släpps därefter ut i gott skick.
diskussion
bröstsmärta är det presenterande klagomålet för mer än 5% av patienterna i akutavdelningar (EDs) i USA. Utvärderingen av patienten med bröstsmärta är en enorm utmaning, till stor del på grund av den breda differentiella diagnosen, men också på grund av risken för feldiagnos. Bland de snabbast dödliga tillstånden i akutmedicin—varav många initialt kan ge akut vård—är akut koronarsyndrom (myokardiell ischemi och infarkt), aortadissektion, lungemboli, perikardit med hjärttamponad, myokardit, spänningspneumotorax och esofageal bristning. Alla dessa tillstånd tenderar att manifesteras med bröstsmärta, och alla bör övervägas tidigt i utvärderingen av patienten med bröstsmärta.
det är läkarens ansvar att utvärdera dessa patienter med listan över potentiella livshot högst upp i differentialdiagnosen. En detaljerad historia, fysisk undersökning (med fokus på hjärt -, lung-och kärlundersökningar) och grundläggande testinformation (t.ex. elektrokardiogram, bröstradiografi) kan ofta snabbt utesluta dessa livshot med rimlig noggrannhet. I de fall där denna initiala snabba bedömning inte utesluter en av de dödliga diagnoserna, kan ytterligare upparbetning i en högre skärpa vara motiverad.
även om typiska symtom på ACS beskrivs som en gradvis början av värk eller trycksmärta i bröstet med strålning till vänster arm, nacke eller käke, kan det atypiska vara mer ”typiskt.”I en stor datasyntes var de mest användbara historiska egenskaperna som ökade sannolikheten för akut hjärtinfarkt strålning till höger arm eller axel, strålning till båda armarna, smärta som förvärrades med ansträngning, diaphoresis och illamående eller kräkningar.1 Vissa delmängder, inklusive kvinnor, diabetiker och äldre är mer benägna att ha anginala symtom som representeras av andfåddhet, kräkningar, diaphoresis, generaliserad svaghet; vissa kan ha smärtfria presentationer.2 även hos de patienter med atypiska symtom som pleuritisk smärta eller påtaglig ömhet i bröstväggen sänks sannolikheten efter testet endast tillräckligt hos dem som redan har låg risk.1 uppräkning av historisk hjärtriskfaktorbörda är av litet prognostiskt värde, särskilt hos patienter äldre än 40 år.3
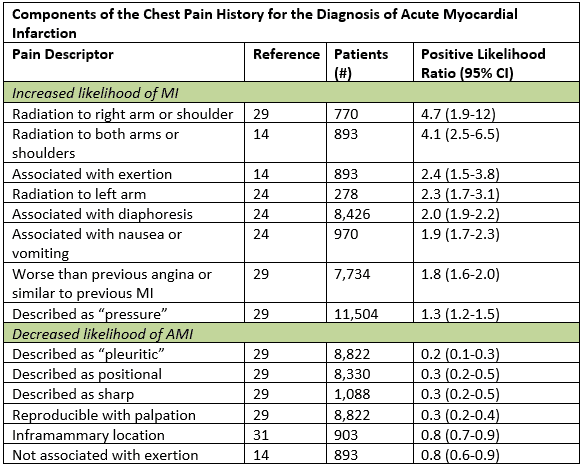
anpassad från Swap CJ, et al. JAMA. 2005;294:2623-2629.
unga patienter (<45 år) representerar en grupp med hög risk för feldiagnos av ACS, främst på grund av en tendens hos läkare att underskatta hjärtrisken. Upp till 10% av hjärtinfarkt i USA förekommer hos patienter <45 år, varav majoriteten är relaterade till aterosklerotisk hjärtsjukdom. Aterosklerotisk sjukdom noterades hos 17% av tonåringarna i en studie,4 och multivessel sjukdom noterades hos 20% av unga vuxna (medelålder: 26 år) i en obduktionsstudie av offer för våld i innerstaden.5 En nyligen genomförd ED-studie visade att 5,4% av patienterna 24 39-åringar i 39-år med bröstsmärta styrde in för ACS och 2,2% hade en negativ hjärthändelse (dvs. död, MI, behov av perkutan koronarintervention eller hjärtbypassoperation) inom 30 dagar.6 Även om den totala förekomsten av ACS är lägre hos unga patienter, bör läkare inte diskontera a avseende HPI baserat enbart på patientens ålder.
Diabetes mellitus (DM) representerar ett annat högrisktillstånd när det gäller potential för feldiagnos av ACS. Patienter med DM är benägna att smärtfria presentationer när de har hjärtischemi. Atypiska presentationer (t.ex. andnöd, förvirring, kräkningar, trötthet) förekommer i upp till 40% av fallen. Diabetespatienter är också mer benägna att ha negativa resultat från ACS.7 behandlande läkare får därför inte förlita sig på typiska presenterande klagomål för att initiera en hjärtupparbetning hos diabetespatienter, och de bör inte heller förlita sig på positiva hjärtbiomarkörer för att få ett aggressivt tillvägagångssätt för behandling hos dessa patienter.
kokainanvändning måste betraktas som en ytterligare oberoende riskfaktor för aterosklerotisk hjärtsjukdom och MI, särskilt hos unga patienter. Vissa författare uppskattar att kokain står för upp till 25% av akut MIs hos patienter <45 år.7 akut användning av kokain kan inducera koronar vasokonstriktion, ökad trombocytaggregation och/eller adrenerg stimulering som leder till dysrytmier och ischemi. Kronisk användning av kokain är också associerad med MI, vilket orsakar markant accelererad aterogenes och efterföljande tidig MI. Sammantaget har kokainanvändare en sjufaldig ökad risk för MI.8
systemisk lupus erythematosus (SLE) är en signifikant men underskattad riskfaktor för tidig ateroskleros och hjärtinfarkt. Unga patienter med SLE beräknas ha en nio gånger ökad risk för tidig MI.9 kvinnor <45 år, i synnerhet, har ökad risk, med uppskattningar av ökad risk för tidig MI så hög som femtio gånger.10 orsaken till för tidig ateroskleros i SLE är sannolikt multifaktoriell, men i stor utsträckning relaterad till samexisterande systemisk inflammation och dyslipidemier.
infektion med humant immunbristvirus (HIV) har också identifierats som en oberoende riskfaktor för för tidig ateroskleros. Bevis tyder på att HIV-infektion orsakar endotelskada på kranskärlskärl, vilket initierar en inflammatorisk kaskad som leder till aterosklerotiska lesioner.11 upptäckten av för tidig ateroskleros är särskilt framträdande hos patienter med senare stadier av HIV-infektion (CD4-tal <200).12 läkemedelsregimerna som för närvarande används vid behandling av HIV (proteashämmare) förvärrar också risken för tidig ateroskleros. Sammantaget är HIV-patienter med ACS närvarande i en ålder som är mer än 10 år yngre än icke-HIV-patienter.13
kronisk njursjukdom (CRD) har också nyligen identifierats som en oberoende riskfaktor för accelererad ateroskleros. CRD är associerad med kronisk inflammation14 och ökad trombocytaggregation.15 dessa faktorer, i kombination med en ökad prevalens av samtidiga konventionella riskfaktorer, ger en oproportionerligt hög risk för hjärthändelser hos dessa patienter.14
även om det bör erhållas och utvärderas inom 10 minuter efter presentation avseende hjärtischemi, bör EKG inte användas för att utesluta ACS. Upp till 50% av patienterna med hjärtischemi eller infarkt kommer att ha ett icke-specifikt eller normalt EKG.16 seriella EKG kan öka diagnosutbytet vid bekräftelse av närvaron av ACS hos patienter med pågående symtom.precis som EKG är hjärtbiomarkörer användbara när de är positiva, men har begränsad nytta när de är normala. Seriell biomarkörtestning under loppet av 3 6 timmar har blivit ett rutinprotokoll i många EDs och har utmärkt känslighet för att upptäcka bevis på MI. Biomarkörer kan emellertid inte åberopas för att utesluta hjärtischemi. Prospektiv validering av” HEART ” -poängen har gett utövare förmågan att på ett tillförlitligt sätt differentiera en delmängd av lågriskpatienter som sannolikt inte skulle dra nytta av ytterligare testning.17
stresstestning och koronarangiografi används oftare tidigt i utvärderingen av patienter med bröstsmärta för att styra i ACS. Även om ett negativt stresstest eller angiogram är förknippat med en lägre risk för underliggande CAD, kan inget test definitivt utesluta ACS eller närvaron av signifikanta underliggande koronartromboser. Majoriteten av stresstestningsmetoderna upptäcker bevis på signifikanta koronarskador med endast 85% till 95% känslighet.18-19 koronarangiografi är också ett ofullständigt test; falska negativa angiografi tolkningar är inte ovanliga i närvaro av diffus sjukdom, excentriska plack, ”flush” ocklusioner, gren ostiala lesioner, överlappande sidogrenar, och även när lesioner finns i den vänstra huvudkransartären.20 ytterligare kompromissa tillförlitligheten av dessa tester är data som indikerar att majoriteten av MIs uppstår från ocklusioner inom artärer som tidigare <50% hindras innan infarkt inträffade.21-23
dessa typer av lesioner är vanligtvis förknippade med negativa stresstester eller ”icke-signifikanta” angiogram om testerna görs före infarkt. Genom sin natur att upptäcka fast koronarstenos kan stresstester inte utvärdera eller förutsäga sårbara koronarplack som riskerar att lossna, vilket leder till en akut koronarhändelse. I en studie av patienter som utvärderades för ACS som hade ett negativt stresstest under de föregående 3 åren nådde över 20% det sammansatta indexet för AMI, positivt stresstest, CABG eller kateterisering med intervention, med de allra flesta negativa tester som inträffade inom 1 år efter presentationen.24 på samma sätt, på ännu mer invasiva tester män och kvinnor med antingen normal eller ”minimal” CAD på hjärtkateterisering (1,2% respektive 3,3%) hade antingen AMI eller död inom 1 år efter uppföljning.25 Det är viktigt att läkaren inte litar på tidigare objektiv testning inför en patient med tecken och symtom som indikerar ACS.
sammanfattning
utvärderingen av bröstsmärta och möjliga ACS är en högrisksträvanden. Beslutet att bedriva en” full hjärtarbete ” bör i första hand baseras på en grundlig HPI. Läkare bör vara medvetna om frekvensen av atypiska presentationer, särskilt hos kvinnor, äldre och diabetespatienter. Unga patienter förtjänar också särskild hänsyn, eftersom deras risk ofta är underskattad. Ytterligare icke-traditionella hjärtriskfaktorer, inklusive kokain, systemisk lupus erythematosus, humant immunbristvirus och kronisk njursjukdom garanterar extra uppmärksamhet. Diagnostisk testning består av elektrokardiografi (användbart att styra i ACS, men inte att utesluta diagnosen) och hjärtbiomarkörstestning, som också är främst användbara när de är positiva. Viktigt är att det negativa stresstestet eller angiogrammet är till stor hjälp vid stratifiering av patienter till låg risk för ACS och CAD, men de utesluter inte definitivt diagnosen.
citat: Palatnik M. En 38-årig man med bröstsmärta. J Brådskande Vård Med. Mars 2018. Finns på: https://www.jucm.com/a-38-year-old-man-with-chest-pain/.
- Byt CJ, Nagurney JT. Värde och begränsningar av bröstsmärtshistoria vid utvärdering av patienter med misstänkta akuta koronarsyndrom. JAMA. 2005;294:2623-2629.
- El-Menyar A, Zubaid M, Sulaiman K. atypisk presentation av akut koronarsyndrom: en signifikant oberoende prediktor för dödlighet på sjukhus. J Cardiol. 2011;57;165-171.han JH, Lindsell CJ, Storrow AB, et al. Rollen av hjärtriskfaktorbördan vid diagnos av akuta koronarsyndrom i akutavdelningen. Ann Emerg Med. 2007;49;145-152.
- Tuzcu EM, Kapadia SR, Tutar E, et al. Hög förekomst av koronar ateroskleros hos asymptomatiska tonåringar och unga vuxna: bevis från intravaskulär ultraljud. Omsättning. 2001;103:2705-2710.han är en av de mest kända i världen. Manifestationer av koronar ateroskleros hos unga traumaoffer-en obduktionsstudie. J Am Coll Cardiol. 1993;222:459-467.
- Marsan RJ Jr., rakapparat KJ, Sease KL, et al. Utvärdering av en klinisk beslutsregel för unga vuxna patienter med bröstsmärta. Acad Emerg Med. 2005;12:26-32.
- Fergus TS, Fazel R, Fang J, et al. Presentation, hantering och resultat av diabetespatienter jämfört med icke-diabetespatienter antagna för akuta koronarsyndrom. Hjärta. 2004;90:1051-1052.det finns en mängd olika typer av produkter. Kokainanvändning och sannolikheten för icke-fatal hjärtinfarkt och stroke: data från den tredje nationella hälso-och näringsundersökningsundersökningen. Omsättning. 2001;103:502-506.det finns många olika typer av spel. För tidig kranskärlssjukdom i systemisk lupus erythematosus med omfattande reocclusion efter bypassoperation av kranskärl. J Invasiv Kardiol. 2003;15:157-163.
- Manzi S, Meilahn EN, Rairie JE, et al. Åldersspecifik incidens av hjärtinfarkt och angina hos kvinnor med systemisk lupus erythematosus: jämförelse med Framingham-studien. Am J Epidemiol. 1997;145:408-415.
- Varriale P, Saravi G, Hernandez E, et al. Akut hjärtinfarkt hos patienter infekterade med humant immunbristvirus. Är Hjärta J. 2004; 147: 55-59.han är en av de mest kända i världen. Progression av ateroskleros enligt bedömning av carotid intima-media tjocklek hos patienter med HIV-infektion. Omsättning. 2004;109:1603-1608.
- Hsue PY, Giri K, Erickson S, et al. Kliniska egenskaper hos akuta koronarsyndrom hos patienter med humant immunbristvirusinfektion. Omsättning. 2004;109:316-319.
- Yerkey MW, Kernis SJ, Franklin BA, et al. Nedsatt njurfunktion och acceleration av kranskärlssjukdom. Hjärta. 2004;90:961-966.
- Aggarwal A, Kabbani SS, Rimmer JM, et al. Bifasiska effekter av hemodialys på trombocytreaktivitet hos patienter med njursjukdom i slutstadiet: en potentiell bidragsgivare till kardiovaskulär risk. Är J Njure Dis. 2002;40:315-322.
- Brady WJ, Aufderheide TP, Chan T, et al. Elektrokardiografisk diagnos av akut hjärtinfarkt. Emerg Med Clin Norr Am. 2001;19:295-320.
- Backus vara, sex AJ, Kelder JC, et al. En prospektiv validering av HJÄRTPOÄNGEN för bröstsmärtpatienter vid akutavdelningen. Int J Kardiologi. 2013;168;2153-2158.det finns många olika typer av produkter att välja mellan. Noggrannhet av bildteknik vid diagnos av akut hjärtischemi i akutavdelningen: en metaanalys. Ann Emerg Med. 2001;37:471-477.
- Lateef F, Gibler WB. Provokativ testning för bröstsmärta. Am J Emerg Med. 2000;18:793-801.
- Schwartz L, Gourassa MG. Utvärdering av patienter med bröstsmärta och normala koronarangiogram. Arch Int Med. 2001;161:1825-1833.
- Giroud D, Li JM, Urban P, et al. Förhållande av platsen för akut hjärtinfarkt till den allvarligaste koronar arteriell stenos vid tidigare angiografi. Am J Cardiol. 1992;69:729-732.
- Hackett D, Davies G, Maseri A. befintliga koronarstenoser hos patienter med första hjärtinfarkt är inte nödvändigtvis allvarliga. Eur Hjärta J. 1988; 9: 1317-23.det finns många olika typer av produkter. Koronarstenoser före och efter akut hjärtinfarkt. Am J Cardiol. 1989;63:1517-1518.
- Walker J, Galuska M, Vega D. kranskärlssjukdom i akutmottagning bröstsmärta patienter med nyligen negativ stresstestning. West J Emerg Med. 2010;11;384-388.Hemingway H, McCallum A, Shipley M, et al. JAMA 2006; 295; 1404-1411.
