utilizarea terminologiei consecvente în cadrul și între studii este esențială pentru a permite un proces eficient de încercare. Standardele CDISC precum CDASH, SDTM, SEND și ADaM standardizează structurile de utilizat la colectarea și trimiterea datelor, dar ce se întâmplă cu valorile datelor în sine?
această postare oferă o imagine de ansamblu asupra terminologiei controlate standardizate a CDISC și a modului în care ar trebui utilizată pentru a colecta și trimite date într-un mod care accelerează încercările și permite analiza încrucișată a studiilor.
Dacă sunteți interesat să citiți mai multe despre standardele CDISC, puteți citi blogurile noastre tot ce trebuie să știți despre SDTM și Introducere în standardele CDISC.
CDISC partener cu NCI pentru a defini terminologia standardizată
CDISC a colaborat cu Institutul Național al cancerului (NCI) pentru a ajuta la aducerea coerenței terminologiei în studiile clinice. Prin această colaborare a fost definit un set standard de terminologie și este actualizat trimestrial, aducând consistență semantică între studii. Folosind această terminologie, aceeași informație va fi reprezentată în același mod în cadrul studiilor.
să luăm un exemplu simplu – sexul:
- ar trebui ca bărbatul să fie reprezentat prin „Bărbat”, „Bărbat”, „M” sau „1”?
- cum ar trebui să fie înregistrată cineva care este intersex?
în zilele trecute, este posibil ca aceste informații să fi fost colectate în moduri diferite pentru fiecare studiu. Standardul terminologic CDISC NCI definește acum că singurele opțiuni permise sunt” F”,” M”,” U „și” nediferențiat „și că o persoană care este intersexuală ar trebui înregistrată ca”nediferențiată”. Puteți vedea cum acest exemplu foarte simplu face deja mult mai ușor să înțelegeți datele subiacente și să segmentați cu ușurință pentru diferite populații în cadrul studiilor.
![]() notă
notă
catalogul standardelor de date FDA impune acum ca terminologia nci standardizată să fie utilizată pentru toate studii noi. Acest lucru face viața unui recenzent mult mai ușoară, deoarece știu să interpreteze datele.

cum este definită terminologia CDISC NCI?
tabelul de mai jos arată modul în care este definită terminologia sexuală standard.
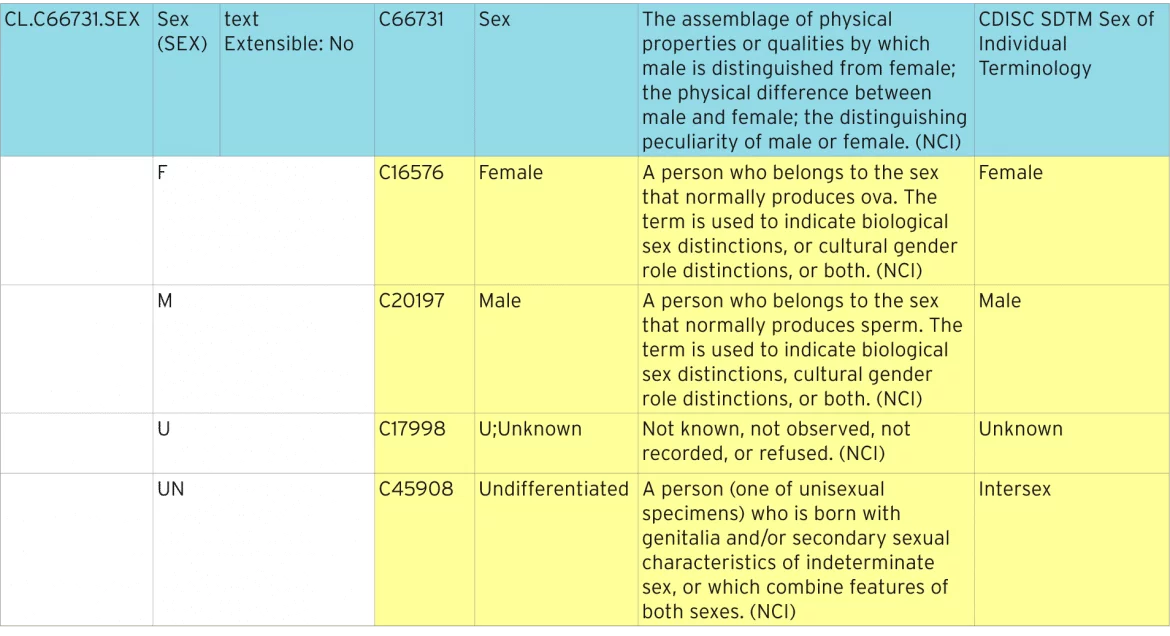
identificarea terminologiei standardizate
linia albastră reprezintă lista de coduri care conține toate codurile individuale. Lista de coduri are un „cod C” standard al „C66731”. Fiecare dintre codurile individuale are propriul cod C, de exemplu „C16576”. Aceste coduri C sunt utilizate în metadatele ODM și Define-XML pentru a identifica listele de coduri ca fiind terminologia standard nci.
extensibilitate
această listă de cod este definită ca fiind non-extensibilă, ceea ce înseamnă că oriunde este utilizată lista de cod nu trebuie să conțină termeni care nu sunt enumerați aici. Listele de coduri care sunt extensibile pot avea termeni suplimentari adăugați. Acești termeni suplimentari trebuie descriși în Define-XML ca fiind Termeni extinși și nu pot fi duplicați sau sinonimi ai Termenilor existenți.
valoarea de transmitere, sinonime, și termenul preferat
valoarea de transmitere este ceea ce trebuie să fie transmise la un regulator. Valoarea afișată efectiv pe un formular poate fi diferită și poate unul dintre sinonime sau termenul preferat.
Disponibil în mai multe culori
standardele terminologice NCI sunt disponibile într-un număr de formate pentru a se potrivi nevoilor diferite, inclusiv Excel, ODM, HTML și RDF. Exemplul de mai sus este preluat din versiunea Excel.
grupate în subseturi pentru CDASH, SDTM, ADaM și multe altele
pentru comoditate, terminologia NCI este grupată într-un număr de subseturi.
- terminologia SDTM conține termeni de utilizare într-o transmitere bazată pe SDTM
- terminologia CDASH conține termeni de utilizare în colectarea datelor bazate pe CDASH
- terminologia ADaM conține termeni de utilizare în seturile de date ADaM
- terminologia SEND conține termeni de utilizare într-o transmitere bazată pe Trimitere
- terminologia Protocolului conține termeni de utilizare cu modelul de reprezentare a Protocolului (PRM) și registrul studiilor clinice XML (CTR-XML)
utilizarea terminologiei cdisc nci într-un studiu
la definirea metadatelor de trimitere în define-XML, listele de coduri sunt utilizate pentru a defini liste fixe valori pentru anumite variabile. Conform regulamentului actual al FDA, aceste liste de coduri trebuie să fie conforme cu terminologia standardizată CDISC NCI, acolo unde există o astfel de terminologie. Acestea sunt legate de terminologia standardizată prin adăugarea de aliasuri la codurile C, de exemplu:
<Alias Name="C66731" Context="nci:ExtCodeID"/>
la definirea metadatelor de colectare a datelor în ODM nu există nicio cerință de a utiliza terminologia standardizată, totuși, acest lucru va elimina necesitatea mapării Termenilor datele colectate la datele trimise. Acest lucru simplifică foarte mult procesul de studiu end-to-end și crește coerența între studii.
gestionarea actualizărilor
gestionarea actualizărilor terminologice poate fi o cantitate semnificativă de muncă, în special cu standardele actualizate atât de regulat. De unde știți ce studii sau standarde organizaționale ar putea fi afectate de noua terminologie? Cum faceți apoi actualizările necesare într-o manieră eficientă și fiabilă?
cel mai simplu mod de a gestiona acest lucru este folosind un depozit de metadate conștient de CDISC care vă permite să definiți standarde organizaționale bazate pe terminologia standardizată și să vă construiți studiile din aceste standarde. Pe măsură ce depozitul înțelege relațiile dintre toate standardele și studiile dvs., poate simplifica procesul de actualizare la noile versiuni ale standardelor terminologice CDISC NCI.
