Ultima modificare: Duminică, 08-Nov-2009 04:44:32 CET
starea documentului: complet
cuarțul este un compus dintr-o parte siliciu și două părți oxigen, dioxid de siliciu, SiO2. Compoziția sa chimică (și elementul siliciu, Si) a fost descoperită de chimistul suedez J. Oktsns Jakob Berzelius în 1823. Dioxidul de siliciu este denumit în mod obișnuit silice.
conform IUPAC, următoarele două nume sunt corecte: dioxid de siliciu și dioxosilan.
![]()
10mm ![]()
1040×800 193kb – 2080×1600 684kb
aceasta este o mică bucată de siliciu pur produs industrial. Este o substanță cristalină ușoară (densitate 2,328 g/cm3), gri, cu luciu metalic puternic. Este foarte greu (cam la fel de greu ca cuarțul și mult mai greu decât majoritatea metalelor), dar fragil și nu maleabil ca metalele. Siliciul este baza industriei semiconductorilor: siliciul pur este doar un conductor slab de electricitate, dar atunci când se adaugă urme de elemente adecvate (siliciul este dopat), conductivitatea sa se apropie de cea a unui metal și, prin alegerea tipului și cantității de oligoelemente, proprietățile electrice ale siliciului dopat pot fi controlate.
reacții
la temperatura camerei, SiO2 în toate modificările este aproape inert și nu reacționează cu majoritatea celorlalte substanțe. Chiar și la temperaturi moderat ridicate, silica este foarte stabilă din punct de vedere chimic. Din acest motiv, cuarțul topit (sticlă de silice) este utilizat pe scară largă pentru aparatele chimice, în special atunci când reacțiile catalitice ale cationilor metalici din sticla obișnuită trebuie evitate. Motivul reactivității scăzute a siliciului este legătura foarte puternică Si-O, dar și structura sa macromoleculară.
fiind anhidritul unui acid în sine (acid ortosilicic, H4SiO4), cuarțul nu va fi în general atacat de acizi. Excepția proeminentă este acidul fluorhidric, HF, care va descompune cuarțul pentru a forma mai întâi fluorură de siliciu SiF4, apoi acid hidrofluorosilicic:
SiO2 este atacat și de substanțe alcaline (cum ar fi hidroxidul de potasiu, KOH). Viteza reacției depinde de modificare și dimensiunea cristalului: cuarțul cristalin se va dizolva doar foarte lent în soluții alcaline apoase fierbinți, în timp ce SiO2 amorf, va fi ușor dizolvat la temperaturile camerei:
reacția este relevantă pentru colector, deoarece soluțiile alcaline și detergenții sunt uneori utilizați pentru a îndepărta mușchiul și lichenii din specimenul mineral. Cristalele de cuarț nu sunt de obicei o problemă, dar aș fi foarte atent atunci când curăț soiurile criptocristaline.
o reacție similară duce la formarea gelurilor de silice în beton, când compușii alcalini ai betonului, de obicei Ca(OH)2, reacționează cu Silice amorfă și cuarț criptocristalin (adică opal și calcedonie). Silicagelul atrage apa, umflă și fisurează betonul în câteva decenii.
toate formele de silice se dizolvă în Natron topit (Na2CO3) sau potasă (K2CO3) pentru a forma silicați:
la temperaturile ridicate ale multor medii geologice, cuarțul acționează ca un acid și reacționează cu multe minerale alcaline. Un exemplu bine cunoscut este formarea mineralului wollastonite ca3si3o9 din cuarț și calcit în contact metamorfice procese la temperaturi de la aproximativ 600 C în sus:
reacția opusă are loc la intemperii rocilor silicate, aici acidul carbonic H2CO3 prezent, de exemplu, în apele meteorice eliberează acid silicic și formează carbonați.
cuarțul este” minereul ” siliciului. Siliciul este recuperat la o temperatură de aproximativ 2000 de centimetrii C în următoarea reacție endotermică (consumatoare de energie:
legătura Si-O este mult mai puternică decât legătura C-o, iar reacția funcționează doar pentru că monoxidul de carbon CO scapă din sistem ca gaz, astfel încât echilibrul sistemului este împins spre partea dreaptă. Formarea monoxidului de carbon în loc de dioxid de carbon CO2 este tipică pentru reacțiile reductive cu carbon la temperaturi ridicate. Siliciul format în acest proces nu este suficient de pur pentru producția de cipuri și trebuie purificat într-o procedură destul de complexă. Deci, în ciuda abundenței minereului său, siliciul pur este relativ scump.
solubilitatea în apă
solubilitatea dioxidului de siliciu în apă depinde de temperatură, presiune, structura sa de suprafață și de modificarea sa structurală. Următorul tabel oferă o imagine de ansamblu a solubilității la temperatura camerei și presiunea normală.
date de la:
– hollemann& Wiberg, 1985
– rykart, 1995
la temperatura camerei cuarțul este practic insolubil în apă. Apa de la robinet este de obicei aproape saturată cu silice dizolvată (în ceea ce privește cuarțul), iar procesul de dizolvare este foarte lent, deci nu este nevoie să vă faceți griji cu privire la deteriorarea cristalelor de cuarț prin curățarea repetată.
cu toate acestea, dizolvarea siliciului în roca de bază și soluri joacă un rol important în climatele calde și umede. Formarea solurilor laterite este legată de silice fiind spălat treptat din straturile de suprafață și o îmbogățire a compușilor care – cel puțin în aceste condiții climatice – sunt mai puțin solubili în apă, cum ar fi oxizii de fier și aluminiu.
la temperaturi de peste 100 de grade Celsius și presiuni ridicate solubilitatea cuarțului crește rapid. La 300 XCT este între 700 și 1200 mg/l, în funcție de presiune.
SiO2 se dizolvă în apă prin formarea acidului ortosilicic, H4SiO4:
acidul Ortosilicic este un acid foarte slab, mai slab decât acidul carbonic, de exemplu. Se disociază cu un pK1 de 9.51 conform
nu există molecule SiO2 sau agregate de tetraedre SiO4 prezente într-o soluție apoasă. Reacția inversată este modul în care cristalele de cuarț cresc, dar o moleculă H4SiO4 nu poate dispune pur și simplu de 2 molecule de apă, are nevoie de o altă moleculă H4SiO4 sau de o moleculă de silice deja prezentă, cu un capăt hidroxil (-OH):
acidul Ortosilicic este stabil doar într-o soluție apoasă diluată, nu se poate extrage acidul pur. Cea mai interesantă proprietate a acidului ortosilicic este tendința sa de a polimeriza în soluții apoase pentru a forma mai întâi un sol și mai târziu un gel de acizi polisilicici: molecule de acid ortosilicic condensate la molecule mari în funcție de reacții și . De îndată ce începeți să concentrați o soluție H4SiO4, moleculele se vor polimeriza. La temperatura camerei în condiții de laborator, punctul final al acestui proces este formarea de Silice amorfă. Gelurile de acid silicic polimerizat sunt, probabil, și predecesorii soiurilor de cuarț opal și criptocristalin (calcedonie într-un sens mai larg) în natură.
structura de bază a silice
SiO2 apare în nu mai puțin de 13 modificări structurale diferite. Structurile lor cristaline (dacă sunt prezente) pot diferi, dar toate au unele proprietăți de bază. Următoarele se aplică tuturor modificărilor de silice, cu excepția cazului în care se menționează. Structura moleculară specifică cuarțului este acoperită în capitolul structură.
legăturile chimice din silice sunt covalente: ele se bazează pe orbitali moleculari în care 2 electroni sunt împărțiți între atomi (spre deosebire de legăturile ionice care se găsesc în săruri ca fluorit sau sare de masă; aici electronii sunt transferați de la un element la altul pentru a forma ioni de sarcină electrică opusă, iar într-un cristal acești ioni sunt ținuți împreună prin atracție electrostatică).
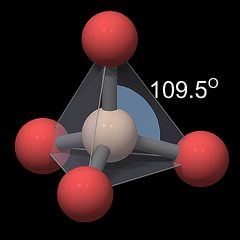
Fig.1: SiO4-tetraedru
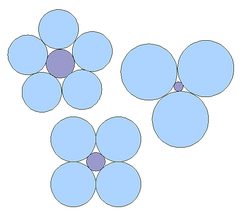
Fig.2

Fig.3: Modelul de legătură SiO4-Ionică
blocul de bază în aproape toate modificările de silice (excepțiile sunt modificări de presiune foarte mare) este unitatea SiO4, în care un atom central de siliciu este înconjurat de patru atomi de oxigen.
. |O| - | - .O-Si-O. - | - |O| .
geometria acestei unități este prezentată într-o redare cu bile și bastoane în Fig.1, cu siliciu simbolizat printr-un Fildeș colorat, oxigen printr-o sferă roșie și legături chimice prin țevi gri între ele. Dimensiunile atomilor nu sunt la scară. Atomii de oxigen ocupă poziții în jurul atomului de siliciu care îi mențin la cea mai mare distanță posibilă unul de celălalt, astfel încât formează cele patru colțuri ale unui tetraedru, simbolizat de piramida gri translucidă. Rețineți că atomii de oxigen nu sunt conectați între ei, liniile gri dintre ele au fost desenate doar pentru a vizualiza geometria tetraedrică. Unghiul legăturilor centrale O-Si-O este foarte apropiat de valoarea într-un tetraedru ideal (109,5 centi, arc gri-albastru în Fig.1), cu o distanță de oxigen de siliciu de aproximativ 0.161 nm pentru toți atomii de oxigen, deci tetraedrul individual are o simetrie aproape cubică.
legătura Si-O este extrem de polară, electronii fiind mai atrași de oxigen, ducând la o distribuție inegală a sarcinilor electrice în tetraedru: colțurile sunt mai negative, centrul este mai încărcat pozitiv.
moleculele individuale construite ca O=Si=O (cu o structură liniară ca cea a dioxidului de carbon CO2) pot fi găsite doar într-un gaz SiO2 la temperaturi de peste 2500 C.
multe manuale explică geometria tetraedrului SiO4 și a altor structuri minerale determinate de dimensiunile relative ale diferiților ioni, așa cum se arată în Fig.2: cu cât dimensiunea relativă a ionului central este mai mare, cu atât sunt necesari mai mulți ioni de sarcină opusă pentru a-l închide. În consecință, tetraedrul SiO4 este adesea desenat ca un cation mic Si4+ închis de patru mari O2 – anioni (Fig.3). Se poate argumenta că acest lucru este inexact: Siliciul și oxigenul sunt conectate prin legături covalente polare ale orbitalilor electronici uniți, deci formează o unitate și nu sunt în același mod separate și mobile liber ca ionii dintr-o sare. Compușii cu ioni Si4+ nu există de fapt. Există unele variații în interpretarea descoperirilor experimentale și, în timp ce unii autori consideră legătura Si-O ca fiind în primul rând covalentă, alții subliniază caracteristicile ionice ale legăturii. Pentru o revizuire, a se vedea Gibbs și colab., 1994 și Cohen, 1994.,
| | O O | | -O-Si-O-Si-O- | | | | O O O O | | | |-O-Si-O-Si-O-Si-O-Si-O- | | | | O O O O | | | | -O-Si-O- | O |
Fig.4: Rețeaua de silice
oxigenul este bivalent, iar atomii de oxigen din colțurile tetraedrului sunt fiecare legați de un alt atom de siliciu dintr-un tetraedru vecin. Deci cuarțul și silica în general pot fi descrise ca o rețea tridimensională de tetraedre SiO4 interconectate. O vedere schematică a structurii sale în simboluri chimice este prezentată în Fig.4. Figuri mai elaborate ale structurii moleculare de cuarț pot fi găsite în capitolul structură.
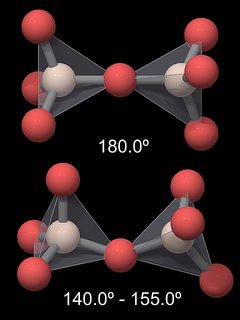
Fig.6
|
legătura Si-O-Si care leagă două tetraedre nu este dreaptă (180 la sută), ci formează un unghi de 144 la sută în cuarț (Fig.5). Ca urmare, structura cristalină generală a cuarțului este destul de complexă. În alte modificări de silice acest unghi este diferit, în timp ce unghiurile din interiorul tetraedrei SiO4 (definite de legătura O-Si-o) rămân practic aceleași. Tabelul următor listează unghiurile și distanțele pentru câteva modificări de silice.
date din:
hollemann & Wiberg, 1985
rykart, 1995
măsurare cu JMol pe baza coordonatelor unității celulare.
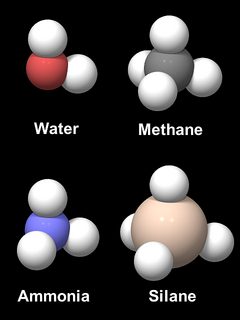
oxigenul are o tendință inerentă de a forma o legătură unghiulară X-O-X, la fel ca vecinii săi din sistemul periodic de elemente. Figura 6 prezintă modele de patru compuși de hidrogen, apă (H2O), metan (CH4), amoniac (NH3) și silan (SiH4). Distanțele interatomice și dimensiunile relative ale C, N, o și Si sunt la scară, dar atomii de hidrogen sunt supradimensionați pentru lizibilitate. Moleculele CH4 și sih4 sunt în mod evident tetraedrice. NH3 și H2O sunt aproape în formă ca o moleculă de metan cu 1 sau 2 atomi de hidrogen îndepărtați, cu un unghi H-O-H de 104,5 XCT și un unghi H-N-H de 106,8 XCT. Motivul acestei similitudini este geometria orbitalilor electronici de legare, cei patru așa-numiți orbitali hibrizi sp3, care formează un tetraedru. Un aranjament tetraedric de patru orbitali hibrizi sp3 se găsește și în siliciu și este principalul motiv pentru forma tetraedrică și rigiditatea unității SiO4 în silice și silicați.
de aici ne-am aștepta ca unghiul Si-O-Si să fie mai mic, deci de ce este mai deschis? În primul rând, deoarece legătura Si-O este foarte polară și atomii de oxigen sunt polarizați negativ, există forțe respingătoare între grupurile SiO4, iar un si-O-Si drept ar menține atomii de oxigen la o distanță mai mare. În plus, lungimea legăturii Si-O este mai mică decât cea calculată pentru o singură legătură: valoarea ar trebui să fie de 0,181 nm, dar este de fapt în jur de 0,161 nm în cuarț și are valori similare în alte modificări de silice. Aceasta este o indicație pentru un caracter parțial dublu obligatoriu al acestei legături (Hollemann & Wiberg, 1985), ceea ce ar explica, de asemenea, puterea sa mare . Această dublă legătură este în conformitate cu unghiul Si-O-Si mai mare decât se aștepta (144 int.de 109,5 int. de). Rețineți că distanța Si-O este cea mai scurtă în tridimit-tridimit, iar această modificare are un unghi Si-o-Si de 180 int. Teoria din spatele caracterului dublu obligatoriu parțial este destul de complexă și nu voi merge mai departe în ea.
silice și silicați
deși silica vorbită chimic este un oxid, în literatura mineralogică Angloamericană cuarțul și toate celelalte modificări ale siliciului sunt de obicei clasificate ca silicați (pe baza unei scheme de clasificare stabilite de Dana). Raționamentul din spatele numirii cuarțului silicat este că este construit de o rețea de tetraedre SiO4. Silicații sunt clasificați în funcție de modul în care tetraedrele SiO4 sunt integrate în structura cristalină și dacă și cum tetraedrele sunt legate între ele și, conform acestui fapt, cuarțul se numește tectosilicat („silicat de rețea” sau „silicat cadru”).
un silicat este o sare a acizilor silicici și a unuia sau mai multor metale. Acidul ortosilicic, H4SiO4, este doar cea mai simplă formă, alți acizi silicici sunt compuși din mai multe unități SiO4 legate cu hidrogen atașat.
s-ar putea crede că silicații se formează atunci când un hidroxid metalic și un acid ortosilicic reacționează, cum ar fi
dar nu acesta este modul în care silicații se formează de obicei în natură. Silicații se pot forma atunci când un oxid de metal sau un carbonat reacționează cu silice, cum ar fi
reacții similare apar de fapt în natură, formarea wollastonitului în timpul proceselor metamorfice a fost deja menționată (reacție ). Dar modul normal de formare a silicatului este cel al unei transformări: silicații reacționează între ei pentru a forma noi silicați. Odată ce tetraedrul SiO4 s-a format, acesta nu este ușor de rupt și poate fi utilizat doar în reacții pentru a forma noi inele, lanțuri, foi sau rețele de tetraedre. Doar foarte rar și în medii foarte speciale se poate găsi siliciu în minerale nesilicate.
puritatea cristalelor de cuarț
spre deosebire de majoritatea mineralelor, un cristal de cuarț clar este întotdeauna chimic pur, Cu un conținut de SiO2 care se apropie de 99,5%, adesea mai mult. Există practic două motive pentru acest lucru.
în primul rând, cuarțul are o structură macromoleculară. Nu conține ioni izolați ai unui element care ar putea fi ușor înlocuit cu un alt element. Dacă, de exemplu, o sare (un compus format din ioni izolați ținuți împreună de forțe electrostatice) crește într-o soluție apoasă, ionii săi ar putea fi înlocuiți aproape arbitrar, atâta timp cât dimensiunea și sarcina ionilor de înlocuire au o valoare identică. Când cuarțul crește dintr-o soluție apoasă, nu există literalmente nimic „atractiv” pe suprafața în creștere față de alți ioni din soluție. Numai dacă, de exemplu, o unitate de grup an este construită în locul unei unități SiO4, structura devine dezechilibrată electric și permite includerea unui cation monovalent mic suplimentar (mai ales H+, dar și Na+ sau Li+). Doar câteva elemente îndeplinesc criteriile pentru a acționa ca un înlocuitor al siliciului în unitatea SiO4, cum ar fi aluminiu în -, fosfor în + sau fier în – și declanșează includerea altor ioni. Interesant este că mineralul berlinit, AlPO4, care ar putea fi interpretat ca formula O2 este un izomorf structural al cuarțului, care prezintă proprietăți structurale și de simetrie aproape identice și proprietăți fizice foarte similare:
| Formula | sistem de cristal | densitate | duritate | indici de refracție | ||
|---|---|---|---|---|---|---|
| Berlinit | alpo4 | trigonal | 2,64 g/cm3 | 7 | 1,524-1,530 | |
| cuarț | SiO2 | trigonal | 2,65 g/cm3 | 7 | 1.544-1. 553 |
În al doilea rând, rețeaua tridimensională a tetraedrei SiO4 este destul de rigidă. Multe minerale pot tolera cantități relativ mari de anumiți alți atomi și / sau ioni în rețeaua lor cristalină fără a prezenta abateri mari în proprietățile lor fizice. Culoarea s-ar putea schimba complet, dar cristalele par clare și uniforme, deoarece rețeaua cristalină este oarecum flexibilă sau spațioasă și își menține structura originală în ansamblu. Cu toate acestea, rețeaua cristalină a cuarțului este strânsă și foarte inflexibilă (făcându-l dur, dar fragil) și numai cantități foarte mici dintr-un număr de alte elemente cu cationi mici (de obicei Li, Na, H) pot fi construite în timpul creșterii fără a distorsiona structura rețelei. Și, de fapt, cantitatea de cationi monovalenți găsiți în cuarț este aproximativ proporțională cu cantitatea de aluminiu. Cuarțul care conține cantități mai mari de alte substanțe este translucid până la opac și adesea plictisitor, deoarece cristalul „crește în jurul” mineralelor închise, iar lumina este împrăștiată la marginile diferitelor materiale.
acest lucru nu este valabil în general pentru celelalte modificări ale silicei și se pare că pentru unele dintre ele Prezența oligoelementelor are de fapt un efect stabilizator asupra structurii lor.dar, în timp ce compoziția generală a cristalelor de cuarț limpede este remarcabil de pură (cel puțin în comparație cu majoritatea celorlalte minerale), impuritățile nu sunt de obicei distribuite uniform în Cristal. Concentrațiile elementelor individuale pot varia cu un ordin de mărime la o distanță de câțiva micrometri. De exemplu, concentrația de aluminiu poate varia între mai puțin de 5 ppma (părți la un milion de atomi) și 10000 ppma într-un singur cristal (hectolitru Perny și colab. 1992). Modelul distribuției oligoelementelor poate fi vizibil cu o tehnică numită catodoluminescență: fasciculele de electroni de mare energie („raze catodice”) induc efecte de luminiscență de scurtă durată care pot fi capturate pe filmul obișnuit. Fotografiile rezultate din felii subțiri de cristale prezintă un model laminar fin. Straturile sunt paralele cu fețele de cristal, similare fantomelor, astfel încât acest model de distribuție a oligoelementelor este cauzat de schimbări rapide în mediul de creștere.
chimic pur este încă de multe ori nu suficient de pur în scopuri tehnice. Un cristal perfect, omogen este la fel de transparent ca un vid, dar oligoelementele provoacă distorsiuni și defecte în rețeaua cristalină, iar acest lucru, la rândul său, afectează proprietățile optice. Majoritatea elementelor încorporate în cuarț (H, Li, al, Na, Ti, Fe) sunt omniprezente și astfel purificarea ulterioară a siliciului este complicată și costisitoare. Din acest motiv, depozitele de cuarț cu un conținut scăzut de oligoelemente sunt încă foarte căutate (a se vedea, de exemplu, articolul de referință, articolul de referință. 2000).
informații suplimentare, Literatură, link-uri
un tabel de proprietăți de cuarț pot fi găsite la mindat.org:
un alt tabel la www.webmineral.com:
note de subsol
1 IUPAC este o organizație care are ca scop eliminarea ambiguităților și amuzant, dar nume familiare, cum ar fi Knalls Unktigure (germană pentru „acid trage”, acid fulminic) din Nomenclatura chimică. Numele vechi sunt încă valabile atâta timp cât sunt lipsite de ambiguitate. 2 unii dintre voi ar putea găsi tentant să facă unele experimente cu fluorură de hidrogen. Fluorura de hidrogen este o substanță foarte periculoasă. Doar căutați un caz într-un manual bun de toxicologie; după prelegere nu veți dori să-l atingeți nici măcar cu un stâlp. Soluția apoasă nu este un acid puternic (HF pur este), iar moleculele mici de HF nedisociate penetrează cu ușurință pielea și leagă calciul în celule pentru a forma fluorit insolubil, CaF2. Calciul este esențial pentru funcțiile vii ale tuturor celulelor corpului. O picătură mică pe un deget care trece neobservată, deoarece nu doare imediat poate – după o anumită întârziere – să provoace daune substanțiale și dureri mari.
să facem rapid matematica: 1 Mol HF = 20g. o picătură (aproximativ 50 unqql) dintr-o soluție de 20% conține 0,00005 L x (200g/l) = 0,01 g. 10 mg, care nu sună prea mult.
1 Mol Ca = 40g și 1 Mol F = 19g.1 Ca va lega 2 F, astfel 40g Ca va lega 38g F de 40G HF. 1 ml din tine țesut corporal conține aproximativ 0,1 mg Ca, iar 0,1 mg HF îl va lăsa să precipite aproape complet. În teorie, 10 mg HF din picătura mică ar putea precipita cea mai mare parte a Ca în țesutul de 100 ml, ucigând toate celulele din acesta.
și nu, nu mă opun fluorizării apei (fără ironie aici).
3termenul „apă meteorică” se referă la originea sa din atmosferă, nu din meteoriți. Grecii credeau că stelele căzătoare provin din aceeași sferă ca și norii: Stelele și planetele erau considerate ființe veșnice, ceva nori și stele căzătoare nu sunt, evident. Gândiți-vă la „meteorologie”.
4de aceea cuarțul din rocile vulcanice este adesea însoțit de calcit.
5aceasta este oarecum contra-intuitivă, dar o soluție saturată se află într-un echilibru termodinamic cu cristalul. Când o moleculă este încorporată într-o structură cristalină, se vor forma noi legături și, în funcție de geometria structurii cristaline, se eliberează sau se consumă mai multă sau mai puțină energie. Pentru a dizolva o substanță, este nevoie de energie pentru a rupe legăturile, dar energia este eliberată și atunci când moleculele de apă se orientează spre molecula dizolvată și formează noi legături electrostatice (energie de hidratizare). O modificare mai stabilă a unui compus este în general mai puțin solubilă, deoarece este necesară mai multă energie pentru a rupe legăturile.
acest lucru nu are nimic de-a face cu viteza de reacție. În anumite condiții, o modificare mai instabilă se va forma mai întâi dintr-o soluție și abia mai târziu va fi înlocuită de modificarea stabilă: Cuarțul criptocristalin se formează de obicei dintr-o soluție apoasă, dar cristobalitul și opalul fiind pași intermediari, deoarece cinetica reacțiilor este în favoarea formării opalului. Și când puneți un cristal de cuarț în 1 litru de apă pură la temperatura camerei, puteți fi destul de sigur că atunci când îl scoateți a doua zi nu va cântări cu 2,9 mg mai puțin. Probabil că va fi foarte greu să măsurați diferența. Poate după o lună sau după un an.
6traedrele din cuarț nu sunt de fapt perfect izometrice ca un tetraedru ideal, dar ușor distorsionate, deoarece Distanța până la atomul central de siliciu este de 0,16101 nm pentru 2 atomi de oxigen și 0,16145 nm pentru ceilalți 2 atomi de oxigen. Această abatere de la forma ideală este neglijabilă în majoritatea scopurilor practice, totuși, deoarece este mai mică de 0,3%.
7numerele de oxidare ale Si și O sunt într-adevăr +4 și, respectiv, -2. Energia necesară pentru a elimina efectiv 4 electroni din Si este prea mare pentru a permite o legătură pur Ionică stabilă. Chiar și SiF4 este un compus cu legături polare, dar covalente, în ciuda electronegativității ridicate a fluorului. Dar compușii Si4-anioni există (cum ar fi Ca2Si).
8Rykart (1995) dă valorile 152.8 și 143.5 pentru cuarț – și, respectiv, pentru cuarț -. Aceasta pare a fi o eroare tipografică, valorile ar trebui să fie comutate.
9dar nu este adevărat că „orice merge”. Când un mineral se formează, elementele și ionii sunt încorporați în rețeaua sa cristalină atunci când îndeplinesc anumite criterii, cum ar fi o sarcină specifică, dimensiune sau electronegativitate, și astfel sunt similare cu cele care formează deja rețeaua.
 versiune prietenoasă cu imprimanta
versiune prietenoasă cu imprimanta