ionizarea chimică (CI) este o tehnică de ionizare moale, care este aplicarea directă a rezultatelor cercetării reacțiilor moleculare și ionice în chimia analitică. Cea mai veche tehnică de ionizare a fost ionizarea cu bombardament electronic (EI). Produsul obținut de EI are multe fragmente, ceea ce este dificil de analizat. CI, care a produs foarte puține fragmente, a început în anii 1950 și are un mare potențial în chimia analitică.
în procesul CI, electronii bombardează mai întâi gazul Reactiv pentru a genera ioni de reactiv. Moleculele eșantionului sunt apoi ionizate de ioni de reactiv prin calea de reacție moleculară și Ionică. Anii 1970 au fost considerați o piatră de hotar în dezvoltarea CI. În acel moment, cercetătorii au rezolvat deficiențele muncii CI într-un mediu de vid, permițând CI să funcționeze în condiții atmosferice. Ionizarea chimică atmosferică furnizează energie din descărcarea coroanei și nu necesită un mediu de vid, ceea ce crește foarte mult gama de aplicații CI. În prezent, CI a fost utilizat pe scară largă în tehnica spectrometriei de masă.
principiul ionizării chimice
principiul CI este de a utiliza ionul reactiv X+ pentru a reacționa cu molecula de analit A pentru a realiza ionizarea analitului:
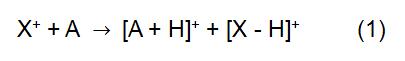
în reacția de mai sus, X+ este derivat din gazul de reacție ionizat. Unele gaze reactive comune includ metan, amoniac, apă și izobutan. Timpul de reacție și Constanta vitezei (k) din formulă pot fi obținute prin literatură sau măsurare. Când ionul reactiv X+ este H3O+, formula (2) este:
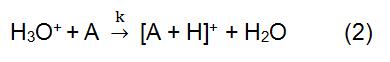
ionul reactiv este produs de o sursă de ioni. Sursele de ioni utilizate în mod obișnuit includ în principal sursa de radiații, sursa de alimentare cu descărcare catodică goală și sursa de alimentare obișnuită cu descărcare strălucitoare. 210Po și 241Am sunt cele mai frecvente surse de radiații. Procesul de ionizare începe cu particulele alfa emise de 210Po și 241am. Are o energie ridicată și se poate ciocni cu gazul Reactiv pentru a genera ioni de reactiv și electroni. Dacă electronii generați sunt suficient de mari, aceștia se pot ciocni cu gazul Reactiv pentru a forma noi ioni de reactiv și electronică. În CI folosind H3O + ca ion reactiv, se folosește în mod obișnuit o sursă de alimentare cu descărcare catodică goală, care poate produce 99,5% din H3O+.
conform condițiilor de ionizare chimică, CI este clasificată în ionizare chimică de joasă presiune (
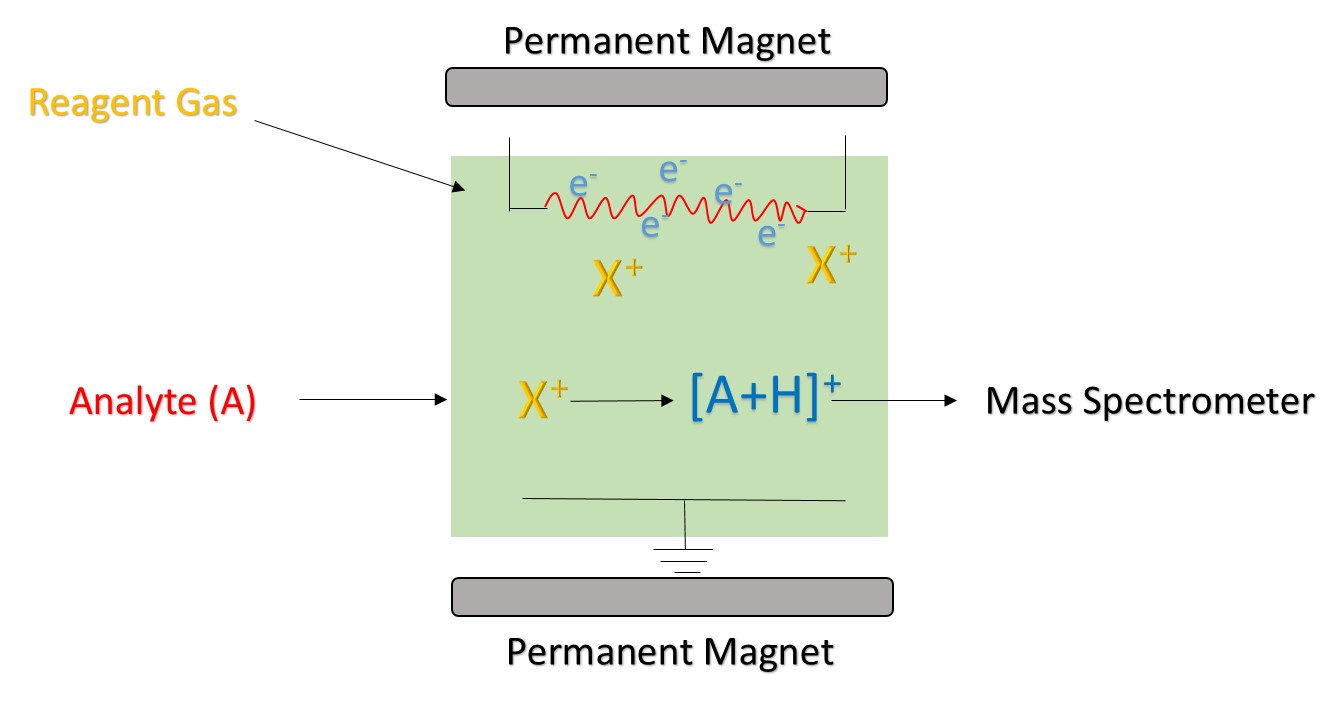 Figura 1. Principiul ionizării chimice
Figura 1. Principiul ionizării chimice
avantajele și dezavantajele CI
rezoluția spectrului CI este simplă și se poate obține greutatea moleculară exactă a analitului. Produsul obținut prin CI are puține fragmente, iar produsele sale sunt în principal molecule și ioni ai analitului. Selectivitatea CI poate fi crescută cu ușurință prin selectarea unui ion de reactiv adecvat. De exemplu, ionul reactiv H3O+ reacționează numai cu o substanță organică având o afinitate protonică mai mare decât H3O+. În plus, CI are sensibilitate ridicată și răspuns rapid (15s). Cu toate acestea, dacă ionii reactivi sunt impuri și o varietate de reacții chimice de ionizare vor avea loc în același timp, spectrometria de masă devine dificilă.
Exemple de aplicații CI
în prezent, CI este utilizat pe scară largă ca sursă de ioni în sistemele de spectrometrie de masă pentru a detecta diverse urme de substanțe. CI poate fi utilizat pentru detectarea substanțelor precum urme de gaze în atmosferă, reziduuri de pesticide în legume și fructe, melamină în lapte praf, plastifianți și erbicide în sol. În plus, CI poate fi utilizat și pentru identificarea materialelor, cum ar fi identificarea calității ceaiului.
- măsurarea compușilor organici volatili (COV)
în măsurarea COV prin CI, H3O+ este utilizat în general ca ion reactiv. H3O + nu reacționează cu majoritatea substanțelor din aer, cum ar fi O2, N2, CO2 etc. Pe de altă parte, majoritatea reacțiilor de transfer de protoni sunt nedisociate, astfel încât ionii produsului sunt unici, ceea ce face ca analiza rezultatelor să fie simplă. Principiul măsurării COV folosind H3O + ca ion reactiv este prezentat în ecuația (3). Produsul final a fost rezolvat prin spectrometrie de masă cu reacție de transfer de protoni.
- determinarea melaminei în laptele praf
în măsurarea melaminei prin CI, N2 este utilizat ca gaz reactiv. Sub acțiunea tensiunii înalte, N2 și H2O suferă reacții fizico-chimice complexe pentru a genera ioni de reactiv H3O+. Procesul de reacție este prezentat în formula (3-6). H3O + reacționează cu melamina în laptele praf, iar principiul reacției este prezentat în formula (2).
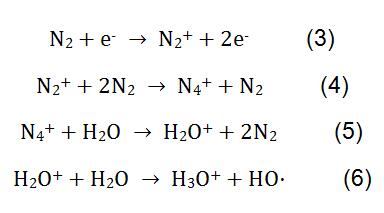
- identificarea calității ceaiului
diferite tipuri de ceai pot fi identificate prin măsurarea substanțelor chimice de pe suprafața frunzelor de ceai cu CI. H3O + reacționează cu suprafața ceaiului cu butanol, geraniol, cofeină și alte substanțe, iar produsele de reacție formează diferite spectre de masă pe spectrometrul de masă. Conținutul aceleiași substanțe în diferite soiuri de ceai este diferit, astfel încât spectrul de masă format prin detectarea CI este diferit. Spectrul de masă poate reflecta într-o oarecare măsură caracteristicile amprentelor chimice ale ceaiului. Prin urmare, CI are o valoare importantă de aplicare practică pentru identificarea rapidă și analiza calității ceaiului.ionizarea chimică este utilizată pe scară largă în spectrometria de masă datorită selectivității sale puternice și sensibilității ridicate. Spectrometria de masă cu ionizare chimică (CIMS) nu numai că permite identificarea spectrometriei de masă în tandem a substanțelor din probe complexe, dar obține și date de amprentă chimică pentru probe pentru analiza chemometrică. Aplicarea CIMS are un efect pozitiv asupra promovării dezvoltării alimentelor, medicamentelor, protecției mediului, Agriculturii și altor industrii.
am introdus pe scurt CI, un tip de metodă de ionizare, care vă poate ajuta să înțelegeți mai multe despre spectrometria de masă. La Creative Proteomics, am dezvoltat platforma profesională de spectrometrie de masă, care conține instrumente de ultimă generație. Prin utilizarea spectrometriei de masă, proteomica creativă poate oferi diferite servicii pentru a îndeplini diverse cerințe, inclusiv:
- Proteomics Service
- Metabolomics Service
- Glycomics Service
- Fales H M; și colab. Compararea spectrelor de masă ale unor compuși biologic importanți, obținute prin diferite tehnici de ionizare. Chimie Analitică, 1975, 47(2):207-219.
- Lindinger W; și colab. Monitorizarea on-line a compușilor organici volatili la niveluri de pptv prin intermediul spectrometriei de masă proton-transfer-reacție (ptr-MS) aplicații medicale, controlul alimentelor și cercetarea mediului. Jurnalul Internațional de spectrometrie de masă & procese ionice, 1998, 173(3):191-241.
- Chen H; și colab. Desorbție de suprafață presiune atmosferică ionizare chimică spectrometrie de masă pentru analiza directă a probei ambientale fără contaminare chimică toxică. Jurnalul de spectrometrie de masă, 2010, 42(8):1045-1056.
- Yang s; și colab. Detectarea melaminei în produsele lactate prin desorbție de suprafață Presiune atmosferică ionizare chimică spectrometrie de masă. Chimie Analitică, 2009, 81(7):2426.
