angiotensina II determină creșterea tensiunii arteriale prin acțiuni la diferite locuri:
- glandele suprarenale: angiotensina II mărește eliberarea hormonului steroid aldosteron, care acționează local pentru a spori retenția de sodiu și secreția de potasiu din rinichi. Efectul net al acestui lucru este retenția de apă, restabilind astfel echilibrul fluidelor.
- rinichi: Angiotensina II crește, de asemenea, retenția de sodiu prin acțiuni directe asupra tubulilor proximali renali, precum și prin afectarea ratei de filtrare glomerulară și a fluxului sanguin renal.
- sistemul Cardiovascular: angiotensina II este un vasoconstrictor endogen puternic, determinând constricția arterelor și venelor de rezistență, creșterea tensiunii arteriale. În plus, atât în vasele de sânge, cât și în inimă, creșterile prelungite ale angiotensinei II încurajează creșterea celulară și hipertrofia rezultată.
- sistemul nervos Central: În creier, angiotensina II acționează asupra glandei pituitare posterioare, stimulând eliberarea hormonului antidiuretic (ADH, cunoscut și sub numele de arginină vasopresină (AVP)). ADH crește reabsorbția apei în canalele de colectare renale. Angiotensina II acționează, de asemenea, asupra organului subfornic din creier pentru a provoca sete crescută, încurajând aportul de apă.
activarea cronică a sistemului RAAS poate duce la remodelarea dăunătoare și creșterea inflamației în inimă, vasculatură și rinichi, precum și hipertensiune arterială și boli renale cronice.
controlul Neural al sistemului Cardiovascular
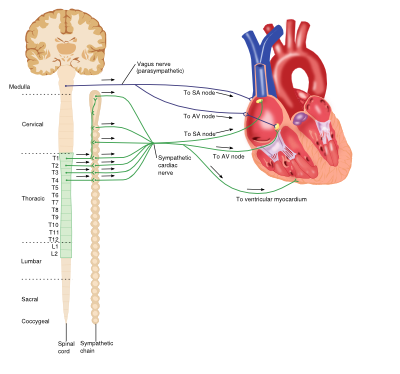
interacțiunea dintre sistemul nervos simpatic și parasimpatic și inima
sistemul nervos simpatic (Adrenergic)
sistemul nervos adrenergic este o componentă vitală a multor procese din organism, inclusiv a sistemului cardiovascular. Catecolaminele circulante (de exemplu, adrenalina și noradrenalina) se leagă și activează receptorii adrenergici de pe membranele celulare. Receptorii adrenergici sunt o clasă de receptori cuplați cu proteina G care provoacă o varietate de efecte specifice țesuturilor și există în mai multe subtipuri.
vasculatura
subtipul predominant de receptor prezent în vasele de sânge este receptorul A1-adrenergic, a cărui activare prin legarea catecolaminelor determină activarea căii de semnalizare intracelulară fosfolipază-c (PLC), inozitol trifosfat (IP3), diacilglicerol (DAG). Acest lucru are ca rezultat în cele din urmă contracția miocitelor, vasoconstricția și creșterea consecutivă a tensiunii arteriale sistemice.
inima
deși inima este miogenică, adică impulsul pentru contracție este auto-inițiat, ieșirea inimii este influențată de sistemul nervos central. Efectul net al sistemului simpatic asupra inimii este creșterea debitului cardiac. Receptorii adrenergici găsiți în inimă aparțin subfamiliei receptorului de la SEC. Legarea catecolaminei de receptorii de la centicolul 1 din inimă determină o creștere a debitului cardiac printr-o serie de mecanisme: efectele cronotrope pozitive, efectele inotrope pozitive au crescut automaticitatea și conducerea atât în miocitele ventriculare, cât și în nodul atrioventricular (AV). Cu toate acestea, activarea receptorului de la sec3 antagonizează aceste acțiuni, producând un efect inotrop negativ și oferind un sistem de control încorporat în inimă.
creșterea prelungită a nivelurilor de catecolamină din circulație (de exemplu, atunci când sunt secretate de tumori suprarenale sau perioade de stres) poate duce la probleme cardiovasculare cronice, cum ar fi hipertensiunea și aritmiile.
sistemul nervos parasimpatic
sistemul parasimpatic se bazează pe legarea neurotransmițătorului acetilcolină (Ach) de receptorii muscarinici și are diferite roluri în tot corpul.
vasculatura
deși vasele de sânge exprimă receptori muscarinici, acestea nu primesc inervație colinergică; cu toate acestea, aplicarea Ach exogenă are ca rezultat o vasodilatație rapidă și profundă.
inima
activarea receptorilor muscarinici (subtipul M2) în inimă prin Ach eliberat din nervul vag determină o reducere a debitului cardiac prin efecte opuse stimulării adrenergice: efecte cronotrope negative și scăderi ale conducerii nodului AV, precum și scăderea forței contracțiilor atriale.
trombocite/sistem de coagulare
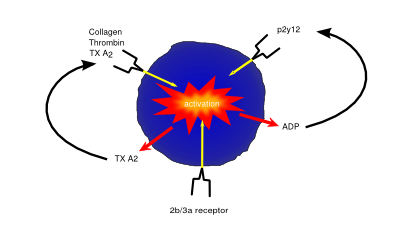
Activarea și inhibarea trombocitelor funcționează prin receptorii de suprafață ai trombocitelor. Buclele de Feedback îmbunătățesc activarea trombocitelor (de ex. ADP eliberat de trombocite crește activarea trombocitelor, prin receptorul ADP)
trombocitele (cunoscute și sub numele de trombocite) sunt celule mici lipsite de nuclee care sunt responsabile de hemostază sau de coagularea sângelui. Sunt detectate leziuni sau leziuni care duc la pierderea de sânge și expunerea fibrelor de colagen extracelular, activând trombocitele. Odată activate, trombocitele devin adezive, lipindu-se atât de peretele vasului deteriorat, cât și unul de celălalt, formând un grup de celule sau ‘cheag’, ajutând la blocarea scurgerii vasului. Apoi încep să secrete citokine care încurajează invazia fibroblastelor prezente în țesutul înconjurător, care formează un plasture mai permanent, fie prin crearea de țesut sănătos, fie prin depunerea matricei extracelulare pentru a forma o cicatrice.
există mai multe afecțiuni în care coagularea anormală poate fi dăunătoare organismului; coagularea excesivă poate duce la blocarea vasculară și ischemie sau accident vascular cerebral; mai puțin frecvent, coagularea deficitară poate duce la pierderea excesivă de sânge, de exemplu în hemofilie. Pentru a combate aceste boli, există medicamente care modulează procesul de coagulare.
anticoagulante
medicamentele care previn coagularea (anticoagulante) sunt importante la cei cu risc crescut de afectare mediată de coagulare, cum ar fi un accident vascular cerebral sau ischemie.pe lângă faptul că este un analgezic și anti-piretic, Aspirina este un agent antitrombotic administrat în doze mici celor cu risc de deteriorare din cauza coagulării (de exemplu, în urma unui atac de cord). Acțiunile anticoagulante ale aspirinei provin din suprimarea factorilor cheie pro-coagulare, cum ar fi prostaglandarea și tromboxanii, prin inactivarea ireversibilă a enzimei ciclooxigenazei PTGS. Această suprimare a unor factori precum tromboxanul A2 reduce agregarea plachetară și astfel previne formarea cheagurilor.
inhibitorii P2Y12, cum este clopidogrelul, își exercită efectul anticoagulant prin inhibarea subtipului P2Y12 al receptorului plachetar ADP. Prin blocarea P2Y12, aceste medicamente împiedică activarea trombocitelor și formarea rețelei de fibrină necesară coagulării.
medicamente precum abciximab și tirofiban împiedică coagularea prin inhibarea receptorului glicoproteinei IIb / IIIa, prevenind atât activarea, cât și agregarea plachetară.
farmacocinetica
când se administrează medicamente unui pacient, este esențial să se cunoască mai multe fapte despre medicament pentru a maximiza eficacitatea și a minimiza efectele secundare / toxicitatea. Acestea includ informații despre ce doză este eficientă, cât timp medicamentul rămâne activ în organism, cât de repede este descompus/eliminat din organism și cât de ușor organismul poate absorbi/utiliza acel medicament. Următorul tabel detaliază aceste proprietăți farmacocinetice și modul în care sunt calculate:
| proprietate | descriere | unități Standard (abreviere) | Formula | |
|---|---|---|---|---|
| doza | Cantitatea de medicament activ administrat pacientului | mg (D) | medicament specific (din studiile clinice) | |
| concentrație | cantitatea de medicament într-un volum plasmatic dat | (c) | = d/vd | |
| EC50 | concentrația de medicament necesară pentru a obține un răspuns la jumătatea distanței dintre răspunsurile zero și maxim. | (EC50) | y = bottom + (Top-Bottom)/(1+ coeficient Hill) | |
| volumul de distribuție | volumul teoretic pe care medicamentul l-ar ocupa dacă ar fi distribuit uniform în țesuturi pentru a obține concentrația plasmatică curentă. | L (Vd) | D/C | |
| constanta de eliminare (rata) | rata la care medicamentul este eliminat din organism. | h-1 (Ke) | ln(2)/t1 / 2 sau CL/Vd | |
| biodisponibilitate | cât din doza administrată este disponibilă pentru utilizarea efectivă de către organism. | nu există unități care să exprime o fracție (f) | 100 (ASC (po), d (iv))/(ASC (iv), d (po))
ASC = aria de sub curbă po = administrare orală iv = administrare intravenoasă |
|
| Cmax sau Cmin | concentrația plasmatică maximă (Cmax)/minimă (Cmin) atinsă după administrarea medicamentului | (Cmax sau Cmin) | identificat prin măsurarea directă a plasmei c | |
| timpul necesar unui medicament pentru a atinge Cmax după administrare | h (tmax) | identificat prin măsurarea directă a plasmei C peste timp | ||
| timp de înjumătățire | timpul necesar unui medicament pentru a atinge jumătate din concentrația inițială | h (t1/2) | ln(2) / Ke | |
| Clearance-ul medicamentului | volumul plasmatic eliminat de medicament într-un timp stabilit | l/h (CL) | VD x ke sau D / Zona de sub curbă |
interacțiuni medicamentoase comune
este important să fiți conștienți de interacțiunile care pot apărea între medicamentele administrate concomitent, deoarece acestea pot afecta eficacitatea și/sau toxicitatea sau pot produce efecte adverse efecte. Astfel de interacțiuni ar putea, de exemplu, să afecteze absorbția medicamentului, biodisponibilitatea sau eficacitatea medicamentului sau să se combine pentru a produce metaboliți nedoriți, precum și să aibă efecte asupra analizelor clinice. Dacă o combinație de două medicamente scade efectul unuia sau al ambelor, interacțiunea este denumită efect antagonist; cu toate acestea, dacă, dimpotrivă, o combinație de două medicamente sporește efectul unuia sau al ambelor, interacțiunea este denumită efect sinergic. Medicamentele care acționează asupra sistemului cardiovascular sunt bogate în interactivitate, ceea ce reprezintă o problemă, deoarece pacienții cardiovasculari primesc în mod normal mai multe medicamente. Unele interacțiuni medicamentoase comune legate de medicamentele cardiovasculare sunt enumerate mai jos:
| Drug | Drugs that drug action | Drugs that ↓ drug action |
|---|---|---|
| Digoxin |
|
|
| warfarină |
|
|
Clopidogrel |
|
|
| Furosemide |
|
|
| ACE Inhibitors |
|
|
| ß-blockers |
|
|
|
există mai multe mecanisme prin care medicamentele sunt defalcate de organism, de obicei prin degradarea de către enzime. O familie comună de enzime implicate în metabolizarea medicamentelor este familia citocromului P450 (CYP); un grup mare și divers de enzime care încurajează oxidarea unei varietăți de substraturi, atât endogene (de ex. hormoni steroizi) și exogeni (de exemplu, toxine și medicamente). Enzimele CYP reprezintă până la 75% din metabolismul medicamentelor, ajutând unele medicamente să-și formeze compușii activi, dar mai ales dezactivând medicamentele în metaboliți inactivi pentru a fi excretați. Enzimele CYP pot influența acțiunile medicamentului în mai multe moduri; pot crește metabolismul medicamentului (fie creșterea acțiunii prin formarea subprodusului activ, fie scăderea acțiunii prin metabolismul medicamentului activ) sau acțiunea lor poate fi inhibată de medicamente care concurează pentru accesul la situsul activ al enzimelor CYP, prevenind interacțiunea normală dintre medicament și enzimă. Multe medicamente își exercită interacțiunile cu alte medicamenteinterferența cu sistemul CYP. De exemplu, dacă medicamentul a este metabolizat de CYP și medicamentul B inhibă activitatea CYP, administrarea concomitentă va duce la o biodisponibilitate scăzută a medicamentului A. la om există 18 familii și 43 de subfamilii ale grupului de enzime CYP, care vizează diferite substraturi. Unele enzime CYP importante în medicina cardiovasculară, substraturile lor cardiovasculare și unele dintre interacțiunile lor sunt prezentate în tabelul de mai jos:
| enzimă | substraturi (de exemplu) | inhibitori (de exemplu) | inductori (de exemplu. C2 P2C19 |
|
|
|---|---|---|---|---|---|
| CP li > statine (atorvastatină)
|
CYP2C9 |
|
|
|
|
| CYP2D6 |
|
|
|
pe lângă interacțiunile medicament-medicament, acțiunile multor medicamente sunt afectate și de alimente sau băuturi. De exemplu, trebuie să aveți grijă la consumul de alcool cu multe tipuri de medicamente, deoarece poate pune stres pe ficat, care lucrează deja din greu pentru a metaboliza medicamentele în organism. Sucul de Grapefruit poate provoca probleme, deoarece se știe că inhibă CYP3a. pentru mai multe informații despre interacțiunile dintre medicamente și alimente/băuturi, consultați acest ghid: Utilizarea generală a medicamentelor
- McMurray JJ, Adamopoulos S, Anker SD, Auricchio A, B Oktihm m, Dickstein K, Falk V, Filippatos G, Fonseca c, Gomez-Sanchez MA, Jaarsma T, K Unktiber L, Lip GY, Maggioni AP, Parkhomenko A, Pieske BM, Popescu Ba, R Oktibnnevik PK, Rutten FH, Schwitter J, Seferovic P, stepinska J, Trindade pt, voors AA, Zannad F, ZEIHER a și Comitetul Esc pentru orientări practice.. Orientări ESC pentru diagnosticul și tratamentul insuficienței cardiace acute și cronice 2012: Grupul de lucru pentru diagnosticul și tratamentul insuficienței cardiace Acute și cronice 2012 al Societății Europene de Cardiologie. Dezvoltat în colaborare cu Asociația de insuficiență cardiacă (HFA) a ESC. Eur Inima J. 2012 Iulie; 33 (14):1787-847. DOI: 10.1093 / eurheartj / ehs104 / PubMed ID:22611136
- Ryd l, Standl e, Bartnik M, Van den Berghe G, Betteridge J, De Boer MJ, Cosentino F, J, Laakso m, Malmberg K, Priori s, Ostergren J, Tuomilehto J, Thrainsdottir I, Vanhorebeek I, Stramba-Badiale m, Lindgren P, Qiao Q, Priori SG, Blanc JJ, budaj a, Camm j, decan v, Deckers J, Dickstein K, Lekakis J, McGregor K, Metra m, Morais J, osterspey a, Tamargo J, Zamorano Jl, Deckers JW, Bertrand m, Charbonnel b, Erdmann e, Ferrannini e, Flyvbjerg a, Gohlke h, Juanatey Jr, Graham i, Monteiro PF, raz i, schernthaner g, Volpe m, lemn D, Task Force on Diabetul și bolile cardiovasculare ale Societății Europene de Cardiologie (ESC)., și Asociația Europeană pentru studiul diabetului (EASD).. Linii directoare privind diabetul, pre-diabetul și bolile cardiovasculare: rezumat executiv. Grupul Operativ pentru diabet și Boli Cardiovasculare al Societății Europene de Cardiologie (ESC) și al Asociației Europene pentru studiul diabetului (EASD). Eur Inima J. 2007 Ianuarie; 28 (1): 88-136. DOI: 10.1093 / eurheartj / Ehl260 / PubMed ID:17220161
- Perk J, De Backer G, Gohlke H, Graham i, Reiner Z, Verschuren M, Albus C, Benlian P, Boysen G, Cifkova R, Deaton C, Ebrahim S, Fisher m, Germano G, Hobbs R, Hoes a, Karadeniz s, Mezzani a, Prescott e, Ryden L, Scherer M, syv c, wood d, Zamorano JL, zannad f, Asociația Europeană pentru prevenirea cardiovasculară & reabilitare (Eacpr)., și Comitetul ESC pentru orientări Practice (CPG).. Orientări europene privind prevenirea bolilor cardiovasculare în practica clinică (versiunea 2012). Al cincilea grup operativ comun al Societății Europene de Cardiologie și al altor societăți privind prevenirea bolilor cardiovasculare în practica clinică (constituit din reprezentanți ai nouă societăți și de experți invitați). Eur Inima J. 2012 Iulie; 33(13):1635-701. DOI: 10.1093 / eurheartj / ehs092 / PubMed ID: 22555213
- grupul de lucru pentru gestionarea infarctului miocardic acut cu supradenivelare de segment ST al Societății Europene de Cardiologie (ESC)., Steg PG, James SK, Atar D, Badano LP, bl Unkstrom-Lundqvist c, Borger MA, di Mario c, Dickstein K, Ducrocq G, Fernandez-Aviles F, Gershlick AH, Giannuzzi P, Halvorsen s, Huber K, Juni P, Kastrati a, Knuuti J, lenzen MJ, Mahaffey KW, Valgimigli M, van ‘t Hof a, Widimsky P, și Zahger D. ghidurile ESC pentru tratamentul infarctului miocardic acut la pacienții cu supradenivelare de segment ST. Eur Inima J. 2012 Octombrie; 33 (20): 2569-619. DOI: 10.1093 / eurheartj | ehs215 / PubMed ID:22922416
- Blomstr-Lundqvist c, Scheinman MM, Aliot EM, Alpert JS, Calkins H, Camm AJ, Campbell WB, Haines de, Kuck KH, Lerman BB, Miller DD, Shaeffer CW Jr, Stevenson WG, Tomaselli GF, Antman EM, Smith SC Jr, Alpert JS, Faxon DP, Fuster V, Gibbons RJ, Gregoratos G, Hiratzka LF, hunt sa, Jacobs ak, Russell ro Jr, priori SG, Blanc JJ, Budaj a, Burgos EF, Cowie m, Deckers JW, Garcia ma, Klein Ww, LEKAKIS J, Lindahl b, Mazzotta g, Morais JC, Oto a, Smiseth o, Trappe Hj, Colegiul American de Cardiologie., Grupul de lucru American Heart Association privind orientările Practice., și Societatea Europeană de Cardiologie Comitetul pentru orientări Practice. Comitetul de scriere pentru a elabora orientări pentru gestionarea pacienților cu aritmii supraventriculare.. Orientări ACC / AHA / ESC pentru managementul pacienților cu aritmii supraventriculare — rezumat executiv: un raport al Colegiului American de Cardiologie/American Heart Association Task Force privind ghidurile de practică și al Societății Europene de Cardiologie Comitetul pentru ghiduri de practică (Comitetul de scriere pentru elaborarea ghidurilor pentru managementul pacienților cu aritmii supraventriculare). Circulație. 2003 14 octombrie; 108 (15):1871-909. DOI: 10.1161 / 01.CIR.0000091380.04100.84/PubMed ID:14557344
- Asociația Europeană pentru prevenirea cardiovasculară & reabilitare., Reiner Z, Catapano AL, De Backer G, Graham I, Taskinen MR, Wiklund O, Agewall s, Alegria e, Chapman MJ, Durrington P, Erdine s, Halcox J, Hobbs R, Kjekshus J, FILARDI PP, Riccardi G, Storey RF, Wood D, și Comitetul ESC pentru orientări Practice (CPG) 2008-2010 și 2010-2012 comitete.. Orientări ESC / EAS pentru gestionarea dislipidemiilor: grupul de lucru pentru gestionarea dislipidemiei al Societății Europene de Cardiologie (ESC) și al Societății Europene de ateroscleroză (EAS). Eur Inima J. 2011 Iulie; 32(14):1769-818. DOI: 10.1093/eurheartj | ehr158 / PubMed ID: 21712404
toate rezumatele Medline: PubMed
