Processo de Formação Individual do embrião
Uma grande variedade de tipos de células compõem o corpo humano, que é composto de cerca de 60 trilhões de células no total. Cada uma dessas células é, em última análise, derivada de um único óvulo fertilizado, que começou a se dividir, eventualmente diferenciando-se em células somáticas de diferentes morfologia e função que formam os vários tecidos e órgãos do corpo humano. Considera-se que as células estaminais pluripotentes têm um potencial semelhante sem diferenciação extraembriónica.
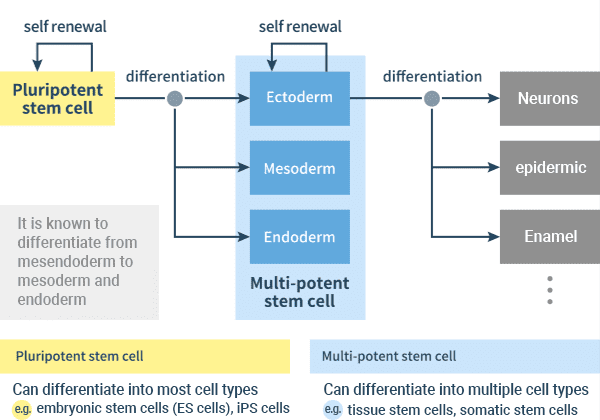
Figure: A indução de vários tecidos tipos de células a partir de células-tronco pluripotentes através de três camadas germinativas
No processo de formação de um indivíduo, as células-tronco de mudança (diferenciar) em células que são diferentes de si mesmos mantendo a proliferação capacidade de se dividir e criar mais células do mesmo tipo, ou diferenciá-los em uma forma especializada. É assim que vários órgãos são criados.
No estágio de blastocisto, um estágio inicial do desenvolvimento embrionário, existem células que são capazes de se diferenciar em quase qualquer tipo de célula que compõe o corpo, uma habilidade conhecida como pluripotentcy.In vitro, células-tronco pluripotentes incluindo o ES células e as células iPS podem se diferenciar em tipos de células derivadas da endoderm, mesoderma e ectoderm, mas não são capazes de desenvolver-se em um organismo completo sozinho. Em contraste, as células-tronco que só podem diferenciar – se em um número limitado de tipos de células, tais como células-tronco tecidulares e células-tronco somáticas, são conhecidas como células-tronco multipotentes.
estas células são usadas não só para pesquisa básica, onde são diferenciadas em células específicas para examinar suas propriedades, mas também para “rastreio de descoberta de drogas” para procurar candidatos a drogas, e “medicina regenerativa” onde são transplantados ou administrados a pacientes como agente terapêutico. No entanto, a cultura de células estaminais pluripotentes é diferente da cultura de células somáticas convencionais em muitos aspectos, e diz-se que é difícil manter o estado indiferenciado e garantir um elevado nível de reprodutibilidade.
Classificação e Características de as Células Estaminais multipotentes e Células-Tronco Pluripotentes
as Células Estaminais multipotentes
as células estaminais multipotentes têm a capacidade de se diferenciar em células que compõem específicas de tecidos e órgãos, e inclui tanto o tecido de células-tronco e células-tronco somáticas.as células estaminais do tecido são específicas do tecido, e têm a capacidade de se auto-renovar por divisão em células filhas do tipo similar ou de se diferenciar em células mais especializadas dentro do tecido.células estaminais somáticas existin vivo e podem diferenciar-se num número limitado de tipos de células. As células-tronco mesenquimais (MSCs) são um tipo de célula-tronco somática, e podem diferenciar-se em osso, cartilagem, vasos sanguíneos e cardiomiócitos. As MSCs são obtidas com relativa facilidade a partir da medula óssea, do tecido do cordão umbilical, do sangue do cordão umbilical e do tecido adiposo.as células estaminais multipotentes têm um efeito anti-inflamatório, um efeito indutor do factor de crescimento, um efeito proangiogénico e desempenham um papel importante na reparação dos tecidos. Além disso, diz-se que eles têm um risco reduzido de cancelamento em comparação com as células estaminais pluripotentes, uma consideração de segurança importante.os medicamentos regenerativos já foram aprovados em todo o mundo para o tratamento de lesões da medula espinhal e transplantação de células estaminais hematopoiéticas após transplante agudo de enxerto versus hospedeiro.
posição numa tabela: Examples of Approved Regenerative Medical Products That Use Human MSCs in the World-
| Regenerative Medical Products | Approved Countries | Manufacturing Distributors | Origin MSC | Applications |
|---|---|---|---|---|
| PROCHYMAL® | Canada, New Zealand | Mesoblast | Allogeneic bone marrow-derived MSC | Acute GVHD*(pediatric) |
| TEMCELL® HS Inj. | Japan | JCR Pharma | Allogeneic bone marrow-derived MSC | Acute GVHD* |
| Stemirac® Inj. | Japan (conditional approval) | Nipro | Autologous bone marrow-derived MSC | Spinal cord injury |
| Heartcellgram-AMI® | South Korea | Pharmicell | Autologous bone marrow-derived MSC | Acute myocardial infarction |
| Cupistem® | South Korea | Anterogen | MSC derived from own fat | Crohn’s disease |
| CARTISTEM® | South Korea, EU | Medipost | Allogeneic cord blood-derived MSC | Knee osteoarthritis |
| Stempeucel® | EU, India (conditional approval) |
Stempeutics Research |
Allogeneic bone marrow-derived MSC | Knee osteoarthritis |
| Allostem® | USA | Allosource | Allogeneic fat derived MSC (A combination product composed of human demineralized bone matrix) |
Bone damage |
| Osteocel® Plus | US | NuVasive | Allogeneic bone marrow-derived MSC (A combination product composed of osteoprogenitor cells and human demineralized bone matrix) |
Bone repair (361HCT/P) |
*GVHD: Graft Versus Host Disease
células-tronco Pluripotentes
– tronco Pluripotentes células-tronco são células que podem se diferenciar em quase todas as células que compõem o corpo. Até à data, os ESCs, as células germinativas embrionárias (AECT) e os ipssc foram estabelecidos como tipos de células estaminais pluripotentes.ESCs são estabelecidos a partir da massa da célula interna dentro do blastocisto oco, que é um estágio inicial de desenvolvimento embrionário após a divisão do zigoto em uma blastula. No Japão, células ES são estabelecidas a partir do suprimento excedente de óvulos fertilizados que são descartados após o tratamento da infertilidade. Os EGCs são desenvolvidos a partir dos precursores celulares do esperma e dos óvulos (células germinais primordiais) e têm quase as mesmas propriedades que os ESCs.
IPSS são criados pela reprogramação de células somáticas para um estado indiferenciado através da introdução de genes específicos. A criação do ipsscs permitiu-nos obter células semelhantes ao ESCs de doadores. Também é possível obter Tecido fornecido por um paciente com uma doença, estabelecer IPSS a partir do tecido, e induzir diferenciação para fornecer um modelo anin vitro da doença. Portanto, as células somáticas, tais como as células nervosas ou cardiomiócitos, criadas pela diferenciação induzida de IPSS têm grande potencial para aplicações como a determinação da etiologia da doença, avaliação da eficácia do fármaco e efeitos colaterais, e transplante em pacientes como terapias de Medicina Regenerativa. No entanto, foram notificadas mutações genéticas não intencionais ao estabelecer culturas de iPSC, bem como ao subculturar ipsscs e ESCs durante longos períodos de tempo. Actualmente, desconhece-se se todas estas mutações genéticas são perigosas e os investigadores estão a discutir a melhor forma de avaliar a sua segurança para utilização prática no futuro.
