Qual é a densidade das células?
Modo Leitor
a densidade do material biológico é responsável pela fixação das células para o fundo dos nossos tubos de laboratório e placas multi-poço e serve como base da centrifugação de rotina que faz parte da vida diária de tantos biólogos. Estas mesmas diferenças de densidade entre as células e o seu exterior aquoso são também a base do contraste que observamos em imagens de microscopia de fase. Estas diferenças também são importantes fora do ambiente do laboratório. Por exemplo, plâncton tem que lidar com esta diferença de densidade para permanecer em uma profundidade no oceano onde a luz solar é abundante em vez de afundar para as profundezas escurecidas. Dado que a maioria dos biólogos e bioquímicos fazem uso da separação baseada na densidade em uma base diária, parece surpreendente como raramente densidades como as coletadas na Tabela 1 são realmente discutidas.
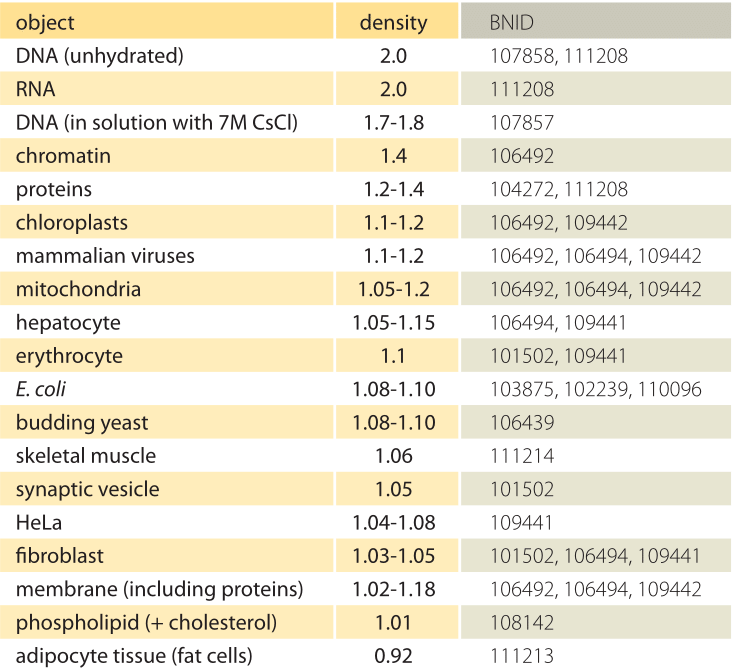
Tabela 1: Densidades de objetos biológicos em relação à água. Isto é quase equivalente a dar-lhes em unidades de g / ml ou 1000 kg / m3. Os valores são ordenados por ordem decrescente. Salvo indicação em contrário, os valores foram medidos em sacarose ou em solução ficoll.
Qual é a base subjacente para as diferentes densidades de diferentes organelas e tipos de células? Em grande medida, estas diferenças podem ser atribuídas à relação entre o teor de água e a massa seca. Proteínas têm uma densidade de ≈1,3-1,4 (BNID 104272, 101502) em relação à água (ou quase equivalentemente em unidades de g/ml ou 1000 kg/m3). Dado o valor de referência de 1 para a densidade da água, um espectro de valores intermédios para a densidade celular entre 1 e 1.3 são obtidos com base na abundância relativa de proteínas e água. Os lípidos estão na extremidade baixa ao lado da água a uma densidade de cerca de 1 (BNID 108142). No outro extremo, grânulos de amido com uma densidade de ≈1,5 (BNID 103206) e nucleótidos a ≈1.7 podem mudar o balanço de massa geral na direção oposta.sabendo que a densidade é muitas vezes baseada no local onde um dado componente biológico se instala quando girado numa centrifugadora contendo um gradiente de concentrações frequentemente produzidas pela sacarose ou, no caso do ADN, cloreto de césio. A densidade reflete a massa dividida pelo volume, mas para compostos carregados em solução, a densidade também é afetada por conchas da chamada água ligada. A densidade, neste caso, torna-se uma densidade efetiva, reduzida pela água ligada, e, portanto, um pouco dependente da concentração de sal (BNID 107858).
a taxa de sedimentação, como ocorre em uma centrifugadora, é quantificada em unidades de Svedberg, que é a origem dos nomes 70, 23S, etc. para o ribossomo e suas subunidades rRNA. Um rRNA 23S irá sedimento a uma velocidade de 23×10-12 m/s sob gravidade normal. Num ultracentrifugador que produz uma aceleração de um milhão de g, A velocidade aumentará proporcionalmente para 23×10-6 m/s ou cerca de 1 mm/min. A taxa de sedimentação depende da densidade, tamanho e forma da molécula. Para formas e densidades semelhantes, as escalas de velocidade de sedimentação são a raiz quadrada da massa molecular. Para tais casos, a massa molecular vai como o quadrado da taxa de sedimentação, de tal forma que o 23S e 16S subunidades do ribossoma, tem uma massa molecular, com uma proporção de cerca de (23/16)2 ou cerca de 2, que está intimamente alinhado com as medições de 0,9 e 0.5 MDa respectivamente (BNID 110972, 110967). Na clínica, a taxa de sedimentação dos eritrócitos (glóbulos vermelhos) é rotineiramente utilizada para medir a inflamação. Taxas muito superiores a 10 mm / hora geralmente indicam a presença do fator de pró-sedimentação fibrinogénio que é um indicador geral de uma condição inflamatória.
é bem conhecido que a água é a fração molecular mais abundante das células, mas quão abundante exatamente? Se examinarmos tecidos de organismos multicelulares, encontrar o conteúdo de água é uma tarefa simples de medir a massa do tecido antes e depois da secagem. Mas como se pode realizar tais medições para as células? Quando pesamos uma massa de células antes e depois da secagem, como medimos apenas as células sem água à sua volta? Mesmo após a centrifugação, há água deixada na célula, resultando em ambiguidade sobre a massa seca em si.
Mais uma vez a rotulagem isotópica radioactiva vem em Socorro (Cayley et al, 1991). Em primeiro lugar, a água marcada (usando trítio, 3H) é medida em um sedimento celular. Isto indica a soma de água dentro e fora das células. Em seguida, outro composto solúvel que é rotulado, mas que não pode entrar na célula, como 14C-inulina ou 3H-PEG, mede o volume de água fora das células em um sedimento centrifugado (por exemplo, em E. coli cerca de 25-35% do volume de sedimentos (BNID)). A diferença indica o teor de água dentro das células. Tais métodos levam a valores típicos que variam de cerca de 60-65% em massa para levedura e glóbulos vermelhos até cerca de 70% para E. coli e a ameba D. discoideum e até cerca de 80% para o músculo do rato e tecidos do coração do porco (BNID 105938, 103689). Uma vez que a contribuição da matéria seca é dominada por constituintes de densidade ≈1.3 (ou seja, proteínas), isto leva à densidade geral característica de ≈1.1 (BNID 103875, 106439, 101502). A partir destas frações características a massa seca por volume pode ser inferida para ser cerca de 300-500 mg / ml (BNID 108131, 108135, 108136), mas durante os valores de crescimento lento pode ser maior. As baixas densidades são comuns em sementes secas e plantas subaquáticas que têm partes flutuantes com densidades inferiores às da água circundante, permitindo-lhes assim flutuar. Densidades inferiores à da água podem ser obtidas quer por gás como em algas e algumas bactérias ou usando solutos de peso molecular (MW) inferiores aos meios circundantes (por exemplo, substituindo sódio por MW≈23 com amônio por MW≈18) Como nos pequenos crustáceos, copépodes Antárticos.os seres humanos são feitos de cerca de 60% de água (40% nas células, 15% no fluido intersticial e 5% no plasma sanguíneo, BNID 110743) e a maioria de nós experimentou os fortes efeitos da desidratação após esquecer-se de beber apenas alguns copos. No entanto, algumas células podem ser surpreendentemente robustas para uma diminuição no seu conteúdo de água. Por exemplo, a taxa de metabolismo da glucose nas células hepáticas do rato não foi afectada por uma perda de 25% de água intracelular. Tal diminuição pode ser obtida através da alteração da osmose da tonicidade (concentração de soluto) do fluido extracelular. Um exemplo extremo é o do notável camarão salmoura. Vivendo em ambientes onde a concentração de sal exterior pode flutuar e ser muito alta, mostrou-se que tem cistos que podem ser dessecados a apenas 2% de água sem danos irreversíveis e em níveis de hidratação superiores a 37% (apenas cerca de metade de seu estado totalmente hidratado) sua fisiologia se comporta como normal. Esta robustez em face da perda de água pode estar relacionada a uma distinção às vezes feita entre duas formas de água no interior da célula. “Água a granel” Normal, que é mais dispensável e” água ligada ” que está associada com os componentes celulares e serve como um solvente que é essencial para o bom funcionamento.





