a primeira abordagem para desenvolver antagonistas canabinóides no final da década de 1980 foi modificar a estrutura do THC, mas os resultados foram decepcionantes. No início da década de 1990, uma nova família de agonistas canabinóides foi descoberta a partir da droga pravadolina (anti-inflamatória não esteróide), que levou à descoberta de antagonistas aminoalquil indole com algum sucesso, mas limitado. Como a busca baseada na estrutura dos agonistas foi decepcionante, não foi surpresa que o primeiro antagonista potente e seletivo de canabinóides pertencesse a uma família química inteiramente nova. Em 1994, o primeiro antagonista selectivo dos canabinóides, SR141716 (rimonabant), foi introduzido pela Sanofi pertencente a uma família de 1,5-diarylpyrazoles.
RimonabantEdit
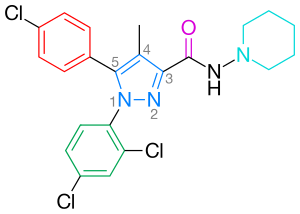
Rimonabant, também conhecido pelo nome sistemático , é um antagonista do receptor CB1 de 1,5-diarilpirazole (Figura 2). Rimonabant não é apenas um ligante potente e altamente seletivo do receptor CB1, mas também é oralmente ativo e antagoniza a maioria dos efeitos dos agonistas canabinóides, tais como THC, tanto in vitro quanto in vivo. Rimonabant demonstrou eficácia clínica clara no tratamento da obesidade.
BindingEdit
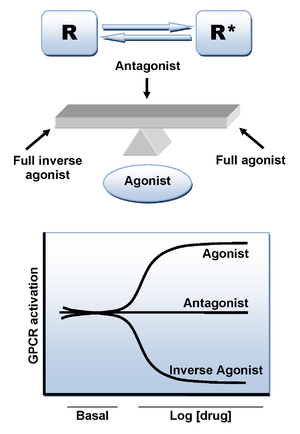
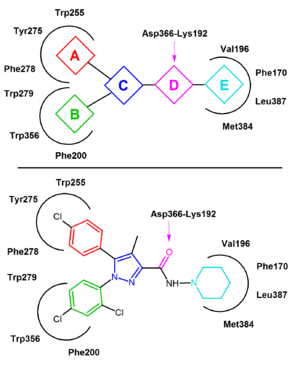
ligação de um ligante agonista ao receptor CB1 provoca uma alteração conformacional e leva ao estado activo do receptor que é responsável pela transdução do sinal. No entanto, há um mecanismo adicional que pode levar ao estado ativo na ausência de ligando. Como inúmeras outras GPCRs, o receptor CB1 exibe um alto nível de atividade constitutiva e, portanto, pode espontaneamente adotar um estado conformacional ativo na ausência de ligação agonista, mantendo elevados níveis basais de sinalização intracelular. Isto pode ser explicado pelos dois modelos de Estado de ativação do receptor em que os receptores estão em equilíbrio entre dois estados, ativos e inativos (r* e R). Um agonista estabilizará o estado ativo levando à ativação, um antagonista neutro se liga igualmente a Estados ativos e inativos, enquanto um agonista inverso estabilizará preferencialmente o estado inativo (Figura 3).Rimonabant tem sido relatado em muitos casos como um agonista inverso ao invés de um antagonista neutro e é provável que se ligue preferencialmente ao estado inativo do CB1, diminuindo assim a ativação da via sinalizadora. A interação chave de ligação é uma ligação de hidrogênio formada entre o grupo carbonil de rimonabant e o resíduo Lys192 do receptor CB1. Esta ligação estabiliza a ponte Salina Lis192-Asp366 da extremidade intracelular das hélices transmembranares 3 e 6 (Figura 4). Esta ponte salina específica está presente no estado inactivo do receptor, mas ausente no estado activo.no estado inactivo do CB1, o rimonabant liga-se dentro da transmembrana-3-4-5-6 microdomain aromático. A ligação do rimonabant envolve interacções directas de empilhamento aromático entre o seu anel 2,4-diclorofenil e os resíduos Trp279/Phe200/Trp356, por um lado, e o anel para-clorofenil e os resíduos Tyr275/Trp255/Phe278, por outro lado. A fracção lipofílica do piperidinilo encaixa perfeitamente numa cavidade formada pelos resíduos de aminoácidos Val196/Fe170/Leu387 e Met384 (Figura 4).
Farmacoforeedit
a maioria dos antagonistas CB1 notificados até agora são análogos próximos ou isosteros de rimonabant. Um modelo geral CB1 agonista farmacóforo inverso pode ser extraído das características comuns destes análogos, diarilpirazóis (Figura 4). Este pharmacophore contém um núcleo cíclico, C, (e.g. pirazole em rimonabant) substituído por dois aromáticos metades, A e B. Uma ligação de hidrogênio acceptor unidade, D, conecta-se C, com um cíclica lipofílico parte, E. Em alguns casos, unidade E se conecta diretamente com o C. Na Figura 4 rimonabant é usado como um exemplo. A unidade A representa um grupo 4-clorofenil e um anel b a 2,4-diclorofenil. A unidade C é o anel pirazol Central e a unidade D representa o grupo carbonilo que serve como aceitador de ligações de hidrogénio. A unidade E representa uma fracção lipofílica aminopiperidinil.
relações estrutura-actividade edit
ligação óptima ao receptor CB1 requer um anel fenílico para-substituído na posição 5 do pirazol. O 5-substituinte do pirazol está envolvido no reconhecimento e antagonismo dos receptores. O para-substituinte do anel fenílico pode ser cloro, bromo ou iodo, mas tem sido demonstrado que uma cadeia Alquil também pode ser tolerada. A numeração do anel pirazol central é apresentada na Figura 2.
um anel fenílico de 2,4-dicloro-substituído na posição 1 do pirazol é preferido para a afinidade assim como para a actividade. Foi demonstrado que halogéneos adicionais neste anel fenílico diminuem a afinidade.
também é favorável a substituição de anel no grupo 3-carboxamida, como o grupo 1-piperidinil no rimonabant. A substituição do amino piperidinil substituinte por amidas Alquil, éteres, cetonas, álcoois ou alcanos resultou principalmente numa diminuição da afinidade. A substituição do piperidinil por pentil ou uma cadeia de heptilo deu aos compostos propriedades agonísticas. Com base nestes resultados, concluiu-se que a 3 posição do pirazol parece estar envolvida em agonismo, enquanto as 1,4,5 posições parecem estar envolvidas em antagonismo.a investigação demonstrou que a ausência de oxigénio carboxamida resulta numa afinidade diminuída. Além disso, a presença de oxigénio carboxamida contribui para conferir as propriedades agonistas inversas, enquanto os análogos sem este oxigénio são considerados antagonistas neutros. Estes resultados suportam a hipótese de que o oxigênio carboxamida forma uma ligação de hidrogênio com o resíduo de Lis192 no receptor CB1.
Derivativesedit Diarilpirazole
SR141716 (rimonabant) análogos têm sido recentemente descritos por vários grupos, levando a uma boa compreensão da relação estrutura-atividade (SAR) dentro deste grupo químico. Embora a maioria dos compostos descritos sejam menos potentes do que o SR141716, vale a pena mencionar dois deles, o SR147778 e o AM251, embora ambos possam ter ação nos receptores opióides mu também.
SR147778 (surinabant), um antagonista de segunda geração, tem uma duração de ação mais longa do que rimonabant e atividade oral aumentada. Esta maior duração de acção deve-se provavelmente à presença do grupo etílico mais estável metabolicamente na 4-posição do seu anel pirazol. Outra mudança é a substituição do cloro 5-fenil pelo bromo.
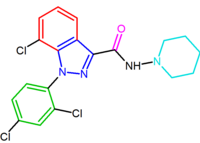
o derivado diarilpirazole, AM251, foi descrito onde o substituinte de cloro foi substituído por iodo na posição para do anel 5-fenil. Este derivado parecia ser mais potente e seletivo do que rimonabant.foram sintetizados análogos
21 possuidores de um amida de alquilo ou de um hidrazida de alquilo com comprimentos variáveis na posição 3. Observou-se que a afinidade aumenta com o aumento do comprimento da cadeia de carbono até cinco carbonos. Também os análogos de amida exibiram maior afinidade do que os análogos de hidrazida. No entanto, nenhum destes análogos possuía afinidade significativamente maior do que o rimonabant, mas, no entanto, eram ligeiramente mais selectivos do que o rimonabant para o receptor CB1 sobre o receptor CB2.várias tentativas foram feitas para aumentar a afinidade dos derivados do diarilpirazol rigidificando a estrutura do rimonabant. Em termos do modelo farmacóforo geral, as unidades A, B e/ou C estão ligadas por ligações adicionais que conduzem a moléculas rígidas. Por exemplo, o pirazol policíclico condensado NESS-0327 mostrou 5000 vezes mais afinidade para o receptor CB1 do que rimonabant. No entanto, este composto possui uma biodisponibilidade central fraca.outro composto, o derivado indazol o-1248, pode ser considerado como um análogo do rimonabant em que o seu grupo 5-aril é fundido à metade pirazol. No entanto, esta modificação estrutural resultou numa diminuição de 67 vezes na afinidade dos receptores CB1.
estes derivados do Rimonabant diarilpirazol estão resumidos na Tabela 1.
 |

|
| SR147778 | AM251 |
 |
 |
| NESS-0327 | O-1248 |
Other derivativesEdit
Structurally different from the 1,5-diarylpyrazoles are the chemical series of the 3,4-diarylpyrazolines. Dentro desta série está o SLV-319 (ibipinabant), um antagonista potente do CB1, que é cerca de 1000 vezes Mais Selectivo para o CB1 em comparação com o CB2 e exibe actividade in vivo semelhante ao rimonabant.outra abordagem utilizada para desenvolver análogos de rimonabant foi substituir o ciclo pirazol central por outro ciclo heterociclo. Um exemplo desta abordagem são 4,5-diarilimidazóis e 1,5-diarilpirrole-3-carboxamidas.foi notificado um grande número de derivados bicíclicos fundidos do diaril-pirazol e imidazóis. Um exemplo disso é um derivado da purina onde um anel pirimidina é fundido a um anel imidazole. Otenabant (CP-945,598) é um exemplo de um derivado bicíclico fundido desenvolvido pela Pfizer.vários grupos de investigação estudaram bioisosteros pirazóis de anel com seis membros. Por exemplo, um derivado 2,3-diarilpiridina mostrou ser potente e seletivo CB1 agonista inverso. A estrutura deste composto demonstra a possibilidade de que o grupo amida de rimonabant poderia ser dividido em uma funcionalidade lipofílica (benziloxi) e polar (nitrilo). Outros análogos de anéis de seis membros são, por exemplo, pirimidinas e pirazinas.para além dos análogos dos anéis de cinco e seis membros, existem outros derivados cíclicos tais como as azetidinas. Um exemplo é o derivado da metilsulfonamida azetidina que tem um grupo 1,1-diaril que imita a metade 1,5-diaril dos diarilpirazóis. O grupo sulfonil serve como um aceitador de ligação de hidrogênio. O grupo 1,1-diaril também está presente em derivados como os benzodioxóis e hidantoinas.foram também notificados análogos acíclicos. Estes análogos contêm um motivo 1,2-diaril que corresponde aos substituintes 1,5-diaril de rimonabant. Um exemplo de um análogo acíclico é o taranabant (MK-0364) desenvolvido pela Merck.os representantes destes análogos estão resumidos na Tabela 2.
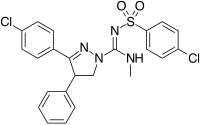 |

|
 |
|
| Type of derivative |
3,4-Diarylpyrazoline (Ibipinabant) | 4,5-Diarylimidazole | 1,5-Diarylpyrrole-3-carboxamides |
 |
 |
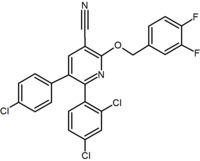 |
|
| Type of derivative |
Purine (pyrimidine ring fused to an imidazole ring) |
Purine derivative (Otenabant) | 2,3-Diarylpyridine |
 |
 |
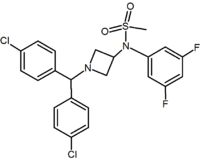 |
|
| Type of derivative |
Pyrimidine | Pyrazine | Methylsulfonamide azetidine |
 |
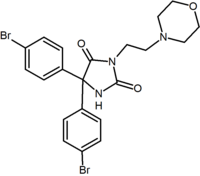 |
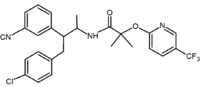 |
|
| Tipo derivativos |
Benzodioxole | Hidantoína | Acíclicas derivativos (Taranabant) |
de receptores CB1 antibodiesEdit
Anticorpos contra os receptores CB1 foram desenvolvidos e introduzidos em uso clínico na Rússia. Eles incluem brizantin (Russo: Бризантин®) e dietressa (russo: Диетресса®). Brizantin está indicado para o tratamento da retirada da nicotina e da cessação tabágica e dietressa está indicada para a perda de peso. Dietressa está disponível na Rússia.
