13.5 D: a Biotina é um CO2 de transporte de coenzima
Lembre-se da seção 6.5 B que muitas enzimas são dependentes da assistência de coenzimas, que são pequenos (em relação à proteína) moléculas orgânicas que vincular – ligadas ou não-ligadas – em uma enzima activa do site e ajudá-lo a catalisar a reação. S-adenosilmetionina (SAM, secção 9.1 a) e ATP (secção 10.2) são dois exemplos que encontramos até agora, e veremos mais alguns nos capítulos à frente. Embora Rubisco (descrito na Parte B desta seção) seja uma exceção, a maioria das enzimas que catalisam reações de carboxilação são dependentes de uma coenzima chamada biotina, que serve como um transportador temporário de dióxido de carbono.
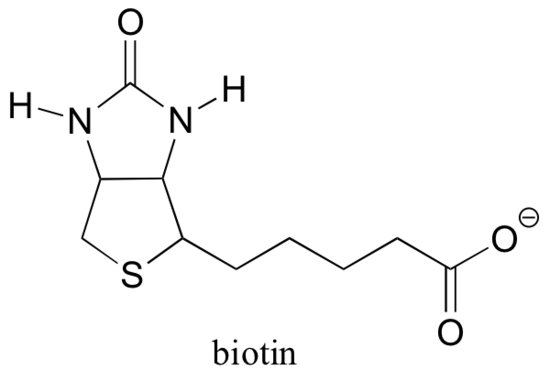
Piruvato carboxylase, a enzima catalisando a primeira etapa do gluconeogensis caminho, é um bom exemplo de um biotina-dependente carboxylation reação. Observe que o CO2 nesta reação é derivado do bicarbonato, ao contrário da reação de Rubisco na qual o CO2 é “fixo” diretamente da atmosfera.

biotina é covalentemente ligada à enzima através de uma ligação amida a um local activo da lisina.
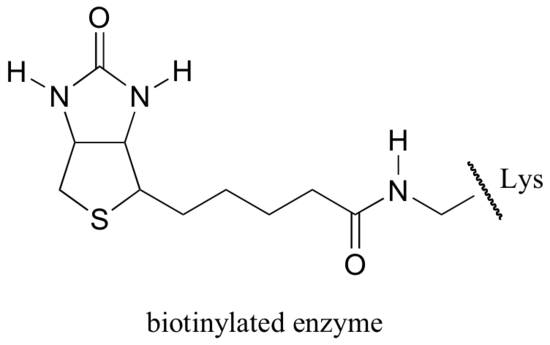
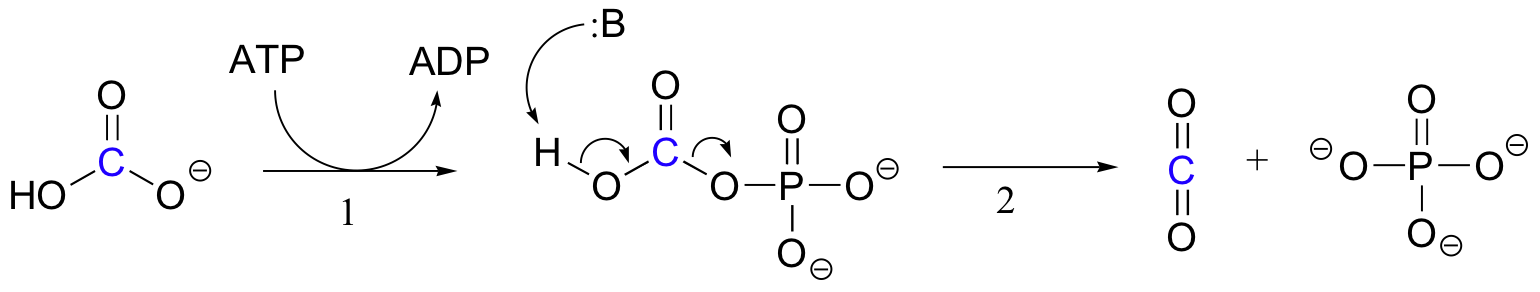
O mecanismo exato pelo qual a biotina-dependente carboxylation reações operar ainda não é completamente entendido, no entanto, o seguinte é uma provável imagem. Em primeiro lugar, o ião bicarbonato é fosforilado pelo ATP (Passo 1, ver secção 10.2), e assim é ativado para a descarboxilação, que gera CO2 livre (Passo 2).
Biotin tem como função manter a molécula de dióxido de carbono até que o piruvato entre no local ativo. A carboxilação da biotina envolve a desprotonação do azoto amida para formar um intermediário tipo enolato (as 3-amidas têm uma pKa de aproximadamente 17, e esta é reduzida pela presença de um ácido local activo perto do oxigénio). Este passo é seguido pelo ataque do nitrogênio nucleofílico sobre o dióxido de carbono para formar a enzima carboxibiotinilada (Passo 4).
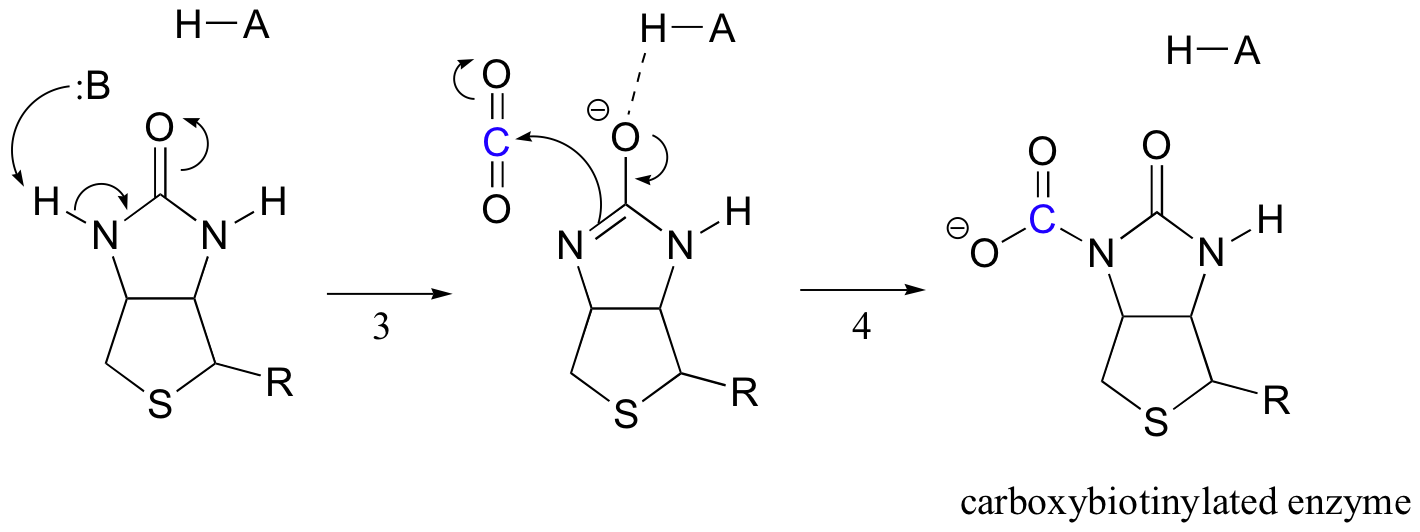
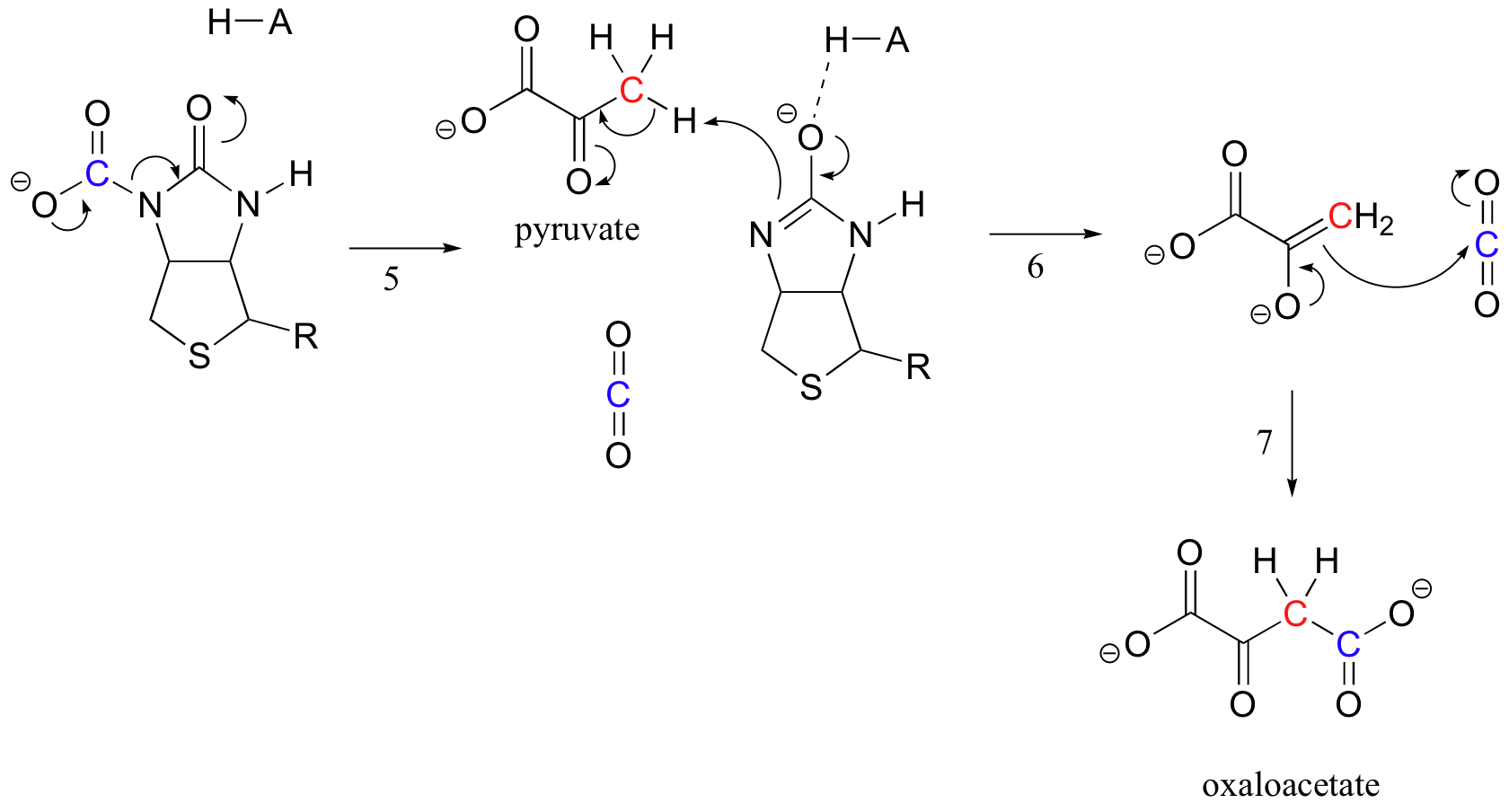
Quando uma molécula de piruvato liga, rearranjo do sítio ativo de arquitetura faz com que o passo anterior para ir em sentido inverso (passo 5), liberando o CO2 e a geração de uma base de biotina para deprotonate alfa-carbono de piruvato, de modo que ele pode condensar, em um aldol-como a moda, com o CO2 para formar oxaloacetate (etapas 6 e 7).
se estudou alguma bioquímica, pode ter ouvido falar da biotina num contexto um pouco diferente do que é discutido nesta secção. Uma proteína chamada avidina, encontrada em abundância em claras de ovo, liga-se não covalentemente e extremamente firmemente à biotina (na verdade, avidin-biotina é o par de ligação proteína-ligando mais forte conhecido pela ciência). Bioquímicos muitas vezes fazem uso desta propriedade ligando covalentemente uma biomolécula de interesse à biotina. As espécies “biotiniladas” podem então ser facilmente isoladas de uma mistura complexa através de uma “coluna de afinidade” revestida de avidina.
