Ostatnia modyfikacja: niedziela, 08-Lis-2009 04:44:32 CET
status dokumentu: kompletny
kwarc jest związkiem jednej części krzemu i dwóch części tlenu, dwutlenku krzemu, SiO2. Jego skład chemiczny (oraz pierwiastek si) został odkryty przez szwedzkiego chemika Jönsa Jakoba Berzeliusa w 1823 roku. Dwutlenek krzemu jest powszechnie nazywany krzemionką.
według IUPAC poprawne są dwie następujące nazwy: dwutlenek krzemu i dioksosilan.
![]()
10mm![]()
1040×800 193kb – 2080×1600 684kb
jest to mały kawałek produkowanego Przemysłowo czystego krzemu. Jest to lekka (gęstość 2,328 g/cm3), szara substancja krystaliczna o silnym metalicznym połysku. Jest bardzo twardy (tak twardy jak kwarc i znacznie twardszy niż większość metali), ale kruchy i nie ciągliwy jak metale. Krzem jest podstawą przemysłu półprzewodników: czysty krzem jest tylko słabym przewodnikiem elektryczności, ale gdy dodaje się śladowe ilości odpowiednich pierwiastków (krzem jest domieszkowany), jego przewodność zbliża się do przewodności metalu, a wybierając rodzaj i ilość pierwiastków śladowych, można kontrolować właściwości elektryczne domieszkowanego krzemu.
reakcje
w temperaturze pokojowej SiO2 we wszystkich modyfikacjach jest prawie obojętny i nie reaguje z większością innych substancji. Nawet w umiarkowanie wysokich temperaturach krzemionka jest chemicznie bardzo stabilna. Z tego powodu topiony kwarc (szkło krzemionkowe) jest szeroko stosowany w aparatach chemicznych, zwłaszcza gdy należy unikać reakcji katalitycznych kationów metali w zwykłym szkle. Przyczyną niskiej reaktywności krzemionki jest bardzo silne wiązanie Si-O, ale także jego struktura makromolekularna.
będąc anhydrytem samego kwasu (kwas ortosilowy, H4SiO4), kwarc na ogół nie będzie atakowany przez kwasy. Wybitnym wyjątkiem jest kwas fluorowodorowy, HF, który rozkłada kwarc, tworząc najpierw fluorek krzemu SiF4, a następnie kwas fluorowodorowy:
SiO2 jest również atakowany przez substancje alkaliczne (takie jak wodorotlenek potasu, KOH). Szybkość reakcji zależy od modyfikacji i wielkości kryształu: krystaliczny kwarc rozpuszcza się bardzo powoli w gorących wodnistych roztworach alkalicznych, podczas gdy amorficzny SiO2 łatwo rozpuszcza się w temperaturze pokojowej:
reakcja ta ma znaczenie dla kolektora, ponieważ roztwory alkaliczne i detergenty są czasami stosowane do usuwania mchów i porostów z próbek mineralnych. Kryształy kwarcu zwykle nie stanowią problemu, ale byłbym bardzo ostrożny przy czyszczeniu odmian kryptokrystalicznych.
podobna reakcja prowadzi do powstawania żeli krzemionkowych w betonie, gdy alkaliczne związki betonu, Zwykle Ca(OH)2, reagują z amorficzną krzemionką i kwarcem kryptokrystalicznym (czyli opalem i chalcedonem). Żel krzemionkowy przyciąga wodę, pęcznieje i pęka beton w ciągu kilku dekad.
wszystkie formy krzemionki rozpuszczają się w stopionym natronie (Na2CO3) lub potażu (K2CO3), tworząc krzemiany:
w wysokich temperaturach wielu środowisk geologicznych kwarc działa jak kwas i reaguje z wieloma minerałami alkalicznymi. Dobrze znanym przykładem jest powstawanie minerału wollastonit Ca3Si3O9 z kwarcu i kalcytu w kontaktowych procesach metamorficznych w temperaturach od około 600°C do góry:
odwrotna reakcja zachodzi przy wietrzeniu skał krzemianowych, tutaj kwas węglowy H2CO3 obecny na przykład w wodach meteorytowych uwalnia kwas krzemowy i tworzy węglany.
kwarc jest „rudą” krzemu. Krzem jest pobierany w temperaturze około 2000°C w następującej reakcji endotermicznej (energochłonnej):
Wiązanie Si-O jest znacznie silniejsze niż Wiązanie C-O, A Reakcja działa tylko dlatego, że tlenek węgla co ucieka z układu jako gaz, więc równowaga układu jest popychana na prawą stronę. Powstawanie tlenku węgla zamiast dwutlenku węgla CO2 jest typowe dla reakcji redukcyjnych z węglem w wysokich temperaturach. Krzem utworzony w tym procesie nie jest wystarczająco czysty do produkcji wiórów i musi zostać oczyszczony w dość złożonej procedurze. Tak więc pomimo obfitości jego rudy, czysty krzem jest stosunkowo drogi.
Rozpuszczalność w wodzie
rozpuszczalność dwutlenku krzemu w wodzie zależy od temperatury, ciśnienia, jego struktury powierzchniowej i jego modyfikacji strukturalnej. Poniższa tabela zawiera przegląd rozpuszczalności w temperaturze pokojowej i normalnym ciśnieniu.
dane z:
– ➛Hollemann& Wiberg, 1985
– ➛Rykart, 1995
w temperaturze pokojowej kwarc jest praktycznie nierozpuszczalny w wodzie. Woda z kranu jest zwykle prawie nasycona rozpuszczoną krzemionką (w odniesieniu do kwarcu), a proces rozpuszczania jest bardzo powolny, więc nie ma potrzeby martwić się o uszkodzenia kryształów kwarcu przez wielokrotne czyszczenie.
jednak rozpuszczanie krzemionki w podłożu skalnym i glebach odgrywa ważną rolę w gorącym, wilgotnym klimacie. Powstawanie gleb laterytowych wiąże się z stopniowym wypłukiwaniem krzemionki z warstw powierzchniowych i wzbogacaniem związków, które – przynajmniej w tych warunkach klimatycznych – są mniej rozpuszczalne w wodzie, jak tlenki żelaza i glinu.
w temperaturach powyżej 100°C i wysokich ciśnieniach rozpuszczalność kwarcu szybko wzrasta. W temperaturze 300°C wynosi od 700 do 1200 mg/l, w zależności od ciśnienia.
SiO2 rozpuszcza się w wodzie, tworząc kwas ortosilowy, H4SiO4:
kwas Ortosilowy jest na przykład bardzo słabym kwasem, słabszym niż kwas węglowy. Dysocjuje z pK1 9.51 zgodnie z
w roztworze wodnym nie występują cząsteczki SiO2 ani Agregaty czworościanu SiO4. Odwrócona reakcja to sposób, w jaki rosną kryształy kwarcu, ale cząsteczka H4SiO4 nie może po prostu pozbyć się 2 cząsteczek wody, potrzebuje innej cząsteczki h4sio4 lub już obecnej cząsteczki krzemionki z zakończeniem hydroksylowym (-OH):
kwas Orthosilicic jest stabilny tylko w rozcieńczonym wodnym roztworze, nie można wyodrębnić czystego kwasu. Najciekawszą właściwością kwasu ortosilowego jest jego tendencja do polimeryzacji w roztworach wodnistych, tworząc najpierw Zol, a później żel kwasów polikilowych: cząsteczki kwasu ortosilowego kondensują się do dużych cząsteczek zgodnie z reakcjami i . Jak tylko zaczniesz koncentrować roztwór H4SiO4, cząsteczki ulegną polimeryzacji. W temperaturze pokojowej w warunkach laboratoryjnych punktem końcowym tego procesu jest tworzenie się amorficznej krzemionki. Żele polimeryzowanego kwasu krzemowego są prawdopodobnie również poprzednikami odmian kwarcu opal i kryptokrystalicznego (Chalcedon w szerszym znaczeniu) w przyrodzie.
podstawowa struktura krzemionki
SiO2 występuje w co najmniej 13 różnych modyfikacjach strukturalnych. Ich struktury krystaliczne (jeśli są obecne) mogą się różnić, ale wszystkie mają pewne podstawowe właściwości. Poniższe zasady mają zastosowanie do wszystkich modyfikacji krzemionki, z wyjątkiem przypadków, w których zaznaczono. Struktura molekularna charakterystyczna dla kwarcu jest opisana w rozdziale struktura.
wiązania chemiczne w krzemionce są kowalencyjne: są one oparte na orbitalach molekularnych, w których 2 elektrony są dzielone między Atomy (w przeciwieństwie do wiązań jonowych, które znajdują się w solach jako fluorytu lub soli kuchennej; tutaj elektrony są przenoszone z jednego elementu do drugiego, tworząc jony o przeciwnym ładunku elektrycznym, aw krysztale jony te są utrzymywane razem przez przyciąganie elektrostatyczne).
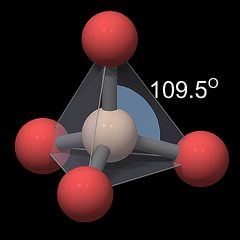
1: SiO4-czworościan
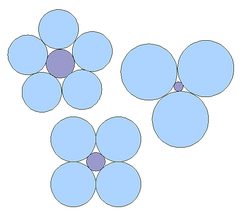
rys.2

3: SiO4-jonowy Model wiązania
podstawowym budulcem w prawie wszystkich modyfikacjach krzemionki (wyjątkami są modyfikacje o bardzo wysokim ciśnieniu) jest jednostka SiO4, w której centralny atom krzemu jest otoczony czterema atomami tlenu.
. |O| - | - .O-Si-O. - | - |O| .
geometria tej jednostki jest pokazana w renderingu kulkowo-drążkowym na Fig.1, z krzemem symbolizowanym przez kolor Kości Słoniowej, tlenem przez czerwoną kulę, a wiązaniami chemicznymi przez szare rury między nimi. Rozmiary atomów nie są skalowane. Atomy tlenu zajmują pozycje wokół atomu krzemu, które utrzymują je w jak największej odległości od siebie, więc tworzą cztery rogi czworościanu, symbolizowane przez półprzezroczystą szarą piramidę. Zauważ, że atomy tlenu nie są ze sobą połączone, szare linie między nimi zostały narysowane tylko w celu wizualizacji geometrii czworościennej. Kąt środkowych wiązań O-Si-O jest bardzo zbliżony do wartości w idealnym czworościanie (109,5°, szaro-niebieski łuk na Fig.1), z Krzemową odległością tlenu około 0.161 nm dla wszystkich atomów tlenu, więc pojedynczy czworościan ma prawie sześcienną symetrię.
Wiązanie Si-O jest wysoce polarne, a elektrony są bardziej przyciągane przez tlen, co prowadzi do nierównomiernego rozkładu ładunków elektrycznych w czworościanie: narożniki są bardziej ujemne, środek jest bardziej dodatnio naładowany.
pojedyncze cząsteczki zbudowane jak O = Si = O(O liniowej strukturze jak dwutlenek węgla CO2) można znaleźć tylko w gazie SiO2 w temperaturach powyżej 2500°C.
wiele podręczników wyjaśnia geometrię czworościanu SiO4 i innych struktur mineralnych, zgodnie z względnymi rozmiarami różnych jonów, jak pokazano na Fig.2: im większy względny rozmiar centralnego jonu, tym więcej jonów o przeciwnym ładunku jest niezbędnych do jego zamknięcia. W związku z tym czworościan SiO4 jest często rysowany jako mały kation Si4+ zamknięty przez cztery duże aniony O2 (Fig.3). Można argumentować, że jest to niedokładne: Krzem i tlen są połączone polarnymi wiązaniami kowalencyjnymi połączonych orbitali elektronowych, więc tworzą jednostkę i nie są w taki sam sposób oddzielone i swobodnie ruchome, jak jony w soli. Związki z jonami Si4+ w rzeczywistości nie istnieją. Istnieją pewne różnice w interpretacji ustaleń eksperymentalnych i podczas gdy niektórzy autorzy postrzegają Wiązanie Si-O jako przede wszystkim kowalencyjne, inni podkreślają jonowe cechy wiązania. Aby zapoznać się z opinią, patrz Gibbs et al., 1994 i Cohen, 1994.,
| | O O | | -O-Si-O-Si-O- | | | | O O O O | | | |-O-Si-O-Si-O-Si-O-Si-O- | | | | O O O O | | | | -O-Si-O- | O |
rys.4: Sieć krzemionkowa
tlen jest dwuwartościowy, a atomy tlenu w rogach czworościanu są połączone z innym atomem krzemu w sąsiednim czworościanie. Kwarc i ogólnie krzemionkę można opisać jako trójwymiarową sieć połączonych ze sobą czworościanów SiO4. Schematyczny widok jego struktury w symbolach chemicznych przedstawiono na Fig.4. Bardziej wyszukane figury struktury molekularnej kwarcu można znaleźć w rozdziale struktura.
rys.6
|
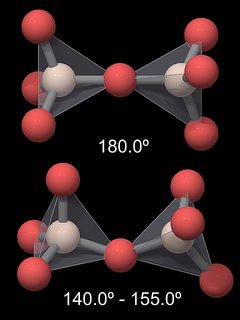
Wiązanie Si-o-Si łączące dwa czworościany nie jest proste (180°), ale tworzy kąt 144° W kwarcu (rys.5). W rezultacie ogólna struktura krystaliczna kwarcu jest dość złożona. W innych modyfikacjach krzemionkowych kąt ten jest inny, podczas gdy kąty wewnątrz czworościanu SiO4 (zdefiniowane przez wiązanie o-Si-O) pozostają zasadniczo takie same. Poniższa tabela wymienia kąty i odległości dla kilku modyfikacji krzemionki.
dane z:
Holl Hollemann& Wiberg, 1985
➛Rykart, 1995
pomiar za pomocą JMol na podstawie współrzędnych komórek jednostkowych.
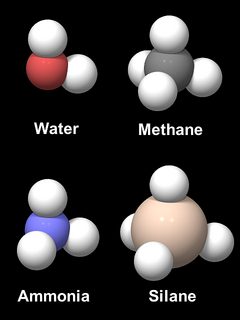
tlen ma wrodzoną tendencję do tworzenia kątowego wiązania X-O-X, podobnie jak jego sąsiedzi w układzie okresowym pierwiastków. 6 przedstawia modele czterech związków Wodoru, wody (H2O), metanu (CH4),amoniaku (NH3) i silanu (SiH4). Odległości międzyatomowe i względne rozmiary C, N, O I Si są skalowane, ale atomy wodoru są przewymiarowane dla czytelności. Cząsteczki CH4 i SiH4 są oczywiście czworościenne. NH3 i H2O mają prawie kształt cząsteczki metanu z usuniętymi 1 lub 2 atomami wodoru, o kącie H-O-H 104,5° i kącie h-N-H 106,8°. Powodem tego podobieństwa jest geometria wiążących orbitali elektronowych, czterech tak zwanych orbitali hybrydowych sp3, które tworzą czworościan. Układ czworościenny czterech orbitali hybrydowych sp3 znajduje się również w krzemie i jest główną przyczyną czworościennego kształtu i sztywności jednostki SiO4 w krzemionce i krzemianach.
od tego można by oczekiwać, że kąt Si-O-Si będzie mniejszy, więc dlaczego jest bardziej otwarty? Po pierwsze, ponieważ Wiązanie Si-O jest wysoce polarne, a atomy tlenu są ujemnie spolaryzowane, istnieją siły odpychające między grupami SiO4, a prosta Si-O-Si utrzymywałaby atomy tlenu w większej odległości. Ponadto długość wiązania Si-O jest krótsza niż obliczona dla pojedynczego wiązania: wartość powinna wynosić 0,181 nm, ale w rzeczywistości wynosi około 0,161 nm w kwarcu i ma podobne wartości w innych modyfikacjach krzemionki. Jest to wskazanie na częściowy podwójny charakter wiązania tego wiązania (Hollemann & Wiberg, 1985), co również wyjaśniałoby jego wielką siłę . To wiązanie podwójne jest zgodne z większym niż oczekiwano kątem Si-o-Si (144° zamiast 109,5°). Zauważ, że odległość Si-O jest najkrótsza w β-tridymicie, a ta modyfikacja ma kąt Si-O-Si równy 180°. Teoria częściowego podwójnego wiązania jest dość złożona i nie będę się w nią zagłębiał.
krzemionka i krzemiany
chociaż chemicznie krzemionka jest tlenkiem, w angloamerykańskiej literaturze mineralogicznej kwarc i wszystkie inne modyfikacje krzemionki są zwykle klasyfikowane jako krzemiany (na podstawie schematu klasyfikacji ustanowionego przez Dana). Rozumowanie nazwania kwarcu krzemianem polega na tym, że jest on zbudowany przez sieć czworościanów SiO4. Krzemiany klasyfikuje się zgodnie ze sposobem zintegrowania czworościanu SiO4 ze strukturą krystaliczną oraz tym, czy i w jaki sposób czworościan jest ze sobą połączony, i zgodnie z tym kwarc nazywany jest tektokrzemianem („krzemian sieciowy” lub „krzemian ramowy”).
krzemian to sól kwasów krzemowych i jednego lub kilku metali. Kwas ortosilowy, H4SiO4, jest tylko najprostszą formą, inne kwasy krzemowe są zbudowane z kilku połączonych jednostek SiO4 z dołączonym Wodorem.
można by pomyśleć, że krzemiany powstają w reakcji wodorotlenku metalu i kwasu ortosilowego, jak
ale nie jest to sposób, w jaki krzemiany zwykle tworzą się w naturze. Krzemiany mogą powstawać, gdy tlenek metalu lub węglan reaguje z krzemionką, jak
podobne reakcje w rzeczywistości zachodzą w przyrodzie, o powstawaniu wollastonitu podczas procesów metamorficznych już wspomniano (reakcja ). Ale normalnym sposobem tworzenia krzemianów jest transformacja: krzemiany reagują ze sobą, tworząc nowe krzemiany. Po uformowaniu się czworościanu SiO4 nie jest on łatwo rozkładany i może być używany tylko w reakcjach do tworzenia nowych pierścieni, łańcuchów, arkuszy lub sieci czworościanu. Tylko bardzo rzadko i w bardzo szczególnych środowiskach można znaleźć krzem w minerałach nie krzemianowych.
czystość kryształów kwarcu
w przeciwieństwie do większości minerałów, czysty kryształ kwarcu jest zawsze chemicznie czysty, o zawartości SiO2 zbliżającej się do 99,5%, często więcej. Zasadniczo istnieją dwa powody tego.
Po pierwsze, kwarc ma strukturę makromolekularną . Nie zawiera izolowanych jonów jakiegoś pierwiastka, który mógłby być łatwo zastąpiony przez inny pierwiastek. Jeśli na przykład sól (związek złożony z izolowanych jonów utrzymywanych razem przez siły elektrostatyczne) rośnie w wodnistym roztworze, jej jony mogą być prawie dowolnie zastępowane, o ile rozmiar i ładunek jonów zastępujących mają identyczną wartość. Kiedy kwarc wyrasta z wodnistego roztworu, na powierzchni rosnącej nie ma dosłownie nic „atrakcyjnego” dla innych jonów w roztworze. Tylko jeśli, na przykład, jednostka-grupowa jest wbudowana zamiast jednostki SiO4, struktura staje się niezrównoważona elektrycznie i pozwala na dołączenie dodatkowego małego monowalentnego kationu (głównie H+, ale także na+ lub Li+). Tylko kilka pierwiastków spełnia kryteria zastępowania krzemu w jednostce SiO4, takich jak aluminium w -, fosfor w + lub żelazo w – i powoduje włączenie kolejnych jonów. Co ciekawe, minerał berlinit, AlPO4, który można zinterpretować jako wzór O2, jest strukturalnym izomorfem kwarcu, wykazującym prawie identyczne właściwości strukturalne i symetryczne oraz bardzo podobne właściwości fizyczne:
| wzór | układ krystaliczny | gęstość | twardość | współczynniki załamania | |
|---|---|---|---|---|---|
| Berlinit | AlPO4 | trigonal | 2,64 g/cm3 | 7 | 1,524-1,530 |
| α-kwarc | SiO2 | trigonal | 2,65 g/cm3 | 7 | 1.544-1.553 |
Po Drugie, trójwymiarowa sieć czworościanu SiO4 jest dość sztywna. Wiele minerałów może tolerować stosunkowo duże ilości niektórych innych atomów i / lub jonów w swojej sieci krystalicznej, nie wykazując dużych odchyleń w ich właściwościach fizycznych. Kolor może się całkowicie zmienić, ale kryształy wydają się jasne i jednolite, ponieważ siatka krystaliczna jest nieco elastyczna lub przestronna i zachowuje swoją pierwotną strukturę jako całość. Siatka krystaliczna kwarcu jest jednak szczelna i bardzo nieelastyczna (czyniąc ją twardą, ale kruchą) i tylko bardzo małe ilości innych elementów o małych kationach (Zwykle Li, Na, H) mogą być wbudowane podczas wzrostu bez zniekształcania struktury sieci. W rzeczywistości ilość kationów monowalentnych znalezionych w kwarcu jest z grubsza proporcjonalna do ilości aluminium. Kwarc, który zawiera większe ilości innych substancji, jest przezroczysty do nieprzezroczystego i często matowy, ponieważ kryształ „rośnie” wokół zamkniętych minerałów, a światło jest rozproszone na granicach różnych materiałów.
nie jest to ogólnie prawdą dla innych modyfikacji krzemionki i wydaje się, że dla niektórych z nich obecność pierwiastków śladowych ma w rzeczywistości stabilizujący wpływ na ich strukturę.
ale podczas gdy ogólny skład przezroczystych kryształów kwarcu jest wyjątkowo czysty (przynajmniej w porównaniu do większości innych minerałów), zanieczyszczenia zwykle nie są równomiernie rozmieszczone w krysztale. Stężenia poszczególnych pierwiastków mogą różnić się o rząd wielkości w odległości kilku mikrometrów. Na przykład stężenie glinu może wahać się od mniej niż 5 ppma (części na milion atomów) do 10000 ppma w pojedynczym krysztale (➛Perny et al. 1992). Wzór rozkładu pierwiastków śladowych można uwidocznić za pomocą techniki zwanej katodoluminescencją: wysokoenergetyczne wiązki elektronów („promienie katodowe”) wywołują krótkotrwałe efekty luminescencji, które można uchwycić na zwykłym filmie. Powstałe zdjęcia cienkich plasterków kryształów pokazują drobny laminarny wzór. Wszystkie warstwy leżą równolegle do powierzchni kryształów, podobnie jak fantomy, więc ten wzór rozkładu pierwiastków śladowych jest spowodowany szybkimi zmianami w środowisku wzrostu.
chemicznie czysta nadal nie jest wystarczająco czysta dla celów technicznych. Doskonały, jednorodny kryształ jest przezroczysty jak próżnia, ale pierwiastki śladowe powodują zniekształcenia i defekty w sieci krystalicznej, a to z kolei wpływa na właściwości optyczne. Większość elementów wbudowanych w Kwarc (h, Li, Al, Na, Ti, Fe) jest wszechobecna, więc dalsze oczyszczanie krzemionki jest skomplikowane i kosztowne. Z tego powodu złoża kwarcu o niskiej zawartości pierwiastków śladowych są nadal bardzo poszukiwane(patrz na przykład ➛Larsen et al. 2000).
więcej informacji, Literatura, linki
tabelę właściwości kwarcu można znaleźć na stronie mindat.org:
kolejna tabela na www.webmineral.com:
Przypisy
1 IUPAC jest organizacją, która ma na celu wyeliminowanie niejasności i zabawnych, ale znanych nazw, takich jak Knallsäure (po niemiecku „walący kwas”, kwas piorunowy) z nomenklatury chemicznej. Stare nazwy są nadal ważne, o ile są jednoznaczne.
2 niektórym z Was może się wydawać kuszące przeprowadzenie eksperymentów z fluorowodorem. Fluorowodór jest bardzo niebezpieczną substancją. Wystarczy spojrzeć na przypadek w dobrym podręczniku toksykologii; po wykładzie nie będziesz chciał go dotknąć nawet kijem. Wodnisty roztwór nie jest mocnym kwasem (czysty HF is), a nierozpuszczalne małe cząsteczki HF łatwo przenikają przez skórę i wiążą wapń w komórkach, tworząc nierozpuszczalny fluoryt, CaF2. Wapń jest niezbędny do żywych funkcji wszystkich komórek ciała. Mała kropla na palcu, która pozostaje niezauważona, ponieważ nie boli od razu, może – po pewnym opóźnieniu-spowodować znaczne uszkodzenia i wielki ból.
szybko Policzmy: 1 Mol HF = 20g. kropla (około 50 µl) 20% roztworu zawiera 0,00005 l x (200g / l) = 0,01 g. 10 mg, to nie brzmi zbyt wiele.
1 Mol Ca = 40g i 1 Mol F = 19g. 1 Ca wiąże 2 F, a więc 40g Ca wiąże 38g F z 40G HF. 1 ml tkanki twojego ciała zawiera około 0,1 mg Ca, a 0,1 mg HF pozwoli jej wytrącić się prawie całkowicie. Teoretycznie 10 mg HF w małej kropli może wytrącić większość Ca w 100 ml tkanki, zabijając wszystkie komórki w niej.
I Nie, Nie jestem przeciwny fluoryzacji wody (tutaj nie ma ironii).
3 termin „woda meteorytowa” odnosi się do jej pochodzenia z atmosfery, a nie z meteorytów. Grecy myśleli, że spadające gwiazdy pochodzą z tej samej kuli co chmury: Gwiazdy i planety były uważane za wieczne istoty, coś chmury i spadające gwiazdy są oczywiście nie. Pomyśl o „meteorologii”.
4 dlatego kwarcowi w skałach wulkanicznych często towarzyszy kalcyt.
5to jest nieco sprzeczne z intuicją, ale nasycony roztwór znajduje się w równowadze termodynamicznej z kryształem. Kiedy cząsteczka jest włączona do struktury krystalicznej, powstają nowe wiązania, a w zależności od geometrii struktury krystalicznej, mniej lub więcej energii jest uwalniane lub zużywane. Aby rozpuścić substancję, potrzebna jest energia do zerwania wiązań, ale energia jest również uwalniana, gdy cząsteczki wody zorientują się w kierunku rozpuszczonej cząsteczki i utworzą nowe wiązania elektrostatyczne (energia hydratacji). Bardziej stabilna modyfikacja związku jest na ogół mniej rozpuszczalna, ponieważ do zerwania wiązań potrzeba więcej energii.
To nie ma nic wspólnego z szybkością reakcji. Pod pewnymi warunkami bardziej niestabilna modyfikacja utworzy się najpierw z rozwiązania, a dopiero później zostanie zastąpiona przez stabilną modyfikację: Kwarc kryptokrystaliczny zwykle tworzy się z wodnistego roztworu, ale cristobalit i opal są etapami pośrednimi, ponieważ Kinetyka reakcji sprzyja powstawaniu opalu. A kiedy umieścisz kryształ kwarcu w 1 litrze czystej wody w temperaturze pokojowej, możesz być pewien, że po wyjęciu go następnego dnia nie będzie ważył o 2,9 mg mniej. Prawdopodobnie bardzo trudno będzie zmierzyć różnicę. Może po miesiącu, albo po roku.
6W rzeczywistości czworościan w kwarcu nie jest idealnie izometryczny jak idealny czworościan, ale nieco zniekształcony, ponieważ odległość do centralnego atomu krzemu wynosi 0,16101 nm dla 2 atomów tlenu i 0,16145 nm dla 2 innych atomów tlenu. To odchylenie od idealnej formy jest jednak znikome dla większości praktycznych celów, ponieważ wynosi mniej niż 0,3%.
7liczby utleniania Si I O wynoszą odpowiednio +4 i -2. Energia potrzebna do usunięcia 4 elektronów z układu Si jest zbyt wysoka, aby umożliwić stabilne Wiązanie czysto jonowe. Nawet SiF4 jest związkiem o wiązaniach polarnych, ale kowalencyjnych, pomimo wysokiej elektroujemności fluoru. Ale związki Si4-anionowe istnieją (jak Ca2Si).
8Rykart (1995) podaje wartości 152,8° i 143,5° odpowiednio dla α – i β-kwarcu. Wydaje się, że jest to błąd typograficzny, wartości powinny być przełączane.
9ale nie jest prawdą, że „wszystko idzie”. Gdy minerał tworzy, pierwiastki i jony są wbudowane w jego siatkę krystaliczną, gdy spełniają określone kryteria, takie jak określony ładunek, rozmiar lub elektroujemność, a zatem są podobne do tych, które już tworzą siatkę.
 Wersja do druku
Wersja do druku