proces powstawania poszczególnych komórek z zarodka
w organizmie człowieka, który składa się z około 60 bilionów komórek, tworzy się wiele różnych typów komórek. Każda z tych komórek ostatecznie pochodzi z jednej zapłodnionej komórki jajowej, która zaczęła się dzielić, ostatecznie różnicując się w komórki somatyczne o różnej morfologii i funkcji, które tworzą różne tkanki i narządy ludzkiego ciała. Uważa się, że pluripotencjalne komórki macierzyste mają podobny potencjał bez różnicowania pozabłonkowego.
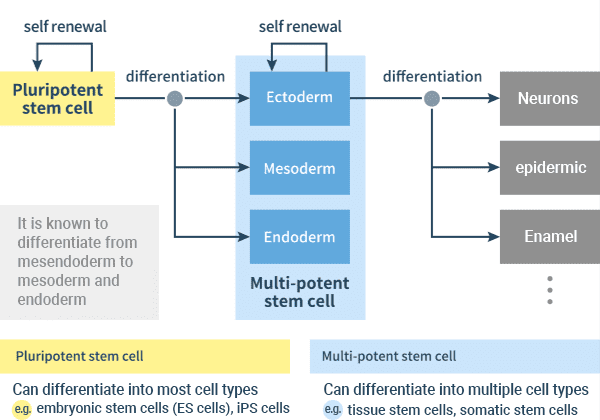
rysunek: Indukcja różnych typów komórek tkankowych z pluripotencjalnych komórek macierzystych poprzez trzy warstwy zarodkowe
w procesie formowania osobnika komórki macierzyste zmieniają się (różnicują) w komórki, które różnią się od siebie, zachowując zdolność proliferacji do dzielenia i tworzenia większej liczby komórek tego samego typu lub dalszego różnicowania się w bardziej wyspecjalizowaną formę. W ten sposób powstają różne narządy.
w stadium blastocysty, wczesnym stadium rozwoju embrionalnego, istnieją komórki, które są zdolne do różnicowania się w prawie każdy typ komórki, który składa się na ciało, zdolność znana jako pluripotentcy.In w warunkach in vitro pluripotencjalne komórki macierzyste, w tym komórki ES i iPS, mogą różnicować się w typy komórek pochodzące z endodermy, mezodermy i ektodermy, ale nie są zdolne do rozwoju w kompletny organizm sam. Natomiast komórki macierzyste, które mogą różnicować się tylko w ograniczoną liczbę typów komórek, takich jak komórki macierzyste tkanek i somatyczne komórki macierzyste, są znane jako multipotentne komórki macierzyste.
komórki te są wykorzystywane nie tylko do badań podstawowych, gdzie są różnicowane w konkretne komórki w celu zbadania ich właściwości, ale także do „badań przesiewowych odkrywania leków” w celu wyszukiwania kandydatów na leki i „Medycyny Regeneracyjnej”, gdzie są przeszczepiane lub podawane pacjentom jako środek terapeutyczny. Jednak kultura pluripotencjalnych komórek macierzystych różni się od konwencjonalnej kultury komórek somatycznych pod wieloma względami i mówi się, że trudno jest utrzymać niezróżnicowany stan i zapewnić wysoki poziom odtwarzalności.
Klasyfikacja i charakterystyka Multipotentnych komórek macierzystych i Pluripotentnych komórek macierzystych
Multipotentnych komórek macierzystych
Multipotentne komórki macierzyste mają zdolność do różnicowania się w komórki, które zawierają określone tkanki i narządy, i obejmują zarówno tkankowe komórki macierzyste, jak i somatyczne komórki macierzyste.
komórki macierzyste tkanki są specyficzne dla tkanek i mają zdolność do samoodnawiania się przez podział na komórki potomne typu podobnego lub do różnicowania się w bardziej wyspecjalizowane komórki w tkance.
somatyczne komórki macierzyste existin vivo i mogą różnicować się w ograniczoną liczbę typów komórek. Mezenchymalne komórki macierzyste (MSCS), są rodzajem somatycznej komórki macierzystej i mogą różnicować się w kości, chrząstki, naczynia krwionośne i kardiomiocyty. MSCs uzyskuje się ze względną łatwością ze szpiku kostnego, tkanki pępowinowej, krwi pępowinowej i tkanki tłuszczowej.
multipotentne komórki macierzyste mają działanie przeciwzapalne, działanie indukujące czynnik wzrostu, działanie proangiogenne i odgrywają ważną rolę w naprawie tkanek. Ponadto mówi się, że mają zmniejszone ryzyko raka w porównaniu do pluripotencjalnych komórek macierzystych, co jest ważnym czynnikiem bezpieczeństwa.
regeneracyjne produkty medyczne zostały już zatwierdzone na całym świecie do leczenia urazu rdzenia kręgowego i ostrej choroby przeszczep przeciwko gospodarzowi po przeszczepieniu krwiotwórczych komórek macierzystych.
tabela: Examples of Approved Regenerative Medical Products That Use Human MSCs in the World-
| Regenerative Medical Products | Approved Countries | Manufacturing Distributors | Origin MSC | Applications |
|---|---|---|---|---|
| PROCHYMAL® | Canada, New Zealand | Mesoblast | Allogeneic bone marrow-derived MSC | Acute GVHD*(pediatric) |
| TEMCELL® HS Inj. | Japan | JCR Pharma | Allogeneic bone marrow-derived MSC | Acute GVHD* |
| Stemirac® Inj. | Japan (conditional approval) | Nipro | Autologous bone marrow-derived MSC | Spinal cord injury |
| Heartcellgram-AMI® | South Korea | Pharmicell | Autologous bone marrow-derived MSC | Acute myocardial infarction |
| Cupistem® | South Korea | Anterogen | MSC derived from own fat | Crohn’s disease |
| CARTISTEM® | South Korea, EU | Medipost | Allogeneic cord blood-derived MSC | Knee osteoarthritis |
| Stempeucel® | EU, India (conditional approval) |
Stempeutics Research |
Allogeneic bone marrow-derived MSC | Knee osteoarthritis |
| Allostem® | USA | Allosource | Allogeneic fat derived MSC (A combination product composed of human demineralized bone matrix) |
Bone damage |
| Osteocel® Plus | US | NuVasive | Allogeneic bone marrow-derived MSC (A combination product composed of osteoprogenitor cells and human demineralized bone matrix) |
Bone repair (361HCT/P) |
*GVHD: choroba przeszczep przeciwko gospodarzowi
pluripotencjalne komórki macierzyste
pluripotencjalne komórki macierzyste są komórkami macierzystymi, które mogą różnicować się w prawie każdą komórkę składającą się na organizm. ESC, embrionalne komórki zarodkowe (EGC) i iPSCs zostały dotychczas ustalone jako typy pluripotencjalnych komórek macierzystych.
ESC powstają z wewnętrznej masy komórkowej wewnątrz wydrążonej blastocysty, która jest wczesnym stadium rozwoju embrionalnego po podziale przez zygotę na blastulę. W Japonii Komórki ES powstają z nadwyżki podaży zapłodnionych jaj, które są odrzucane po leczeniu niepłodności. EGC powstają z komórkowych prekursorów plemników i jaj (pierwotnych komórek zarodkowych) i mają prawie takie same właściwości jak ESC.
iPSCs są tworzone przez przeprogramowanie komórek somatycznych do stanu niezróżnicowanego poprzez wprowadzenie określonych genów. Utworzenie iPSCs umożliwiło nam pozyskiwanie komórek podobnych do RSG od dawców. Możliwe jest również uzyskanie tkanki dostarczonej przez pacjenta z chorobą, ustalenie iPSCs z tkanki i wywołanie różnicowania w celu zapewnienia modelu Anin vitro choroby. Dlatego komórki somatyczne, takie jak komórki nerwowe lub kardiomiocyty, utworzone przez indukowane różnicowanie iPSCs mają duży potencjał do zastosowań, takich jak określenie etiologii choroby, ocena skuteczności leku i skutków ubocznych oraz przeszczep u pacjentów jako terapie medycyny regeneracyjnej. Jednak, niezamierzone mutacje genów donoszono przy ustanawianiu kultur iPSC, jak również subculturing iPSCs i ESCs przez długi okres czasu. Obecnie nie wiadomo, czy wszystkie te mutacje genetyczne są niebezpieczne, a naukowcy dyskutują, jak najlepiej ocenić ich bezpieczeństwo do praktycznego wykorzystania w przyszłości.
