Jonizacja chemiczna (CI) jest techniką jonizacji miękkiej, która jest bezpośrednim zastosowaniem wyników badań reakcji molekularnych i jonowych w chemii analitycznej. Najwcześniejszą techniką jonizacji była jonizacja elektronowa (ei). Produkt otrzymany przez EI posiada wiele fragmentów, które są trudne do analizy. CI, który wyprodukował bardzo niewiele fragmentów, rozpoczął się w 1950 roku i ma duży potencjał w chemii analitycznej.
w procesie CI elektrony najpierw bombardują Gaz odczynnika, aby wytworzyć jony odczynnika. Cząsteczki próbki są następnie jonizowane przez jony odczynnika poprzez szlak reakcji molekularnej i jonowej. Lata 70. były uważane za kamień milowy w rozwoju CI. W tym czasie naukowcy rozwiązali niedociągnięcia pracy CI w środowisku próżniowym, umożliwiając CI pracę w warunkach atmosferycznych. Jonizacja chemiczna w atmosferze zapewnia energię z wyładowania koronowego i nie wymaga środowiska próżniowego, co znacznie zwiększa zakres zastosowań CI. Obecnie CI jest szeroko stosowany w technice spektrometrii masowej.
zasada jonizacji chemicznej
zasada CI polega na użyciu odczynnika jonu X+ do reakcji z cząsteczką analitu a w celu uzyskania jonizacji analitu:
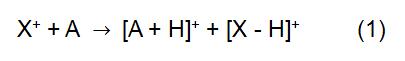
w powyższej reakcji X+ pochodzi ze zjonizowanego gazu reakcyjnego. Niektóre typowe gazy odczynnikowe obejmują metan, amoniak, wodę i izobutan. Czas reakcji i stałą szybkości (k) we wzorze można otrzymać za pomocą literatury lub pomiaru. Gdy odczynnikiem jonu X+ jest H3O+, wzór (2) wynosi:
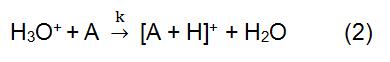
Jon odczynnika jest wytwarzany przez źródło jonów. Powszechnie stosowane źródła jonów obejmują głównie źródło promieniowania, źródło wyładowania pustej katody i zwykłe źródło wyładowania jarzeniowego. 210Po i 241Am są najczęstszymi źródłami promieniowania. Proces jonizacji rozpoczyna się od cząstek alfa emitowanych przez 210po i 241am. Ma wysoką energię i może zderzać się z gazem odczynnika w celu wytworzenia jonów i elektronów odczynnika. Jeśli generowane elektrony są wystarczająco wysokie, mogą zderzyć się z gazem odczynnika, tworząc nowe jony odczynnika i elektronikę. W CI wykorzystującym H3O+ jako Jon odczynnika powszechnie stosuje się źródło wyładowania z pustą katodą, które może wytworzyć 99,5% H3O+.
zgodnie z warunkami jonizacji chemicznej, CI klasyfikuje się do jonizacji chemicznej pod niskim ciśnieniem (
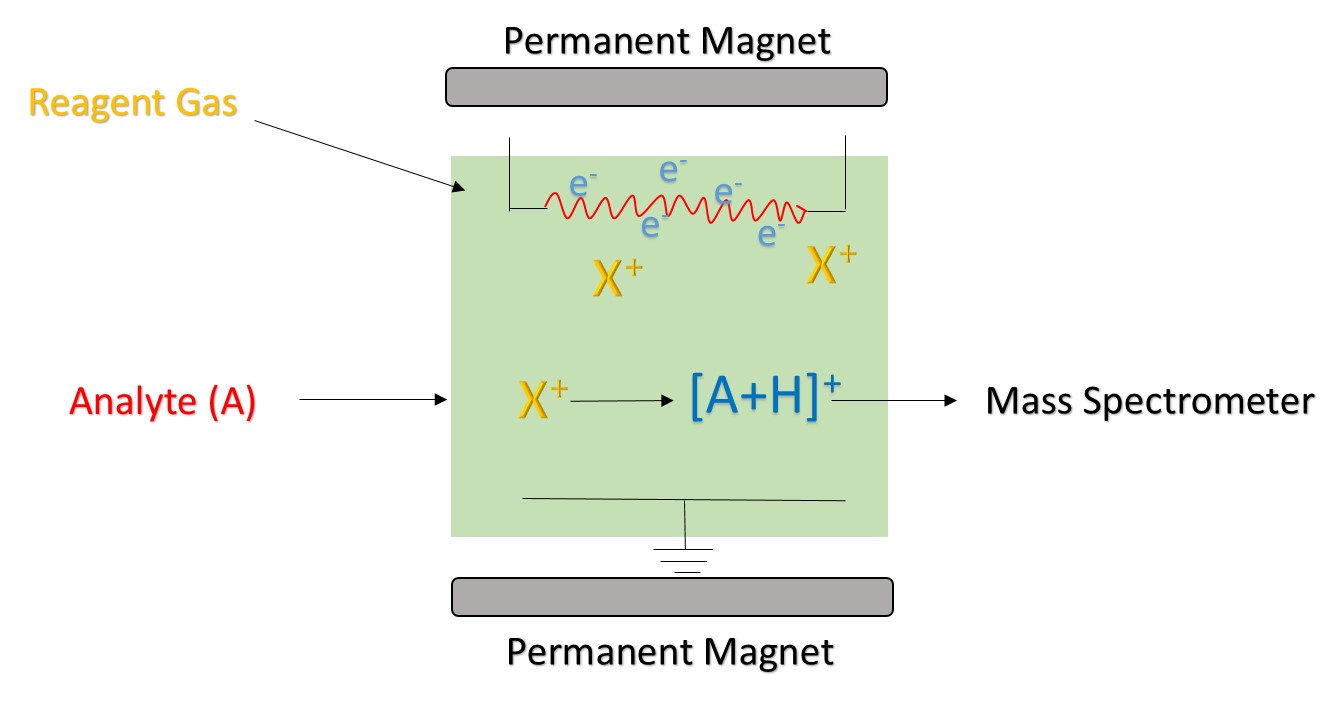 Rysunek 1. Zasada jonizacji chemicznej
Rysunek 1. Zasada jonizacji chemicznej
zalety i wady CI
rozdzielczość widma CI jest prosta i można uzyskać dokładną masę cząsteczkową analitu. Produkt otrzymany przez CI ma niewiele fragmentów,a jego produktami są głównie cząsteczki i jony analitu. Selektywność CI można łatwo zwiększyć poprzez wybór odpowiedniego jonu reagenta. Na przykład odczynnik jon H3O+ reaguje tylko z substancją organiczną o powinowactwie protonowym większym niż H3O+. Ponadto CI ma wysoką czułość i szybką reakcję (15s). Jeśli jednak reaktywne jony są nieczyste i w tym samym czasie zachodzą różne chemiczne reakcje jonizacji, spektrometria mas staje się trudna.
Przykłady zastosowań CI
obecnie CI jest szeroko stosowany jako źródło jonów w systemach spektrometrii masowej do wykrywania różnych substancji śladowych. CI może być stosowany do wykrywania substancji, takich jak gazy śladowe w atmosferze, pozostałości pestycydów w warzywach i owocach, Melamina w mleku w proszku, plastyfikatory i herbicydy w glebie. Ponadto CI może być również używany do identyfikacji materiału, takiego jak identyfikacja jakości herbaty.
- pomiar lotnych związków organicznych (VOC)
w pomiarze VOC przez CI, H3O+ jest zwykle stosowany jako Jon reagenta. H3O+ nie reaguje z większością substancji w powietrzu, takich jak O2, N2, CO2 itp. Z drugiej strony, większość reakcji transferu protonów nie jest dysocjowana, więc jony produktu są pojedyncze, co sprawia, że analiza wyników jest prosta. Zasada pomiaru LZO przy użyciu H3O+ jako jonu odczynnika przedstawiona jest w równaniu (3). Produkt końcowy został rozwiązany za pomocą spektrometrii mas reakcji transferu protonów.
- oznaczanie melaminy w mleku w proszku
w pomiarze melaminy przez CI, N2 jest stosowany jako gaz odczynnikowy. Pod działaniem wysokiego napięcia N2 i H2O przechodzą złożone reakcje fizykochemiczne w celu wytworzenia jonów odczynnika H3O+. Proces reakcji przedstawiono we wzorze (3-6). H3O+ reaguje z melaminą w mleku w proszku, a zasada reakcji jest pokazana we wzorze (2).
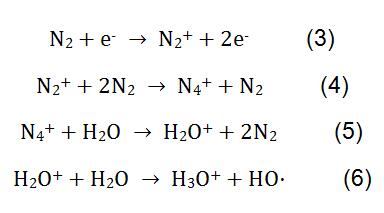
- Identyfikacja jakości herbaty
różne rodzaje herbaty można zidentyfikować, mierząc substancje chemiczne na powierzchni liści herbaty za pomocą CI. H3O+ reaguje z powierzchnią herbaty z butanolem, geraniolem, kofeiną i innymi substancjami, a produkty reakcji tworzą różne widma masowe na spektrometrze masowym. Zawartość tej samej substancji w różnych odmianach herbaty jest inna, więc widmo masowe utworzone przez wykrywanie CI jest inne. Spektrum masowe może w pewnym stopniu odzwierciedlać chemiczne cechy odcisków palców herbaty. Dlatego CI ma ważną praktyczną wartość zastosowania do szybkiej identyfikacji i analizy jakości herbaty.
Jonizacja chemiczna jest szeroko stosowana w spektrometrii masowej ze względu na silną selektywność i wysoką czułość. Chemiczna spektrometria mas jonizacji (CIMS) umożliwia nie tylko tandemową identyfikację substancji w złożonych próbkach, ale także uzyskuje chemiczne dane odcisków palców dla próbek do analizy chemometrycznej. Zastosowanie CIMS ma pozytywny wpływ na wspieranie rozwoju przemysłu spożywczego, medycznego, Ochrony Środowiska, Rolnictwa i innych gałęzi przemysłu.
krótko wprowadziliśmy CI, rodzaj metody jonizacji, która może pomóc ci zrozumieć więcej na temat spektrometrii masowej. W Creative Proteomics opracowaliśmy profesjonalną platformę spektrometrii masowej, która zawiera najnowocześniejsze Instrumenty. Korzystając ze spektrometrii masowej, kreatywna proteomika może świadczyć różne usługi, aby spełnić różne wymagania, w tym:
- serwis proteomiki
- serwis Metabolomiki
- serwis Glikomiki
- Porównanie widm masowych niektórych biologicznie ważnych związków uzyskanych różnymi technikami jonizacji. Chemia Analityczna, 1975, 47(2):207-219.
- Lindinger W; et al. Monitorowanie on-line lotnych związków organicznych na poziomie pptv za pomocą spektrometrii mas transferowych (PTR-MS) zastosowań medycznych, kontroli żywności i badań środowiskowych. International Journal of Mass Spectrometry & procesy jonowe, 1998, 173(3):191-241.
- Chen H; et al. Desorpcja powierzchniowa chemiczna spektrometria masowa z jonizacją pod ciśnieniem atmosferycznym do bezpośredniej analizy próbek otoczenia bez toksycznego zanieczyszczenia chemicznego. Journal of Mass Spectrometry, 2010, 42(8):1045-1056.
- Yang s; et al. Detekcja melaminy w produktach mlecznych metodą desorpcji powierzchniowej, chemiczna spektrometria masowa jonizacji pod ciśnieniem atmosferycznym. Chemia Analityczna, 2009, 81(7):2426.
