kompleksy transferu ładunku wykazują przejścia transferu ładunku, w których absorpcja wyzwala transfer elektronu od dawcy do akceptora.
gdy jod rozpuszcza się w roztworach rozpuszczalników dawców, uderzający fioletowy kolor jodu molekularnego zastępuje się kolorem żółto-brązowym. Dzieje się tak dlatego, że kompleksy transferu ładunku, takie jak te utworzone przez \(I_2\), mogą absorbować światło w sposób, który ani dawca, ani akceptor nie mogą samodzielnie. W szczególności kompleksy transferu ładunku wykazują pasma transferu ładunku (pasma CT) w widmach absorpcji. W przejściu transferu ładunku początkowy częściowy transfer ładunku z zasady dawcy Lewisa do akceptora kwasu Lewisa w kompleksie transferu ładunku jest popychany dalej przez fotoeksycytację.
\
charakter tych przejść transferu ładunku jest widoczny z orbitalnego opisu wiązania dla kompleksów transferu ładunku jodu. Kiedy zespół dawcy-I2 tworzy wiązanie dawcy-I2 i antybondujące orbitale powodują przesunięcie\(I2 \sigma \rightarrow\ sigma*\) do wyższego poziomu energii a powstanie nowego pasma przenoszenia ładunku związanego z wzbudzeniem elektronu z orbitalu Amino-I2 \(\sigma\) w dużej mierze skoncentrowanego na aminie orbitalu Amino-I2 \(\sigma*\).
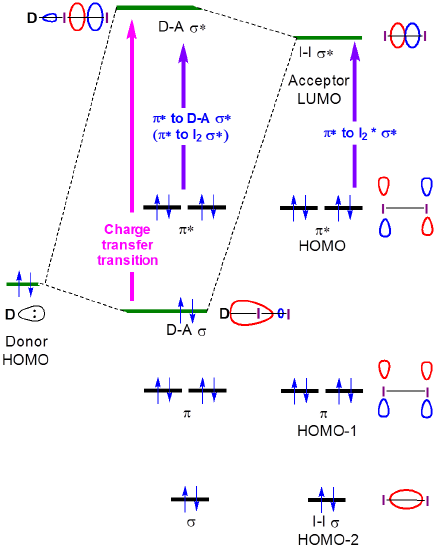
rysunek 6.4.2.\( \PageIndex{2}\). Graniczne interakcje orbitalne, które powodują zmiany w widmach absorpcji jodu, gdy tworzy on kompleks transferu ładunku z dawcą Zasady Lewisa.
roztwory I2 jako mieszaniny z zasadami Lewisa, takimi jak aminy i w rozpuszczalnikach dawców, wyraźnie obciążają pasma przenoszenia. Kilka takich widm przedstawiono na rysunku 6.4.2.3.
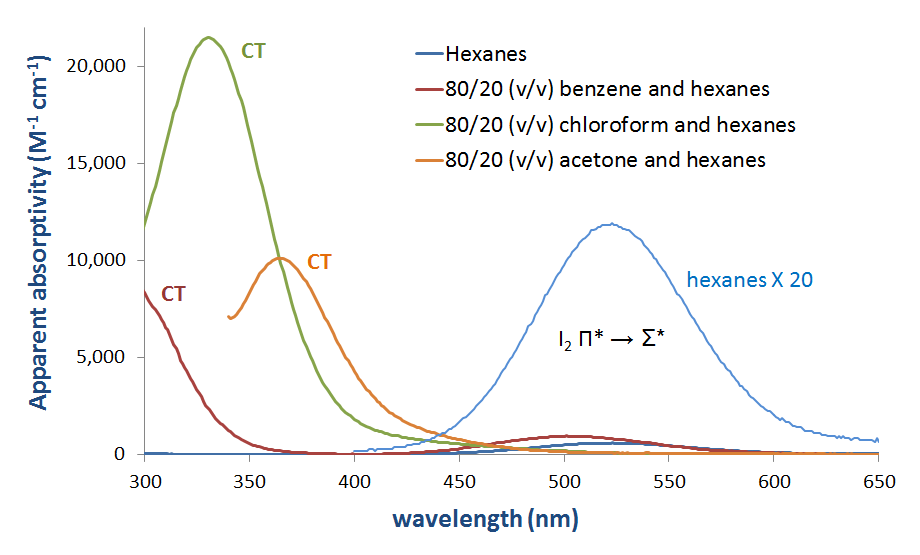
rysunek 6.4.2.\( \PageIndex{3}\). Widmo absorpcyjne jodu molekularnego (I2)w różnych rozpuszczalnikach pokazujące pojawienie się pasma CT w rozpuszczalnikach dawców.*
zasadniczo Energie zarówno transferu ładunku, jak i \(I_2~\pi *~\rightarrow ~D-A~ \sigma *\) zarówno zwiększają się wraz z siłą dawcy, jak pokazano na rysunku 6.4.2.4.
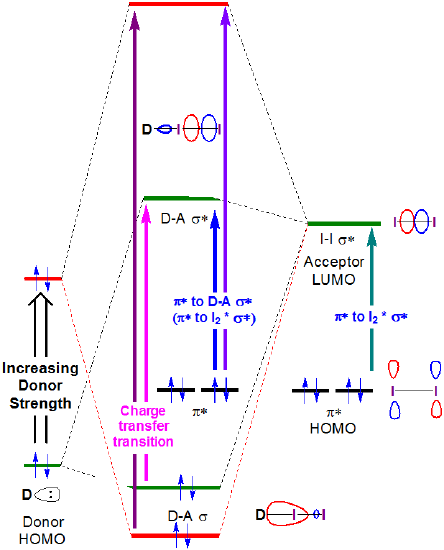
rysunek 6.4.2.\( \PageIndex{4}\). Oczekiwana zmiana granicznych energii orbitalnych związanych z tworzeniem kompleksu akceptora dawcy I2, gdy energia HOMO dawcy wzrasta.
Jak widać na rysunku 6.4.2. można się spodziewać, że energia pasma przenoszenia ładunku wzrośnie wraz ze wzrostem energii donora HOMO, aby zbliżyć się w energii do akceptora LUMO. Chociaż należy zachować ostrożność podczas interpretacji widm fazy rozwiązania I2, to oczekiwanie jest potwierdzone pobieżną i jakościową analizą widm na rysunku 6.4.2.3. Energia przejścia CT przesuwa się w kierunku niższych długości fal (a tym samym większej energii), ponieważ najwyższa zajmowana energia orbitalna atomu dawcy wzrasta z acetonu (tlen, -15,85 eV) DO chloroformu (chlor, -13,67 EV) i wreszcie benzenu (węgiel, -10.66 eV).**
pasma przenoszenia ładunku w chemii metali przejściowych
przejścia przenoszenia ładunku odpowiadają za intensywny kolor wielu kompleksów metali przejściowych. W tych przypadkach jednak słaba interakcja Lewisa z kwasem zasadowym polega na niekompletnym oddaniu elektronu i akceptacji w \(p \pi-d \pi\) (lub \(P\pi-d\pi*\))-wiązaniu między metalem a ligandem. Pasma przenoszenia ładunku w widmach absorpcyjnych tych kompleksów obejmują przenoszenie elektronów między metalem a ligandem. W szczególności,
- pasma transferu ładunku metalu do ligandu (MLCT lub CTTL) obejmują transfer elektronu z wypełnionego lub częściowo wypełnionego orbitalu metalu d do orbitalu typu ligand \(\pi*\).

- pasma ligandu do ładunku metalu (LMCT lub CTTL) obejmują transfer elektronu z wypełnionego lub częściowo wypełnionego ligandu orbitalnego do metalowego orbitalu D.

- pasma przenoszenia ładunku metalu do metalu można zaobserwować w niektórych kompleksach bimetalicznych. Jednakże, są one zazwyczaj traktowane tylko jako przeniesienie elektronu niż jako przesunięcie w stanie interakcji kwas-zasada Lewisa.
ponieważ pasma transferu ładunku metal-ligand obejmują międzycząsteczkowy transfer elektronów między metalem a ligandem w celu wytworzenia wysokoenergetycznego stanu redoks, stan wzbudzony CT jest zarówno lepszym utleniaczem, jak i reduktorem niż stan podstawowy. W związku z tym przeprowadzono intensywne badania nad rozwojem kompleksów metali, których Stany wzbudzone przenoszące ładunek są silnymi utleniaczami i reduktorami w oczekiwaniu, że będą one w stanie napędzać utlenianie fotokatalityczne i redukcję substratów.
* pozorną absorpcję I2 w heksanach obliczono z widma absorpcji 215 µM I2 w heksanach. Wszystkie pozostałe absorpcje pozorne obliczono na podstawie widm absorpcyjnych roztworów o wielkości 44 µM w I2.
** pozycje pasma nie są energiami pasma CT, A podane Energie HOMO są poziomami energii atomowej i niekoniecznie odpowiadają HOMO dawcy w roztworze. Z powodu tego i innych uproszczeń analiza ta nie ma na celu zastąpienia rygorystycznej analizy obliczeniowej czynników, które powodują pozycje pasma CT.
1. Meyerstein, D.; Treinin, A., Charge-transfer complexes of JOD and inorganic anions in solution. Transactions of the Faraday Society 1963, 59 (0), 1114-1120.
2. Baskar, A. J. A.; Rajpurohit, A. S.; Panneerselvam, M.; Jaccobb, M.; RoopSingh, D.; Kannappan, V., Experimental and theoretical analysis of substituent effect on charge transfer complexes of JOD and some alkylbenzenes in n-hexane solution at 303K. Chemical Data Collections 2017, 7-8, 80-92.
