13.5 D: biotyna jest koenzymem przenoszącym CO2
Przypomnijmy z punktu 6.5 b, że wiele enzymów jest zależnych od pomocy koenzymów, które są małymi (w stosunku do białka) cząsteczkami organicznymi, które wiążą-kowalencyjnie lub nie – kowalencyjnie-w miejscu aktywnym enzymu i pomagają mu katalizować jego reakcję. S-adenozylometionina (sam, sekcja 9.1 A) i ATP (sekcja 10.2) to dwa przykłady, z którymi do tej pory się spotkaliśmy i zobaczymy kilka kolejnych w kolejnych rozdziałach. Chociaż Rubisco (opisany w części B tej sekcji) jest wyjątkiem, większość enzymów katalizujących reakcje karboksylacji zależy od koenzymu zwanego biotyną, który służy jako tymczasowy nośnik dwutlenku węgla.
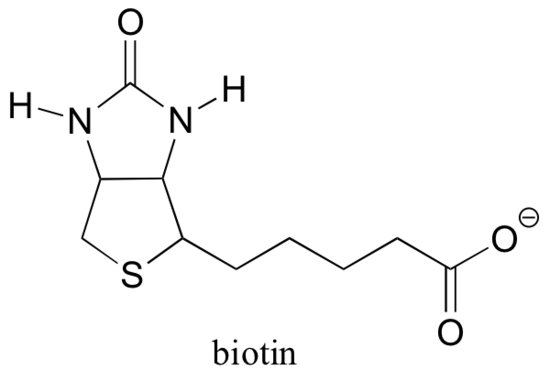
karboksylaza Pirogronianowa, enzym katalizujący pierwszy etap szlaku glukoneogensis, jest dobrym przykładem reakcji karboksylacji zależnej od biotyny. Zauważ, że CO2 w tej reakcji pochodzi z wodorowęglanu, w przeciwieństwie do reakcji Rubisco, w której CO2 jest „stałe” bezpośrednio z atmosfery.

Biotyna jest kowalencyjnie przyłączona do enzymu poprzez wiązanie amidowe z lizyną w miejscu aktywnym.
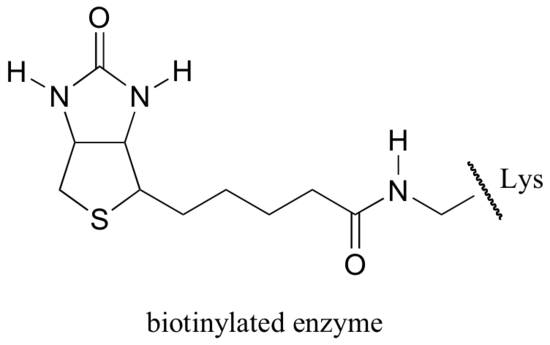
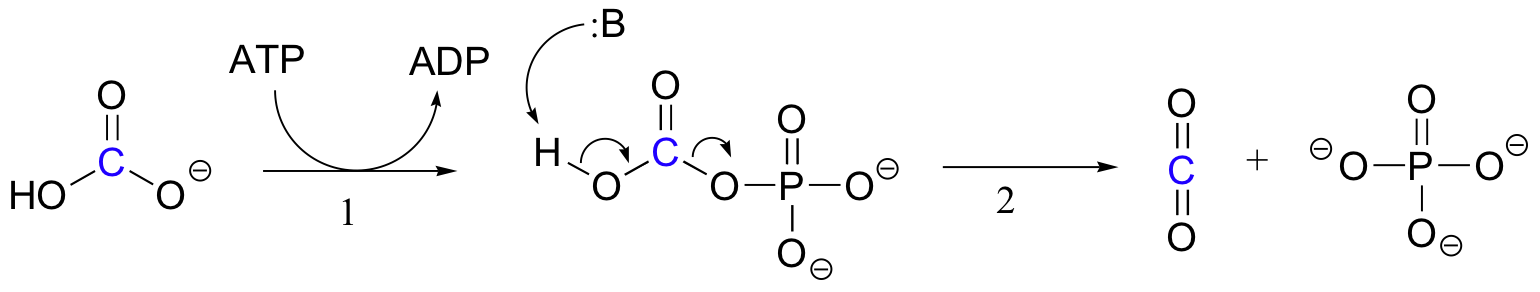
dokładny mechanizm działania zależnych od biotyny reakcji karboksylacji nadal nie jest do końca poznany, jednak poniżej znajduje się prawdopodobny obraz. Po pierwsze, jon wodorowęglanowy jest fosforylowany przez ATP (Etap 1, patrz punkt 10.2) i w ten sposób jest aktywowany do dekarboksylacji, która wytwarza wolny CO2 (etap 2).
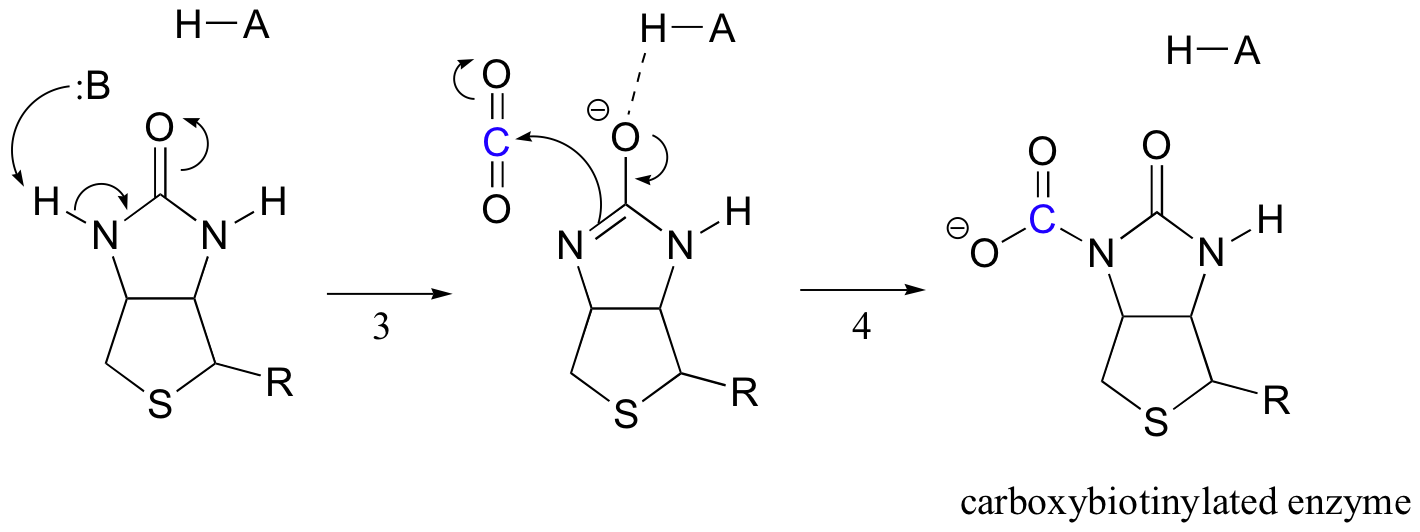
zadaniem biotyny jest utrzymywanie cząsteczki dwutlenku węgla, dopóki pirogronian nie wejdzie do miejsca aktywnego. Karboksylacja biotyny polega na deprotonacji azotu amidowego w celu utworzenia półproduktu podobnego do enolatu (etap 3-amidy mają pKa około 17, a to jest obniżane przez obecność kwasu w miejscu aktywnym w pobliżu tlenu). Po tym etapie następuje atak nukleofilowego azotu na dwutlenek węgla w celu utworzenia enzymu karboksybiotynylowanego (Etap 4).
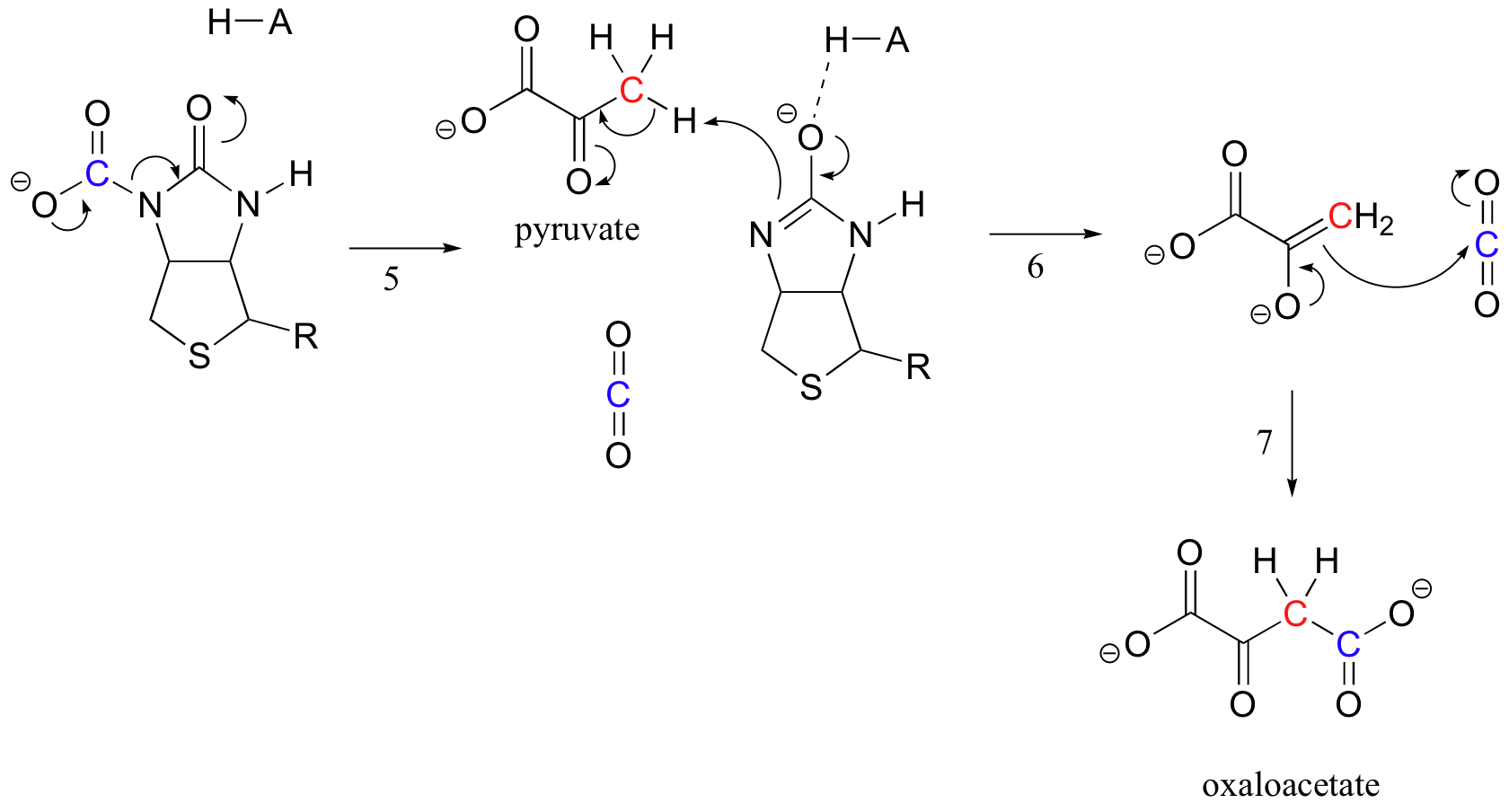
gdy cząsteczka pirogronianu wiąże się, zmiana architektury miejsca aktywnego powoduje cofnięcie się poprzedniego kroku (Krok 5), uwalniając CO2 i generując zasadę biotyny w celu deprotonacji Alfa-węgla z cząsteczki pirogronianu.pirogronian, aby mógł kondensować, w sposób podobny do aldolu, z CO2, tworząc szczawiooctan (etapy 6-7).
jeśli studiowałeś biochemię, być może słyszałeś o biotynie w nieco innym kontekście niż to, co omówiono w tej sekcji. Białko zwane awidyną, znajdujące się w obfitości w białku jaja, wiąże się nie kowalencyjnie i niezwykle ściśle z biotyną (w rzeczywistości awidyna-Biotyna jest najbardziej szczelną parą wiążącą białko-ligand znaną nauce). Biochemicy często wykorzystują tę właściwość kowalencyjnie łącząc interesującą biomolekułę z biotyną. „Biotynylowane” gatunki można następnie łatwo wyizolować ze złożonej mieszaniny przez przepuszczenie mieszaniny przez „kolumnę powinowactwa” pokrytą awidyną.
