proces van individuele vorming uit embryo
een grote verscheidenheid aan celtypen vormen het menselijk lichaam, dat bestaat uit ongeveer 60 biljoen cellen in totaal. Elk van die cellen wordt uiteindelijk afgeleid van één bevruchte eicel, die begon te verdelen, uiteindelijk onderscheidend in de somatische cellen van verschillende morfologie en functie die de verschillende weefsels en organen van het menselijk lichaam vormen. Pluripotent stamcellen worden beschouwd om gelijkaardig potentieel zonder extraembryonic differentiatie te hebben.
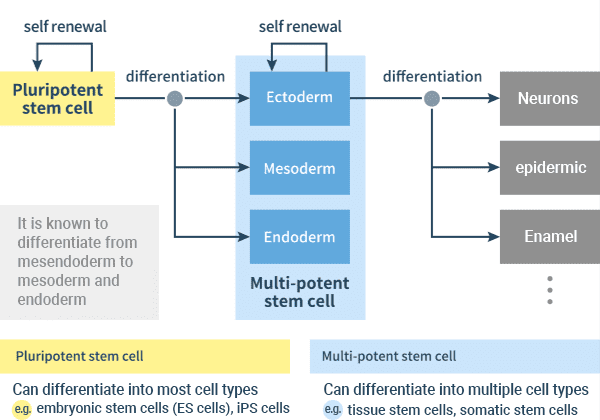
figuur: Inductie van de verschillende weefselceltypes uit pluripotente stamcellen via drie kiemlagen
tijdens het proces van vorming van een individu veranderen de stamcellen (differentiëren) in cellen die van zichzelf verschillen, terwijl het proliferatievermogen behouden blijft om meer cellen van hetzelfde type te delen en te creëren, of verder te differentiëren in een meer gespecialiseerde vorm. Zo ontstaan verschillende organen.
in het blastocyststadium, een vroeg stadium van embryonale ontwikkeling, zijn er cellen die kunnen differentiëren in bijna elk celtype waaruit het lichaam bestaat, een vermogen dat bekend staat als pluripotentcy.In vitro, pluripotent stamcellen met inbegrip van ES cellen en IPS cellen kunnen in de celtypes onderscheiden die van endoderm, mesoderm, en ectoderm worden afgeleid, maar kunnen zich niet tot volledig organisme alleen ontwikkelen. Daarentegen zijn de stamcellen die in een beperkt aantal celtypes, zoals de cellen van de weefselstam en somatische stamcellen slechts kunnen onderscheiden, genoemd geworden multipotente stamcellen.
deze cellen worden niet alleen gebruikt voor fundamenteel onderzoek, waarbij ze worden onderverdeeld in specifieke cellen om hun eigenschappen te onderzoeken, maar ook voor “drug discovery screening” om te zoeken naar geneesmiddelkandidaten, en “regeneratieve geneeskunde” waar ze worden getransplanteerd of toegediend aan patiënten als therapeutisch middel. Nochtans, is de cultuur van pluripotent stamcellen verschillend van conventionele somatische celcultuur op vele manieren, en het wordt gezegd om moeilijk te zijn om de ongedifferentieerde staat te handhaven en een hoog niveau van reproduceerbaarheid te verzekeren.
classificatie en kenmerken van multipotente stamcellen en pluripotente stamcellen
multipotente stamcellen
multipotente stamcellen kunnen differentiëren in cellen die specifieke weefsels en organen omvatten, en omvatten zowel weefselstamcellen als somatische stamcellen.
Weefselstamcellen zijn weefselspecifiek en hebben het vermogen om zichzelf te vernieuwen door deling in dochtercellen van hetzelfde type of om te differentiëren in meer gespecialiseerde cellen binnen het weefsel.
somatische stamcellen existin vivo en kunnen differentiëren in een beperkt aantal celtypes. Mesenchymal stamcellen (MSCs), zijn een type van somatische stamcel, en kunnen in been, kraakbeen, bloedvat, en cardiomyocytes onderscheiden. MSCs wordt verkregen met relatief gemak van beendermerg, navelstrengweefsel, navelstrengbloed, en vetweefsel.
multipotente stamcellen hebben een ontstekingsremmend effect, een groeifactor-inducerend effect, een proangiogeen effect en spelen een belangrijke rol bij weefselherstel. Bovendien, worden zij gezegd om risico van kanker in vergelijking met pluripotent stamcellen, een belangrijke veiligheidsoverweging te hebben verminderd.
regeneratieve medische producten zijn al wereldwijd goedgekeurd voor de behandeling van ruggenmergletsel en post-hematopoëtische stamceltransplantatie acute graft-versus-host ziekte.
tabel: Examples of Approved Regenerative Medical Products That Use Human MSCs in the World-
| Regenerative Medical Products | Approved Countries | Manufacturing Distributors | Origin MSC | Applications |
|---|---|---|---|---|
| PROCHYMAL® | Canada, New Zealand | Mesoblast | Allogeneic bone marrow-derived MSC | Acute GVHD*(pediatric) |
| TEMCELL® HS Inj. | Japan | JCR Pharma | Allogeneic bone marrow-derived MSC | Acute GVHD* |
| Stemirac® Inj. | Japan (conditional approval) | Nipro | Autologous bone marrow-derived MSC | Spinal cord injury |
| Heartcellgram-AMI® | South Korea | Pharmicell | Autologous bone marrow-derived MSC | Acute myocardial infarction |
| Cupistem® | South Korea | Anterogen | MSC derived from own fat | Crohn’s disease |
| CARTISTEM® | South Korea, EU | Medipost | Allogeneic cord blood-derived MSC | Knee osteoarthritis |
| Stempeucel® | EU, India (conditional approval) |
Stempeutics Research |
Allogeneic bone marrow-derived MSC | Knee osteoarthritis |
| Allostem® | USA | Allosource | Allogeneic fat derived MSC (A combination product composed of human demineralized bone matrix) |
Bone damage |
| Osteocel® Plus | US | NuVasive | Allogeneic bone marrow-derived MSC (A combination product composed of osteoprogenitor cells and human demineralized bone matrix) |
Bone repair (361HCT/P) |
*GVHD: Graft Versus Host Disease
pluripotente stamcellen
pluripotente stamcellen zijn stamcellen die zich kunnen onderscheiden in bijna elke cel waaruit het lichaam bestaat. ESCs, embryonale geslachtscellen (EGCs), en iPSCs zijn tot nu toe gevestigd als types van pluripotent stamcellen.
ESC ‘ s worden vastgesteld uit de binnenste celmassa in de holle blastocyst, een vroeg stadium van embryonale ontwikkeling na deling door de zygote in een blastula. In Japan worden ES-cellen vastgesteld uit het overschot aan bevruchte eieren die na behandeling van onvruchtbaarheid worden weggegooid. EGCs worden ontwikkeld uit de cellulaire precursoren van sperma en eieren (primordiale kiemcellen) en hebben bijna dezelfde eigenschappen als ESCs.
iPSCs worden gecreeerd door somatische cellen aan een ongedifferentieerde staat door de introductie van specifieke genen te herprogrammeren. De oprichting van iPSCs heeft ons toegelaten om cellen gelijkaardig aan ESCs van donoren te verkrijgen. Het is ook mogelijk om weefsel door een patiënt met een ziekte wordt geleverd te krijgen, iPSCs van het weefsel te vestigen, en differentiatie te veroorzaken om anin vitro model van de ziekte te verstrekken. Daarom hebben somatische cellen, zoals zenuwcellen of cardiomyocytes, die door veroorzaakte differentiatie van iPSCs worden gecreeerd groot potentieel voor toepassingen zoals de bepaling van ziekteetiologie, evaluatie van drugdoeltreffendheid en bijwerkingen, en transplantatie in patiënten als regeneratieve geneeskundetherapieën. Nochtans, zijn de onbedoelde genveranderingen gemeld wanneer het vestigen van IPSC culturen, evenals het subculturen van iPSCs en ESCs over lange periodes van tijd. Het is op dit moment onbekend of al deze genetische mutaties gevaarlijk zijn, en onderzoekers bespreken hoe ze hun veiligheid het best kunnen evalueren voor praktisch gebruik in de toekomst.
