chemische ionisatie (CI) is een zachte ionisatietechniek, die de directe toepassing is van de onderzoeksresultaten van moleculaire en ionenreacties in de Analytische Chemie. De vroegste ionisatietechniek was elektronenbombardement ionisatie (EI). Het door EI verkregen product bevat vele fragmenten, die moeilijk te analyseren zijn. CI, die zeer weinig fragmenten produceerde, begon in de jaren 1950 en heeft een groot potentieel in Analytische Chemie.
in het CI-proces bombarderen elektronen eerst het reagensgas om reagensionen te genereren. De steekproefmolecules worden dan geïoniseerd door reagensionen door moleculaire en ionenreactie weg. De jaren zeventig werden beschouwd als een mijlpaal in de ontwikkeling van CI. Op dat moment losten onderzoekers de tekortkomingen van het werk van CI op in een vacuümomgeving, waardoor CI onder atmosferische omstandigheden kon werken. Atmosferische chemische ionisatie levert energie uit corona-ontlading en vereist geen vacuümomgeving, waardoor het bereik van CI-toepassingen sterk toeneemt. Momenteel is CI wijd gebruikt in de massaspectrometrietechniek.
het principe van chemische ionisatie
het principe van CI is om het reagens ion X+ te gebruiken om te reageren met het analytmolecuul A om ionisatie van de analyt te bereiken:
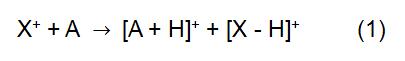
bij de bovenstaande reactie wordt X+ afgeleid van het geïoniseerde reactiegas. Sommige gemeenschappelijke reagensgassen omvatten methaan, ammoniak, water en isobutaan. De reactietijd en de snelheidsconstante (k) in de formule kunnen worden verkregen door middel van literatuur of meting. Wanneer het reagens-ion X+ H3O+ is, is de Formule (2)::
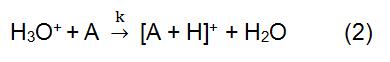
reagens-ion wordt geproduceerd door een ionenbron. Veelgebruikte ionenbronnen omvatten voornamelijk stralingsbron, holle kathodeontlading krachtbron en gewone gloeiontlading krachtbron. 210Po en 241Am zijn de meest voorkomende stralingsbronnen. Het ionisatieproces begint met de alfadeeltjes die door 210Po en 241Am worden uitgezonden. Het heeft een hoge energie en kan met het reagensgas botsen om reagensionen en elektronen te produceren. Als de gegenereerde elektronen hoog genoeg zijn, kunnen ze botsen met het reagensgas om nieuwe reagensionen en elektronica te vormen. In CI die H3O+ als reagension gebruiken, wordt een holle kathodeontladingskrachtbron algemeen gebruikt, die 99,5% van H3O+kan produceren.
volgens de omstandigheden van chemische ionisatie wordt CI ingedeeld in chemische ionisatie bij lage druk (
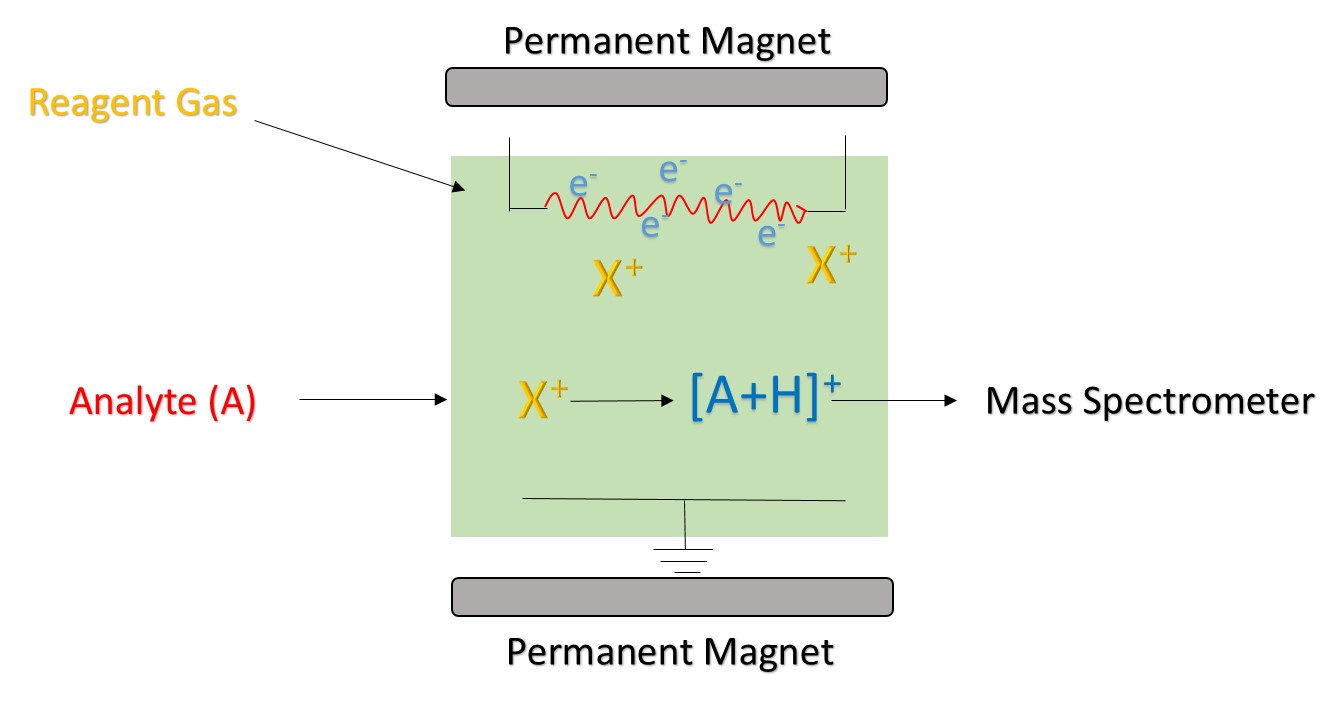 figuur 1. Het principe van chemische ionisatie
figuur 1. Het principe van chemische ionisatie
voor-en nadelen van CI
De resolutie van het CI-spectrum is eenvoudig en het exacte molecuulgewicht van de analyt kan worden verkregen. Het door CI verkregen product heeft weinig fragmenten, en zijn producten zijn hoofdzakelijk molecules en ionen van analyt. De selectiviteit van CI kan gemakkelijk worden verhoogd door een geschikt reagens-ion te selecteren. Het reagens-ion H3O + reageert bijvoorbeeld alleen met een organische stof met een proton-affiniteit groter dan H3O+. Bovendien heeft CI een hoge gevoeligheid en snelle respons (15s). Nochtans, als de reactieve ionen onzuiver zijn en een verscheidenheid van chemische ionisatiereacties tegelijkertijd zullen voorkomen, wordt de massaspectrometrie moeilijk.
voorbeelden van CI-toepassingen
momenteel wordt CI op grote schaal gebruikt als ionenbron in massaspectrometriesystemen om verschillende sporenstoffen op te sporen. CI kan worden gebruikt voor de detectie van stoffen zoals sporengassen in de atmosfeer, residuen van bestrijdingsmiddelen in groenten en fruit, melamine in melkpoeder, weekmakers en herbiciden in de bodem. Daarnaast kan CI ook worden gebruikt voor materiaalidentificatie, zoals het identificeren van de kwaliteit van thee.
- meting van vluchtige organische stoffen (vos)
bij de meting van Vos door CI wordt H3O+ over het algemeen gebruikt als reagens-ion. H3O + reageert niet met de meeste stoffen in de lucht zoals O2, N2, CO2, enz. Aan de andere kant, de meeste van de Proton overdracht reacties zijn niet-dissociated, zodat de productionen zijn single, wat de analyse van de resultaten eenvoudig maakt. Het principe van het meten van Vos met H3O+ als reagension is weergegeven in vergelijking (3). Het eindproduct werd opgelost door Proton transfer reaction massaspectrometrie.
- bepaling van melamine in melkpoeder
bij de meting van melamine door CI wordt N2 gebruikt als reagensgas. Onder de actie van hoog voltage, ondergaan N2 en H2O complexe fysicochemische reacties om reagensionen H3O+te produceren. Het reactieproces wordt weergegeven in formule (3-6). H3O + reageert met melamine in het melkpoeder en het reactieprincipe wordt weergegeven in Formule (2).
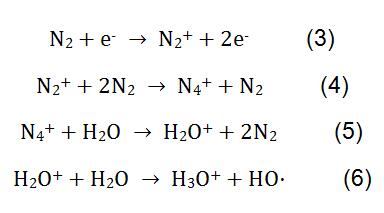
- Identificatie van de theekwaliteit
verschillende soorten thee kunnen worden geïdentificeerd door de chemische stoffen op het oppervlak van theebladeren met CI te meten. H3O + reageert met het oppervlak van de thee met butanol, geraniol, cafeïne en andere stoffen, en de reactieproducten vormen verschillende massaspectra op de massaspectrometer. Het gehalte aan dezelfde stof in verschillende soorten thee is anders, dus het massaspectrum gevormd door CI-detectie is anders. Het massaspectrum kan tot op zekere hoogte de chemische vingerafdrukkenmerken van de thee weerspiegelen. Daarom heeft CI een belangrijke praktische Toepassingswaarde voor de snelle identificatie en kwaliteitsanalyse van thee.
chemische ionisatie wordt veel gebruikt in massaspectrometrie vanwege zijn sterke selectiviteit en hoge gevoeligheid. De chemische ionisatiemassaspectrometrie (CIMS) laat niet alleen tandemmassaspectrometrie identificatie van substanties in complexe steekproeven toe, maar verkrijgt ook chemische vingerafdrukgegevens voor steekproeven voor chemometrische analyse. De toepassing van CIMS heeft een positief effect op het bevorderen van de ontwikkeling van voedsel, geneeskunde, milieubescherming, landbouw en andere industrieën.
we hebben kort de CI geïntroduceerd, een type ionisatiemethode, die u kan helpen meer te begrijpen over massaspectrometrie. Bij Creative Proteomics hebben we het professionele massaspectrometrieplatform ontwikkeld, dat state-of-the-art instrumenten bevat. Door massaspectrometrie te gebruiken, kan Creatieve Proteomics verschillende diensten verlenen om aan diverse vereisten te voldoen, met inbegrip van:
- Proteomics Service
- Metabolomics Service
- Glycomics Service
- Fales H M; et al. Vergelijking van massaspectra van sommige biologisch belangrijke samenstellingen zoals verkregen door diverse ionisatietechnieken. Analytische Chemie, 1975, 47(2):207-219.
- Lindinger W; et al. Online monitoring van vluchtige organische stoffen op PPTV-niveaus door middel van proton-transfer-reaction massaspectrometrie (PTR-MS) medische toepassingen, voedselcontrole en milieuonderzoek. International Journal of Mass Spectrometry & ion Processes, 1998, 173(3):191-241.
- Chen h; et al. Oppervlakte desorptie Atmosferische druk chemische ionisatie massaspectrometrie voor directe omringende steekproefanalyse zonder toxische chemische verontreiniging. Tijdschrift voor massaspectrometrie, 2010, 42(8):1045-1056.
- Yang s; et al. Detectie van Melamine in melkprodukten door Oppervlaktedesorptie Atmosferische druk chemische ionisatie massaspectrometrie. Analytische Chemie, 2009, 81(7):2426.
