Chelant Science
een chelant, soms aangeduid als een sequestrant of een bouwer, is een gespecialiseerde molecule ontworpen om te binden aan positief geladen metaalionen, meestal calcium en magnesium, in oplossing en zo te voorkomen dat deze ionen onoplosbare precipitaten vormen met andere ionen die aanwezig kunnen zijn. Er zijn twee basistypen chelanten, aangeduid als hard en zacht:
- harde chelanten, bijvoorbeeld EDTA (ethyleendiamine tetra azijnzuur) en NTA (Nitrilotriazijnzuur), vormen zeer stabiele complexen met een:1 stoichiometrie. Dat wil zeggen dat één EDTA-molecuul reageert met één enkel metaalion.
- zachte chelanten, bijvoorbeeld polymeren van acryl-en maleïnezuur, vormen minder stabiele complexen en functioneren door de kristalgroei te voorkomen in plaats van door echte chelatie.
zowel calcium-als magnesiumionen vormen met carbonaation zeer stabiele onoplosbare precipitaten. Bicarbonaat is alomtegenwoordig in oppervlaktewater. Het wordt gedeprotoneerd om carbonaat te geven door de hoge pH van de meeste reinigingsformules. Onoplosbare precipitaten zijn moeilijk te verwijderen zonder het gebruik van een zure reiniger. Deze moeilijk te verwijderen afzettingen worden harde waterschaal genoemd, en dus wordt water dat calcium-en magnesiumionen bevat hard water genoemd. Er zijn twee gemeenschappelijke methoden om met hard water om te gaan. De eerste is om zacht water te gebruiken. Verzacht water heeft de calcium-en magnesiumionen verwijderd. Dit wordt vaak bereikt door het gebruik van een waterontharder die natriumionen uitwisselt voor de calcium-en magnesiumionen in oplossing. De tweede methode is het gebruik van chelatoren in de formulering van het reinigingsproduct. Het cheleren van de calcium-en magnesiumionen in oplossing voorkomt ook effectief de vorming van deze afzettingen.
Calcium-en magnesiumionen vormen ook onoplosbare precipitaten met veel anionogene oppervlakteactieve stoffen, met name vetzuurcarboxylaten (zeep). De vorming van calciumzeepcomplexen is zo efficiënt dat de concentratie van de vrije oppervlakteactieve stof die beschikbaar is voor het reinigen, wordt verminderd tot effectief nul totdat al het calcium uit de oplossing is verwijderd, hetzij door chelatie, hetzij door de vorming van het onoplosbare zeepadduct. Zonder de in een reinigingsproduct aanwezige chelant zou meer oppervlakteactieve stof nodig zijn om ervoor te zorgen dat een effectieve concentratie vrije oppervlakteactieve stof beschikbaar is voor reiniging. Met andere woorden, de consument zou meer van het reinigingsproduct moeten gebruiken om een gewenst resultaat te verkrijgen. Verder zou het onoplosbare calciumzeep-adduct van oplossing neerslaan op het te reinigen oppervlak, wat leidt tot een groezelig uiterlijk en een stijf gevoel op de gewassen stof. Aldus, worden chelators gebruikt voor deze doeleinden soms aangeduid als “bouwers” aangezien zij helpen bouwen op de prestaties van de oppervlakteactieve stof.
naast het verzachten van het water van de reinigingsoplossing zijn chelanten ook effectief bij het verwijderen van bepaalde vlekken, met name die met een hoge calciumconcentratie, zoals kaasvlekken. Vlekken hebben een complexe en gevarieerde moleculaire structuur en veel omvatten metaalionen cross linking en stabilizing de vlek structuur. Chelanten die aanwezig zijn in de reinigingsoplossing binden zich met deze verschillende metaalionen en helpen ze uit de vlek te verwijderen, waardoor de vlekstructuur wordt verzwakt en de verwijdering ervan wordt vergemakkelijkt.
naast calcium en magnesium binden chelanten met alle polyvalente metaalionen in oplossing. Ijzer en mangaan, hoewel minder voorkomend, kunnen ook leiden tot aanzienlijke reinigingsproblemen, waaronder de vorming van onoplosbare precipitaten zoals ijzeroxide, roest en mangaandioxide. Daarom zijn speciale reinigingsmiddelen vaak geformuleerd met zeer efficiënte ijzerchelatoren om te binden met deze ionen, opnieuw het elimineren van de problemen die ze anders zouden kunnen veroorzaken…of in het helpen elimineren van roest en ijzer vlekken die al zijn gevormd.
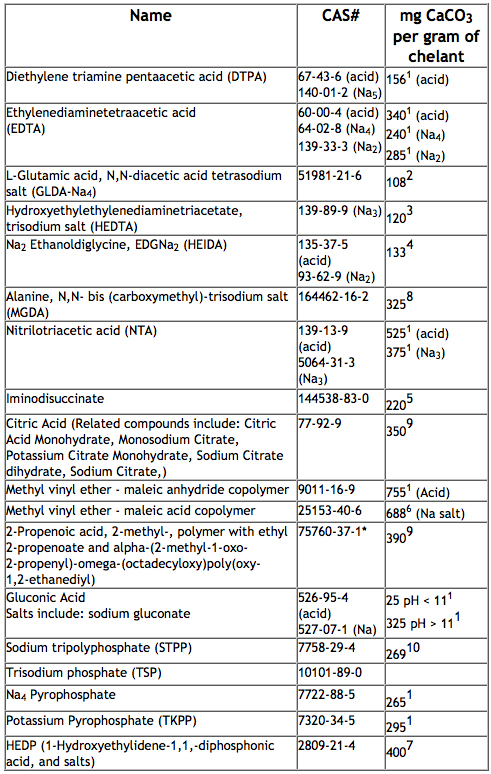
de onderstaande tabel toont vele voorbeelden van chelaatvormers die in geformuleerde producten worden gebruikt en hun theoretische vermogen om calcium uit water te binden of op te nemen om de reinigingsprestaties te verbeteren: