angiotensine II veroorzaakt verhogingen van de bloeddruk door acties op verschillende plaatsen:
- bijnieren: angiotensine II versterkt de afgifte van het steroïdhormoon aldosteron, dat lokaal werkt om natriumretentie en kaliumsecretie uit de nieren te verhogen. Het netto effect hiervan is het vasthouden van water, waardoor de vochtbalans wordt hersteld.
- nieren: Angiotensine II verhoogt ook de natriumretentie via directe effecten op de renale proximale tubuli, en beïnvloedt de glomerulaire filtratiesnelheid en de renale bloedstroom.
- cardiovasculair systeem: angiotensine II is een krachtige endogene vasoconstrictor, waardoor resistentieslagaders en-aders samentrekken, waardoor de bloeddruk stijgt. Bovendien stimuleren langdurige verhogingen van angiotensine II in zowel de bloedvaten als het hart de celgroei en de daaruit voortvloeiende hypertrofie.
- centraal zenuwstelsel: In de hersenen werkt angiotensine II op de achterste hypofyse, waardoor de afgifte van antidiuretisch hormoon (ADH, ook bekend als Arginine vasopressine (AVP)) wordt gestimuleerd. ADH verhoogt de reabsorptie van water in de renale opvangkanalen. Angiotensine II handelt ook op het subfornical orgaan binnen de hersenen om verhoogde dorst te veroorzaken, het aanmoedigen van wateropname.
chronische activering van het RAAS-systeem kan leiden tot schadelijke remodellering en toegenomen ontsteking in het hart, vasculatuur en nieren, evenals hypertensie en chronische nierziekte.
neurale controle van het cardiovasculaire systeem
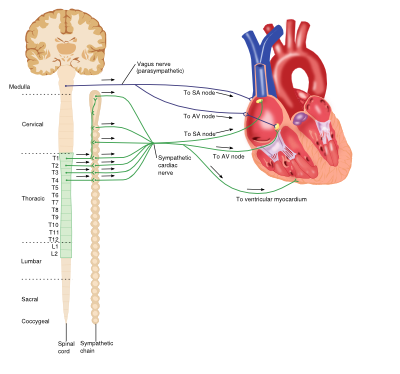
interactie tussen het sympathische en parasympatische zenuwstelsel en het hart
sympathisch (adrenerge) zenuwstelsel
adrenerge zenuwstelsel is een essentieel onderdeel van vele processen door het hele lichaam, met inbegrip van het cardiovasculaire systeem. Circulerende catecholamines (bv. adrenaline en noradrenaline) binden aan en activeren adrenerge receptoren op celmembranen. Adrenerge receptoren zijn een klasse van G-proteã ne gekoppelde receptoren die een verscheidenheid van weefsel-specifieke gevolgen opwekken en in verscheidene subtypes bestaan.
vasculatuur
het overheersende receptorsubtype aanwezig in bloedvaten is de A1-adrenerge receptor, waarvan activering door catecholaminebinding de intracellulaire signaalweg fosfolipase-C (PLC), inositoltrifosfaat (IP3), diacylglycerol (DAG) veroorzaakt. Dit resulteert uiteindelijk in samentrekking van de myocyten, vasoconstrictie en daaruit voortvloeiende verhogingen van de systemische bloeddruk.
hart
hoewel het hart myogeen is, dat wil zeggen dat de impuls voor contractie zelf wordt geïnitieerd, wordt de output van het hart beïnvloed door het centrale zenuwstelsel. Het netto effect van het sympathische systeem op het hart is om de cardiale output te verhogen. De adrenerge receptoren in het hart behoren tot de ß-receptor subfamilie en omvatten ß1 en ß3 receptoren. Catecholamine binding aan ß1-receptoren in het hart veroorzaakt een toename van het cardiale output via een aantal mechanismen: positieve chronotrope effecten, positieve inotrope effecten verhoogde automaticiteit en geleiding in zowel ventriculaire myocyten en de atrioventriculaire (AV) knoop. De ß3-receptoractivering antagoneert deze acties echter, die een negatief inotroop effect veroorzaken en een ingebouwd controlesysteem in het hart verstrekken.
langdurige verhoging van de catecholaminespiegels in de bloedsomloop (bijvoorbeeld wanneer deze worden uitgescheiden door bijniertumoren of tijden van stress) kan leiden tot chronische cardiovasculaire problemen zoals hypertensie en aritmieën.
parasympathisch zenuwstelsel
het parasympathisch systeem is gebaseerd op de binding van de neurotransmitter acetylcholine (Ach) aan muscarinereceptoren en heeft verschillende rollen in het hele lichaam.
vasculatuur
hoewel de bloedvaten muscarinereceptoren tot expressie brengen, ontvangen ze geen cholinerge innervatie; toepassing van exogeen Ach resulteert echter in een snelle en diepgaande vasodilatatie.
hart
activering van muscarinereceptoren (M2-subtype) in het hart door Ach afgegeven uit de nervus vagus veroorzaakt een vermindering van het cardiale output via tegengestelde effecten van adrenerge stimulatie: negatieve chronotrope Effecten en een afname van de AV-knoopgeleiding alsook een afname van de kracht van atriale contracties.
bloedplaatjes / stollingssysteem
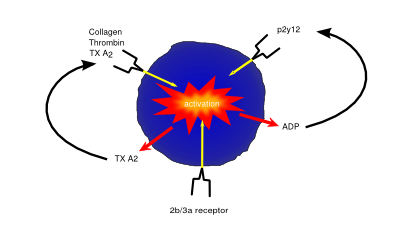
Bloedplaatjesactivatie en-remming werkt via oppervlakte-receptoren op bloedplaatjes. Feedback lussen verbeteren bloedplaatjes activering (bijv. ADP afgegeven door bloedplaatjes verhoogt de bloedplaatjesactivatie, via de ADP-receptor)
bloedplaatjes (ook bekend als trombocyten) zijn kleine cellen zonder kernen die verantwoordelijk zijn voor hemostase of bloedstolling. Schade of letsel die leidt tot bloedverlies en blootstelling van extracellulaire collageenvezels wordt gedetecteerd, waardoor bloedplaatjes worden geactiveerd. Eenmaal geactiveerd, worden bloedplaatjes klevend, klevend aan zowel de beschadigde vaatwand als aan elkaar, waardoor een klomp cellen ontstaat, of ‘stolsel’, wat helpt om het lek van het bloedvat te Dammen. Zij beginnen dan cytokines af te scheiden die invasie van fibroblasten huidig in het omringende weefsel aanmoedigen die een meer permanente flard vormen, of door gezond weefsel te creëren, of extracellulaire matrijs te deponeren om een litteken te vormen.
Er zijn verschillende aandoeningen waarbij abnormale stolling schadelijk kan zijn voor het lichaam; overmatige stolling kan leiden tot vasculaire verstopping en ischemie of beroerte; minder vaak kan deficiënte stolling leiden tot overmatig bloedverlies, bijvoorbeeld bij hemofilie. Om deze ziekten te bestrijden, zijn er medicijnen die het stollingsproces moduleren.
anticoagulantia
geneesmiddelen die stolling voorkomen (anticoagulantia) zijn belangrijk bij patiënten met een verhoogd risico op stollingsgemedieerde schade, zoals een beroerte of ischemie.
aspirine is een analgeticum en antipyreticum en is een antitrombotisch middel dat in lage doses wordt toegediend aan mensen die risico lopen op stolling (bijvoorbeeld na een hartaanval). Aspirine ‘ s anti-coagulant acties komen uit de onderdrukking van de belangrijkste pro-stollingsfactoren zoals prostaglanding en thromboxanen via irreversibele inactivering van het ptgs cyclo-oxygenase enzym. Deze onderdrukking van factoren zoals thromboxaan A2 vermindert de bloedplaatjesaggregatie en voorkomt zo stolselvorming.
P2Y12 remmers zoals clopidogrel oefenen hun antistollingseffect uit door remming van het P2Y12 subtype van de bloedplaatjes ADP receptor. Door P2Y12 te blokkeren, voorkomen deze geneesmiddelen de activering van bloedplaatjes en de vorming van het fibrinenetwerk dat nodig is voor stolling.
geneesmiddelen zoals abciximab en tirofiban voorkomen stolling door remming van de glycoproteïne IIb/IIIa receptor waardoor zowel bloedplaatjesactivering als aggregatie worden voorkomen.
farmacokinetiek
bij toediening van geneesmiddelen aan een patiënt is het van cruciaal belang om verschillende feiten over het geneesmiddel te kennen om de werkzaamheid te maximaliseren en bijwerkingen / toxiciteit te minimaliseren. Deze omvatten informatie over welke dosis effectief is, hoe lang het medicijn actief blijft in het lichaam, hoe snel het wordt afgebroken/verwijderd uit het lichaam, en hoe gemakkelijk het lichaam dat medicijn kan absorberen/gebruiken. De volgende tabel geeft een overzicht van deze Farmacokinetische eigenschappen en hoe ze worden berekend:
| Goederen | Beschrijving | Standaard eenheden (Afkorting) | Formule |
|---|---|---|---|
| Dosis | aantal werkzame medicijnen gegeven aan patiënt | mg (D) | Drug Specifieke (Van klinische studies) |
| Concentratie | Hoeveelheid van het geneesmiddel in een bepaalde plasma-volume | µg/ml (C) | = D / Vd |
| EC50 | De concentratie van de drug nodig om het uitlokken van een reactie halverwege tussen de nul en de maximale reacties. | µg / ml (EC50) | y = bottom + (Top-Bottom)/(1+ Hill Coefficient) |
| verdelingsvolume | het theoretische volume dat het geneesmiddel zou innemen indien gelijkmatig verdeeld over de weefsels om de huidige plasmaconcentratie te verkrijgen. | L (Vd) | D/C | Eliminatieconstante (snelheid) | De snelheid waarmee het geneesmiddel uit het lichaam wordt verwijderd. | H-1 (Ke) | ln(2) / t1/2 of CL / Vd | biologische beschikbaarheid | hoeveel van de toegediende dosis beschikbaar is voor daadwerkelijk gebruik door het lichaam. | geen eenheden als de uiting van een fractie (f) | 100 × (AUC (po)×D (iv))/(AUC (iv)×D (po))
AUC = Area under curve po = orale toediening iv = intraveneus administratie |
| Cmax of Cmin | De maximale (Cmax) / minimum (Cmin) plasma concentratie drug bereikt volgende drug administration | µg/ml (Cmax of Cmin) | Geïdentificeerd via directe meting van plasma-C |
| tmax | De tijd die het duurt voor een drug te bereiken Cmax na toediening | h (tmax) | Geïdentificeerd via directe meting van plasma-C over tijd |
| Half-life | De tijd die het duurt voor een drug te bereiken helft van de oorspronkelijke concentratie | h (t1/2) | ln(2) / Ke |
| Klaring | Het volume van de plasma ‘ s gewist van het geneesmiddel gedurende een bepaalde tijd | l/h (CL) | Vd x-Ke of D / Oppervlakte onder de curve |
Common Drug-Drug Interactions
Het is belangrijk om bewust te zijn van de interacties die kunnen optreden tussen gelijktijdig toegediende geneesmiddelen, als ze van invloed zijn op de werkzaamheid en/of de toxiciteit, of het produceren van negatieve kant effect. Dergelijke interacties kunnen bijvoorbeeld invloed hebben op de absorptie van geneesmiddelen, de biologische beschikbaarheid van geneesmiddelen of de werkzaamheid, of combineren om ongewenste metabolieten te produceren, evenals mogelijk effecten hebben op klinische analyses. Als een combinatie van twee drugs het effect van één of allebei van hen vermindert, wordt de interactie genoemd een antagonistisch effect; nochtans als, omgekeerd, een combinatie van twee drugs het effect van één of allebei van hen verbetert, wordt de interactie genoemd een synergetisch effect. Geneesmiddelen die inwerken op het cardiovasculaire systeem zijn hoog in interactiviteit, wat een probleem is omdat cardiovasculaire patiënten normaal meer dan één medicijn krijgen. Enkele veel voorkomende geneesmiddelinteracties met betrekking tot cardiovasculaire geneesmiddelen zijn hieronder vermeld:
| Drug | Drugs that drug action | Drugs that ↓ drug action |
|---|---|---|
| Digoxin |
|
|
| Warfarin |
|
|
| Clopidogrel |
|
|
| Furosemide |
|
|
| ACE Inhibitors |
|
|
| ß-blockers |
|
|
| Statines |
|
|
Er zijn verschillende mechanismen die drugs worden afgebroken door het lichaam, meestal via afbraak door enzymen. Een gemeenschappelijke familie van enzymen betrokken bij drugmetabolismeis de cytochroom P450 (CYP) familie; een grote, diverse groep van enzymen die oxidatie van een verscheidenheid van substraten, zowel endogene (bijv. steroïde hormonen) en exogene (bijv. toxinen en geneesmiddelen). CYP-enzymen zijn verantwoordelijk voor maximaal 75% van het drugmetabolisme, het helpen van sommige drugs om hun actieve samenstellingen te vormen maar meestal het deactiveren van drugs in inactieve metabolites om te worden uitgescheiden. CYP-enzymen kunnen de werking van het geneesmiddel op verschillende manieren beïnvloeden; ze kunnen het metabolisme van het geneesmiddel verhogen (ofwel de werking verhogen door de vorming van het actieve bijproduct of de werking verminderen door het metabolisme van het actieve geneesmiddel) of hun werking kan worden geremd door geneesmiddelen die concurreren om toegang tot de actieve plaats van de CYP-enzymen, waardoor de normale interactie tussen geneesmiddel en enzym wordt voorkomen. Veel drugs oefenen hun interactie met andere drugs uit viainterferentie met het CYP-systeem. Bijvoorbeeld, als Drug a door CYP wordt gemetaboliseerd en Drug B CYP activiteit remt, zal gelijktijdige toediening resulteren in een verminderde biologische beschikbaarheid van Drug A. Bij mensen zijn er 18 families en 43 subfamilies van de CYP groep van enzymen, die verschillende substraten richten. Enkele CYP-enzymen die belangrijk zijn in de cardiovasculaire geneeskunde, hun cardiovasculaire-geneesmiddel substraten en enkele van hun interacties zijn weergegeven in onderstaande tabel:
| enzym | substraten (bijv.) | remmers (bijv.) | inductoren (bijv.) |
|---|---|---|---|
| C2 P2C19 |
|
|
|
| CP Li > statinen (atorvastatine)
|
|||
| CYP2C9 |
|
|
|
| CYP2D6 |
|
|
|
naast geneesmiddelinteracties worden de werking van veel geneesmiddelen ook beïnvloed door voedsel of drank. Bijvoorbeeld, moet de zorg worden genomen met alcoholconsumptie met vele soorten drugs, aangezien het druk op de lever kan zetten die al hard werkt om drugs in het lichaam te metaboliseren. Grapefruitsap kan ook problemen veroorzaken, omdat bekend is dat het CYP3a remt. voor meer informatie over interacties tussen geneesmiddelen en voedsel/dranken zie deze gids: General Use of Medicine
- McMurray JJ, Adamopoulos S, Anker SD, Auricchio A, Böhm M, Dickstein K, Falk V, Filippatos G, Fonseca C, Gomez-Sanchez MA, Jaarsma T, Køber L, Lip GY, Maggioni AP, Parkhomenko A, Pieske BM, Popescu BA, Rønnevik PK, Rutten FH, Schwitter J, Seferovic P, Stepinska J, Trindade Pt, voors aa, zannad F, Zeiher A, en ESC Committee for Practice Guidelines.. ESC richtlijnen voor de diagnose en behandeling van acuut en chronisch hartfalen 2012: De taskforce voor de diagnose en behandeling van acuut en chronisch hartfalen 2012 van de European Society of Cardiology. Ontwikkeld in samenwerking met de Heart Failure Association (HFA) van het ESC. EUR Heart J. 2012 Jul; 33(14): 1787-847. DOI: 10.1093 / eurheartj / ehs104 / PubMed ID:22611136
- Rydén L, Standl E, Bartnik M, Van den Berghe G, Betteridge J, de Boer MJ, Cosentino F, Jönsson B, Laakso M, Malmberg K Priori S, Ostergren J, Tuomilehto J, Thrainsdottir ik, Vanhorebeek ik, Stramba-Badiale M, Lindgren P, Qiao Q, Priori SG, Blanc JJ, Budaj Een, Camm J, Dean V, J Deckers, Dickstein K, Lekakis J, McGregor K, Metra M, Morais J, Osterspey Een, Tamargo J, Zamorano JL, Deckers JW, Bertrand M, Charbonnel B, Erdmann E, Ferrannini E, Flyvbjerg Een, Gohlke H, Juanatey JR, Graham ik, Monteiro PF, Parhofer K, Pyörälä K, Raz ik, Schernthaner G, Volpe M, Hout D, Task Force op Diabetes en hart-en vaatziekten van de European Society of Cardiology (ESC)., en European Association for the Study of Diabetes (EASD).. Richtlijnen voor diabetes, pre-diabetes en hart-en vaatziekten: samenvatting. De Task Force Diabetes en hart-en vaatziekten van de European Society of Cardiology (ESC) en van de European Association for the Study of Diabetes (EASD). EUR Hart J. 2007 Jan;28 (1): 88-136. DOI: 10.1093 / eurheartj / ehl260 / PubMed ID:17220161
- Perk J, De Backer G, Gohlke H, Graham I, Reiner Z, Verschuren M, Albus C, Benlian P, Boysen G, Cifkova R, Deaton C, Ebrahim S, Fisher M, Germano G, Hobbs R, Hoes a, Karadeniz S, Mezzani A, Prescott E, Ryden L, Scherer M, Syvänne m, Scholte op Reimer WJ, Vrints C, Wood D, Zamorano jl, zannad F, European Association for Cardiovascular Prevention & Rehabilitation (Eacpr). en ESC-Comité voor praktijkrichtlijnen (CPG).. European Guidelines on cardiovascular disease prevention in clinical practice (versie 2012). De vijfde gezamenlijke taskforce van de European Society of Cardiology and Other Societies over de preventie van hart-en vaatziekten in de klinische praktijk (samengesteld door vertegenwoordigers van negen verenigingen en door uitgenodigde deskundigen). Eur Heart J. 2012 Jul; 33(13): 1635-701. DOI: 10.1093 / eurheartj / ehs092 / PubMed ID: 22555213
- Task Force on the management of ST-segment elevation acute myocardinfarct of the European Society of Cardiology (ESC)., Steg PG, James SK, Atar D, Badano LP, Blömstrom-Lundqvist C, Borger MA, Di Mario C, Dickstein K, Ducrocq G, Fernandez-Aviles F, Gershlick AH, Giannuzzi P, Halvorsen S, Huber K, Juni P, Kastrati a, Knuuti J, Lenzen MJ, Mahaffey KW, Valgimigli M, Van ’t Hof A, Widimsky P, en Zahger D. behandeling van acuut myocardinfarct bij patiënten met ST-segmentstijging. Eur Heart J. 2012 Oct; 33(20): 2569-619. DOI: 10.1093 / eurheartj / ehs215 / PubMed ID:22922416
- Blomström-Lundqvist C, Scheinman MM, Aliot EM, Alpert JS, Calkins H, Camm AJ, Campbell WB, Haines DE, Kuck KH, Lerman BB, Miller DD, Shaeffer CW Jr, Stevenson WG, Tomaselli GF, Antman EM, Smith SC Jr, Alpert JS, Faxon DP, Fuster V, Gibbons RJ, Gregoratos G, Hiratzka LF, Jacht SA, Jacobs AK, Russell RO Jr, Priori SG, Blanc JJ, Budaj Een, Burgos EF, Cowie M, Deckers JW, Garcia MA, Klein WW, Lekakis J, Lindahl B, Mazzotta G, Morais JC, Oto A, Smiseth O, Trappe HJ, American College of Cardiology. American Heart Association Task Force on Practice Guidelines., en European Society of Cardiology Committee for Practice Guidelines. Schrijfcommissie om richtlijnen te ontwikkelen voor de behandeling van patiënten met supraventriculaire aritmieën.. ACC / AHA / ESC guidelines for the management of patients with supraventricular aritmias — executive summary: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines and the European Society of Cardiology Committee for Practice Guidelines (Writing Committee to Develop Guidelines for the Management of Patients With Supraventricular Aritmias). Circulatie. 2003 Oct 14; 108 (15):1871-909. DOI: 10.1161 / 01.CIR.0000091380.04100.84/PubMed ID:14557344
- European Association for Cardiovascular Prevention & revalidatie., Reiner Z, Catapano AL, de Backer G, Graham I, Taskinen MR, Wiklund O, Agewall S, Alegria E, Chapman MJ, Durrington P, Erdine s, Halcox J, Hobbs R, Kjekshus J, Filardi PP, Riccardi G, Storey RF, Wood D, en ESC Committee for Practice Guidelines (CPG) 2008-2010 en 2010-2012 commissies.. ESC / EAS-richtsnoeren voor de behandeling van dyslipidemieën: de Task Force voor het beheer van dyslipidemieën van de European Society of Cardiology (ESC) en de European Atherosclerosis Society (EAS). Eur Heart J. 2011 Jul; 32(14): 1769-818. DOI: 10.1093 / eurheartj / ehr158 / PubMed ID: 21712404
alle Medline abstracts: PubMed
