introductie
cel-of weefselvernieuwing en-regeneratie zijn de twee belangrijkste ontwikkelingsvereisten van volwassen organismen. Beide processen hebben als uitgangspunt een populatie stamcellen, normaal gelokaliseerd in een specifiek milieu genoemd de “niche” , die hen de vereiste signalen verstrekt om de stamnesseigenschappen te handhaven, of om aan de vereiste verschillende celtypes te onderscheiden (figuur 1). Stamcelproliferatie en differentiatie moeten worden gecoördineerd met de dood van de cellen die moeten worden vervangen. Bovendien zijn processen zoals celmigratie, epigenetica en cellulaire communicatie ook noodzakelijk voor een goede celvernieuwing . Fast renewaltissues kunnen worden herkend door een hogere mitotische activiteit. Omgekeerd, bevatten de langzame vernieuwingsweefsels minder mitose, en kunnen niet gemakkelijk van niet-vernieuwend gebieden worden herkend die somemitosis ook kunnen voorstellen . De lotsbeslissingen van stamcellen tijdens proliferatiedirect beïnvloeden weefselvernieuwing en homeostase. Daarom is het van cruciaal belang om inzicht te krijgen in de regulerende mechanismen die een evenwichtige celverdeling en differentiatie ondersteunen. De extracellulaire signalen (b.v., weefselmicromilieu, intracellular ROS, en cytokines) evenals intracellular factoren (b. v., epigenetic machines, transcriptionfactoren en de schadereactie van DNA) zijn de oorzaak van theregulation van de afdeling van de stamcel.
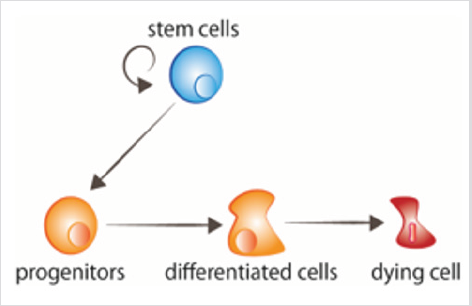
figuur 1: celomzet stamcellen vermenigvuldigen, waardoor voorlopercellen ontstaan die daarna de signalen ontvangen om te verschillen. Oude cellen ontvangen signalen om te sterven.
stamcellen tonen drie mogelijke opties voor deling: asymmetrische deling, waarbij één stamcel en één geënte dochtercel ontstaan zijn; symmetrische binding, die twee geëngageerde dochtercellen omvat; en symmetrische deling,die twee dochtercellen oplevert die de stamceleigenschappen behouden Figuur 2. Hoewel kan worden voorspeld dat asymmetrische verdeling het enige mechanisme is dat het behoud van een stabiele populatie van stamcellen mogelijk maakt, toonden de huidige gegevens van lineagetracingexperimenten aan dat in de meeste weefsels het evenwicht tussen stamcelproliferatie en het genereren van differentiëleverschuiving wordt bereikt op het niveau van de gehele stamcelpopulatie.Het verlies van stamcellen toe te schrijven aan differentiatie of celschade, veroorzaakt symmetrische verdeling om dit hiaat te vullen . Na de deling van de stamcel, gaan de cellen die het differentiatieproces volgen door verschillende stadia door die door een combinatie van transcriptiefactoren worden bepaald die de activiteit van het aangewezen repertoire van genen controleren, en hun verplichting en einddifferentiatie toestaan. Voor elke cellijn is het eindproduct van de volgorde van beslissingen een specifiek verschillend celtype figuur 3a. onder de meeste omstandigheden is de cellulaire identiteit – het product van normale differentiatie – stabiel in weefsels,en het onderhoud ervan is cruciaal voor normale weefselfunctie. Dergelijke stabiliteit wordt bereikt door epigenetische regelgeving-b. v .histone demethylation en acetylation – die in erfelijke patronen van weefsel-specifieke genuitdrukking resulteert.
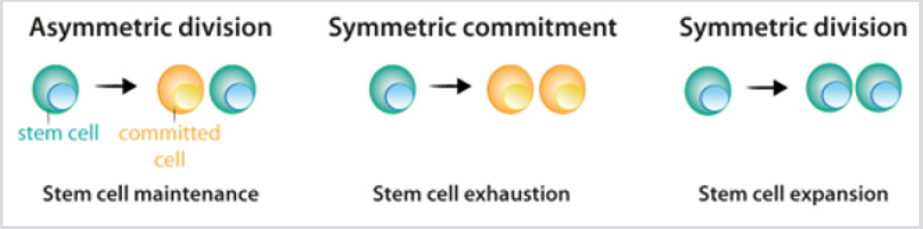
figuur 2: Delingspatroon van stamcellen.
a) tijdens asymmetrische deling geven stamcellen aanleiding tot één stamcel, die de stamcelpopulatie handhaaft, en één cel die zich inzet voor differentiatie.
b) tijdens symmetrische commitment geeft stamceldeling aanleiding tot twee dochtercellen die zich aandifferentiatie hebben gecommitteerd.
c) tijdens symmetrische deling geeft stamcelafdeling aanleiding tot twee stamcellen. Zoals uitgelegd in de tekst, geeft de huidige experimentaldata aan dat de Drie Wijzen van deling kunnen voorkomen met behoud van de stamcelpopulatie.
echter, verlies van celidentiteit kan optreden. Inderdaad, cellen vandrosophila imaginal disc zijn in staat om transdetermineren en acquirea nieuwe volwassen lot na transplantatie . In deze situatie,lijken extracellulaire cues om sommige voorloper of verschillende cellen te herprogrammeren om kenmerken van of een meer stamstaat of een nieuwe gedifferentieerde staat te verwerven. Er zijn twee mechanismendoor welke een cel zijn identiteit kan veranderen: dedifferentiation, entransdifferentiation. Dedifferentiation verwijst naar het proces waardoor een gedifferentieerde of geëngageerde cel kenmerken van een minder rijpe celfiguur 3b verwerft. Het meest dramatische voorbeeld van dedifferentiatie is de in vitro omzetting van terminaal gedifferentieerde cellen in pluripotente cellen (geïnduceerde pluripotentstem cellen, iPSCs), door de overexpressie van een beperkt aantal transcriptiefactoren . De transdifferentiatie, daarentegen, komt voor wanneer een gedifferentieerde cel het transcriptional programma verandert en in een ander gedifferentieerd celtype omzet. Het proces kan plaatsvinden door middel van een tussenstap van dedifferentiatie naar een minder volwassen stadium vóór de omzetting in de nieuwe differentiatedcel, of direct, zonder de intermediate fase figuur 3c-D.de directe omzetting van fibroblasten in myoblasten door de ectopicexpressie van MyoD is een voorbeeld van het tweede proces .
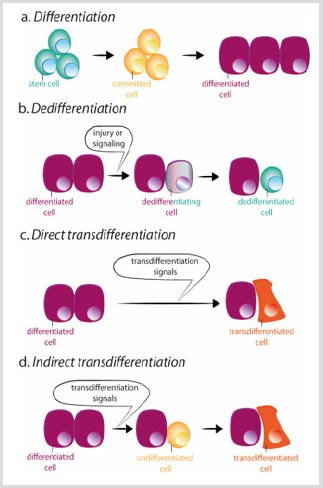
figuur 3: schema ‘ s van differentiatie, dedifferentiatie en transdifferentiatie.
a) tijdens normale differentiatie geven stamcellen aanleiding tot geëngageerde cellen die op hun beurt differentiëren in verschillende celtypen.
b) Dedifferentiatie bestaat uit het verwerven van stamceleigenschappen door een gedifferentieerde cel. Transdifferentiatie kan direct of indirect plaatsvinden.
c) tijdens directe transdifferentiatie verwerft een gedifferentieerde cel het transcriptionele programma van een ander celtype, dat gewoonlijk nauw verwant is, zoals bijvoorbeeld exocriene met endocriene pancreascellen, en wordt een verschillende gedifferentieerde cel.
d) tijdens indirecte transdifferentiatie dedifferentieert een gedifferentieerde cel voordat het nieuwe transcriptieprogramma van het andere celtype wordt aangenomen.
Dedifferentiatie en transdifferentiatie komen ook op een natuurlijke manier voor als reactie op een verwonding of weefselverlies .Dedifferentiatie, bijvoorbeeld, komt van nature voor tijdens limbregeneratie in de urodele amfibieën. Na amputatie van ledematen,dedifferentieren de cellen naast de wond, die een blastema vormen dat bestaat uit ongedifferentieerde cellen die zich verspreiden en uiteindelijk,herdifferentieren in hetzelfde celtype om alle componenten van het verloren ledemaat te creëren. De natuurlijke transdifferentiatie komt indirect voor: eerst, de cel dedifferentiates; en dan wordt het natuurlijke ontwikkelingsprogramma geactiveerd, toestaand de cel om in de nieuwe lijn te onderscheiden. Tsonis en medewerkers beschreven een natuurlijk mechanisme van transdifferentiatie in een salamander. Ze vonden dat wanneerlenses worden verwijderd, gepigmenteerde epitheliale cellen uit de dorsale iristransdifferentiate, en regenereren het ontbrekende Weefsel. Om dit te bereiken, moeten de gepigmenteerde epitheliacellen eerst dedifferentiate en verspreiden om nieuwe lenscellen tot stand te brengen, en dan in de cellen van de lens differentiëren . In beide situaties-dedifferentiatie en redifferentiatie in hetzelfde celtype of transdifferentiatie naar een nieuw celtype – kan een complex netwerk van signalerende wegen het transcriptionele programma controleren dat door elke cel in het perfecte tijdstip wordt verworven.
hus, is de spatiotemporale controle van genexpressie continu vereist tijdens dierlijke homeostase en tijdens een generatief proces. Nochtans, tijdens regeneratie, moeten de cellen zich aanpassen aan de nieuwe situatie, die het maken van meer professionele beslissingen op cellulair niveau vereist, vaak met inbegrip van processen vandifferentiatie en transdifferentiatie die tijdens homeostase schaars zijn.
- Clevers h, Loh KM, Nusse R (2014) stam cell signaling. Een integralprogramma voor weefselvernieuwing en regeneratie Wnt signalering en stemcell controle. Wetenschap 346 (6205): 1-9.
- Leblond C P, Walker B(1956) Renewal of cell population 36 (2): 255-276.
- Roostaee a, Benoit YD, Boudjadi S ,Beaulieu JF (2016) Epigenetics inIntestinal Epithelial Cell Renewal. J Celfysiol 231 (11): 2361-2367.
- Ito K, Ito K (2016) Metabolism and the Control of Cell Fate Decisions andStem Cell Renewal. Annu Rev Cell Dev Biol 32: 399-409.
- Simons BD, Clevers H (2011) Strategies for homeostatic stam cell selfrenewalin adult tissues. Cel 145 (6): 851-862.
- Yang Y, Akinci E, Dutton JR, Banga a, Slack JM W, et al. (2013) het Stagespecific herprogrammeren van de levercellen van het muizenembryo aan een BÃ tacel-likephenotype. Mech Dev 130 (11-12): 602-612.
- Merrell AJ, Stanger BZ (2016) volwassen celplasticiteit in vivo: dedifferentiatie en transdifferentiatie zijn terug in stijl. Nat Rev MolCell Biol 17 (7): 413-425.
- Worley MI, Setiawan L, Hariharan IK (2012) Regeneration andtransdetermination in Drosophila imaginal discs. Annu Rev Genet 46: 289-310.
- Raff M (2003) volwassen Stamcelplasticiteit: feit of Artefact? Annu Rev CellDev Biol 19: 1-22.
- Takahashi K, Yamanaka S (2006) Induction of Pluripotent stam cells from Mouse Embryonic and Adult Fibroblast Cultures by DefinedFactors. Cel 126 (4): 663-676.
- Tapscotr SJ, Davis RL, Thayer MJ, Cheng PF, Weintraub H, et al. (1988)MyoDi: a Nuclear Phosphoprotein Reqiring a Myc Homology Region toConvert fibroblasten to myoblasten. Wetenschap 242 (4877): 405-411.
- Jopling C, Boue S, Izpisua Belmonte JC (2011) Dedifferentiation,transdifferentiation and reprogramming: three routes to regeneration.Nat Rev Mol Cell Biol 12 (2): 79-89.
- Tsonis PA, Madhavan M, Tancous EE, Del Rio-Tsonis K (2004) Del Rio-Tsonis, K. A newt s eye view of lens regeneration. Int. J Dev Biol 48 (8-9): 975-980.
