Introduksjon
Celle-eller vevsfornyelse og regenerering er de to hovedutviklings kravene til voksne organismer. Begge prosessene har som utgangspunkt en populasjon av stamceller, som normalt befinner seg i et bestemt miljø kalt «nisje», som gir dem de nødvendige signalene for å opprettholde stemnessegenskapene, eller å skille til de nødvendige forskjellige celletyper (Figur 1). Stemcell proliferasjon og differensiering må samordnes meddøden til cellene som må byttes ut. I tillegg prosesserslik som cellemigrasjon, epigenetikk og mobilkommunikasjon, er også nødvendig for riktig cellefornyelse . Rask fornyelsevev kan gjenkjennes av en høyere mitotisk aktivitet. Omvendt, langsom fornyelse vev inneholder mindre mitose, og kan ikke lett gjenkjennes fra ikke-fornyende områder som også kan presentere somemitosis . Skjebnen beslutninger av stamceller under proliferasjondirekte påvirke vev fornyelse og homeostase. Derfor er forståelse av reguleringsmekanismer som opprettholder en balansertcell-divisjon og differensiering kritisk. Ekstracellulære signaler (f. eks. vevsmikromiljø, intracellulær ROS og cytokiner) samt intracellulære faktorer (f.eks. epigenetiske maskiner, transkripsjonsfaktorer og DNA-skaderespons) er ansvarlige for regulering av stamcelledeling.
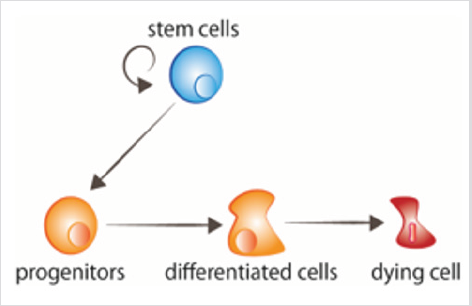
figur 1: Celleomsetning Stamceller sprer seg, girstige til progenitorer som deretter mottar signalene tildifferensiere. Eldre celler mottar signaler for å dø.
Stamceller viser tre mulige alternativer for divisjon: asymmetrisk divisjon, hvor en stamcelle og en begått dattercelle er oppstått; symmetrisk forpliktelse, som gir to engasjerte datterceller; Og symmetrisk deling,som gir to datterceller som opprettholder stamcelleegenskaper Figur 2. Selv om det kan forutses at asymmetriskdivisjon er den eneste mekanismen som muliggjør vedlikehold av en stabil populasjon av stamceller, viste de nåværende dataene fra lineagetracingeksperimenter at i de fleste vev oppnås balansen mellom stamcelleproliferasjon og generering av differensiertavkom på nivået av hele stamcellepopulasjonen.Tapet av stamceller på grunn av differensiering eller celleskader, induserersymmetrisk deling for å fylle dette gapet . Etter stamcelledeling, celler som følger differensieringsprosessen, går gjennom forskjelligestadier som er definert av en kombinasjon av transkripsjonsfaktorersom styrer aktiviteten til det aktuelle repertoaret av gener, ogtillate deres engasjement og terminal differensiering. For hver celllineage sluttproduktet av sekvensen av beslutninger er en spesifikkdifferensiert celletype Figur 3a. under de fleste omstendigheter er cellulær identitet – produktet av normal differensiering-stabiltinnenfor vev, og vedlikeholdet er avgjørende for normalt vevfunksjon. Slik stabilitet oppnås gjennom epigenetisk regulering-f. eks. histondemetylering og acetylering – som resulterer i arvelige mønstre av vevsspesifikt genuttrykk .
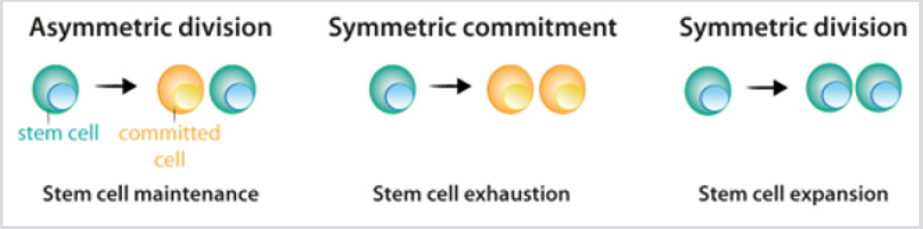
figur 2: Delingsmønster av stamceller.under asymmetrisk deling gir stamceller opphav til en stamcelle, som opprettholder stamcellepopulasjonen, og en cellesom blir forpliktet til differensiering.
b) under symmetrisk engasjement gir stamcelledeling opphav til to datterceller som ble forpliktet tildifferensiering.
c) under symmetrisk deling gir stamcelledeling opphav til to stamceller. Som forklart i teksten, nåværende eksperimentelldata indikerer at de tre divisjonsmodusene kan oppstå mens stamcellepopulasjonen opprettholdes.
imidlertid kan tap av celleidentitet forekomme. Faktisk er celler fradrosophila imaginal disc i stand til å transdefinere og skaffe segen ny voksen skjebne etter transplantasjon . I denne situasjonen synes ekstracellulære signaler å omprogrammere noen forløper ellerdifferentierte celler for å skaffe seg egenskaper av enten en mer stammetilstand eller en ny differensiert tilstand. Det er to mekanismerhvor en celle kan endre sin identitet: dedifferentiering ogtransdifferensiering. Dedifferentiering refererer til prosessen vedsom en differensiert eller forpliktet celle oppnår egenskaperav en mindre moden celle Figur 3b. Det mest dramatiske eksempelet på dedifferensiering er in vitro konvertering av terminaltdifferensierte celler til pluripotente celler (induserte pluripotentstemceller, iPSCs), ved overuttrykk av et begrenset antalltranscription faktorer . Transdifferentiering skjer derimot når en differensiert celle endrer det transkripsjonelle programmet ogkonverterer til en annen differensiert celletype. Prosessen kan skje gjennom en mellom trinn av dedifferensiering mot aless modne scenen før konverteringen til den nye differensiert celle, eller direkte, uten mellomstadiet Figur 3c-d. den direkte konvertering av fibroblaster til myoblaster ved ektopiskuttrykk Av MyoD er et eksempel på Den andre prosessen .
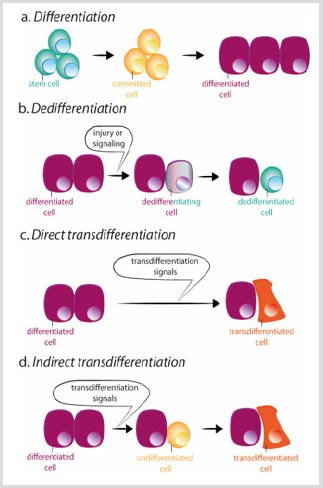
figur 3: Ordninger for differensiering, dedifferensiering og trans differensiering.
a) under normal differensiering gir stamceller opphav til engasjerte celler som igjen skiller seg i forskjellige celletyper.
b) Dedifferentiering består av oppkjøpet av stamcelleegenskaper ved en differensiert celle. Trans differensiering kan forekommepå en direkte eller indirekte måte.
c) under direkte transdifferensiering kjøper en differensiert celle det transkripsjonelle programmet av en annen celletype, vanligvisnært relatert, som for eksempel eksokrin til endokrine bukspyttkjertelceller, blir en annen differensiert celle.
d) under indirekte transdifferensiering dedifferensierer en differensiert celle før det nye transkripsjonsprogrammet av den andre celletypen tas i bruk.
Dedifferentiering og transdifferentiering forekommer også ien naturlig måte som svar på en skade eller vevstap .Dedifferentiering forekommer for eksempel naturlig under limbregenerasjon i urodele-amfibier. Etter lem amputasjon, celler ved siden av såret dedifferensiere, danner en blastema sombestår av utifferentierte celler som sprer seg og til slutt redifferentierer i samme celletype for å lage alle komponenteneav den tapte lemmen. Naturlig transdifferensiering skjer indirekte: først dedifferentierer cellen; og så aktiveres det naturlige utviklingsprogrammet, slik at cellen kan skille seg inn i ny avstamning. Tsonier og samarbeidspartnere beskrev en naturligtransdifferentiasjonsmekanisme i en newt. De fant at nårlinser fjernes, pigmenterte epitelceller fra dorsal iristransdifferensiere og regenerere det manglende vevet. For å oppnådette, pigmenterte epitelceller må først dedifferensiere ogspredning for å skape nye linseceller, og deretter differensiere tilmodne celler i linsen . I begge situasjoner – dedifferensiering og redifferensiering i samme celletype eller transdifferensiering til en ny celletype-kan et komplekst nettverk av signalveier kontrollere det transkripsjonelle programmet som er oppnådd av hver celle iperfekt tidspunkt.
hus, den romlig kontroll av genuttrykk er kontinuerlig nødvendig under dyr homeostase, og under aregenerative prosessen. Men under regenerering må cellenejustere seg til den nye situasjonen, noe som krever å gjøre merrofound beslutninger på mobilnivå, ofte inkludert prosesser avdedifferensiering og transdifferentiering som under homeostaserer knappe.
- Clevers H, Loh KM, Nusse R (2014) Stamcellesignalering. Et integrert program For vevsfornyelse Og regenerering Wnt signalering og stemcell kontroll. Vitenskap 346 (6205): 1-9.
- Leblond C P, Walker B(1956) Fornyelse av cellepopulasjon 36(2): 255-276.
- Roostaee A, Benoit YD, Boudjadi S, Beaulieu jf (2016) Epigenetikk inIntestinal Epitelcellefornyelse. J Celle Physiol 231 (11): 2361-2367.
- Ito K, Ito K (2016) Metabolisme og Kontroll Av Celle Skjebne Beslutninger andStem Celle Fornyelse. Annu Rev Celle Dev Biol 32: 399-409.
- Simons BD, Clevers H (2011) Strategier for homeostatisk stamcelle selvrenewalin voksent vev. Celle 145 (6): 851-862.
- Yang Y, Akinci E, Dutton JR, Banga A, Slack JM W, et al. (2013) Stagespesifikk omprogrammering av musembryoleverceller til en betacelle-likefenotype. Mech Dev 130 (11-12): 602-612.
- MERRELL AJ, Stanger BZ (2016) Voksen celle plastisitet in vivo: dedifferentiationand transdifferentiation er tilbake i stil. Nat Rev MolCell Biol 17 (7): 413-425.
- Worley MI, Setiawan L, Hariharan IK (2012) Gjenfødelse andtransbestemmelse I Drosophila imaginal plater. Annu Rev Genet 46: 289-310.
- Raff M (2003) Voksen Stamcelleplastisitet: Fakta eller Artefakt? Annu Rev CellDev Biol 19: 1-22.
- Takahashi K, Yamanaka S (2006) Induksjon Av Pluripotente Stamcellerfra Musembryonale Og Voksne Fibroblastkulturer Per Definedfaktorer. Celle 126 (4): 663-676.
- Tapscotr SJ, Davis RL, Thayer MJ, Cheng PF, Weintraub H, et al. (1988) MyoDi: A Nuclear Phosphoprotein Reqiring A Myc Homology Region toConvert Fibroblaster Til Myoblaster. Vitenskap 242 (4877): 405-411.
- Jopling C, Boue S, Izpisua Belmonte JC (2011) Dedifferensiering, transdifferensiering og omprogrammering: tre veier til regenerering.Nat Rev Mol Celle Biol 12 (2): 79-89.
- Tsonis PA, Madhavan M, Tancous EE, Del Rio-Tsonis K (2004) Del Rio-Tsonis, K. et newts øyesyn på objektivregenerering. Int J Dev Biol 48 (8-9): 975-980.
