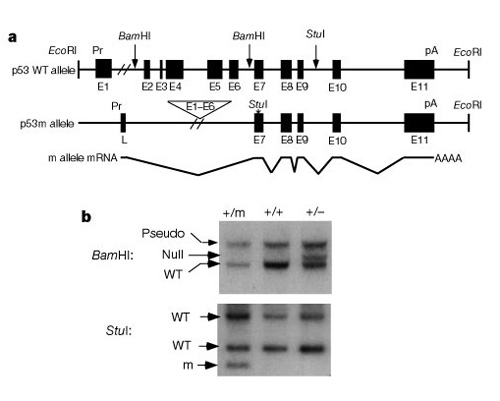
Una parte importante della comprensione di come questi sistemi funzionano per controllare la divisione cellulare è stata la scoperta che p53 ha un impatto sia sul cancro che sull’invecchiamento. Tyner et al. (2002) ha ideato una strategia agenetica nei topi per confrontare gli effetti dell’assenza di p53 o di una proteina p53 più piccola del normale. Le due linee di topo transgeniche mutanti avevano una delezione completa del gene p53 (p53-) o una forma troncata di p53 (p53m, mutante)che non aveva i primi sei esoni del gene p53 (Figura 2).
Il primo semestre di studio a confronto tre gruppi di topi:gruppo 1, p53+/p53(deletionof una copia di p53); gruppo 2, p53+/p53m(parziale mutante di delezione); gruppo 3, p53+/p53+(wild type, normale). La tabella 1 mostra questi tre gruppi e i loro risultati sperimentali correlati ai fenotipi del cancro e dell’invecchiamento. È interessante notare che nessuno dei topi nel gruppo 2, con la proteina p53 troncata, ha sviluppato tumori potenzialmente letali, mentre il 45% del gruppo 3 (tipo selvaggio) e oltre l ‘ 80% del gruppo 1 si sono sviluppati tumori potenzialmente letali. I topi del gruppo 2 avevano anche una durata di vita intermedia tra la durata molto breve del gruppo 1 e la durata più lunga dei topi del gruppo 3. La conclusione da questi dati è che la mutazione p53 parziale ha ridotto l’incidenza dicancro e allo stesso tempo sembrava causare un deficit nella durata della vita, non una durata prolungata.
| Tabella 1. Experimental results from genetic mousestudies with p53 mutants | |||
| Genotype | Cancer phenotype | Agingphenotype | |
| Group 1 | p53+/p53- (complete deletion) | 80%had tumors | Muchshorter life span |
| Group 2 | p53+/p53m (partial mutant) | None | Shorterlife span |
| Group 3 | p53+/p53+ (wild type) | 45%had tumors | Normallife span |
| Adattato da Tyner etal. 2002 | |||
Gli autori alsonoted che il gruppo 2 topi sviluppato fenotipi caratteristici di topi vecchi, le rinomate rallentare la ricrescita dei capelli e gobbi spine a causa di alterazioni scheletriche, earlierthan i topi wild-type ha fatto (Figura 3).

Nella seconda metà dello studio, Tyner e colleghiha chiesto se il mutante p53 funzionasse diversamente in presenza di p53 normale. Hanno allevato un’ulteriore linea di topi transgenici con mutantalleli p53 – / p53m e hanno scoperto che questi topi non avevano la forte protezione del tumore e mostravano un effetto di durata molto minore. Quindi il mutante p53 in qualche modo aveva bisogno di lavorare inconcert con il normale p53 per avere un effetto. Come osservazione generale, i ricercatori hanno riferito che le cellule dell’eterozigote p53 + / p53m si sono rivelate circa tre volte più difficili da trasformare delle cellule di tipo selvaggio. Pertanto, sebbene queste cellule fossero resistenti acancro, questo fondo p53+/ p53m ha anche causato un invecchiamento precedente. In effetti, l’attività di p53 in questieterozigoti sembrava essere notevolmente superiore alla sua attività in natura type.It sembrava che un tale cambiamento, mentre apriori, sarebbe buono sia contro il cancro e la senescenza, ma che turnedout non essere il caso.
Più tardi, Mooreet al. dimostrato che in culturacellule con la stessa mutazione che causa la proteina p53 troncata, questa proteina troncata è entrata nel nucleo e colocalizzata con la normale p53. Hanno anche studiato l’emivita della proteina p53 all’interno delle cellule e hanno scoperto che gli eterozigoti con una copia del mutante p53 avevano un triplice aumento della stabilità della normale proteina p53, rispetto alla stabilità nel solo tipo selvaggio, il che significa che la stabilità della proteina è stata migliorata rispetto al normale. Questi risultati in cellule coltivate hanno esteso e confermato lo studio condotto da Tyner et al. nei topi. Inoltre, questo è stato il primo percorso di risposta alla divisione cellulare scoperto per funzionare tramite p53 e modulare chiaramente sia l’incidenza del cancro che l’invecchiamento.
Nella via Rb, che può segnalare l’uscita dal ciclo di divisione cellulare, eventi come il danno al DNA o la replicazione insufficiente che portano a telomeri corti alle estremità dei cromosomi causano una diminuzione della segnalazione CDK. Questo, inturn, aumenta l’attività della proteina chinasi Rb e di conseguenza aumenta l’attività del fattore di trascrizione E2F. Qual è il significato di E2F? Questo fattore di trascrizione si lega ai promotori delle subunità della RNA polimerasi e di altre proteine necessarie per iniziare la fase S, e aiuta a iniziare la divisione cellulare (Campisi 2003; Weinberg 1995). Così sembra che sia il p53 che i percorsi Rb incidano sugli stessi meccanismi di controllo del ciclo cellulare.
