L’angiotensina II provoca aumenti della pressione sanguigna mediante azioni in vari siti:
- Ghiandole surrenali: l’angiotensina II aumenta il rilascio dell’ormone steroideo aldosterone, che agisce localmente per aumentare la ritenzione di sodio e la secrezione di potassio dal rene. L’effetto netto di questo è la ritenzione idrica, ripristinando così l’equilibrio dei liquidi.
- Reni: L’angiotensina II aumenta anche la ritenzione di sodio attraverso azioni dirette sui tubuli prossimali renali, oltre a influenzare la velocità di filtrazione glomerulare e il flusso sanguigno renale.
- Sistema cardiovascolare: l’angiotensina II è un potente vasocostrittore endogeno, che causa la costrizione delle arterie e delle vene di resistenza, aumentando la pressione sanguigna. Inoltre, sia nei vasi sanguigni che nel cuore, aumenti prolungati dell ‘ angiotensina II favoriscono la crescita cellulare e la conseguente ipertrofia.
- Sistema Nervoso Centrale: Nel cervello, l’angiotensina II agisce sulla ghiandola pituitaria posteriore, stimolando il rilascio dell’ormone antidiuretico (ADH, noto anche come Arginina vasopressina (AVP)). L’ADH aumenta il riassorbimento dell’acqua nei dotti di raccolta renali. L’angiotensina II agisce anche sull’organo subfornico all’interno del cervello per causare un aumento della sete, incoraggiando l’assunzione di acqua.
L’attivazione cronica del sistema RAAS può portare a rimodellamento deleterio e aumento dell’infiammazione nel cuore, nel sistema vascolare e nei reni, nonché ipertensione e malattia renale cronica.
Controllo Neurale del Sistema Cardiovascolare
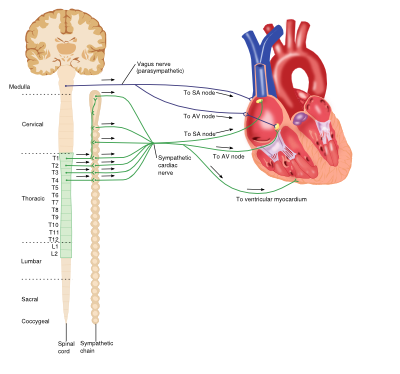
Interazione tra il phon e parasympathic sistema nervoso e il cuore
Simpatico (Adrenergico) Sistema nervoso
Il sistema nervoso adrenergico è un componente essenziale di molti processi in tutto il corpo, compreso il sistema cardiovascolare. Le catecolamine circolanti (ad es. adrenalina e noradrenalina) si legano e attivano i recettori adrenergici sulle membrane cellulari. I recettori adrenergici sono una classe di recettori accoppiati alla proteina G che suscitano una varietà di effetti specifici del tessuto ed esistono in diversi sottotipi.
Vasculature
Il sottotipo recettoriale predominante presente nei vasi sanguigni è il recettore a1-adrenergico, la cui attivazione mediante il legame catecolaminico provoca l’attivazione della via di segnalazione intracellulare della fosfolipasi-C (PLC), dell’inositolo trifosfato (IP3), del diacilglicerolo (DAG). Ciò si traduce in definitiva nella contrazione dei miociti, nella vasocostrizione e nei conseguenti aumenti della pressione arteriosa sistemica.
Cuore
Sebbene il cuore sia miogenico, cioè l’impulso per la contrazione è auto-iniziato, l’uscita del cuore è influenzata dal sistema nervoso centrale. L’effetto netto del sistema simpatico sul cuore è quello di aumentare la gittata cardiaca. I recettori adrenergici presenti nel cuore appartengono alla sottofamiglia dei recettori ß e comprendono i recettori ß1 e ß3. Il legame della catecolamina con i recettori ß1 nel cuore provoca aumenti della gittata cardiaca attraverso una serie di meccanismi: effetti cronotropi positivi, effetti inotropi positivi hanno aumentato l’automaticità e la conduzione sia nei miociti ventricolari che nel nodo atrioventricolare (AV). Tuttavia l’attivazione del recettore ß3 antagonizza queste azioni, producendo un effetto inotropico negativo e fornendo un sistema di controllo integrato all’interno del cuore.
Un aumento prolungato dei livelli di catecolamina nella circolazione (ad es. quando secreto da tumori surrenali o periodi di stress) può portare a problemi cardiovascolari cronici come ipertensione e aritmie.
Sistema nervoso parasimpatico
Il sistema parasimpatico si basa sul legame del neurotrasmettitore acetilcolina (Ach) ai recettori muscarinici e ha vari ruoli in tutto il corpo.
Vasculature
Sebbene i vasi sanguigni esprimano recettori muscarinici, non ricevono innervazione colinergica; tuttavia l’applicazione di Ach esogeno provoca una vasodilatazione rapida e profonda.
Cuore
L’attivazione dei recettori muscarinici (sottotipo M2) nel cuore da Ach rilasciato dal nervo vago provoca una riduzione della gittata cardiaca attraverso effetti opposti alla stimolazione adrenergica: effetti cronotropi negativi e diminuzione della conduzione del nodo AV oltre a diminuire la forza delle contrazioni atriali.
Sistema piastrinico/coagulante
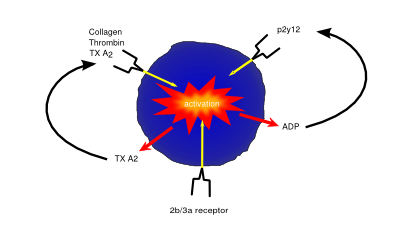
L’attivazione e l’inibizione piastrinica opera attraverso i recettori superficiali sulle piastrine. I cicli di retroazione migliorano l’attivazione piastrinica (ad es. L’ADP rilasciato dalle piastrine aumenta l’attivazione piastrinica, attraverso il recettore ADP)
Le piastrine (note anche come trombociti) sono piccole cellule prive di nuclei responsabili dell’emostasi o della coagulazione del sangue. Vengono rilevati danni o lesioni che portano alla perdita di sangue e all’esposizione di fibre di collagene extracellulare, attivando le piastrine. Una volta attivate, le piastrine diventano adesive, attaccandosi sia alla parete del vaso danneggiata che l’una all’altra, formando un ciuffo di cellule, o “coagulo”, contribuendo a bloccare la perdita del vaso. Quindi iniziano a secernere citochine che incoraggiano l’invasione dei fibroblasti presenti nel tessuto circostante che formano una patch più permanente, creando tessuto sano o depositando la matrice extracellulare per formare una cicatrice.
Ci sono diverse condizioni in cui la coagulazione anormale può essere dannosa per il corpo; la coagulazione in eccesso può portare a blocco vascolare e ischemia o ictus; meno comunemente, una coagulazione carente può portare a una perdita di sangue in eccesso, ad esempio nell’emofilia. Per combattere queste malattie, ci sono farmaci che modulano il processo di coagulazione.
Anticoagulanti
I farmaci che prevengono la coagulazione (anticoagulanti) sono importanti in quelli con un aumentato rischio di danni mediati dalla coagulazione come un ictus o un’ischemia.
Oltre ad essere un analgesico e un antipiretico, l’aspirina è un agente anti-trombotico somministrato a basse dosi a coloro che sono a rischio di danni da coagulazione (ad esempio a seguito di un attacco cardiaco). Le azioni anticoagulanti dell’aspirina derivano dalla soppressione di fattori chiave pro-coagulazione come prostaglanding e trombossani attraverso l’inattivazione irreversibile dell’enzima cicloossigenasi PTGS. Questa soppressione di fattori come il trombossano A2 riduce l’aggregazione piastrinica e quindi impedisce la formazione di coaguli.
Gli inibitori di P2Y12 come clopidogrel esercitano il loro effetto anticoagulante attraverso l’inibizione del sottotipo P2Y12 del recettore ADP piastrinico. Bloccando P2Y12, questi farmaci impediscono l’attivazione delle piastrine e la formazione della rete di fibrina necessaria per la coagulazione.
Farmaci come abciximab e tirofiban prevengono la coagulazione attraverso l’inibizione del recettore della glicoproteina IIb/IIIa impedendo sia l’attivazione che l’aggregazione piastrinica.
Farmacocinetica
Quando si somministrano farmaci a un paziente, è fondamentale conoscere diversi fatti sul farmaco al fine di massimizzare l’efficacia e minimizzare gli effetti collaterali / tossicità. Questi includono informazioni su quale dose è efficace, per quanto tempo il farmaco rimane attivo nel corpo, quanto velocemente viene scomposto/rimosso dal corpo e quanto facilmente il corpo può assorbire/utilizzare quel farmaco. La seguente tabella descrive queste proprietà farmacocinetiche e come vengono calcolate:
| Proprietà | Descrizione | unità Standard (Abbreviazione) | Formula |
|---|---|---|---|
| Dosaggio | Quantità di farmaco attivo dato al paziente | mg (D) | Interazioni Specifiche (studi clinici) |
| Concentrazione | Quantità di droga in un dato volume di plasma | µg/ml (C) | = D / Vd |
| EC50 | La concentrazione di farmaco necessaria per suscitare una risposta a metà strada tra zero e massime risposte. | µg / ml (EC50) | y = bottom + (Top-Bottom)/(1+ Hill Coefficient) |
| Volume di distribuzione | Il volume teorico che il farmaco occuperebbe se distribuito uniformemente nei tessuti per suscitare l’attuale concentrazione plasmatica. | L (Vd) | D/C |
| Costante di eliminazione (Velocità) | La velocità con cui il farmaco viene rimosso dal corpo. | h-1 (Ke) | ln(2)/t1 / 2 o CL/Vd |
| Biodisponibilità | La quantità della dose somministrata è disponibile per l’uso effettivo da parte dell’organismo. | nessuna unità come espressione di una frazione (f) | 100 × (AUC (po)×D (iv))/(AUC (iv)×D (po))
AUC = Area sotto la curva po = somministrazione orale iv = somministrazione endovenosa |
| Cmax o Cmin | massima (Cmax) / minimo (Cmin) plasma la concentrazione di farmaco raggiunto dopo la somministrazione del farmaco | µg/ml (Cmax o Cmin) | Identificato tramite la misura diretta di plasma C |
| tmax | Il tempo necessario per un farmaco per raggiungere la Cmax, a seguito di somministrazione | h (tmax) | Identificato tramite la misura diretta di plasma C il tempo |
| Half-life | Il tempo necessario per un farmaco per raggiungere la metà della sua concentrazione iniziale | h (t1/2) | ln(2) / Ke |
| Liquidazione Droga | Il volume di plasma cancellato del farmaco per un tempo | l/h (CL) | Vd Ke x o D / Area sotto la curva |
Comune Interazioni tra farmaci
e ‘ importante essere a conoscenza delle interazioni che possono verificarsi tra somministrato in concomitanza farmaci, e come essi possono influenzare l’efficacia e/o di tossicità, o produrre collaterali negativi effetto. Tali interazioni potrebbero ad esempio influenzare l’assorbimento del farmaco, la biodisponibilità o l’efficacia del farmaco, o combinarsi per produrre metaboliti indesiderati, oltre ad avere effetti sulle analisi cliniche. Se una combinazione di due farmaci diminuisce l’effetto di uno o entrambi, l’interazione è definita un effetto antagonista; tuttavia se, al contrario, una combinazione di due farmaci aumenta l’effetto di uno o entrambi, l’interazione è definita un effetto sinergico. I farmaci che agiscono sul sistema cardiovascolare sono ad alto contenuto di interattività, che è un problema in quanto i pazienti cardiovascolari normalmente ricevono più di un farmaco. Alcune interazioni farmaco-farmaco comuni relative ai farmaci cardiovascolari sono elencate di seguito:
| Drug | Drugs that drug action | Drugs that ↓ drug action |
|---|---|---|
| Digoxin |
|
|
| Warfarin |
|
|
| Clopidogrel |
|
|
| Furosemide |
|
|
| ACE Inhibitors |
|
|
| ß-blockers |
|
|
| Statine |
|
|
Ci sono diversi meccanismi con cui i farmaci sono ripartito per il corpo, di solito tramite la degradazione da parte degli enzimi. Una famiglia comune di enzimi coinvolti nel metabolismo dei farmaci è la famiglia del citocromo P450 (CYP); un gruppo ampio e diversificato di enzimi che incoraggiano l’ossidazione di una varietà di substrati, sia endogeni (ad es. ormoni steroidei) ed esogeni (es. tossine e farmaci). Gli enzimi CYP rappresentano fino al 75% del metabolismo dei farmaci, aiutando alcuni farmaci a formare i loro composti attivi ma soprattutto disattivando i farmaci in metaboliti inattivi da escreto. Gli enzimi CYP possono influenzare le azioni dei farmaci in diversi modi; possono aumentare il metabolismo dei farmaci (aumentando l’azione attraverso la formazione del sottoprodotto attivo o diminuendo l’azione tramite il metabolismo del farmaco attivo) o la loro azione può essere inibita da farmaci che competono per l’accesso al sito attivo degli enzimi CYP, impedendo la normale interazione tra Molti farmaci esercitano le loro interazioni con altri farmaci viainterferenza con il sistema CYP. Ad esempio, se il farmaco A viene metabolizzato dal CYP e il farmaco B inibisce l’attività del CYP, la co-somministrazione si tradurrà in una diminuzione della biodisponibilità del farmaco A. Nell’uomo ci sono 18 famiglie e 43 sottofamiglie del gruppo di enzimi CYP, che mirano a diversi substrati. Alcuni enzimi CYP importanti nella medicina cardiovascolare, i loro substrati di farmaci cardiovascolari e alcune delle loro interazioni sono mostrati nella tabella seguente:
| Enzima | Substrati (es.) | Inibitori (es.) | Induttori (es.) |
|---|---|---|---|
| CYP2C19 |
|
|
|
| CYP3A4 |
|
|
|
| CYP2C9 |
|
|
|
| CYP2D6 |
|
|
|
Oltre alle interazioni farmaco-farmaco, le azioni di molti farmaci sono influenzate anche da cibo o bevande. Ad esempio, si dovrebbe prestare attenzione con il consumo di alcol con molti tipi di farmaci, in quanto può mettere sotto stress il fegato che sta già lavorando duramente per metabolizzare i farmaci nel corpo. Anche il succo di pompelmo può causare problemi, poiché è noto per inibire il CYP3a. Per ulteriori informazioni sulle interazioni tra farmaci e cibo/bevande, vedere questa guida: Generale l’Uso della Medicina
- McMurray JJ, Adamopoulos S, Anker SD, Auricchio A, Böhm M, Dickstein K, Falk V, Filippatos G, Fonseca C, Gomez Sanchez MA, Jaarsma T, Køber L, Labbro GY, Maggioni AP, Parkhomenko Una, Pieske BM, Popescu, BA, Rønnevik PK, Rutten FH, Schwitter J, Seferovic P, Stepinska J, Trindade PT, Voors AA, Zannad F, Zeiher Un, e ESC Comitato per le Linee guida di Pratica.. Linee guida ESC per la diagnosi e il trattamento dell’insufficienza cardiaca acuta e cronica 2012: La Task Force per la diagnosi e il trattamento dell’insufficienza cardiaca acuta e cronica 2012 della Società europea di Cardiologia. Sviluppato in collaborazione con la Heart Failure Association (HFA) del CES. Eur Cuore J. 2012 Luglio;33(14):1787-847. DOI: 10.1093/eurheartj | ehs104 / PubMed ID:22611136
- Rydén L, Ls E, Bartnik M, Van den Berghe G, Betteridge J, de Boer MJ, Cosentino F, Jönsson B, Laakso M, Malmberg K, Priori, S, Ostergren J, Tuomilehto J, Thrainsdottir io, Vanhorebeek io, Stramba-Badiale M, Lindgren P, Qiao Q, Priori SG, Blanc JJ, Budaj Una, Camm J, Dean V, Deckers J, Dickstein K, Lekakis J, McGregor K, Metra M, Morais, J, Osterspey Una, Tamargo J, Zamorano JL, Deckers JW, Bertrand M, Charbonnel B, Erdmann E, Ferrannini E, Flyvbjerg Una, Gohlke H, Juanatey JR, Graham io, Monteiro PF, Parhofer K, Pyörälä K, Raz io, Schernthaner G, Volpe M, Legno D, Task Force Diabete e malattie cardiovascolari della Società Europea di Cardiologia (ESC)., e Associazione Europea per lo studio del Diabete (EASD).. Linee guida su diabete, pre-diabete e malattie cardiovascolari: sintesi. La Task Force sul diabete e le malattie cardiovascolari della Società Europea di Cardiologia (ESC) e dell’Associazione Europea per lo studio del diabete (EASD). Eur Cuore J. 2007 Gen;28(1): 88-136. DOI: 10.1093/eurheartj | ehl260 / PubMed ID:17220161
- Perk J, De Backer G, Gohlke H, Graham io, Reiner Z, Verschuren M, Albus C, Benlian P, Boysen G, Cifkova R, Deaton C, Ebrahim S, Fisher M, Germano G, Hobbs R, Zappe A, Karadeniz S, Mezzani A, Prescott E, Ryden L, Scherer M, Syvänne M, Scholte op Reimer WJ, Vrints C, Legno D, Zamorano JL, Zannad F, Associazione europea per la Prevenzione Cardiovascolare & Riabilitazione (EACPR)., e Comitato ESC per le linee guida pratiche (CPG).. Linee guida europee sulla prevenzione delle malattie cardiovascolari nella pratica clinica (versione 2012). La Quinta Task force congiunta della Società Europea di Cardiologia e altre società sulla prevenzione delle malattie cardiovascolari nella pratica clinica (costituita da rappresentanti di nove società e da esperti invitati). Eur Cuore J. 2012 Luglio;33(13):1635-701. DOI: 10.1093/eurheartj | ehs092 / PubMed ID: 22555213
- Task Force sulla gestione dell’elevazione del segmento ST infarto miocardico acuto della Società europea di Cardiologia (ESC). Steg PG, James SK, Atar D, Badano LP, Blömstrom-Lundqvist C, Borger MA, Di Mario C, Dickstein K, Ducrocq G, Fernandez Aviles F, Gershlick AH, Giannuzzi P, Halvorsen S, Huber K, Juni P, Kastrati Una, Knuuti J, Lenzen MJ, Mahaffey KW, Valgimigli M, van ‘t Hof, Widimsky P, e Zahger D. ESC Linee guida per la gestione dell’infarto miocardico acuto in pazienti che si presentano con elevazione del tratto ST. Eur Cuore J. 2012 Ottobre;33(20):2569-619. DOI: 10.1093/eurheartj | ehs215 / PubMed ID:22922416
- Blomström-Lundqvist C, Scheinman MM, Aliot EM, Alpert JS, Calkins H, Camm AJ, Campbell WB, Haines DE, Kuck KH, Lerman BB, Miller DD, Schaeffer CW Jr, Stevenson WG, Tomaselli GF, Antman EM, Smith SC Jr, Alpert JS, Faxon, DP, Fuster V, Gibbons RJ, Gregoratos G, Hiratzka LF, Caccia SA, Jacobs AK, Russell RO Jr, Priori SG, Blanc JJ, Budaj Una, Burgos EF, Cowie M, Deckers JW, Garcia MA, Klein WW, Lekakis J, Lindahl B, Mazzotta G, Morais JC, Oto A, Smiseth O, Trappe, HJ, American College of Cardiology., American Heart Association Task Force sulle linee guida di pratica., e Società Europea di Comitato di Cardiologia per linee guida di pratica. Comitato di scrittura per sviluppare linee guida per la gestione di pazienti con aritmie sopraventricolari.. ACC/AHA/ESC linee guida per la gestione dei pazienti con aritmie sopraventricolari–sintesi: un rapporto della American College of Cardiology/American Heart Association Task Force sulle Linee guida per la Pratica e la Società Europea di Cardiologia Comitato per le Linee guida di Pratica (Comitato di redazione di Sviluppare Linee guida per la Gestione dei Pazienti Con Aritmie Sopraventricolari). Circolazione. 2003 Ottobre 14; 108 (15): 1871-909. DOI: 10.1161 / 01.CIR.0000091380.04100.84/PubMed ID:14557344
- Associazione Europea per la Prevenzione Cardiovascolare & Riabilitazione., Reiner Z, Catapano AL, De Backer G, Graham I, Taskinen MR, Wiklund O, Agewall S, Alegria E, Chapman MJ, Durrington P, Erdine S, Halcox J, Hobbs R, Kjekshus J, Filardi PP, Riccardi G, Storey RF, Legno D, e Comitato ESC per le linee guida pratiche (CPG) 2008-2010 e 2010-2012 Comitati.. Linee guida ESC / EAS per la gestione delle dislipidemie: la Task Force per la gestione delle dislipidemie della Società Europea di Cardiologia (ESC) e della European Atherosclerosis Society (EAS). Eur Cuore J. 2011 Luglio;32(14):1769-818. DOI: 10.1093/eurheartj | ehr158 / PubMed ID: 21712404
Tutti gli abstract Medline: PubMed
