incidencia, kezelési stratégiák és hatás
az FN incidenciája akár 50% is lehet a szilárd tumorokban és 80% a hematológiai malignus tumorokban . Globálisan az FN-hez kapcsolódó halálozási arány a rákos betegek körében rendkívül magas, 10-21% . A kemoterápiával-indukált neutropeniával-összefüggő szövődmények a rákos betegeknél, beleértve a gombás fertőzéseket, a súlyos baktériumok okozta szepszist, a tüdőgyulladást és más légúti fertőzéseket,a cerebrovascularis betegségeket, valamint a máj-és veseműködési zavarokat .Globálisan az FN-hez kapcsolódó halálozási arány a rákos betegek körében rendkívül magas, 10-21% között . A halálozás kockázata tovább nő a társbetegségek jelenléte miatt, ami további kockázatot jelent, ezek közé tartoznak a betegspecifikus jellemzők, mint például az életkor, a rosszindulatú daganat típusa, a kezelési rendszer, a teljesítményállapot, az egészségi állapot és a táplálkozási állapot, valamint a fertőző szövődmények (2 .ábra).
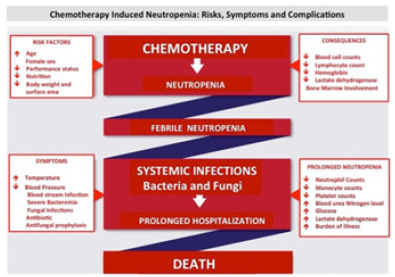
2.ábra: a kezdeti neutropenia vázlatos ábrázolása éskomplikációi.
a jelenlegi kezelés során, ha a CIN a kemoterápia első néhány ciklusában jelentkezik, az jelentős dóziscsökkentést és a következő ciklusok késleltetését eredményezi, veszélyeztetve a kezelés hatékonyságát és a betegségmentes / teljes túlélést a gyógyító szándékkal kezelt betegeknél . A növekvő életkor társula rák nagyobb kockázata. Ezenkívül az életkor csökkenti a csontszűkület tartalékát és veszélyezteti a tüdő -, vese-és májfunkciókat,tovább növelve a kemoterápia által kiváltott szövődmények kockázatát. A neutropenia kialakulásának nagyobb kockázatához hozzájáruló egyéb változók közé tartozik a kezelési rend, a kemoterápiás gyógyszervagy a gyógyszerek kombinációja és a kapcsolódó toxicitás (2 .ábra).
CIN lázzal együtt kell kezelniazonnal, mivel a szervezet már nem képes megvédeni magát az anaktív folyamatos fertőzés ellen, ami szisztémás fertőzést ésszepszist eredményezhet . A betegeket be kell vinni a kórházbaa további értékeléshez és a széles spektrumú antibiotikumokkal történő kezeléshez a láz kialakulását követő néhány órán belül el kell kezdeni. A beteget a kórházban figyelik, amíg a neutrofilek teljesen meg nem számoljákvisszaállítani. Terápiás injekciókat kaphatnak myeloid növekedési faktorok (pl. granulocita kolónia-stimuláló faktor (G-CSF) a neutrofil termelés fokozására . A kórházi kezelés időtartamaa neutropenia időtartamától és mélységétől függően néhány naptól hétig változik . Az FN-betegeket ki lehet engedni a kórházból, ha neutrofilszámuk nagyobb, mint 0, 5×109/föld nem találtak fertőzésre utaló bizonyítékot. Sok betegben, különösen 60 év felettieknél, valamint malignus hematológiai betegségben szenvedő betegeknél a neutrofilek visszanyerése nagyon lassú, ami hosszabb kórházi kezelést és többszörös vértranszfúziót tesz szükségessé .
továbbá lázas neutropeniában szenvedő betegek profilaktikus G–CSF-et kaphatnak a következő és az azt követő kemoterápiás ciklusok során. A profilaktikus G — CSF jelentősen csökkentheti a neutropeniás mélypont mélységét és időtartamát . A hosszú hatású Peg-filgrasztimnak számos előnye van, többek között a beteg számára történő alkalmazás kényelmessége, a jobb megfelelés és a nagyobb hatékonyság . Több randomizált, kontrollált vizsgálat (RCT)igazolta a CSF alkalmazásának biztonságosságát és hatásosságát azoknál a betegeknél, akiket a rák kemoterápiáját követően FN-vel fogadtak be a kórházba. Az antibiotikumok mellett G–CSF-et kapott FN-betegek közelmúltbeli áttekintése azonban nem mutatott szignifikáns hatást az átfogó halandóságra . Bár a neutropeniák időtartama és mélysége a G–CSF-et és az antibiotikumot kapó betegekhez képest csökkent, a G — CSF nem csökkentette jelentősen a fertőzések és a kapcsolódó szövődmények kockázatát a neutropeniás epizód során. A szisztémás fertőzések és a szepszis kockázata a neutropenia súlyosságával és időtartamával arányosan nő . Egy másik vizsgálat kimutatta, hogy bár a myeloid növekedési faktorok, mint például a G–CSF csökkentik a neutropenia időtartamát és mélységét (3.ábra), a fertőzést és a kapcsolódó morbiditást és mortalitást nem csökkentik.
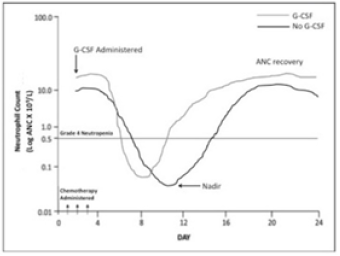
3.ábra: a neutropeniás mélypont időtartama és mélysége a terápiától, a dózistól, a kezelés módjától és a beteg állapotától függ. Az ANC helyreállítása a kezelési rendtől és a beteg állapotától függ. A G-CSF csökkenti a neutrofilnadir időtartamát és intenzitását.
a Multinational Association of Supportive Care of Cancer(Mascc) risk–index pontozási rendszert a CIN magas kockázatával rendelkező rákos betegek azonosítására tervezték . Az eszköz a következőkből áll: 8 tényező, amelyek könnyen értékelhetők az FN-vel való felvételkor.A 21-nél nagyobb pontszámmal rendelkező betegeket alacsony kockázatnak tekintik, ésaz alacsonyabb pontszámmal rendelkező betegeket nagyobb kockázatnak tekintik, és intenzívebb kezelésre van szükségük. A prognózis rossz előrejelzői közé tartozik60-nál nagyobb életkor, mérsékelt tünetek lázas neutropeniával, hipotenzió, kiszáradás, fekvőbeteg állapotés előzetes fungalinfekció . A MASCC kockázati Index képes azonosítani azokat a betegeket, akiknél alacsony a szövődmények kockázata, és fel lehet használni a betegek kiválasztására a költséghatékony terápiák további nyomon követésére és beadására.A MASCC Risk — Index pontozási rendszert az (1.táblázat) mutatja. Ezt az eszközt 2002-ben hagyta jóvá az Amerikai Fertőző Betegségek Társasága, és az Európai Orvosi Onkológiai Társaság is elfogadta . A MASCC kockázati pontozási rendszer rendkívül hasznos, mivel lehetővé teszi az egészségügyi szolgáltatók számára, hogy meghatározzák a beteg kockázatát a CIN és a fertőzések okozta orvosi szövődmények kialakulására.A beteg kezelési tervét a kockázatuk alapján lehet meghatároznikategória. Fontos tudni, hogy a beteg várhatóan megverte-e az FN kialakulásának magas kockázatát, vagy kórtörténetében szerepel-E FN, annak érdekében, hogy megtegyemmegfelelő megelőző intézkedések . A CIN részletes kezelési tervét és klinikai kezelését az alábbiakban ismertetjük .
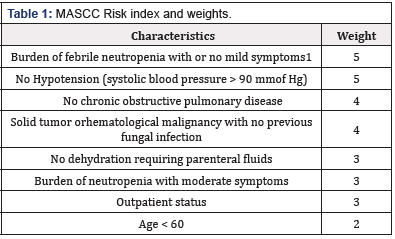
1.táblázat: MASCC kockázati index és súlyok.
a lázas neutropenia terhe általános klinikai állapotra utala neutropeniás epizód hatása alatt. Pontszám nincs ormild tünet –5, mérsékelt tünet –3, súlyos tünet — 0, haldokló — 0.
a maximális lehetséges pontszám 26. A > 21 pontszámot alacsony kockázatnak tekintik, és
Az Európai Rákkutatási és kezelési szervezet (EORTC) javasolja a G–CSF rutinszerű profilaktikus alkalmazását azoknál, akik 20% – nál nagyobb FN kockázati pontszámmal rendelkeznek a hatékony kemoterápiás dózisintenzitás fenntartása érdekében (4.ábra). Azoknál a betegeknél, akiknek a kockázati pontszáma 10-20% egyéni értékelést kell végezni a G–CSF beadásának eldöntéséhez. Ez a köztes kategória a daganatos betegek 52,5% – át képviseli, és a kezelésben jelentős eltérések vannak . Sok ebbe a kategóriába tartozó beteg gyakrantapasztalja az FN-t a kemoterápia első ciklusa alatt. Ezután magas kockázatúnak minősülnek,és a következő ciklusokban G–CSF-et kapnak. Ezért további kutatásokra van szükség a köztes rendszerekben az Fn kockázatának kitett betegek azonosításához. Az EORTC nem javasolja a G–CSF alkalmazását, ha a kockázat 10% – nál kisebb (5.ábra). Azoknál a betegeknél azonban, akiknél a dózis intenzív kemoterápiás rendszer vélhetően előnyös profilaktikus G-CSF-et tartanak szükségesnek a túlélési előny elérése érdekében. G — CSF is tanácsos, ha az adag intenzív kemoterápiát elengedhetetlennek tartják a hatékony rákkezeléshez . A cinea időben történő felismerése és diagnosztizálása ezért lehetővé tenné az időben történő és megfelelő G–CSF profilaxis alkalmazását is.
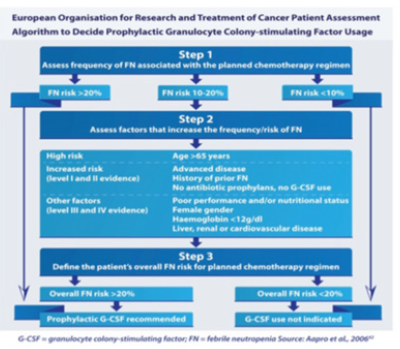
4. ábra: Kockázati modellek és a neutropenia (EORTC) kezelése.
az FN-hez társuló mortalitás és társbetegségek azonnali kórházi kezelést és antimikrobiális szerekkel történő kezelést igényelnek . Egy nemrégiben készült tanulmány, amely az Ír egészségügyi rendszeren belül értékelte az FN kórházi ellátásának erőforrás-felhasználását és költségeit, megállapította, hogy az FN-epizódonkénti átlagos költség 6915 718 volt . A Centers for Disease Control and Prevention által végzett tanulmány megállapította, hogy 2012-ben 108 419 (91 560 felnőtt és 16 859 gyermek) rákos beteg került kórházba a CIN-vel, összesen 2,7 milliárd dollár költséggel . A felnőttek és a gyermekek átlagos tartózkodási ideje 9,6, illetve 8,5 nap volt, a kórházi tartózkodás átlagos költsége 24 770, illetve 26 000 dollár volt . Ezenkívül az FN gyakran rontja a kemoterápiás kezelést azáltal, hogy a kezelési ciklusok dóziscsökkentését és/vagy késleltetését igényli, ezáltal befolyásolja a kezelés eredményét . Ezért a CIN kezelése továbbra is kielégítetlen klinikai igény a rákos kemoterápia.
a National Confidential Enquiry intoPatient Outcome and Death (NSPOD) által 2008-ban végzett felmérés, melynek címe: “SystemicAnti Cancer Therapy: jóban vagy Rosszban?”a kemoterápiát követő 30 napon belül elhunyt betegek gondozásának áttekintése számos súlyos hiányosságot azonosított a CIN kezelésében a meglévő gyakorlatban . Súlyos hiányosságokat állapítottak meg az oktatásban és az FN kockázatainak tudatosításában mind a beteg, mind az egészségügyi szakember esetében. A betegek értékelésére, kezelésére és kórházi felvételére vonatkozó egyértelmű protokollok szintén nem álltak rendelkezésre, vagy nem hajtották végre megfelelően. Az NCEPOD azt ajánlotta, hogy a lázcsillapítás diagnosztizálására és kezelésére szolgáló hatékony stratégiáknak minden rákápolási szolgáltatás alapvető összetevőjének kell lenniük. Egy, a rákkal összefüggő elhullásokkal összefüggő várható gazdasági terhekről és termelékenységvesztésről szóló friss jelentés becslése szerint 233 000-re becsülik az Írországban 2011 és 2030 között bekövetkezett valamennyi invazív rák okozta halálesetet . Ez a termelékenység 73 milliárd dollárra becsült csökkenését eredményezi . Ezek a veszteségek Írország GDP-jének mintegy 1,4% – át teszik ki évente. A halálozás évi 1% – os csökkenése az összes invazív rák miatti termelékenységi veszteséget 8,5 milliárddal csökkenti 20 év alatt . Bár a cikk nem tárgyalta konkrétan a terhek által rótt Cinazonban a CIN miatt bekövetkező, körülbelül 20% – os rákhoz kapcsolódó halálesetek lehetséges hatása nyilvánvaló. Egy nemrégiben készült tanulmány értékelte ésbecsülte az FN-vel való kórházi ápolás költségeit és terheit a saját egészségügyi rendszerükön belül, és megállapította, hogy az FN-epizódonkénti átlagos költség 8915 718 volt . Ez a nagy költség volt a kórházban stayat €6851 ± 549, valamint a további költségek közé tartoznak az antibiotikumok €760 ± 156laboratory vizsgálatok €538 ± 47, valamint a vérátömlesztés €525 ± 189 .A vizsgálat nem tartalmazta a betegeknek adott G — CSF költségét. A tartózkodás időtartama 7,3 0,5 nap volt. A dublini Egyetemi Oktató Kórházban 42 FN-hez kapcsolódó kórházi felvétel történt ebben a tanulmányban egy év alatt (2008 .augusztus – 2009. július). Ez egyértelműen felvázolja az Fn előfordulását és hatását, valamint az egészségügyi rendszerre nehezedő jelentős terhet. Ezért azonnali és sürgős klinikai szükség van a neutropenia gyors felismerésére és a szepszis megelőzésére a beteg túlélésének és a rákkezelés kimenetelének javítása érdekében.
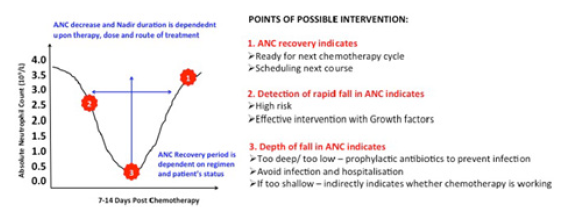
5.ábra: az abszolút neutrofilszám (ANC) monitorozása, amely a CIN időben történő diagnosztizálásához és jobb kezeléséhez vezet. Az 1,2,3 jelzi a lehetséges beavatkozási pontokat, ahol az ANC monitorozása előnyt jelenthet a betegek kezelésében. Az ANC monitorozása a CIN időben történő felismeréséhez és megelőzéséhez vezet, elkerülve a kórházi kezelést és a kezelést. Az ANC monitorozása segíthet azon betegek azonosításában is, akik részesülhetnek a G-CSF kezelésében. Az ANC segíthet a következő kemoterápia adagjának és idejének meghatározásában is.
