a kémiai ionizáció (Ci) egy lágy ionizációs technika, amely a molekuláris és ionreakciók kutatási eredményeinek közvetlen alkalmazása az analitikai kémiában. A legkorábbi ionizációs technika az elektronbombázás ionizációja (Ei) volt. Az EI által nyert terméknek sok töredéke van, amelyet nehéz elemezni. A CI, amely nagyon kevés töredéket termelt, az 1950-es években kezdődött, és nagy potenciállal rendelkezik az analitikai kémia területén.
A CI folyamatban az elektronok először bombázzák a reagensgázt reagensionok előállításához. A mintamolekulákat ezután reagensionok ionizálják molekuláris és ionreakció útján. Az 1970-es éveket mérföldkőnek tekintették a CI fejlesztésében. Abban az időben a kutatók megoldották a CI munkájának hiányosságait vákuum környezetben, lehetővé téve a CI számára, hogy légköri körülmények között dolgozzon. A légköri kémiai ionizáció a koronakisülésből származó energiát szolgáltat, és nem igényel vákuumos környezetet, ami nagymértékben növeli a CI alkalmazások körét. Jelenleg a CI-t széles körben használják a tömegspektrometriás technikában.
a kémiai ionizáció elve
A CI elve az X + reagension használata az a analitmolekulával való reakcióhoz az analit ionizációjának elérése érdekében:
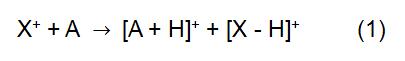
a fenti reakcióban az X+ az ionizált reakciógázból származik. Néhány gyakori reagens gáz a metán, az ammónia, a víz és az izobután. A reakcióidő és a sebességi állandó (k) a képletben irodalommal vagy méréssel nyerhető. Ha az X + reagension H3O+, a (2) képlet az:
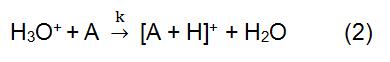
a Reagensiont ionforrás állítja elő. Az általánosan használt ionforrások elsősorban a sugárforrást, az üreges katód kisülési áramforrást és a szokásos izzító kisülési áramforrást tartalmazzák. A 210po és a 241Am a leggyakoribb sugárforrások. Az ionizációs folyamat a 210po és 241Am által kibocsátott alfa részecskékkel kezdődik. Nagy energiával rendelkezik, és ütközhet a reagensgázzal reagensionok és elektronok előállításához. Ha a keletkező elektronok elég magasak, ütközhetnek a reagensgázzal, hogy új reagensionokat és elektronikát képezzenek. A H3O + reagensionként alkalmazott CI-ben általában üreges katód kisülési áramforrást használnak, amely 99,5% H3O+ – ot képes előállítani.
a kémiai ionizáció feltételei szerint a CI alacsony nyomású kémiai ionizációba van besorolva (
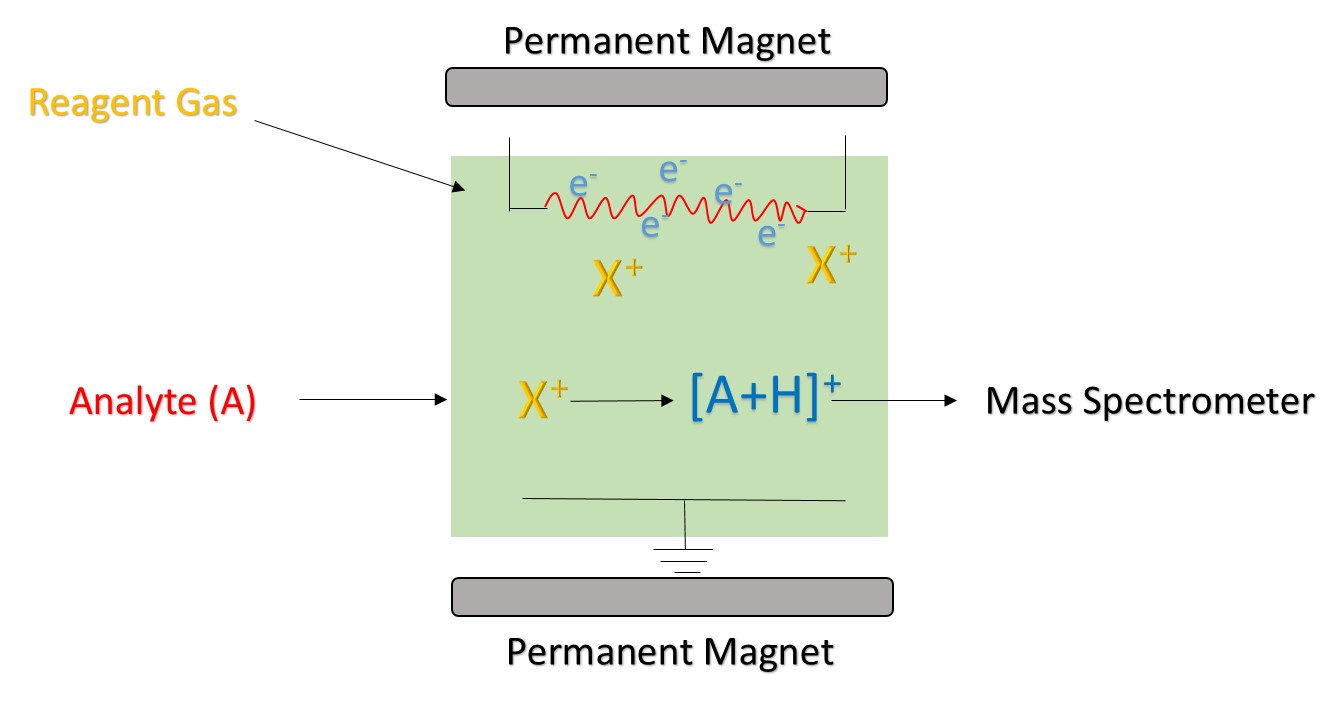 1.ábra. A kémiai ionizáció elve
1.ábra. A kémiai ionizáció elve
A CI előnyei és hátrányai
A CI spektrum felbontása egyszerű, és az analit pontos molekulatömege elérhető. A CI-vel nyert termék kevés fragmenst tartalmaz, termékei elsősorban az analit molekulái és ionjai. A CI szelektivitása megfelelő reagension kiválasztásával könnyen növelhető. Például a reagension H3O+ csak olyan szerves anyaggal reagál, amelynek proton affinitása nagyobb, mint H3O+. Ezenkívül a CI nagy érzékenységgel és gyors válaszadással rendelkezik (15S). Ha azonban a reaktív ionok tisztátalanok, és egyidejűleg különféle kémiai ionizációs reakciók lépnek fel, a tömegspektrometria nehézzé válik.
példák a CI alkalmazásokra
jelenleg a CI-t széles körben használják ionforrásként tömegspektrometriás rendszerekben különböző nyomanyagok kimutatására. A CI felhasználható olyan anyagok kimutatására, mint a légkörben lévő nyomgázok, a zöldségekben és gyümölcsökben található növényvédőszer-maradványok, a tejporban lévő Melamin, a lágyítók és a gyomirtó szerek a talajban. Ezenkívül a CI felhasználható anyagazonosításra is, például a tea minőségének azonosítására.
- illékony szerves vegyületek (VOC) mérése
a VOC CI általi mérésében a H3O+ – t általában reagensionként használják. H3O + nem reagál a levegőben lévő legtöbb anyaggal, például O2, N2, CO2STB. Másrészt a protontranszfer-reakciók többsége nem disszociált, tehát a termékionok egyedülállóak, ami egyszerűvé teszi az eredmények elemzését. A VOC H3O+ reagension alkalmazásával történő mérésének elvét a (3) egyenlet mutatja. A végterméket protontranszfer reakció tömegspektrometriával oldottuk meg.
- a melamin meghatározása tejporban
a melamin CI-vel történő mérésekor az N2-t reagensgázként használják. Nagyfeszültség hatására az N2 és a H2O komplex fizikai-kémiai reakciókon megy keresztül, hogy reagensionokat hozzon létre H3O+. A reakció folyamatát a (3-6) képlet mutatja. A H3O + reakcióba lép a tejporban lévő melaminnal, és a reakció elvét a (2) képlet mutatja.
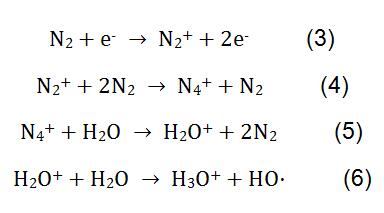
- a tea minőségének azonosítása
a tealevelek felületén lévő kémiai anyagok CI-vel történő mérésével különböző teafajták azonosíthatók. A H3O+ a tea felületével butanollal, geraniollal, koffeinnel és más anyagokkal reagál, és a reakciótermékek különböző tömegspektrumokat alkotnak a tömegspektrométeren. Ugyanazon anyag tartalma különböző teafajtákban eltérő, tehát a CI detektálással létrehozott tömegspektrum eltérő. A tömegspektrum bizonyos mértékben tükrözheti a tea kémiai ujjlenyomat-jellemzőit. Ezért a CI fontos gyakorlati alkalmazási értékkel rendelkezik a tea gyors azonosításához és minőségelemzéséhez.
a kémiai ionizációt széles körben használják a tömegspektrometriában erős szelektivitása és nagy érzékenysége miatt. A kémiai ionizációs tömegspektrometria (CIMS) nemcsak a komplex mintákban lévő anyagok tandem tömegspektrometriás azonosítását teszi lehetővé, hanem kémiai ujjlenyomatadatokat is szerez a mintákhoz a kemometriai elemzéshez. A CIMS alkalmazása pozitív hatással van az élelmiszer, az orvostudomány, a környezetvédelem, a mezőgazdaság és más iparágak fejlődésének előmozdítására.
röviden bemutattuk a CI-t, az ionizációs módszer egyik típusát, amely segíthet többet megérteni a tömegspektrometriáról. A Creative Proteomicsnál kifejlesztettük a professzionális tömegspektrometriai platformot, amely a legkorszerűbb eszközöket tartalmazza. Tömegspektrometria alkalmazásával a kreatív proteomika különböző szolgáltatásokat nyújthat a különféle követelmények teljesítéséhez, beleértve:
- proteomikai szolgálat
- Metabolomikai szolgálat
- Glikomikai szolgálat
- Fales H M; et al. Egyes biológiailag fontos vegyületek tömegspektrumainak összehasonlítása különböző ionizációs technikákkal. Analitikai Kémia, 1975, 47(2):207-219.
- Lindinger W; et al. Illékony szerves vegyületek on-line monitorozása pptv szinten proton-transzfer-reakció tömegspektrometriával (PTR-MS) orvosi alkalmazások, élelmiszer-ellenőrzés és környezeti kutatás segítségével. Nemzetközi Tömegspektrometriai folyóirat & ion folyamatok, 1998, 173(3):191-241.
- Chen H; et al. Felszíni deszorpció légköri nyomás kémiai ionizációs tömegspektrometria közvetlen környezeti minta elemzéséhez mérgező kémiai szennyeződés nélkül. Journal of Mass Spectrometry, 2010, 42(8):1045-1056.
- Yang s; et al. Melamin kimutatása tejtermékekben felületi Deszorpcióval légköri nyomás kémiai ionizációs tömegspektrometria. Analitikai Kémia, 2009, 81(7):2426.
