Bevezetés
a sejtek vagy szövetek megújulása és regenerációja a felnőtt szervezetek két fő fejlődési követelménye. Mindkét folyamat kiindulópontja az őssejtek populációja, amely általában egy “niche” nevű speciális környezetben helyezkedik el , amely biztosítja számukra a szükséges jeleket az őstulajdonságok fenntartásához, vagy a szükséges különböző sejttípusok megkülönböztetéséhez (1.ábra). Az őssejtek proliferációját és differenciálódását össze kell hangolni a pótolni kívánt sejtek halálával. Ezen kívül folyamatokmint például a sejtmigráció, az epigenetika és a sejtkommunikáció, szintén szükségesek a sejtek megfelelő megújulásához . Gyors megújulása szöveteket magasabb mitotikus aktivitással lehet felismerni. Ezzel szemben a lassú megújulású szövetek kevesebb mitózist tartalmaznak, és nem biztos, hogy könnyen felismerhetők a nem megújuló területekről, amelyek szintén jelenhetnek meg . Az őssejtek sorsa a proliferáció soránközvetlenül befolyásolja a szövetek megújulását és a homeosztázist. Ezért kritikus fontosságú megérteni azokat a szabályozási mechanizmusokat, amelyek fenntartják a balancedcell felosztást és differenciálást. Az extracelluláris jelek (pl. szöveti mikrokörnyezet, intracelluláris ROS és citokinek), valamint intracelluláris faktorok (pl. epigenetikus gépek, transzkripciós faktorok és DNS károsodásra adott válasz) felelősek az őssejtosztódás szabályozásáért.
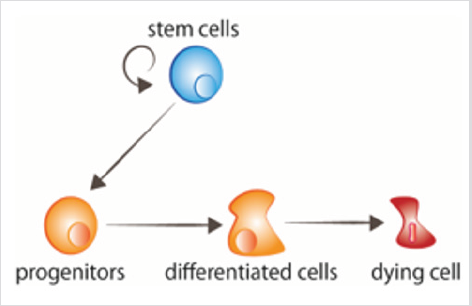
1.ábra: a sejtforgalom az őssejtek szaporodnak, emelkedést adva a progenitoroknak, amelyek ezt követően megkapják a jeleket a differenciálódáshoz. Az idős sejtek jeleket kapnak, hogy meghaljanak.
Az őssejtek három lehetséges osztódási lehetőséget mutatnak: aszimmetrikus osztódás, amelyben egy őssejt és egy elkötelezett leánysejt származik; szimmetrikus elkötelezettség, amely két elkötelezett leánysejtet eredményez; és szimmetrikus osztódás,amely két leánysejtet eredményez, amelyek fenntartják az őssejt tulajdonságait 2.ábra. Bár megjósolható, hogy az aszimmetrikusosztódás az egyetlen mechanizmus, amely lehetővé teszi az őssejtek stabil populációjának fenntartását, a lineagetracingkísérletekből származó jelenlegi adatok azt mutatták, hogy a legtöbb szövetben az őssejtek proliferációja és a differenciált utódok kialakulása közötti egyensúly a teljes őssejtpopuláció szintjén érhető el.Az őssejtek elvesztése a differenciálódás vagy a sejtkárosodás miatt indukáljaszimmetrikus osztódás, hogy kitöltse ezt a rést . Az őssejt-osztódás után a differenciálódási folyamatot követő sejtek különböző szakaszokon mennek keresztül, amelyeket transzkripciós faktorok kombinációja határoz meg, amelyek szabályozzák a megfelelő gén repertoár aktivitását, éslehetővé teszik elkötelezettségüket és terminális differenciálódásukat. Minden egyes sejtvonal esetében a döntési sorrend végterméke egy specifikusdifferenciált sejttípus 3a. ábra. a legtöbb esetben a sejtazonosság – a normál differenciálódás terméke-stabila szövetekben, és fenntartása döntő fontosságú a normál szövetbenfunkció. Ezt a stabilitást epigenetikai szabályozással-például hiszton demetilezéssel és acetilezéssel – érik el, ami a szövetspecifikus génexpresszió örökölhető mintáit eredményezi .
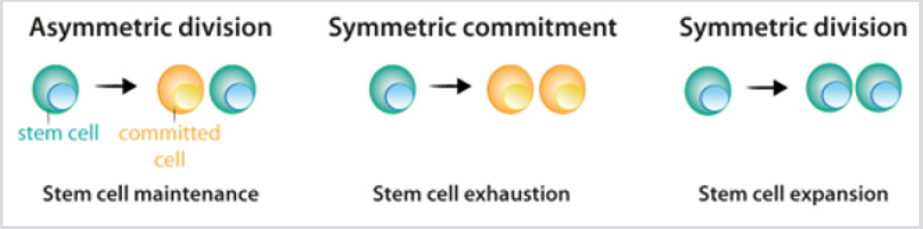
2.ábra: Az őssejtek osztódási mintája.
a) az aszimmetrikus osztódás során az őssejtek egy őssejtet hoznak létre, amely fenntartja az őssejtpopulációt, és egy sejtet, amely elkötelezett a differenciálódás iránt.
b) a szimmetrikus elkötelezettség során az őssejt-osztódás két leánysejtet eredményez, amelyek elköteleződtek a differenciálódás mellett.
c) a szimmetrikus osztódás során az őssejt-osztódás két őssejtet eredményez. Amint azt a szövegben kifejtettük, a jelenlegi kísérletiaz adatok azt jelzik, hogy a három osztódási mód az őssejtpopuláció fenntartása mellett fordulhat elő.
a sejtazonosság elvesztése azonban előfordulhat. Valójában a Drosophila imaginal disc sejtjei képesek transzdeterminálni és új felnőtt sorsot szerezni a transzplantáció után . Ebben a helyzetben úgy tűnik,hogy az extracelluláris jelek újraprogramoznak néhány prekurzort vagydifferenciált sejtet, hogy megszerezzék vagy egy ősállapot, vagy egy új differenciált állapot jellemzőit. Két mechanizmus létezik, amellyel egy sejt megváltoztathatja identitását: dedifferenciálás éstranszdifferenciálás. A dedifferenciálás a folyamatra utalamelyet egy differenciált vagy elkötelezett sejt megszerez jellemzőkkevésbé érett sejt 3b ábra. A dedifferenciálódás legdrámaibb példája a véglegesen differenciált sejtek in vitro átalakulása pluripotens sejtekké (indukált pluripotentstem sejtek, iPSC-k), korlátozott számú transzkripciós tényező túlzott expressziójával . A transzdifferenciálás ezzel szemben előfordulamikor egy differenciált sejt megváltoztatja transzkripciós program éskonvertálódik egy másik differenciált sejttípusba. A folyamat a differenciálódás közbenső lépésén keresztül történhet az aless érett szakasz felé, mielőtt az új differenciált cellává alakulna, vagy közvetlenül, a 3C-d. a fibroblasztok myoblasztokká történő közvetlen átalakulása a myod ektopikus expressziójával példa a második folyamatra .
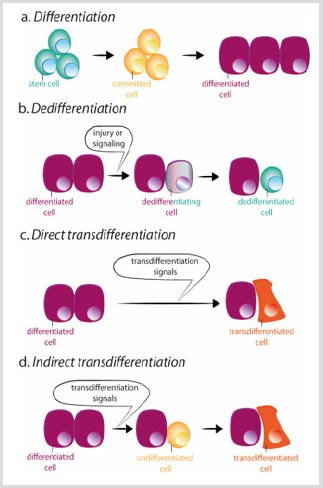
3.ábra: differenciálási, dedifferenciálási és transzdifferenciálási rendszerek.
a) a normál differenciálódás során az őssejtek elkötelezett sejteket eredményeznek, amelyek viszont különböző sejttípusokban differenciálódnak.
b) a Dedifferenciálás az őssejt tulajdonságainak differenciált sejt általi megszerzéséből áll. Transz differenciálás fordulhat előközvetlen vagy közvetett módon.
c) a közvetlen transzdifferenciálás során egy differenciált sejt megszerzi egy másik sejttípus transzkripciós programját, általábanszoros kapcsolatban áll, mint például az exokrin az endokrin hasnyálmirigy sejtekhez, más differenciált sejtté válva.
d) a közvetett transzdifferenciálás során egy differenciált sejt dedifferenciálódik, mielőtt elfogadja a másik sejttípus új transzkripciós programját.
Dedifferenciálódás és transzdifferenciálódás is előfordul természetes módon egy sérülés vagy szövetvesztés hatására .A differenciálódás például természetesen a limbregeneráció során fordul elő az urodele kétéltűekben. A végtag amputációja után a seb melletti sejtek dedifferenciálódnak,így blasztémát képeznek, amely differenciálatlan sejtekből áll, amelyek szaporodnak, és végül ugyanabba a sejttípusba redifferenciálódnak, hogy létrehozzák az elveszett végtag összes összetevőjét. A természetes transzdifferenciálás közvetett módon történik:először a sejt dedifferenciálódik; majd aktiválódik a természetes fejlesztési program, lehetővé téve a sejt számára, hogy új vonalra differenciálódjon. Tsonis és munkatársai a transzdifferenciálás természetes mechanizmusát írták le egy Gőte. Azt találták, hogy amikor a lencséket eltávolítják, a pigmentált hámsejtek a hátsó íriszből átalakulnak, és regenerálják a hiányzó szövetet. Ennek elérése érdekében a pigmentált hámsejteknek először dedifferenciálódniuk kell ésproliferálniuk kell, hogy új lencsesejteket hozzanak létre, majd differenciálódjanak aa lencse éretlen sejtjei . Mindkét helyzetben-dedifferenciálásés redifferenciálódás ugyanabba a sejttípusba vagy transzdifferenciálásegy új sejttípusba – a jelátviteli utak komplex hálózata vezérelheti az egyes cellák által a tökéletes időpontban megszerzett transzkripciós programot.
hus, a génexpresszió térbeli időbeli szabályozása folyamatosan szükséges az állati homeosztázis, valamint az aregeneratív folyamat során. A regeneráció során azonban a sejteknek újra hozzá kell igazodniuk az új helyzethez, amely megköveteli, hogy a sejtek szintjén alaposabb döntéseket hozzanak, gyakran beleértve a differenciálódás és a transzdifferenciálódás folyamatait is, amelyek a homeosztázis alatt szűkösek.
- Cleversh, Loh KM, Nusse R (2014) őssejt jelzés. Egy integrális program a szövetek megújulásához és regenerációjához Wnt jelátvitel és stemcell kontroll. Tudomány 346 (6205): 1-9.
- Leblond C P, Walker B(1956) a sejtpopuláció megújulása 36(2): 255-276.
- Roostaee A, Benoit YD, Boudjadi S, Beaulieu JF (2016) epigenetika inintestinalis hámsejtek megújulása. J Sejt Fiziol 231 (11): 2361-2367.
- Ito K, Ito K (2016) metabolizmus és a sejtek sorsának döntései és a sejtek megújulása. Annu Rev Cell Dev Biol 32: 399-409.
- Simons BD, Clevers H (2011) stratégiák homeosztatikus őssejt selfrenewalin felnőtt szövetek. Cella 145 (6): 851-862. yang Y, Akinci e, Dutton JR, Banga a, Slack JM W, et al. (2013) az egér embrió májsejtjeinek specifikus átprogramozása béta-sejtszerűfenotípussá. Mech Dev 130(11-12): 602-612.
- Merrell AJ, Stanger BZ (2016) felnőtt sejtek plaszticitása in vivo: dedifferenciálásés a transzdifferenciálódás visszatért a stílusba. Nat Rev MolCell Biol 17(7): 413-425.
- Worley MI, Setiawan L, Hariharan IK (2012) regeneráció éstranszdetermináció a Drosophila imaginal lemezekben. Év Rev Genet 46:289-310.
- Raff M (2003) felnőtt őssejt plaszticitás: tény vagy műtárgy? Annu Rev CellDev Biol 19: 1-22.
- Takahashi K, Yamanaka S (2006) pluripotens őssejtek indukciója egér embrionális és felnőtt fibroblaszt tenyészetekből meghatározott tényezők által. Cella 126(4): 663-676.
- Tapscotr SJ, Davis RL, Thayer MJ, Cheng PF, Weintraub H, et al. (1988) MyoDi: egy nukleáris foszfoprotein, amely egy Myc Homológiai régiót idéz elő a fibroblasztok myoblastokká alakításához. Tudomány 242 (4877): 405-411.
- Jopling C, Boue S, Izpisua Belmonte JC (2011) Dedifferenciálás,transzdifferenciálás és újraprogramozás: három út a regenerációhoz.Nat Rev Mol Sejt Biol 12(2): 79-89.
- Tsonis PA, Madhavan M, Tancous EE, Del Rio-Tsonis K (2004) Del Rio-Tsonis, K. egy Gőte szeme a lencse regenerációjáról. Int J Dev Biol 48 (8-9): 975-980.
