sürgős üzenet: amikor egy viszonylag fiatal beteg mellkasi fájdalommal jelentkezik sürgősségi ellátásra, lehet, hogy “tipikus” oka van. A kockázati tényezők gyors értékelése és pontos értékelése elengedhetetlen a hatékony ellátáshoz és gyakran a beteg túléléséhez.
Max Palatnik, MD
eset bemutatása
egy 35 éves férfi bemutatott 21:59-kor a fő panasz a mellkasi fájdalom; 22:03-kor, megjegyeztük, a következő:
Temp: 98.9
pulzus: 103
ill: 16
Syst: 122
Diast: 69
O2Sat: 99%
a történelem jelenlegi betegség (22:47) (szó szerint)
Pt. 38 éves férfi PMH myocarditis és pericarditis 1983-ban és 1991-ben, aki 6:30-kor vacsorázott, és 7:30-kor TV-nézés közben kezdte érezni a nyomást az elülső mellkasán. – olyan érzés volt, mintha “néhányan a mellkasomon ültek”. Kapcsolódó zokogás és sugárzás a vállát és a bal kezét”bizsergés”. Gyomorégése volt, de ez másképp érezte magát. Szódabikarbónát vett be (amit általában gyomorégése miatt szed), és ez nem segített. Nincs ájulás, hányinger, hányás, láz, RUQ fájdalom vagy az anamnézisben szereplő ételintolerancia. Volt néhány vírusos tünete 2 héttel ezelőtt (nem produktív köhögés, sinus HA és PND, amelyek mind megoldódtak.) Nem orthopnea, PND, kapcsolatban a fájdalom a testmozgás, mellkasi trauma, pleuritic komponens
korábbi kórtörténet/Triage
gyógyszert, gyakori allergia: nincs
PMH: szívizomgyulladás/Pericarditis
PSH: nincs
SocHx: nem dohányzó
FamHx: pozitív CAD 52 éves testvér MI, apa CABG 53
vizsga (22:52)
Általános: jól megjelenő; jól táplált; nincs látható szorongás.
Fej: Normocephalic; atraumatikus.
Szemek: PERLA; EOM ép
ENT:TM normális; normál orr; nincs orrfolyás; a torok vörös, enyhe váladék.. Nedves nyálkahártya.
nyak: rugalmas; nontender; nincs nyaki lymphadenopathia. Nincs meningealis jelek
kardiovaszkuláris: normál S1, S2; nincs morajlás, dörzsölés vagy vágta. Nincs reprodukálható mellkasi fájdalom
légzés: normál mellkasi kirándulás légzéssel; a légzés tiszta és egyenlő kétoldalúan; nincs sípolás, rhonchi vagy rales.
has: normál bélhangok; nem kitágult; nontender; nincs tapintható organomegalia.
végtagok: normál ROM mind a négy végtagban; nem tapintható; a disztális impulzusok normálisak és egyenlőek.
bőr: Normál életkor és a faj; meleg; száraz; jó turgor; nincs látható elváltozások vagy váladék
haladás Megjegyzések (23: 12)
kapott 2 baba aszpirin és SL NTG enyhítésére mellkasi diszkomfort. Ezután volt 1 hüvelyk Nitropaste elhelyezett. 00:44-kor visszatért a fájdalma, és megismételték az EKG-jét. 15mg Maalox-ot kapott javulás nélkül, majd több NTP-t, amely enyhítette a kellemetlenséget.
eredmények
EKG 1: lapított T hullámok gyengébb és V2-V6.EKG 2: nincs változás Labs
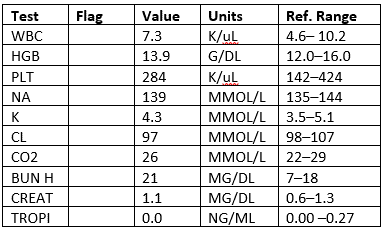
CXR: negatív
diagnózis (01:57)
mellkasi fájdalom, kórtörténet szívizomgyulladás
diszpozíció (02: 02)
a beteget telemetria alapján engedték be a kórházba.
kórházi tanfolyam
Pt. soros enzimeken esett át, majd reggel megismételte az EKG-t. Kizárta az MI – t, és elengedték. Az ezt követő stressz-visszhang 12,5 perces edzés után negatív volt, mellkasi diszkomfort vagy EKG-változás nélkül.
második látogatás
- a beteg követte a PCP-jét, GERD-t diagnosztizáltak, és PPI-vel kezdték.
- a beteg 6 héttel később mellkasi szorítással és nehézlégzéssel tért vissza az ED-be étkezés közben. Tünetei súlyosbodtak az erőkifejtés következtében, nyugalmi állapotban jelentkeztek, és javultak függőleges helyzetben, valamint Prilosec-kel.
- nincs kapcsolódó láz, köhögés, sugárzás, verejtékezés, borjúfájdalom, perifériás ödéma.
- a betegnek normális létfontosságú jelei vannak, figyelemre méltó, megfelelő vizsgálattal.
- az EKG feltárja a TWI-t az aVL-ben, valamint az új q-hullámokat a V1-V2 és az NSST változásokban.
- CXR negatív.
- a laborok olyan troponint mutatnak, amely> a normál felső határ 20-szorosa.
- a beteg aszpirint, heparint, Plavixot, nitroglicerint kap, és akut koszorúér-szindrómát kap.
- a beteg perkután koronária beavatkozáson (PCI) megy keresztül sikeres stent elhelyezéssel, majd ezt követően jó állapotban ürítik.
beszélgetés
a mellkasi fájdalom a betegek több mint 5% – ának panasza sürgősségi osztályok (EDs) az Egyesült Államokban. A mellkasi fájdalomban szenvedő beteg értékelése óriási kihívás, nagyrészt a széles differenciáldiagnózis miatt, de a téves diagnózissal járó kockázat miatt is. A sürgősségi orvoslás leggyorsabban halálos állapotai között-amelyek közül sok kezdetben sürgős ellátásra kerülhet-az akut koszorúér-szindróma (miokardiális ischaemia és infarktus), aorta disszekció, tüdőembólia, szívburokgyulladás szívtamponáddal, szívizomgyulladás, feszültség pneumothoraxés nyelőcső szakadás. Mindezek a feltételek általában mellkasi fájdalommal jelentkeznek, és mindegyiket figyelembe kell venni a mellkasi fájdalomban szenvedő beteg értékelésének korai szakaszában.
az orvos felelőssége, hogy értékelje ezeket a betegeket a differenciáldiagnózis tetején található lehetséges életveszélyek listájával. A részletes kórtörténet, a fizikális vizsgálat (a szív -, tüdő-és érrendszeri vizsgálatokra összpontosítva) és az alapvető vizsgálati információk (pl. elektrokardiogram, mellkasröntgen) gyakran ésszerű pontossággal gyorsan kizárhatják ezeket az életveszélyeket. Azokban az esetekben azonban, amikor ez a kezdeti gyors értékelés nem zárja ki az egyik halálos diagnózist, további munka magasabb élességű környezetben indokolt lehet.
bár az ACS tipikus tüneteit a mellkasi fájdalom vagy nyomás fokozatos kialakulásaként írják le, a bal kar, a nyak vagy az állkapocs sugárzásával, valójában az atipikus lehet ” tipikusabb.”Egy nagy adatszintézis során a leghasznosabb történelmi jellemzők, amelyek növelték az akut miokardiális infarktus valószínűségét, a jobb kar vagy a váll sugárzása, mindkét kar sugárzása, az erőfeszítéssel súlyosbodott fájdalom, izzadásés hányinger vagy hányás.1 bizonyos részhalmazok, köztük a nők, a cukorbetegek és az idősek nagyobb valószínűséggel rendelkeznek anginás tünetekkel, amelyeket dyspnoe, hányás, diaphoresis, generalizált gyengeség képvisel; néhánynak fájdalommentes bemutatása lehet.2 még azoknál a betegeknél is, akiknél atipikus tünetek vannak, például pleuritikus fájdalom vagy tapintható érzékenység a mellkas falában, a posttest valószínűsége csak azoknál csökken, akik már alacsony kockázattal járnak.1 A történelmi szív kockázati tényező terhelésének felsorolása kevés prognosztikai értékkel bír, különösen 40 évesnél idősebb betegeknél.3
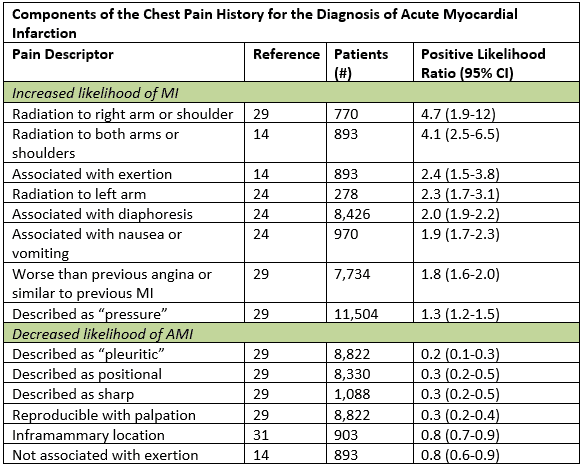
a Swap CJ-től adaptálva, et al. JAMA. 2005;294:2623-2629.
a fiatal betegek (<45 évesek) az ACS téves diagnózisának magas kockázatának kitett csoportot képviselik, elsősorban azért, mert az orvosok hajlamosak alábecsülni a szívkockázatot. Az Egyesült Államokban a myocardialis infarctusok legfeljebb 10% – a <45 éves betegeknél fordul elő, amelyek többsége atheroscleroticus szívbetegséghez kapcsolódik. Az atheroscleroticus betegséget a tizenévesek 17% – ánál figyelték meg egy vizsgálatban,4 és a multivessel-betegséget a fiatal felnőttek 20% – ánál (átlagéletkor: 26 év) a belvárosi erőszak áldozatainak boncolási vizsgálatában.5 Egy nemrégiben készült ED tanulmány megállapította, hogy a betegek 5,4%-a 24 69 éves, mellkasi fájdalommal járó, ACS-ben uralkodott, 2,2% – uknak volt káros kardiális eseménye (azaz halál, MI, perkután koszorúér-beavatkozás vagy szív bypass műtét) 30 napon belül.6 bár az ACS általános előfordulási gyakorisága fiatal betegeknél alacsonyabb, az orvosok nem engedhetik meg a HPI-re vonatkozó a-t pusztán a beteg életkora alapján.
A Diabetes mellitus (DM) egy másik magas kockázatú állapotot jelent az ACS téves diagnosztizálásának lehetősége szempontjából. A DM-ben szenvedő betegek hajlamosak fájdalommentes előadásokra, ha szív ischaemiájuk van. Nehézlégzés, zavartság, hányás, fáradtság) az esetek 40% – ában fordul elő. A cukorbetegek is nagyobb valószínűséggel vannak káros eredmények az ACS – től.7 a kezelőorvosok ezért nem támaszkodhatnak tipikus panaszokra a szívműködés megindításához cukorbetegeknél, sem a pozitív szív biomarkerekre, hogy agresszív megközelítést váltsanak ki ezeknél a betegeknél.
a Kokainhasználatot az atheroscleroticus szívbetegség és az MI további független kockázati tényezőjének kell tekinteni, különösen fiatal betegeknél. Egyes szerzők becslése szerint a kokain az akut MIs 25% – át teszi ki <45 éves betegeknél.7 a kokain akut használata koszorúér-érszűkületet, fokozott vérlemezke-aggregációt és/vagy adrenerg stimulációt okozhat, ami ritmuszavarokhoz és ischaemiához vezethet. A kokain krónikus használata az MI-vel is összefügg, ami jelentősen felgyorsult aterogenezist és az azt követő korai MI-t okoz. Összességében a kokainhasználók hétszeresére nőtt az MI kockázata.8
a szisztémás lupus erythematosus (SLE) a korai atherosclerosis és a myocardialis infarctus jelentős, de alulértékelt kockázati tényezője. A becslések szerint az SLE-ben szenvedő fiatal betegeknél kilencszer nagyobb a korai MI kockázata.9 nők <különösen a 45 éves nők vannak fokozott kockázatnak kitéve, becslések szerint a korai MI kockázata akár ötvenszeresére is megnő.10 az SLE korai érelmeszesedésének oka valószínűleg multifaktoriális, de nagyrészt az egyidejűleg fennálló szisztémás gyulladással és diszlipidémiákkal függ össze.
A humán immundeficiencia vírus (HIV) fertőzést a korai atherosclerosis független kockázati tényezőjeként is azonosították. A bizonyítékok arra utalnak, hogy a HIV-fertőzés endothel sérülést okoz a koszorúerekben, gyulladásos kaszkádot kezdeményezve, amely ateroszklerotikus elváltozásokhoz vezet.11 a korai érelmeszesedés megállapítása különösen kiemelkedő a HIV-fertőzés későbbi stádiumában szenvedő betegeknél (CD4 szám <200).12 a HIV (proteáz inhibitorok) kezelésében jelenleg alkalmazott gyógyszeres kezelések szintén súlyosbítják a korai érelmeszesedés kockázatát. Összességében az ACS-ben szenvedő HIV-betegek olyan korban vannak jelen, amely több mint 10 évvel fiatalabb, mint a nem HIV-betegek.13
a krónikus vesebetegséget (CRD) a közelmúltban a gyorsított atherosclerosis független kockázati tényezőjeként is azonosították. A CRD krónikus gyulladással jár14 és fokozott thrombocyta aggregációval.15 ezek a tényezők, kombinálva az egyidejűleg alkalmazott hagyományos kockázati tényezők megnövekedett prevalenciájával, aránytalanul magas kardiális események kockázatát idézik elő ezeknél a betegeknél.14
bár a kardiális ischaemia bemutatását követő 10 percen belül meg kell szerezni és értékelni kell, az EKG nem használható az ACS kizárására. A szív ischaemiában vagy infarktusban szenvedő betegek legfeljebb 50% – ánál nem specifikus vagy normál EKG lesz.16 Soros EKG növelheti a diagnosztikai hozamot az ACS jelenlétének megerősítésekor folyamatos tünetekkel rendelkező betegeknél.
az EKG-hez hasonlóan a szív biomarkerek akkor hasznosak, ha pozitívak, de normálisak esetén korlátozott hasznosságuk van. A Soros biomarker tesztelés 3 6 óra alatt rutinprotokollá vált számos EDs-ben, és kiváló érzékenységgel rendelkezik az MI bizonyítékainak kimutatására. A biomarkerekre azonban nem lehet támaszkodni a szív ischaemia kizárására. A “szív” pontszám prospektív validálása lehetővé tette a szakemberek számára, hogy megbízhatóan megkülönböztessék az alacsony kockázatú betegek egy részét, amelyek valószínűleg nem részesülnének további vizsgálatokból.17
a stressztesztet és a koszorúér angiográfiát gyakrabban használják a mellkasi fájdalomban szenvedő betegek értékelésének korai szakaszában, hogy uralkodjanak az ACS-ben. Bár a negatív stresszteszt vagy angiogram a mögöttes CAD alacsonyabb kockázatával jár, egyik teszt sem tudja véglegesen kizárni az ACS-t vagy a jelentős mögöttes koszorúér-trombózisok jelenlétét. A stressztesztelési módszerek többsége kimutatja a szignifikáns koszorúér-elváltozásokat, csak 85-95% – os érzékenységgel.18-19 a koszorúér angiográfia szintén tökéletlen teszt; a hamis negatív angiográfiás értelmezések nem ritkák diffúz betegség, excentrikus plakkok, “flush” elzáródások, elágazó ostiális elváltozások, átfedő oldalágak jelenlétében, sőt akkor is, ha a bal fő koszorúérben elváltozások vannak jelen.20 ezen vizsgálatok megbízhatóságát tovább veszélyeztetik azok az adatok, amelyek azt mutatják, hogy a MIs többsége az artériákon belüli elzáródásokból származik, amelyek korábban <50% – ban elzáródtak az infarktus előtt.21-23
Az ilyen típusú elváltozások általában negatív stressztesztekkel vagy “nem jelentős” angiogramokkal társulnak, ha a vizsgálatokat az infarktus előtt végzik. Jellegüknél fogva a rögzített koszorúér-szűkület kimutatása, a stressztesztek nem képesek értékelni vagy megjósolni azokat a sérülékeny koszorúér-plakkokat, amelyek ki vannak téve az elmozdulás kockázatának, ami akut koszorúér-eseményhez vezet. Az ACS szempontjából értékelt betegek egyik vizsgálatában, akiknek negatív stressztesztje volt az előző 3 évben, több mint 20% elérte az ami összetett indexét, a pozitív stressztesztet, a CABG-t vagy a katéterezést beavatkozással, a negatív tesztek túlnyomó többségével a bemutatástól számított 1 éven belül.24 Hasonlóképpen, a még invazívabb tesztelés során a szívkatéterezésen normál vagy “minimális” CAD-vel rendelkező férfiak és nők (1,2%, illetve 3,3%) vagy AMI-t vagy halált szenvedtek a nyomon követéstől számított 1 éven belül.25 létfontosságú, hogy a klinikus ne támaszkodjon előzetes objektív tesztelésre az ACS-re utaló jelekkel és tünetekkel rendelkező betegekkel szemben.
összefoglaló
a mellkasi fájdalom és a lehetséges ACS értékelése magas kockázatú törekvés. A “teljes szívműködés” folytatására vonatkozó döntésnek elsősorban alapos HPI-n kell alapulnia. Az orvosoknak tisztában kell lenniük az atípusos megjelenések gyakoriságával, különösen nőknél, időseknél és cukorbetegeknél. A fiatal betegek szintén külön figyelmet érdemelnek, mivel kockázatukat gyakran alábecsülik. További nem hagyományos kardiális kockázati tényezők, beleértve a kokaint, a szisztémás lupus erythematosust, az emberi immunhiányos vírust és a krónikus vesebetegséget, különös figyelmet igényelnek. A diagnosztikai tesztelés elektrokardiográfiából áll (hasznos az ACS-ben, de nem zárja ki a diagnózist) és a szív biomarker teszteléséből, amelyek szintén elsősorban akkor hasznosak, ha pozitívak. Fontos, hogy a negatív stresszteszt vagy angiogram nagyon hasznos a betegek rétegződésében az ACS és a CAD alacsony kockázatára, de nem zárják ki véglegesen a diagnózist.
idézet: Palatnik M. Egy 38 éves férfi mellkasi fájdalommal. J Sürgősségi Ellátás Med. Március 2018. Elérhető: https://www.jucm.com/a-38-year-old-man-with-chest-pain/.
- csere CJ, Nagurney JT. A mellkasi fájdalom anamnézisének értéke és korlátai az akut koszorúér-szindrómák gyanúja esetén. JAMA. 2005;294:2623-2629.
- El-Menyar a, Zubaid M, Sulaiman K. az akut koszorúér-szindróma atipikus bemutatása: a kórházi halálozás jelentős független előrejelzője. J Cardiol. 2011;57;165-171.han JH, Lindsell CJ, Storrow AB, et al. A szív kockázati tényező terhelésének szerepe az akut koszorúér-szindrómák diagnosztizálásában a sürgősségi osztályon. Ann Emerg Med. 2007;49;145-152.
- Tuzcu EM, Kapadia SR, Tutar E, et al. Magas prevalenciája koszorúér atherosclerosis tünetmentes tinédzserek és fiatal felnőttek: bizonyíték intravaszkuláris ultrahang. Keringés. 2001;103:2705-2710.Joseph a, Ackerman D, Talley JD, et al. A koszorúér atherosclerosis megnyilvánulása fiatal trauma áldozatoknál-boncolási vizsgálat. Cardiol Vagyok. 1993;222:459-467.
- Marsan RJ Jr., Shaver KJ, Sease KL, et al. Klinikai döntési szabály értékelése mellkasi fájdalomban szenvedő fiatal felnőtt betegek számára. Acad Emerg Med. 2005;12:26-32.Fergus TS, Fazel R, Fang J, et al. A diabéteszes betegek bemutatása, kezelése és eredményei az akut koronária szindrómák miatt befogadott nem diabéteszes betegekhez képest. Szív. 2004;90:1051-1052.
- Qureshi AI, Suri MF, Guterman LR, et al. Kokainhasználat és a nem halálos miokardiális infarktus és stroke valószínűsége: a harmadik Nemzeti Egészségügyi és táplálkozási vizsgálati felmérés adatai. Keringés. 2001;103:502-506.d ‘ Agate DJ, Kokolis S, Belilos E, et al. Korai koszorúér – betegség szisztémás lupus erythematosusban, kiterjedt kiújulással a koszorúér bypass műtétét követően. J Invazív Cardiol. 2003;15:157-163.
- Manzi S, Meilahn EN, Rairie JE, et al. A myocardialis infarctus és angina életkor-specifikus előfordulási aránya szisztémás lupus erythematosusban szenvedő nőknél: összehasonlítás a Framingham-vizsgálattal. Am J Epidemiol. 1997;145:408-415.Varriale P, Saravi G, Hernandez E, et al. Akut miokardiális infarktus humán immundeficiencia vírussal fertőzött betegeknél. Szív Vagyok J. 2004; 147: 55-59.
- Hsue PY, Lo JC, Franklin A, et al. Az atherosclerosis előrehaladása a carotis intima-media vastagságával értékelve HIV-fertőzésben szenvedő betegeknél. Keringés. 2004;109:1603-1608.
- Hsue PY, Giri K, Erickson S, et al. Az akut koszorúér-szindrómák klinikai jellemzői humán immunhiányos vírusfertőzésben szenvedő betegeknél. Keringés. 2004;109:316-319.
- Yerkey MW, Kernis SJ, Franklin BA, et al. Veseműködési zavar és a koszorúér-betegség gyorsulása. Szív. 2004;90:961-966.
- Aggarwal A, Kabbani SS, Rimmer JM, et al. A hemodialízis kétfázisú hatásai a thrombocyta reaktivitásra végstádiumú vesebetegségben szenvedő betegeknél: potenciálisan hozzájárul a kardiovaszkuláris kockázathoz. Am J Vese Dis. 2002;40:315-322.Brady WJ, Aufderheide TP, Chan T, et al. Az akut miokardiális infarktus elektrokardiográfiás diagnózisa. Emerg Med Clin Észak Am. 2001;19:295-320.
- Backus BE, Six aj, Kelder JC, et al. A mellkasi fájdalomban szenvedő betegek szívértékének leendő validálása a sürgősségi osztályon. Int J Kardiológia. 2013;168;2153-2158.
- Ioannidis JPA, Salem D, Chew PW, et al. A képalkotó technológiák pontossága az akut szív ischaemia diagnosztizálásában a sürgősségi osztályon: metaanalízis. Ann Emerg Med. 2001;37:471-477.
- Lateef F, Gibler WB. Provokatív vizsgálat mellkasi fájdalomra. Am J Emerg Med. 2000;18:793-801.
- Schwartz L, GOURASSA MG. Mellkasi fájdalommal és normál coronaria angiogrammal rendelkező betegek értékelése. Arch Int Med. 2001;161:1825-1833.
- Giroud D, Li JM, Urban P, et al. Az akut miokardiális infarktus helyének viszonya a legsúlyosabb koszorúér artériás stenosishoz az előzetes angiográfia során. Cardiol Vagyok. 1992;69:729-732.
- Hackett D, Davies G, Maseri A. az első miokardiális infarktusban szenvedő betegeknél a már meglévő koszorúér-szűkületek nem feltétlenül súlyosak. Eur Szív J. 1988; 9: 1317-23.
- Hackett D, Verwilghen J, Davies G, et al. Coronaria stenosis akut myocardialis infarctus előtt és után. Cardiol Vagyok. 1989;63:1517-1518.
- Walker J, Galuska M, Vega D. koszorúér-betegség a sürgősségi osztályon mellkasi fájdalomban szenvedő betegek a közelmúltban negatív stresszteszttel. West J Emerg Med. 2010;11;384-388.
- Hemingway H, McCallum A, Shipley M, et al. JAMA 2006;295; 1404-1411.
