Kemiallinen ionisaatio (CI) on pehmeä ionisointitekniikka, joka on molekyyli-ja ionireaktioiden tutkimustulosten suora soveltaminen analyyttisessä kemiassa. Varhaisin ionisointitekniikka oli elektronipommitusionisaatio (EI). EI: n saamassa tuotteessa on paljon fragmentteja, joita on vaikea analysoida. CI, joka tuotti hyvin vähän fragmentteja, alkoi 1950-luvulla ja sillä on suuri potentiaali analyyttisessä kemiassa.
CI-prosessissa elektronit pommittavat ensin reagenssikaasua, jolloin syntyy reagenssi-ioneja. Tämän jälkeen näytemolekyylit ionisoituvat reagenssi-ionien avulla molekyyli-ja ionireaktioreitin kautta. 1970-lukua pidettiin merkkipaaluna CI: n kehityksessä. Tuolloin tutkijat ratkaisivat CI: n työn puutteet tyhjiöympäristössä, mikä mahdollisti CI: n työskentelyn ilmakehän olosuhteissa. Ilmakehän kemiallinen ionisaatio tuottaa energiaa koronapurkauksesta eikä vaadi tyhjiöympäristöä, mikä lisää huomattavasti CI-sovellusten valikoimaa. Tällä hetkellä CI: tä on käytetty laajalti massaspektrometriatekniikassa.
kemiallisen ionisaation periaate
CI: n periaate on käyttää reagenssi-Ionia X+ reagoidakseen analyyttimolekyyli A: n kanssa analyytin ionisoitumisen aikaansaamiseksi:
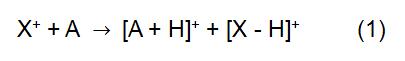
edellä mainitussa reaktiossa X+ saadaan ionisoituneesta reaktiokaasusta. Joitakin yleisiä reagenssikaasuja ovat metaani, ammoniakki, vesi ja isobutaani. Reaktioaika ja kaavassa oleva nopeusvakio (k) voidaan saada kirjallisuudella tai mittaamalla. Kun reagenssi-ioni X+ on H3O+, kaava (2) on:
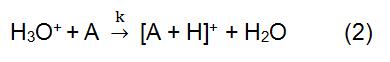
reagenssi-ioni syntyy ionilähteestä. Yleisesti käytettyjä ionilähteitä ovat pääasiassa säteilylähde, onttokatodipurkausvirtalähde ja tavallinen hehkupurkausvirtalähde. 210Po ja 241am ovat yleisimmät säteilylähteet. Ionisaatioprosessi alkaa 210po: n ja 241am: n lähettämillä alfahiukkasilla. Sillä on suuri energia ja se voi törmätä reagenssikaasuun synnyttäen reagenssien ioneja ja elektroneja. Jos syntyvät elektronit ovat riittävän korkeita, ne saattavat törmätä reagenssikaasuun muodostaen uusia reagenssien ioneja ja elektroniikkaa. Reagenssi-ionina H3O+: a käyttävässä CI: ssä käytetään yleisesti onttoa katodin purkausvirtalähdettä, joka voi tuottaa 99,5% H3O+: sta.
kemiallisen ionisaation olosuhteiden mukaan CI luokitellaan matalapaineiseen kemialliseen ionisaatioon (
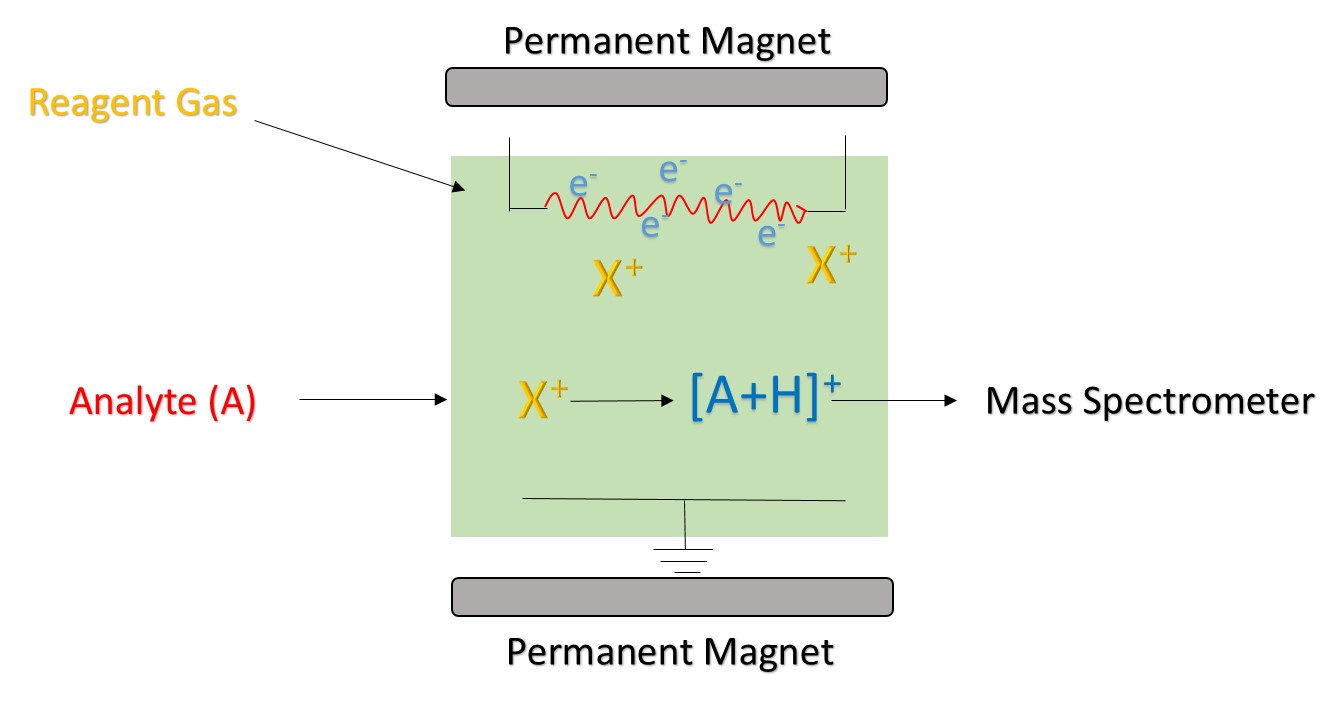 Kuva 1. Kemiallisen ionisaation periaate
Kuva 1. Kemiallisen ionisaation periaate
CI: n edut ja haitat
CI: n spektrin resoluutio on yksinkertainen ja analyytin tarkka molekyylipaino voidaan saada. CI: n tuottamassa tuotteessa on vain vähän fragmentteja, ja sen tuotteet ovat pääasiassa tutkittavan aineen molekyylejä ja ioneja. CI: n selektiivisyyttä voidaan helposti lisätä valitsemalla sopiva reagenssi-ioni. Esimerkiksi reagenssi-ioni H3O+ reagoi vain sellaisen orgaanisen aineen kanssa, jonka protonin affiniteetti on suurempi kuin H3O+. Lisäksi CI: llä on korkea herkkyys ja nopea vaste (15s). Jos reaktiiviset ionit ovat kuitenkin epäpuhtaita ja samaan aikaan tapahtuu erilaisia kemiallisia ionisaatioreaktioita, massaspektrometria vaikeutuu.
esimerkkejä CI-sovelluksista
nykyisin CI: tä käytetään laajalti ionilähteenä massaspektrometriajärjestelmissä erilaisten hivenaineiden havaitsemiseen. CI: tä voidaan käyttää muun muassa ilmakehän jäämäkaasujen, kasvisten ja hedelmien torjunta-ainejäämien, maitojauheen melamiinin, pehmittimien ja rikkakasvien torjunta-aineiden havaitsemiseen maaperässä. Lisäksi CI: tä voidaan käyttää myös materiaalin tunnistamiseen, kuten teen laadun tunnistamiseen.
- haihtuvien orgaanisten yhdisteiden (VOC) mittaus
CI: n suorittamassa VOC: n mittauksessa H3O+: a käytetään yleensä reagenssi-ionina. H3O+ ei reagoi useimpien ilmassa olevien aineiden, kuten O2: n, N2: n, CO2: n jne.kanssa. Toisaalta suurin osa protoninsiirtoreaktioista on dissosioitumattomia, joten tuote-ionit ovat yksittäisiä, mikä tekee tulosten analysoinnista yksinkertaista. Periaate, jonka mukaan VOC mitataan käyttämällä H3O+: a reagenssi-ionina, esitetään yhtälössä (3). Lopputuote ratkaistiin protoninsiirtoreaktion massaspektrometrialla.
- määritettäessä melamiinia maitojauheesta
CI: n suorittamassa melamiinin mittauksessa käytetään Reagenssikaasuna N2: ta. Suurjännitteen vaikutuksesta N2 ja H2O käyvät läpi monimutkaisia fysikaalis-kemiallisia reaktioita reagenssi-ionien H3O+tuottamiseksi. Reaktioprosessi esitetään formula_3-6. H3O + reagoi maitojauheessa melamiinin kanssa ja reaktioperiaate esitetään kaavassa (2).
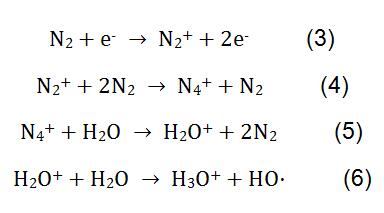
- teelaadun tunnistaminen
eri teelajit voidaan tunnistaa mittaamalla teelehtien pinnalta kemiallisia aineita CI: llä. H3O+ reagoi teen pinnan kanssa butanolin, geraniolin, kofeiinin ja muiden aineiden kanssa ja reaktiotuotteet muodostavat massaspektrometrissä erilaisia massaspektrejä. Saman aineen pitoisuus eri teelajikkeissa on erilainen, joten CI-tunnistuksen muodostama massaspektri on erilainen. Massaspektri voi heijastaa jonkin verran teen kemiallisia sormenjälkiominaisuuksia. Siksi CI: llä on tärkeä käytännön käyttöarvo teen nopeaan tunnistamiseen ja laadun analysointiin.
kemiallista ionisaatiota käytetään laajalti massaspektrometriassa sen voimakkaan selektiivisyyden ja suuren herkkyyden vuoksi. Kemiallinen ionisaatiomassaspektrometria (CIMS) ei ainoastaan mahdollista aineiden tandem-massaspektrometristä tunnistamista monimutkaisissa näytteissä, vaan se myös hankkii kemiallisen sormenjälkitiedon näytteille kemometristä analyysia varten. Täytäntöönpanotoimenpiteiden soveltaminen vaikuttaa myönteisesti elintarvike -, lääke -, ympäristönsuojelu -, maatalous-ja muiden teollisuudenalojen kehityksen edistämiseen.
olemme lyhyesti ottaneet käyttöön CI: n, eräänlaisen ionisaatiomenetelmän, joka voi auttaa ymmärtämään enemmän massaspektrometriaa. Creative Proteomicsilla olemme kehittäneet ammattimaisen massaspektrometria-alustan, joka sisältää huipputeknisiä instrumentteja. Massaspektrometriaa käyttämällä Creative Proteomics voi tarjota erilaisia palveluja erilaisten vaatimusten täyttämiseksi, mukaan lukien:
- Proteomiikkapalvelu
- Glykomiikkapalvelu
Metabolomiikkapalvelu
- Fales H M; et al. Joidenkin biologisesti tärkeiden yhdisteiden massaspektrien vertailu eri ionisaatiotekniikoilla. Analyyttinen Kemia, 1975, 47(2):207-219.
- Lindinger W; et al. Haihtuvien orgaanisten yhdisteiden online-seuranta pptv-tasoilla protoninsiirtoreaktion massaspektrometrian (PTR-MS) avulla lääketieteellisissä sovelluksissa, elintarvikevalvonnassa ja ympäristötutkimuksessa. International Journal of Mass Spectrometry & ion Processes, 1998, 173(3):191-241.
- Chen H; et al. Pintadesorptio Ilmanpaine kemiallinen ionisaatiomassaspektrometria suoraa ympäristön näytteen analysointia varten ilman myrkyllistä kemiallista kontaminaatiota. Journal of Mass Spectrometry, 2010, 42(8):1045-1056.
- Yang S; et al. Melamiinin osoittaminen maitotuotteissa Pintadesorptiolla ilmanpaineen kemiallisella Ionisaatiomassaspektrometrialla. Analyyttinen Kemia, 2009, 81(7):2426.
