ensimmäinen tapa kehittää kannabinoidiantagonisteja 1980-luvun lopulla oli muuttaa THC: n rakennetta, mutta tulokset olivat pettymyksiä. 1990-luvun alussa löydettiin uusi kannabinoidiagonistien perhe NSAID: stä (ei-steroidiset anti-inflammatoriset) pravadoliini-lääke, joka johti aminoalkyyli-indoliantagonistien löytämiseen, jolla oli jonkin verran mutta heikkoa menestystä. Koska agonistien rakenteeseen perustuva haku oli pettymys, ei ollut yllätys, että ensimmäinen voimakas ja selektiivinen kannabinoidiantagonisti kuului täysin uuteen kemialliseen perheeseen. Vuonna 1994 Sanofi toi markkinoille ensimmäisen selektiivisen kannabinoidiantagonistin SR141716 (rimonabantti), joka kuuluu 1,5-diaryylipyratsoliperheeseen.
RimonabantEdit
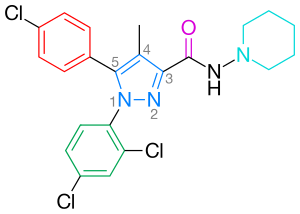
rimonabantti, joka tunnetaan myös systemaattisella nimellä , on 1,5-diaryylipyratsolin CB1-reseptoriantagonisti (kuva 2). Rimonabantti ei ole vain voimakas ja erittäin selektiivinen CB1-reseptorin ligandi, vaan se on myös oraalisesti aktiivinen ja estää suurimman osan kannabinoidiagonistien, kuten THC: n, vaikutuksista sekä in vitro että In vivo. Rimonabantilla on todettu selvä kliininen teho lihavuuden hoidossa.
Sidonta
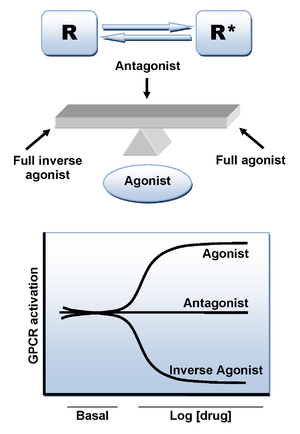
agonistiligandin sitoutuminen CB1-reseptoriin aiheuttaa konformaatiomuutoksen ja johtaa signaalin transduktiosta vastaavan reseptorin aktiiviseen tilaan. On kuitenkin olemassa lisämekanismi, joka voi johtaa aktiiviseen tilaan ligandin puuttuessa. Kuten monet muut GPC-reseptorit, CB1-reseptori näyttää voimakasta konstitutiivista aktiivisuutta ja siten se voi spontaanisti omaksua aktiivisen konformaatiotilan ilman agonistisitoutumista, pitäen kohonneita solunsisäisen signaloinnin perusarvoja. Tämä voidaan selittää reseptoriaktivaation kahden tilan mallilla, jossa reseptorit ovat tasapainossa kahden tilan, aktiivisen ja inaktiivisen (R* ja R) välillä. Agonisti vakauttaa aktiivisen tilan, joka johtaa aktivaatioon, neutraali antagonisti sitoutuu yhtä lailla aktiiviseen ja inaktiiviseen tilaan, kun taas käänteinen agonisti stabiloi inaktiivisen tilan mieluiten (kuva 3).
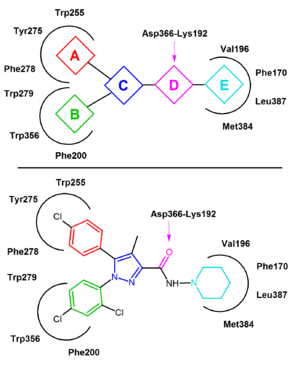
rimonabantin on raportoitu monissa tapauksissa käyttäytyvän käänteisagonistina neutraalin antagonistin sijaan ja on todennäköistä, että se sitoutuu ensisijaisesti CB1: n inaktiiviseen tilaan, mikä vähentää signalointireitin aktivoitumista. Keskeinen sitova vuorovaikutus on rimonabantin karbonyyliryhmän ja CB1-reseptorin lys192-jäämän välille muodostunut vetysidos. Tämä sidos stabiloi transmembraanikierteiden 3 ja 6 solunsisäisen pään Lys192-Asp366 suolasillan (Kuva 4). Tämä spesifinen suolasilta on läsnä reseptorin inaktiivisessa tilassa, mutta ei aktiivisessa tilassa.
CB1: n inaktiivisessa tilassa rimonabantti sitoutuu transmembraaniin-3-4-5-6 aromaattista mikrodomaania. Rimonabantin sitoutumiseen liittyy sen 2,4-dikloorifenyylirenkaan ja sen toisella puolella olevien trp279/Fe200/Trp356-jäämien ja toisella puolella olevan parafenyylirenkaan ja Tyr275/Trp255/Phe278-jäämien välisiä suoria aromaattisia pinoamisvuorovaikutuksia. Lipofiilinen piperidinyyliosa sopii hyvin aminohappojäämien Val196/Phe170/Leu387 ja Met384 muodostamaan onteloon (Kuva 4).
Farmakoforeedit
useimmat tähän mennessä ilmoitetut CB1-antagonistit ovat rimonabantin läheisiä analogeja tai isostereita. Näiden analogien yhteisistä piirteistä, diaryylipyratsoleista, voidaan erottaa yleinen CB1-käänteisagonistin farmakoforimalli (Kuva 4). Tässä farmakofoorumissa on syklinen ydin, C, (esim.pyratsoli rimonabantissa), joka on korvattu kahdella aromaattisella osalla, A: lla ja B: llä. vetysidoksen hyväksymisyksikkö, D, yhdistää C: n sykliseen lipofiiliseen osaan, E. joissakin tapauksissa yksikkö E yhdistyy suoraan C: hen. Kuvassa 4 käytetään esimerkkinä rimonabanttia. Yksikkö A edustaa 4-kloorifenyyliryhmää ja yksikkö B 2,4-dikloorifenyylirengasta. Yksikkö C on pyratsolin keskusrengas ja yksikkö D edustaa karbonyyliryhmää, joka toimii vetysidoksen hyväksyjänä. Yksikkö E edustaa lipofiilistä aminopiperidinyyliosaa.
rakenne-aktiivisuussuhteet
optimaalinen sitoutuminen CB1-reseptoriin edellyttää parasubstituoitua fenyylirengasta pyratsolin 5-asennossa. Pyratsolin 5-substituentti osallistuu reseptorintunnistukseen ja antagonismiin. Fenyylirenkaan para-substituentti voisi olla kloori, bromi tai jodi, mutta on osoitettu, että myös alkyyliketju voisi olla siedettävissä. Keskimmäisen pyratsolirenkaan numerointi on esitetty kuvassa 2.
pyratsolin 1-asemassa olevaa 2,4-dikloorisubstituoitua fenyylirengasta suositellaan affiniteetin ja aktiivisuuden kannalta. On osoitettu, että tämän fenyylirenkaan ylimääräiset halogeenit vähentävät affiniteettia.
myös rengassubstituutio on suotuisa 3-karboksamidiryhmässä, kuten 1-piperidinyyliryhmässä rimonabantissa. Amino – piperidinyylisubstituentin korvaaminen alkyyliamideilla, eettereillä, ketoneilla, alkoholeilla tai alkaaneilla johti useimmiten affiniteetin vähenemiseen. Piperidinyylin korvaaminen pentyyli-tai heptyyliketjulla antoi yhdisteille agonistisia ominaisuuksia. Näiden tulosten perusteella pääteltiin, että pyratsolin 3-kanta näyttää liittyvän agonismiin,kun taas 1 -, 4 -, 5-kanta näyttää liittyvän antagonismiin.
tutkimukset ovat osoittaneet, että karboksamidin hapen puuttuminen johtaa affiniteetin vähenemiseen. Lisäksi karboksamidin hapen läsnäolo edistää käänteisten agonististen ominaisuuksien aikaansaamista, kun taas analogien, joilla ei ole tätä happea, on todettu olevan neutraaleja antagonisteja. Nämä tulokset tukevat hypoteesia, jonka mukaan karboksamidin happi muodostaa vetysidoksen LYS192-jäännöksen kanssa CB1-reseptorissa.
Diaryylipyratsolijohdannaiset
SR141716 (rimonabantti)-analogeja on äskettäin kuvattu useissa ryhmissä, mikä johtaa hyvään ymmärrykseen rakenne-aktiivisuussuhteesta (SAR) tässä kemiallisessa ryhmässä. Vaikka useimmat kuvatut yhdisteet ovat vähemmän voimakkaita kuin SR141716, kaksi niistä on syytä mainita, SR147778 ja AM251, vaikka molemmilla saattaa olla vaikutusta myös mu-opioidireseptoreihin.
SR147778 (surinabantti), toisen sukupolven antagonisti, on pitkäkestoisempi kuin rimonabantti, ja sen vaikutus suun kautta lisääntyy. Vaikutusajan pidentyminen johtuu todennäköisesti metabolisesti stabiilimman etyyliryhmän esiintymisestä pyratsolirenkaan 4-asemassa. Toinen muutos on 5-fenyylikloorisubstituentin korvaaminen bromilla.
diaryylipyratsolijohdannainen AM251 on kuvattu, jossa kloorisubstituentti on korvattu jodilla 5-fenyylirenkaan para-asennossa. Tämä johdannainen näytti olevan voimakkaampi ja selektiivisempi kuin rimonabantti.
21 analogia, joilla oli joko alkyyliamidi tai varianttipituinen alkyylihydratsidi asemassa 3, syntetisoitiin. Havaittiin, että affiniteetti kasvaa hiiliketjun pituuden kasvaessa jopa viiteen hiileen. Myös amidianalogeilla oli suurempi affiniteetti kuin hydratsidianalogeilla. Yhdelläkään näistä analogeista ei kuitenkaan ollut merkitsevästi suurempaa affiniteettia kuin RIMONABANTILLA, mutta ne olivat kuitenkin hieman selektiivisempiä kuin rimonabantti CB1-reseptoriin verrattuna CB2-reseptoriin.
diaryylipyratsolijohdosten affiniteettia on yritetty lisätä useita kertoja jäykistämällä rimonabantin rakennetta. Yleisen pharmacophore-mallin mukaan yksiköt A, B ja / tai C on liitetty toisiinsa jäykiksi molekyyleiksi johtavilla lisäsidoksilla. Esimerkiksi kondensoituneen polysyklisen pyratsolin Ness – 0327 affiniteetti CB1-reseptoriin oli 5000 kertaa suurempi kuin rimonabantilla. Yhdisteellä on kuitenkin huono keskeinen hyötyosuus.
toista yhdistettä, indatsolijohdannaista O-1248, voidaan pitää rimonabantin analogina, jossa sen 5-aryyliryhmä fuusioituu pyratsoliosaksi. Tämä rakenteellinen muutos johti kuitenkin 67-kertaiseen CB1-reseptorin affiniteetin vähenemiseen.
näistä rimonabantin diaryylipyratsolijohdannaisista on yhteenveto taulukossa 1.
 |
 |
| SR147778 | AM251 |
 |
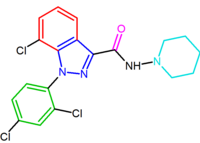 |
| NESS-0327 | O-1248 |
Other derivativesEdit
Structurally different from the 1,5-diarylpyrazoles are the chemical series of the 3,4-diarylpyrazolines. Tähän sarjaan kuuluu SLV-319 (ibipinabantti), voimakas CB1-antagonisti, joka on noin 1000 kertaa selektiivisempi CB1: lle verrattuna CB2: een ja jolla on samanlainen in vivo-aktiivisuus kuin rimonabantilla.
toinen tapa kehittää rimonabantin analogeja oli korvata keskinen pyratsolirengas toisella heterosyklillä. Esimerkkejä tästä lähestymistavasta ovat 4,5-diaryyli-imidatsolit ja 1,5-diaryylipyrroli-3-karboksamidit.
suuri määrä diaryylipyratsolin ja imidatsolien fuusioituja bisyklisiä johdannaisia on raportoitu. Esimerkki näistä on puriinijohdannainen, jossa pyrimidiinirengas fuusioituu imidatsolirenkaaksi. Otenabantti (CP-945,598) on esimerkki Pfizerin kehittämästä fuusioidusta bisyklisestä johdannaisesta.
useat tutkimusryhmät ovat tutkineet kuusihenkisiä rengaspyratsolin bioisostereita. Esimerkiksi yksi 2,3-diaryylipyridiinijohdannainen osoitettiin voimakkaaksi ja selektiiviseksi CB1-käänteisagonistiksi. Yhdisteen rakenne osoittaa, että rimonabantin amidiosa voisi jakautua lipofiiliseksi (bentsyylioksi) ja polaariseksi (nitriili) toiminnallisuudeksi. Muita kuusihenkisiä rengasanalogeja ovat esimerkiksi pyrimidiinit ja pyratsiinit.
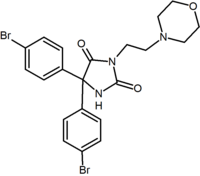
viisi-ja kuusijäsenisten rengasanalogien lisäksi on muitakin syklisiä johdannaisia, kuten atsetidiinit. Yksi esimerkki on metyylisulfonamidin atsetidiinijohdannainen, jonka 1,1-diaryyliryhmä jäljittelee diaryylipyratsolien 1,5-diaryyliosaa. Sulfonyyliryhmä toimii vetysidoksen hyväksyjänä. 1,1-diaryyliryhmää esiintyy myös johdannaisissa kuten bentsodioksoleissa ja hydantoiineissa.
asyklisiä analogeja on myös raportoitu. Nämä analogit sisältävät 1,2-diaryylimotiivin, joka vastaa rimonabantin 1,5-diaryylisubstituentteja. Esimerkki asyklisestä analogista on Merckin kehittämä taranabantti (MK-0364).
näiden analogien edustajat on esitetty yhteenvetona taulukossa 2.
 |
 |
||
| Type of derivative |
3,4-Diarylpyrazoline (Ibipinabant) | 4,5-Diarylimidazole | 1,5-Diarylpyrrole-3-carboxamides |
 |
 |
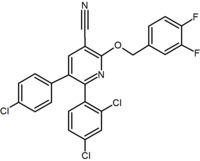 |
|
| Type of derivative |
Purine (pyrimidine ring fused to an imidazole ring) |
Purine derivative (Otenabant) | 2,3-Diarylpyridine |
 |
 |
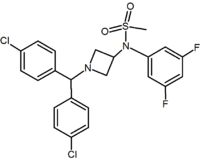 |
|
| Type of derivative |
Pyrimidine | Pyrazine | Methylsulfonamide azetidine |
 |
 |
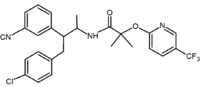 |
|
|
johdannaisen Tyyppi |
Bentsodioksoli | hydantoiini | asyklinen johdannainen (Taranabantti) |
CB1-reseptorin antibodiesedit
vasta-aineita CB1-reseptoria vastaan on kehitetty ja otettu kliiniseen käyttöön Venäjällä. Niitä ovat brizantin (venäjäksi Бризантин®) ja Dietressa (venäjäksi Диетресса®). Brizantin on tarkoitettu nikotiinin vieroitusoireiden ja tupakoinnin lopettamisen hoitoon ja dietressa on tarkoitettu painonpudotukseen. Dietressa on saatavilla Venäjällä.

