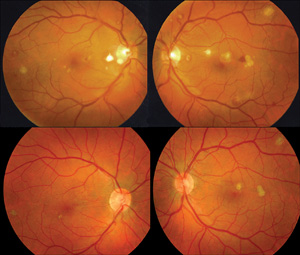
kuva 1. Väri silmänpohja valokuva molemmista silmistä suonensisäisellä huumeiden väärinkäyttäjällä ennen peräkkäistä kahdenvälistä vitrectomiaa (ylärivi) ja sen jälkeen vitrectomiaa (alarivi). Ennen vitrectomiaa oli lievä vitriitti ja muutama lasiaisen samentuma molemminpuolisesti. Hemorragisen retinochoroidiitin alueet ovat läsnä. Kahdesti viikossa annettujen vitrektomian ja viiden amfoterisiini-B: n sarjaruiskutuksen jälkeen jäljellä olevat retinochoroidaaliset arvet voidaan nähdä verkkokalvon verenvuodon ja lasiaisen sameuden häviämisenä. Tämä potilas sai myös kuukauden suun kautta ketokonotsolia.
endogeeninen endoftalmiitti on harvinainen, mutta mahdollisesti tuhoisa silmänsisäinen infektio, jossa taudinaiheuttajat päätyvät verenkiertoon. Endogeeninen endoftalmiitti on harvinaisempi kuin eksogeeninen endoftalmiitti, sillä se on 2-8 prosenttia kaikista endoftalmiittitapauksista eri tutkimuksissa.1, 2 lapsipotilaiden endogeeninen endoftalmiitti on vielä harvinaisempi, eli 0, 1-4 prosenttia kaikista endogeenisistä endoftalmiittitapauksista.2, 3
altistavat tilat ovat tärkeitä potilaan endogeenisen endoftalmiitin riskin määrittämisessä. Potilailla, joilla on akuutti tai krooninen panuveiitti epäselvä alkuperä, invasiivisia diagnostisia menettelyjä, yleisimmin pars plana vitrectomia, voi olla tarpeen tehdä diagnoosi. Endogeenisen endoftalmiitin tunnistettuja riskitekijöitä ovat: krooniset sairaudet (esim. diabetes mellitus, munuaisten vajaatoiminta, maligniteetit ja hankittu immuunipuutosoireyhtymä); immunosuppressiivinen hoito; äskettäinen invasiivinen leikkaus; suonensisäinen lääkkeiden väärinkäyttö; sisuskatetri; endokardiitti; maksa-ja sappitulehdukset; elinsiirrot; raskaus tai synnytys; urogenitaaliset leikkaukset; tai hammaslääketieteelliset toimenpiteet.4 suonensisäisten huumeiden käyttöhistorian selvittäminen on erityisen tärkeää ja usein vaikeaa, kun otetaan huomioon potilaiden haluttomuus keskustella tästä asiasta. Positiivisia taustasairauksia, kuten diabetesta, sydänsairauksia ja maligniteettia, raportoitiin 90 prosentilla potilaista Annabelle A. Okadan ja kollegoiden raportissa vuonna 1994.Endogeenista endoftalmiittia sairastavilla potilailla tehdyssä laajassa tutkimuksessa raportoitiin 56-68 prosentissa tapauksista silmätulehdukselle altistavia perussairauksia.6 Zenith H. Wu ja kollegat raportoivat, että 90,9 prosentilla potilaista todettiin edeltävä altistava tila ja yleisin todettu systeeminen tila oli diabetes mellitus (50 prosenttia).7
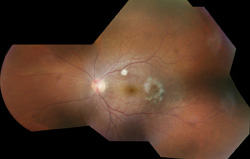
kuva 2. Väri silmänpohja valokuva Candida endogeenista endoftalmiittia sairastavan potilaan vasemmasta silmästä vitrectomyn jälkeen ja viisi kahdesti viikossa annettua amfoterisiini-B: n intravitreaalista injektiota, joissa näkyy valkoisia retinokoroidisia leesioita makulassa sekä eksentrinen makulan reikä sienen endoftalmiitin jälkitautina. Näöntarkkuus oli 20/30. Tämä potilas sai myös kuukauden suun kautta ketokonotsolia.
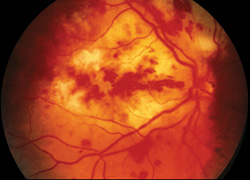
kuva 3. Värivalokuva aspergilluksen aiheuttamasta endogeenisestä endoftalmiitista kärsivän potilaan oikeasta silmästä. Potilaalla oli ollut suonensisäisiä lääkkeitä, ja häntä hoidettiin intravitreaalisella ja systeemisellä amfoterisiini B: llä, mutta näkökyky oli huono.
endogeenisen endoptalmiitin aiheuttaa useimmiten bakteeri tai sieni. Aiheuttajaeliöt vaihtelevat maantieteellisesti. Tutkimus Bascom Palmer Eye Institute raportoitu sienet yleisempi syy kuin bakteerit (62 prosenttia sieniä vs. 38 prosenttia bakteeri), 8 kun taas Hong Kong tutkimus raportoitu bakteerit yleisempi syy endogeenisen endoftalmiitti (72,7 prosenttia bakteeri vs. 27,3 prosenttia sieni).7 Itä-Aasian kirjallisuus ilmoitti gramnegatiivisten organismien olevan yleisin syy (70 prosenttia) ja Klebsiellan olevan yleisin aiheuttava organismi (60 prosenttia).9 Pohjois-Amerikasta ja Euroopasta saadut tiedot osoittivat gramnegatiivisten organismien kasvavan 32 prosentista vuonna 1986 52 prosenttiin vuonna 2003.6 hiivat ovat yleisempi syy ja liittyvät parempiin visuaalisiin tuloksiin verrattuna homeisiin sieni-endogeenisessä endoftalmiitissa.10,11 Candida on yleisin sieni-endogeenisen endoftalmiitin aiheuttaja.Immunosuppressiopotilailla, kuten AIDS-potilailla, epätyypillisillä organismeilla kuten Cryptococcus, Mycobacterium avium, Nocardia ja Pneumocystis jiroveci on otettava huomioon.
mukana olevassa silmässä voi olla kipua, punoitusta, kelluntaa tai näkökyvyn heikkenemistä. Diagnoosi viivästyy lapsipotilailla, koska oireita ei pystytä ilmoittamaan ajoissa. Kahdenvälinen esiintyminen on raportoitu 14-25 prosentissa tapauksista ja yleisemmin sienillä ja bakteereilla, kuten meningokokki, Escherichia coli ja Klebsiella.Endogeeninen endoftalmiitti voi olla aluksi yksipuolinen ja sen jälkeen kehittyä kanssasilmässä. Bakteeri-tai sieni-infektiot voivat ilmetä iiris mikroabscess, hypopyon, eri asteita lasiaisen haze, diskreetti verkkokalvon kyhmyt, perivaskulaarinen verkkokalvon verenvuoto, arteriolaarinen emboli tai nekroottinen verkkokalvo. Vaikeat tapaukset voivat johtaa panoftalmiittiin. Suklaanruskean eritteen esiintyminen etukammiossa viittaa bacilluksen olevan vastuussa oleva organismi, kun taas Listeria on ominaista ruskealle hypopyonille ja Serratia punaiselle hypopyonille.
Candida-sienen endogeenisessä endoftalmiitissa voi olla kuohkeita palloja lasiaisessa, korioretiniitissa, hypopyonissa, perivaskuliitissa, optikusneuriitissa tai korioretinaalisissa leesioissa (kermaisia, syviä ja hyvin rajattuja). Infektio muotit kuten Aspergillus on enemmän fulminantti, tyypillisesti rajoittuu subretinal tilaa ja voi olla chorioretinal leesioita (confluent kanssa epäselviä marginaalit), intraretinal hemorrhages, verisuonten tukos tai koko paksuus verkkokalvon nekroosi. Positiivisia lasimaisia aspiraatioviljelmiä on vaikeampi saada homeista kuin hiivoja, ehkä siksi, että homeissa lasiaista ei käytetä yhtä yleisesti kuin hiivoja.
endogeeninen endoftalmiitti saattaa jäljitellä sidekalvontulehdusta, ei-tarttuvaa anteriorista uveiittia, iriittiä, akuuttia glaukoomaa, selluliittia, kaihia ja erityisesti retinoblastoomaa lapsilla. Virheellisiä diagnooseja on ilmoitettu 16-63 prosentissa tapauksista, mikä viivästyttää diagnoosia ja asianmukaista hoitoa.6,12
endogeenisen endoftalmiitin diagnoosi tehdään tyypillisesti silmänsisäisestä näytteestä (vesipitoisesta tai lasiaisesta) saadun mikrobiologisen näytön perusteella. Positiiviset viljelmät verestä, aivo-selkäydinnesteestä tai mistä tahansa silmän ulkopuolisesta kohdasta voivat olla hyvin vihjaavia. Veriviljelmän positiivisuusaste vaihtelee suuresti, 33 prosentista 94 prosenttiin tapauksista.6, 8 koska paikallisia oireita ei esiinny, endogeenisen Aspergillus-endoftalmiitin diagnostisen verituoton on raportoitu olevan hyvin alhainen.14 viljelmää on kasvatettava sekä aerobisella että anaerobisella alustalla (suklaa-agar, lampaanveriagar ja Sabouraud agar), ja niitä on inkuboitava enintään kaksi viikkoa. Gram tahra käytetään yleisesti arvioida bakteerien. Sienikasvu voidaan vahvistaa Geimsa – tai Kalkkifluorivalkoisilla tahroilla. Kudosnäytteen polymeraasiketjureaktiotutkimus on nopea menetelmä vastuullisten organismien tunnistamiseksi, mutta sen haittana on, että sitä ei voitu käyttää antibiootti-tai sienilääkkeiden herkkyyden arvioimiseen.
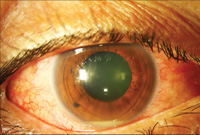
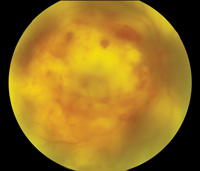
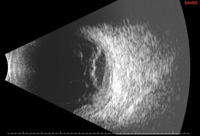
kuva 4. Nocardia endogeeninen endoftalmiitti. Ensimmäinen lasiaisbiopsia oli negatiivinen ja vain subretinaalibiopsia tuotti positiivisia viljelmiä. Ylimmässä kuvassa (4a) näkyy esitysvaiheessa oleva hypopyon. Keskimmäinen kuva (4b) näyttää silmänpohjan löydökset, mukaan lukien suuri submakulaarinen paise. B-scan ultraäänitutkimus (4c) osoittaa neurosensori irtoaminen ja submacular massa.
silmän ultraäänitutkimus B on tärkeä määritettäessä lasiaisen eritteiden laajuutta ja tyyppiä, kovakalvon paksuutta, suonikalvon abcessia ja verkkokalvon irtaumaa. Tietokonetomografia skannaa kiertoradalla auttaa tunnistamaan kiertoradan osallistuminen. Muut tutkimukset, kuten rintakehän röntgenkuvaus, ultraääni vatsa, CT vatsa, kaikukardiografia ja Gallium-67 skannaa voi auttaa tunnistamaan systeeminen painopiste infektio.
hoito
* bakteerin endogeeninen endoftalmiitti. Soon-Phaik Chee ja kollegat raportoivat, että systeemiset antibiootit voivat saavuttaa terapeuttisia pitoisuuksia silmässä johtuen häiriintyneestä verisilmäesteestä.1 kuitenkin systeemisiä aineita useimmiten täydennetään intravitreaalisilla mikrobilääkkeillä ja vitrectomylla, erityisesti näkyvän lasiaisen yhteydessä. Vankomysiini (1 mg/0, 1 mL) ja keftatsidiimi (2, 25 mg/0, 1 mL) ovat edelleen valittuja suonensisäisiä antibiootteja. Katsaustutkimuksen mukaan pars Planan vitrectomy-silmille tehdään kolme kertaa todennäköisemmin hyödyllinen näkö kuin niille, joille ei tehty vitrectomiaa.6 Myös nämä silmät vaativat kolme kertaa vähemmän sisälmysten poistoa tai enukleaatiota. Laajakirjoiset systeemiset antibiootit, kuten vankomysiini, siprofloksasiini, aminoglykosidit tai kolmannen sukupolven kefalosporiinit, olivat aiemmin hoidon päätekijä, mutta nyt niitä käytetään paikallisen hoidon ohella. Suositellut antibiootit ovat laajakirjoisia antibiootteja, jotka kattavat suurimman osan grampositiivisista ja negatiivisista organismeista. Systeemiset antibiootit ovat tyypillisesti jatketaan vähintään kolme-neljä viikkoa tai kuin ekstraocular infektio potilaan sanelee.
* sieni-endogeeninen endoftalmiitti. Hoito riippuu silmäoireiden laajuudesta. Pelkkä systeeminen hoito riittää, kun infektio on eristetty verkkokalvolle ja suonikalvoon. Systeemisen hoidon yhteydessä suositellaan vitrectomiaa ja intravitreaalista sienilääkettä.
laskimoon annettu amfoterisiini-B on klassisesti valittu lääkeaine, mutta sen systeemisen toksisuuden vuoksi sitä on seurattava tarkoin. Suun kautta otettavaa vorikonotsolia tai flukonatsolia käytetään yhä enemmän yhdessä paikallisen hoidon kanssa. Joko vorikonatsoli-injektio silmän lasiaiseen (100 µg / 0.1 ml) tai amfoterisiini-B (5-10 µg/0, 1 ml) takaa välittömästi riittävän sienilääkepitoisuuden takasegmentissä. Vorikonatsolilla voi olla parempi kattavuus Aspergillus-lajeilla ja joillakin Candida-lajeilla (kuten C. glabrata ja C. krusei), joissa flukonatsoli tai amfoterisiini-B eivät tehoa. Uudemmilla sienilääkkeillä, kuten posakonatsolilla, ekinokandiineilla, mikafungiinilla, kaspofungiinilla ja anidulafungiinilla, on heikko silmän läpäisy, eikä niitä suositella käytettäväksi endoftalmiitin hoidossa.16 Vitrectomia auttaa vähentämään infektiokuormaa ja parantamaan sienilääkkeiden saatavuutta silmänsisäisiin rakenteisiin. Toistuvien intravitreaali-injektioiden tarpeen tulee perustua kliiniseen paranemiseen, silmän tilaan (vitrectomized vs non-vitrectomized) ja sienilääkkeen farmakokinetiikkaan.
paikallisia tai systeemisiä kortikosteroideja vältetään yleensä sieni-endoftalmiitin hoidossa,10 joskin niiden käyttö on edelleen kiistanalaista.14,15
tulos
endogeenisten endoftalmiittitapausten näkökyky on yleensä huono. Näöntarkkuus laskee sormia tai enemmän on raportoitu 22.2-41 prosenttia tapauksista.17,18 sokeudesta, suolistosta tai enukleaatiosta johtuvaa näön menetystä on raportoitu 55-69 prosentissa tapauksista.6 endogeenisen Aspergillus-Endoftalmiitin näkökyky hoidon jälkeen on huonompi Candida-tapauksiin verrattuna, ja se voi johtua Candida-infektion aikaisemmasta toteamisesta, mikä johtaa hoidon oikea-aikaisempaan aloittamiseen.15
potilailla, joilla on silmän ulkopuolisia bakteeri-infektiopesäkkeitä, on raportoitu kuolleisuus 5-32 prosenttia.19 tekijät, kuten infektio virulent organismien, huono isäntä puolustus, väärä diagnoosi johtaa viivästynyt hoito, riittämätön hoito, käyttö sopimattomia antibiootteja, panoftalmiitti katsotaan liittyvän huono ennuste. Sieni-infektioon liittyy korkea kuolleisuus, ja systeemisen Candida-infektion kuolleisuus on 7 prosenttia.
endogeeninen endoftalmiitti on mahdollisesti tuhoisa silmätulehdus, joka on diagnosoitava ja hoidettava nopeasti. Yhdistelmäantibioottien ja systeemisten antibioottien käyttö on yleistä. Systeeminen samanaikainen infektio on yleinen ja siihen liittyy korkea kuolleisuus.
tohtori Relhan on Vireoretinaalisten sairauksien ja uveiitin tutkija Bascom Palmer Eye-Instituutissa. Hän oli aiemmin nuorempi konsultti lasiaisleikkauksessa LV Prasad Eye Institutessa Hyderabadissa Intiassa. Dr. Albini on kliinisen silmätautiopin apulaisprofessori, joka on erikoistunut vitreoretinaalisiin sairauksiin ja uveiittiin Bascom Palmer Eye Institutessa. Flynn on silmälääketieteen professori, joka on erikoistunut silmäleikkauksiin Bascom Palmerissa. Tiedustelut tulisi suunnata Dr. Albinille osoitteeseen [email protected].
1. Chee SP, Jap A. endogeenisen endoftalmiitin. Curr Opinophthalmol 2001;12(6): 464-70.
2. Rachitskaja AV, Flynn HW, Davis JL. Endogeeninen endoftalmiitti, jonka aiheuttaa salmonellan serotyyppi B immunokompetentilla 12-vuotiaalla lapsella. Arch Ophthalmol 2012; 130 (6):802-4. doi: 10.1001/archofthalmol.2011.1862.
3. Chaudhry IA, Shamsi FA, Al-Dhibi H, Khan AO. Pediatric endogenetic bacterial endophthalmitis: Case report and review of the literature. J AAPOS 2006;10(5): 491-3. Epub 2006 Syys 7.
4. Flynn HW Jr. endogeenisen endoftalmiitin kliininen haaste. Retina 2001;21(6): 572-4.
5. Okada AA, Johnson RP, Liles WC, D ’ Amico DJ, Baker AS. Endogeenisen bakteerin endophthalmitis-Report of a ten-year retrospective study. Ophthalmology 1994;101: 832-8.
6. Jackson TL, Eykyn SJ, Graham EM, Stanford MR (2003). Endogeenisen bakteerin endoftalmiitti: a 17-year prospective series and review of 267 reported cases. Surv Ophthalmol 2003; 48(4): 403-23.
7. Wu ZH, Chan RP, Luk FO, Liu DT, Chan CK, Lam DS, Lai TY. Endogeenisen Endoftalmiitin kliinisten ominaisuuksien, mikrobiologisen spektrin ja hoitotulosten tarkastelu 8 vuoden ajalta. J Oftalmol 2012:265078. doi: 10.1155/2012/265078. Epub 2012 23.Helmikuuta.
8. Schiedler V, Scott IU, Flynn HW Jr, Davis JL, Benz MS, Miller D. Culture-todistettu endogeeninen endoftalmiitti: kliiniset ominaisuudet ja näöntarkkuuden tulokset. Am J Oftalmol 2004;137: 725-31.
9. Wong JS, Chan TK, Lee HM, Chee SP. Endogeeninen bakteeriperäinen endoftalmiitti: itäaasialainen kokemus ja vakavan silmävaivan uudelleenarviointi. Ophthalmology 2000;107: 1483-91.
10. Lingappan A, Wykoff CC, Albini TA, Miller D, Pathengay A, Davis JL, Flynn HW Jr. endogeeninen sieni-endoftalmiitti: Aiheuttaja-organismit, hoitostrategiat ja näöntarkkuuden tulokset. Am J Oftalmol 2012;153: 162-6.e1. doi: 10.1016 / J.ajo.2011.06.020. Epub 2011 Syys 13.
11. Sridhar J, Flynn HW Jr, Kuriyan AE, Miller D, Albini T. endogeeninen sieni-endoftalmiitti: Home-ja hiivatulehdusten riskitekijät, kliiniset ominaisuudet ja hoitotulokset. 2013; Sep 20; 3 (1): 60. doi: 10.1186 / 1869-5760-3-60.
12. Binder MI, Chua J, Kaiser PK, Procop GW, Isada CM. Endogeeninen endoftalmiitti: 18-vuotinen katsaus viljelmäpositiivisiin tapauksiin kolmannen asteen hoitolaitoksessa. Lääketiede (Baltimore) 2003;82(2):97-105.
13. Rao NA, Hidayat AA. Endogeeninen mykoottinen endoftalmiitti: kliinisten ja histopatologisten muutosten muutokset kandidiaasissa verrattuna aspergilloosiin. Am J Oftalmol 2001;132(2): 244-51.
14. Weishaar PD1, Flynn HW Jr, Murray TG, Davis JL, Barr CC, Gross JG, Mein CE, McLean WC Jr, Killian JH. Endogeeninen Aspergillus endoftalmiitti. Kliiniset ominaisuudet ja hoitotulokset. Ophthalmology 1998;105: 57-65.
15. Brod RD, Flynn HW, Miller D. endogeeninen sieni-endoftalmiitti. Julkaisussa: Duane ’ s clinical oftalmology. Hagerstown: Harper and Row; 2004. CD-ROM. ch 11
16. Bouza E1, Cobo-Soriano R, Rodríguez-Créixems M, Muñoz P, Suárez-Leoz M, Cortés C. mahdollinen haku silmän vaurioita sairaalahoidossa potilailla, joilla on merkittävä bakteremia. Clin Infect Dis 2000; 30(2): 306-12.
17. Riddell J 4th1, Comer GM, Kauffman CA. Endogeenisen sieni-endoftalmiitin hoito: keskitytään uusiin sienilääkkeisiin. Clin Infect Dis 2011; 52 (5): 648-53. doi: 10, 1093 / cid / ciq204. Epub 2011 Tammi 16.
18. Greenwald MJ, wohl LG, Sell CH. Metastaattinen bakteeri endoftalmiitti: nykyaikainen uudelleenarviointi. Surv Ophthalmol 1986;31(2): 81-101.
19. Chen YJ1, Kuo HK, Wu PC, Kuo ML, Tsai HH, Liu CC, Chen CH. Endogeenisen endoftalmiitin tulosten 10-vuotinen vertailu: itäaasialainen kokemus Klebsiella pneumoniae-infektiosta. Retina 2004;24(3): 383-90.
20. Menezes AV1, Sigesmund DA, Demajo WA, Devenyi RG. Candida endoftalmiittia sairastavien sairaalapotilaiden kuolleisuus. Arch Intern Med 1994;154(18): 2093-7.
