last modified: Sunday, 08-Nov-2009 04:44:32 CET
Document status: complete
Quartz is a complete of one part pii and two parts of happi, piidioksidi, SiO2. Sen kemiallisen koostumuksen (ja alkuaineen pii, Si) löysi ruotsalainen kemisti Jöns Jakob Berzelius vuonna 1823. Piidioksidia kutsutaan yleisesti piidioksidiksi.
IUPAC: n mukaan seuraavat kaksi nimeä ovat oikein: piidioksidi ja dioksosilaani.
![]()
10mm![]()
1040×800 193kb – 2080×1600 684kb
Tämä on pieni pala teollisesti tuotettua puhdasta piitä. Se on kevyt (tiheys 2,328 g/cm3), harmaa kiteinen aine, jolla on vahva metallinen kiilto. Se on erittäin kovaa (noin yhtä kovaa kuin kvartsi ja paljon kovempaa kuin useimmat metallit), mutta hauras ja ei muokattavaksi kuten metallit. Pii on puolijohdeteollisuuden perusta: puhdas pii on vain heikko sähkön johdin, mutta kun siihen lisätään pieniä määriä sopivia alkuaineita (pii on seostettu), sen johtavuus lähestyy metallin johtavuutta, ja valitsemalla hivenaineiden tyyppi ja määrä, seostetun piin sähköisiä ominaisuuksia voidaan kontrolloida.
reaktiot
huoneenlämpötilassa SiO2 on kaikissa muunnoksissa lähes inertti eikä reagoi useimpien muiden aineiden kanssa. Jopa kohtalaisen korkeissa lämpötiloissa piidioksidi on kemiallisesti hyvin stabiilia. Tästä syystä sulatettua kvartsia (piidioksidilasia) käytetään laajalti kemiallisissa laitteissa, erityisesti silloin, kun tavallisen lasin metallikationien katalyyttisiä reaktioita on vältettävä. Syynä piidioksidin alhaiseen reaktiivisuuteen on hyvin vahva Si-O-sidos, mutta myös sen makromolekyylinen rakenne.
koska itse happo (ortosiilihappo, H4SiO4) on anhydriitti, hapot eivät yleensä hyökkää kvartsia vastaan. Merkittävä poikkeus on fluorivetyhappo, HF, joka hajottaa kvartsia muodostaen ensin piifluoridia SiF4, sitten fluorivetyhappoa:
SiO2 + 6 HF → H2SiF6 + 2 H2O
SiO2: n kimppuun hyökkäävät myös emäksiset aineet (kuten kaliumhydroksidi, KOH). Reaktion nopeus riippuu muunnoksesta ja kidekoosta: kiteinen kvartsi liukenee vain hyvin hitaasti kuumiin vetisiin emäksisiin liuoksiin, kun taas amorfinen SiO2 liukenee helposti huoneenlämpötilassa:
reaktiolla on merkitystä kerääjälle, sillä emäksisiä liuoksia ja pesuaineita käytetään joskus sammalten ja jäkälien poistamiseen mineraalinäytteestä. Kvartsikiteet eivät yleensä ole ongelma, mutta olisin erittäin varovainen, kun puhdistan kryptokiteisiä lajikkeita.
samankaltainen reaktio johtaa betonin silikageelien muodostumiseen, kun betonin emäksiset yhdisteet, tyypillisesti Ca(OH)2, reagoivat amorfisen piidioksidin ja kryptokiteisen kvartsin (eli opaalin ja kalkedonin) kanssa. Silikageeli vetää puoleensa vettä, turpoaa ja särkee betonin muutamassa vuosikymmenessä.
kaikki piidioksidin muodot liukenevat sulaan natroniin (Na2CO3) tai potaskaan (K2CO3) muodostaen silikaatteja:
monien geologisten ympäristöjen korkeissa lämpötiloissa kvartsi toimii happona ja reagoi monien emäksisten mineraalien kanssa. Tunnettu esimerkki on mineraalin wollastoniitin ca3si3o9 muodostuminen kvartsista ja kalsiitista kontaktissa metamorfisissa prosesseissa noin 600°C: sta ylöspäin:
3 SiO2 + 3 CaCO3 → Ca3si3o9 + 3 CO2
päinvastainen reaktio tapahtuu silikaattikivien rapautuessa, tässä esimerkiksi meteorivesissä esiintyvä hiilihappo H2CO3 vapauttaa piihappoa ja muodostaa karbonaatteja.
kvartsi on piin ”Malmi”. Pii noudetaan noin 2000°C: n lämpötilassa seuraavassa endotermisessä (energiaa kuluttavassa) reaktiossa:
Si-O-sidos on paljon voimakkaampi kuin C-O-sidos, ja reaktio toimii vain, koska hiilimonoksidi CO karkaa systeemistä kaasuna, joten systeemin tasapaino työntyy oikealle puolelle. Hiilimonoksidin muodostuminen hiilidioksidin CO2 sijasta on tyypillistä pelkistävissä reaktioissa hiilen kanssa korkeissa lämpötiloissa. Tässä prosessissa muodostunut pii ei ole tarpeeksi puhdasta sirujen valmistukseen, ja se on puhdistettava melko monimutkaisessa menettelyssä. Puhdas pii on siis malmiensa runsaudesta huolimatta suhteellisen kallista.
liukoisuus veteen
piidioksidin liukoisuus veteen riippuu lämpötilasta, paineesta, sen pintarakenteesta ja sen rakenteellisesta modifikaatiosta. Seuraavassa taulukossa esitetään yhteenveto liukoisuudesta huoneenlämmössä ja normaalipaineessa.
tiedot:
– ➛Hollemann & Wiberg, 1985
– ➛Rykart, 1995
huoneenlämpötilassa kvartsi on käytännössä veteen liukenematonta. Vesijohtovesi on yleensä lähes kyllästetty liuenneella piidioksidilla (kvartsin suhteen), ja liukeneminen on hyvin hidasta, joten ei tarvitse huolehtia kvartsikiteiden vaurioitumisesta toistuvassa puhdistuksessa.
kuitenkin piidioksidin liukenemisella kallioperään ja maaperään on tärkeä rooli kuumassa kosteassa ilmastossa. Lateriittimaiden muodostuminen liittyy siihen, että piidioksidi huuhtoutuu vähitellen pois pintakerroksista ja rikastuu yhdisteillä, jotka – ainakin näissä ilmasto – olosuhteissa-liukenevat vähemmän veteen, kuten rauta-ja alumiinioksidit.
yli 100°C: n lämpötiloissa ja suurissa paineissa kvartsin liukoisuus kasvaa nopeasti. 300°C: ssa se on 700-1 200 mg/l paineesta riippuen.
SiO2 liukenee veteen muodostaen ortosiilihappoa, H4SiO4:
Ortosiilihappo on hyvin heikko happo, heikompi kuin esimerkiksi hiilihappo. Se hajoaa pK1: n kanssa 9.51 mukaan
H4SiO4 + H2O ↔ H3SiO4- + H3O+
vetisessä liuoksessa ei ole SiO2-molekyylejä tai SiO4-tetraedrin aggregaatteja. Käänteinen reaktio on tapa, jolla kvartsikiteet kasvavat, mutta h4sio4-molekyyli ei voi yksinkertaisesti hävittää 2 molekyyliä vettä, se tarvitsee toisen h4sio4-molekyylin tai jo olemassa olevan piidioksidimolekyylin, jonka hydroksyyli (- OH) – pääte on:
Ortosiilihappo on stabiili vain laimennetussa vetisessä liuoksessa, puhdasta happoa ei voida erottaa. Ortosiilihapon kiinnostavin ominaisuus on sen taipumus polymeroitua vetisissä liuoksissa muodostaen ensin Solin ja myöhemmin monikiteisten happojen geelin: ortosiilihappomolekyylit kondensoituvat suuriksi molekyyleiksi reaktioiden mukaan ja . Heti kun alat konsentroida h4sio4-liuosta, molekyylit polymeroituvat. Huoneenlämmössä laboratorio-olosuhteissa tämän prosessin päätepiste on amorfisen piidioksidin muodostuminen. Polymeroituneen piihapon geelit ovat todennäköisesti myös opaali-ja kryptokiteisten kvartsilajikkeiden (kalsedonia laajemmassa merkityksessä) edeltäjiä luonnossa.
piidioksidin perusrakenne
SiO2 tapahtuu peräti 13 erilaisessa rakenteellisessa muutoksessa. Niiden kiderakenteet (jos niitä on) saattavat erota toisistaan, mutta niillä kaikilla on joitakin perusominaisuuksia. Seuraava koskee kaikkia piidioksidin muunnoksia, ellei toisin mainita. Kvartsille ominainen molekyylirakenne käsitellään lukurakenteessa.
piidioksidin kemialliset sidokset ovat kovalenttisia: ne perustuvat molekyyliorbitaaleihin, joissa atomit jakavat 2 elektronia (toisin kuin ionisidokset, joita esiintyy suoloissa fluoriittina tai pöytäsuolana; tässä elektronit siirtyvät alkuaineesta toiseen muodostaen ioneja, joilla on vastakkainen sähkövaraus, ja kiteessä nämä ionit pysyvät yhdessä sähköstaattisen vetovoiman avulla).
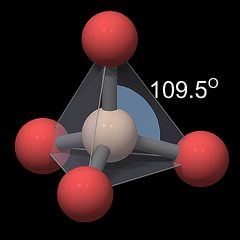
Fig.1: SiO4-tetraedri
viikuna.2

Fig.3: SiO4-Ionisidosmalli
perusrakenneosa lähes kaikissa piidioksidin modifikaatioissa (poikkeuksena ovat hyvin korkeapaineiset modifikaatiot) on SiO4-yksikkö, jossa keskeistä piiatomia ympäröi neljä happiatomia.
. |O| - | - .O-Si-O. - | - |O| .
tämän yksikön geometria esitetään pallo-ja tikkurenderöinnissä kuviossa.1, jossa pii symboloi norsunluun värinen, happi punainen pallo, ja kemialliset sidokset harmaat putket niiden välillä. Atomien kokoa ei saa skaalata. Happiatomit ovat piiatomin ympärillä sijainneissa asemissa, jotka pitävät ne mahdollisimman kaukana toisistaan, joten ne muodostavat tetraedrin neljä kulmaa, joita läpikuultava harmaa pyramidi symboloi. Huomaa, että happiatomit eivät ole yhteydessä toisiinsa, vaan niiden väliset harmaat viivat on piirretty vain tetraedrisen geometrian visualisoimiseksi. Keskeisten O-Si-O-sidosten kulma on hyvin lähellä arvoa ideaalisessa tetraedrissa (109,5°, harmaansininen kaari Viikunassa.1), jossa piihapen etäisyys on noin 0.161 nm kaikille happiatomeille, joten yksittäisen tetraedrin symmetria on lähes kuutiollinen.
Si-O-sidos on erittäin polaarinen, ja elektroneja vetää enemmän puoleensa happi, mikä johtaa sähkövarausten epätasaiseen jakautumiseen tetraedrin sisällä: kulmat ovat negatiivisemmat, keskusta on positiivisesti varautunut.
yksittäisiä molekyylejä, jotka on rakennettu kuten O=Si=O (joiden lineaarinen rakenne muistuttaa hiilidioksidin CO2: ta), löytyy vain SiO2-kaasusta yli 2500°C: n lämpötilassa.
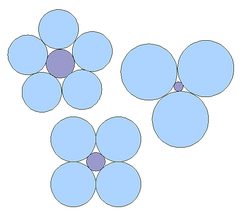
monet oppikirjat selittävät SiO4-tetraedrin ja muiden mineraalirakenteiden geometriaa, joka määräytyy eri ionien suhteellisten kokojen mukaan, kuten kuvassa esitetään.2:Mitä suurempi on Keski-ionin suhteellinen koko, sitä enemmän vastakkaisen varauksen ioneja tarvitaan sen sulkemiseen. Niinpä SiO4 – tetraedri piirretään usein neljän suuren O2-anionin ympäröimänä pienenä Si4+ kationina (Kuva.3). Voidaan väittää, että tämä on epätarkka: Pii ja happi ovat yhteydessä toisiinsa liittyneiden elektroniorbitaalien polaarisilla kovalenttisilla sidoksilla, joten ne muodostavat yksikön, eivätkä ole samalla tavalla erotettuja ja vapaasti liikuteltavia kuin suolan ionit. Yhdisteitä, joissa on Si4+ – ioneja, ei itse asiassa ole olemassa. Kokeellisten havaintojen tulkinnassa on jonkin verran vaihtelua, ja vaikka jotkut kirjoittajat pitävät Si-O-sidosta ensisijaisesti kovalenttisena, toiset painottavat sidoksen ionisia ominaisuuksia. Katsauksen, katso Gibbs et al., 1994 ja Cohen 1994.,
| | O O | | -O-Si-O-Si-O- | | | | O O O O | | | |-O-Si-O-Si-O-Si-O-Si-O- | | | | O O O O | | | | -O-Si-O- | O |
Fig.4: Silikaverkosto
happi on kaksiarvoinen, ja tetraedrin kulmien happiatomit ovat kukin sidoksissa viereisen tetraedrin toiseen piiatomiin. Kvartsia ja yleensä piidioksidia voidaan siis kuvata toisiinsa kytkeytyvien SiO4-tetraedrien kolmiulotteisena verkostona. Kaaviokuva sen rakenteesta kemiallisissa symboleissa on esitetty kuvassa.4. Yksityiskohtaisempia lukuja kvartsimolekyylirakenteesta löytyy lukurakenteesta.
| Fig.5 | 480×640 29kb |
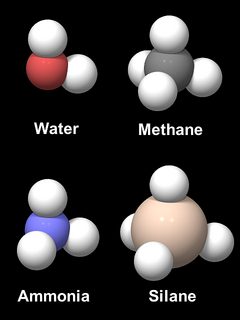
Fig.6
kaksi tetraedriä yhdistävä si-O-Si-sidos ei ole suora (180°), vaan muodostaa kvartsissa 144°: n kulman (Kuva.5). Tämän seurauksena kvartsin yleinen kiderakenne on melko monimutkainen. Muissa piidioksidimodifikaatioissa tämä kulma on erilainen, kun taas SiO4-tetraedrin sisällä olevat (o-Si-O-sidoksen määrittelemät) kulmat pysyvät periaatteessa samoina. Seuraavassa taulukossa on lueteltu muutaman piidioksidimuunnoksen kulmat ja etäisyydet.
tiedot:
➛Hollemann & Wiberg, 1985
➛Rykart, 1995
mittaus jmol: lla yksikkösolukoordinaattien perusteella.
hapella on luontainen taipumus muodostaa kulmikas X-O-X-sidos, kuten sen naapureilla alkuaineiden jaksollisessa järjestelmässä. Kuvassa 6 on mallit neljästä vetyyhdisteestä, jotka ovat vesi (H2o), metaani (CH4),ammoniakki (NH3) ja silaani (sih4). Atomien väliset etäisyydet ja C: n, N: N, O: n ja Si: n suhteelliset koot ovat suuruusluokkaa, mutta vetyatomit ovat ylimitoitettuja luettavuuden vuoksi. CH4-ja SiH4-molekyylit ovat ilmeisesti tetraedrisiä. NH3 ja H2O ovat lähes metaanimolekyylin muotoisia, joista on poistettu 1 tai 2 vetyatomia, joiden h-O-h-kulma on 104,5° ja h-N-h-kulma 106,8°. Syy samankaltaisuuteen on sidoselektroniorbitaalien eli neljän niin kutsutun SP3-hybridiorbitaalin geometria, jotka muodostavat tetraedrin. Piissä esiintyy myös neljän SP3-hybridiorbitaalin tetraedrijärjestely, joka on pääsyy tetraedrimuotoon ja SiO4-yksikön jäykkyyteen piidioksidissa ja silikaateissa.
tästä voisi odottaa si-O-Si-kulman olevan pienempi, joten miksi se on avoimempi? Ensinnäkin, koska Si-O-sidos on erittäin polaarinen ja happiatomit ovat negatiivisesti polarisoituneita, SiO4-ryhmien välillä on vastenmielisiä voimia, ja suora Si-O-Si pitäisi happiatomit suuremmalla etäisyydellä. Lisäksi si-O-sidoksen pituus on lyhyempi kuin yhdelle sidokselle laskettu: arvon pitäisi olla 0,181 nm, mutta se on itse asiassa noin 0,161 nm kvartsissa ja sillä on samanlaiset arvot muissakin piidioksidimodifikaatioissa. Tämä on osoitus tämän sidoksen osittaisesta kaksinkertaisesta sitomisesta (Hollemann & Wiberg, 1985), mikä selittäisi myös sen suuren vahvuuden . Tämä kaksoissidos on odotettua suuremman si-O-Si-kulman mukainen (144° sijasta 109,5°). Huomaa, että si-O-etäisyys on β-tridymiitissä Lyhin, ja tämän muunnoksen si-O-Si-kulma on 180°. Osittaisen kaksoissidonnaisuuden taustalla oleva teoria on melko monimutkainen, enkä mene siihen sen enempää.
piidioksidi ja silikaatit
vaikka kemiallisesti puhuttu piidioksidi on oksidi, Angloamerikan mineralogisessa kirjallisuudessa kvartsi ja kaikki muut piidioksidin muunnokset luokitellaan yleensä silikaateiksi (Danan laatiman luokittelujärjestelmän perusteella). Perustelu kvartsin kutsumiselle silikaatiksi on se, että se rakentuu SiO4-tetraedrin verkostosta. Silikaatit luokitellaan sen mukaan, miten SiO4-tetraedri integroituu kiderakenteeseen ja jos ja miten tetraedri liittyy toisiinsa, ja sen mukaan kvartsia kutsutaan tektosilikaatiksi (”verkostosilikaatti ”tai”kehyssilikaatti”).
silikaatti on piihappojen ja yhden tai useamman metallin suola. Ortosiilihappo, H4SiO4, on vain yksinkertaisin muoto, muut piihapot on valmistettu useista toisiinsa liittyneistä SiO4-yksiköistä, joihin on liitetty vetyä.
voisi ajatella, että silikaatteja muodostuu metallihydroksidin ja ortosiilihapon reagoidessa, kuten
, mutta näin silikaatteja ei luonnossa yleensä muodostu. Silikaatteja voi muodostua metallioksidin tai karbonaatin reagoidessa piidioksidin kanssa, kuten
vastaavat reaktiot tapahtuvatkin luonnossa, wollastoniitin muodostuminen metamorfisissa prosesseissa on jo mainittu (reaktio ). Silikaattien normaali muodostumistapa on kuitenkin transformaatio: silikaatit reagoivat keskenään muodostaen uusia silikaatteja. Kun SiO4-tetraedri on muodostunut, se ei hajoa helposti, ja sitä voidaan käyttää vain reaktioissa uusien tetraedrin renkaiden, ketjujen, levyjen tai verkkojen muodostamiseen. Vain hyvin harvoin ja hyvin erikoisissa ympäristöissä voidaan löytää piitä ei-silikaattimineraaleista.
kvartsikiteiden puhtaus
toisin kuin useimmat mineraalit, kirkas kvartsikide on aina kemiallisesti puhdas, SiO2-pitoisuus lähestyy 99,5%, usein enemmän. Tähän on periaatteessa kaksi syytä.
ensinnäkin kvartsilla on makromolekyylinen rakenne. Se ei sisällä jonkin alkuaineen eristettyjä ioneja, jotka voitaisiin helposti korvata toisella alkuaineella. Jos esimerkiksi suola (sähköstaattisten voimien yhdessä pitämistä eristetyistä ioneista koostuva yhdiste) kasvaa vetisessä liuoksessa, sen ionit voidaan korvata lähes mielivaltaisesti, kunhan korvaavien ionien koolla ja varauksella on sama arvo. Kun kvartsi kasvaa vetisestä liuoksesta, kasvupinnalla ei ole kirjaimellisesti mitään ”houkuttelevaa” liuoksen muihin ioneihin verrattuna. Vain jos esimerkiksi an – ryhmän yksikkö on rakennettu SiO4-yksikön sijaan, rakenne saa sähköisesti epätasapainon ja mahdollistaa ylimääräisen pienen monovalenttisen kationin (useimmiten H+, mutta myös Na+ tai Li+). Vain muutama alkuaine täyttää kriteerit toimia piin korvaajana SiO4-yksikössä, kuten alumiini in -, fosfori in + tai rauta in-ja käynnistää uusien ionien sisällyttämisen. Mielenkiintoista on, että berliniitin mineraali AlPO4, joka voidaan tulkita kaavaksi O2, on kvartsin rakenteellinen isomorfi, jolla on lähes identtiset rakenne-ja symmetriaominaisuudet ja hyvin samanlaiset fysikaaliset ominaisuudet:
| kaava | kidejärjestelmä | tiheys | kovuus | taitekerroin | /tr> |
|---|---|---|---|---|---|
| Berliniitti | alpo4 | trigonaalinen | 2, 64 g/cm3 | 7 | 1, 524-1, 530 |
| α-kvartsi | trigonaalinen | 2, 65 g/cm3 | 7 | 1.544-1, 553 |
toiseksi SiO4-tetraedrin kolmiulotteinen verkko on melko jäykkä. Monet mineraalit voivat sietää suhteellisen suuria määriä tiettyjä muita atomeja ja / tai ioneja kidehilassaan ilman, että niiden fysikaalisissa ominaisuuksissa on suuria poikkeamia. Väri saattaa muuttua kokonaan, mutta kiteet näyttävät selkeiltä ja yhtenäisiltä, sillä kidehila on jonkin verran joustava tai tilava ja säilyttää alkuperäisen rakenteensa kokonaisuutena. Kvartsin kidehila on kuitenkin tiivis ja hyvin joustamaton (tehden siitä kovan mutta hauraan), ja vain hyvin pieniä määriä muita alkuaineita, joilla on pienet kationit (yleensä Li, Na, H), voidaan rakentaa kasvun aikana vääristämättä hilan rakennetta. Itse asiassa kvartsissa olevien monovalenttien kationien määrä on suurin piirtein verrannollinen alumiinin määrään. Kvartsi, joka sisältää suurempia määriä muita aineita, on läpikuultavaa tai läpinäkymätöntä ja usein tylsää, koska kide ”kasvaa” suljettujen mineraalien ympärille ja valo siroaa eri materiaalien rajoille.
tämä ei yleensä päde muihin piidioksidin muunnoksiin, ja näyttää siltä, että joidenkin niistä hivenaineiden läsnäololla on itse asiassa stabiloiva vaikutus niiden rakenteeseen.
mutta vaikka kirkkaiden kvartsikiteiden kokonaiskoostumus on huomattavan puhdas (ainakin verrattuna useimpiin muihin mineraaleihin), epäpuhtaudet eivät tyypillisesti jakaudu tasaisesti Kiteen sisällä. Yksittäisten alkuaineiden pitoisuudet voivat vaihdella suuruusluokkaa muutaman mikrometrin etäisyydellä. Esimerkiksi alumiinin pitoisuus voi vaihdella alle 5 ppma: n (miljoonasosan) ja 10000 ppma: n välillä yhden Kiteen sisällä (➛perny ym. 1992). Hivenainejakauman kuvio voidaan tehdä näkyväksi katodoluminesenssiksi kutsutulla tekniikalla: korkeaenergiset elektronisäteet (”katodisäteet”) aiheuttavat lyhytikäisiä luminesenssiefektejä, jotka voidaan kaapata tavalliselle kalvolle. Ohuista kristalliviipaleista otetuissa valokuvissa näkyy hieno laminaarinen kuvio. Kaikki kerrokset ovat samansuuntaisia kristallisivujen kanssa, jotka muistuttavat aaveita, joten tämä hivenaineiden jakautumisen kuvio johtuu kasvuympäristön nopeista muutoksista.
kemiallisesti puhdas ei edelleenkään useinkaan ole tarpeeksi puhdas teknisiin tarkoituksiin. Täydellinen, homogeeninen kide on yhtä läpinäkyvä kuin tyhjiö, mutta hivenaineet aiheuttavat vääristymiä ja vikoja kidehilaan, mikä puolestaan vaikuttaa optisiin ominaisuuksiin. Suurin osa kvartsiksi rakennetuista elementeistä (H, Li, Al, Na, Ti, Fe) on kaikkialla, joten piidioksidin edelleen puhdistaminen on monimutkaista ja kallista. Tästä syystä kvartsikerrostumat, joiden hivenainepitoisuus on alhainen, ovat edelleen haluttuja (KS. esimerkiksi ➛Larsen et al. 2000).
lisätietoja, kirjallisuutta, linkkejä
taulukko kvartsin ominaisuuksista löytyy osoitteesta mindat.org:
Another table at www.webmineral.com:
alaviitteet
1 IUPAC on järjestö, jonka tavoitteena on poistaa kemiallisesta nimikkeistöstä epäselvyyksiä ja hauskoja, mutta tuttuja nimiä kuten Knallsäure (saksaksi ”paukutteleva happo”, fulmiinihappo). Vanhat nimet ovat edelleen voimassa, kunhan ne ovat yksiselitteisiä.
2josta saattaisi tuntua houkuttelevalta tehdä joitakin kokeita vetyfluoridilla. Vetyfluoridi on erittäin vaarallinen aine. Etsi vain tapaus hyvästä toksikologian oppikirjasta; luennon jälkeen et halua koskea siihen edes tangolla. Vetinen liuos ei ole vahva happo (puhdas HF on), ja hajoamattomat pienet HF-molekyylit tunkeutuvat helposti ihoon ja sitovat soluissa olevaa kalsiumia muodostaen liukenematonta fluoriittia, CaF2: ta. Kalsium on välttämätöntä kaikkien kehon solujen eläville toiminnoille. Pieni tippa sormeen, joka jää huomaamatta, koska se ei heti satu, voi – jonkin viiveen jälkeen – aiheuttaa huomattavaa vahinkoa ja suurta kipua.
lasketaanpa nopeasti: 1 Mol HF = 20g. pisara (noin 50 µl) 20-prosenttisesta liuoksesta sisältää 0,00005 l x (200g/l) = 0,01 g.10 mg, se ei kuulosta paljolta.
1 Mol Ca = 40g ja 1 Mol F = 19g. 1 Ca sitoo 2 F, jolloin 40g Ca sitoo 38g F 40g HF: stä. 1 ml kehon kudosta sisältää noin 0, 1 Mg Ca, ja 0, 1 mg HF antaa sen saostua lähes kokonaan. Teoriassa 10 mg HF pienessä pisarassa voisi saostaa suurimman osan Ca: sta 100 ml: n kudokseen, tappaen kaikki siinä olevat solut.
ja Ei, En vastusta veden fluorausta (ei ironiaa tässä).
3meteorinen vesi viittaa siihen, että se on peräisin ilmakehästä, ei meteoriiteista. Kreikkalaiset luulivat tähdenlentojen tulevan samasta pallosta kuin pilvet: Tähtiä ja planeettoja pidettiin ikuisina olentoina, mitä pilvet ja tähdenlennot eivät ilmeisesti ole. Ajattele meteorologiaa.
4tämän vuoksi vulkaanisissa kivissä olevaan kvartsiin liittyy usein kalsiittia.
5This on jossain määrin vastavaikutteinen, mutta kylläinen liuos on termodynaamisessa tasapainossa Kiteen kanssa. Molekyylin liittyessä kiderakenteeseen muodostuu uusia sidoksia, ja kiderakenteen geometriasta riippuen vapautuu tai kuluu enemmän tai vähemmän energiaa. Aineen liuottamiseen tarvitaan sidosten hajottamiseen energiaa, mutta energiaa vapautuu myös vesimolekyylien suunnatessa kohti liuennutta molekyyliä ja muodostaessa uusia sähköstaattisia sidoksia (hydrataatioenergia). Stabiilimpi muunnos yhdisteestä on yleensä vähemmän liukeneva, koska sidosten katkeamiseen tarvitaan enemmän energiaa.
tällä ei ole mitään tekemistä reaktion nopeuden kanssa. Tietyissä olosuhteissa epävakaampi muunnos muodostuu ensin liuoksesta ja vasta myöhemmin se korvataan stabiililla muunnoksella: Kryptokrystinen kvartsi muodostuu tyypillisesti vetisestä liuoksesta, mutta cristobaliitin ja opaalin ollessa välivaiheita, koska reaktioiden kinetiikka puoltaa opaalin muodostumista. Ja kun laitat kvartsikiteen 1 litraan puhdasta vettä huoneenlämmössä, voit olla melko varma, että kun otat sen seuraavana päivänä, se ei paina 2,9 mg vähemmän. Todennäköisesti eroa on hyvin vaikea mitata. Ehkä kuukauden tai vuoden kuluttua.
6 kvartsin tetraedri ei itse asiassa ole täydellisesti isometrinen kuten ideaalinen tetraedri, vaan hieman vääristynyt, koska etäisyys keskeiseen piiatomiin on 0,16101 nm 2 happiatomille ja 0,16145 nm 2 muulle happiatomille. Tämä poikkeama ihanteellisesta muodosta on kuitenkin useimmissa käytännön tarkoituksissa vähäinen, sillä se on alle 0,3%.
7 si: n ja O: n hapetusluvut ovat vastaavasti +4 ja -2. Energia, joka tarvitaan 4 elektronin irrottamiseen Si: stä, on liian suuri, jotta se mahdollistaisi vakaan puhtaasti ionisidoksen. Jopa SiF4 on yhdiste, jossa on polaarisia, mutta kovalenttisia sidoksia fluorin korkeasta elektronegatiivisuudesta huolimatta. Mutta si4-anioniyhdisteitä on olemassa (kuten ca2si).
8rykart (1995) antaa α – kvartsille arvot 152,8° ja β-kvartsille 143,5°. Tämä näyttää olevan kirjoitusvirhe, arvot pitäisi vaihtaa.
9But it ’ s not true that ”anything goes”. Mineraalin muodostuessa sen kidehilaan rakentuu alkuaineita ja ioneja, kun ne täyttävät tietyt kriteerit, kuten tietyn varauksen, koon tai elektronegatiivisuuden, ja ovat siten samanlaisia kuin hilan jo muodostavat.
 Tulostinystävällinen versio
Tulostinystävällinen versio
