Última modificación: Domingo, 08-Nov-2009 04:44:32 CET
Estado del documento: completo
El cuarzo es un compuesto de una parte de silicio y dos partes de oxígeno, dióxido de silicio, SiO2. Su composición química (y el elemento silicio, Si) fue descubierto por el químico sueco Jöns Jakob Berzelius en 1823. El dióxido de silicio se denomina comúnmente sílice.
De acuerdo con la IUPAC, los dos nombres siguientes son correctos: dióxido de silicio y dioxosilano.
![]()
10mm ![]()
1040×800 193kb – 2080×1600 684kb
Esto es una pequeña parte de la producción industrial de silicio puro. Es una sustancia cristalina gris, ligera (densidad 2,328 g / cm3) con un fuerte brillo metálico. Es muy duro (casi tan duro como el cuarzo y mucho más duro que la mayoría de los metales), pero frágil y no maleable como los metales. El silicio es la base de la industria de semiconductores: el silicio puro es solo un conductor débil de electricidad, pero cuando se agregan pequeñas cantidades de elementos apropiados (el silicio está dopado), su conductividad se acerca a la de un metal, y al elegir el tipo y la cantidad de oligoelementos, se pueden controlar las propiedades eléctricas del silicio dopado.
Reacciones
A temperatura ambiente, el SiO2 en todas las modificaciones es casi inerte y no reacciona con la mayoría de las otras sustancias. Incluso a temperaturas moderadamente altas, la sílice es químicamente muy estable. Por esa razón, el cuarzo fundido (vidrio de sílice) se usa ampliamente para aparatos químicos, especialmente cuando se deben evitar las reacciones catalíticas de los cationes metálicos en vidrio ordinario. La razón de la baja reactividad de la sílice es el muy fuerte enlace Si-O, pero también su estructura macromolecular.
Siendo la anhidrita de un ácido en sí (ácido ortosilícico, H4SiO4), el cuarzo en general no será atacado por ácidos. La excepción prominente es el ácido fluorhídrico, HF, que descompondrá el cuarzo para formar primero fluoruro de silicio SiF4, luego ácido hidrofluorosilícico:
El SiO2 también es atacado por sustancias alcalinas (como hidróxido de potasio, KOH). La velocidad de la reacción depende de la modificación y del tamaño del cristal: El cuarzo cristalino se disolverá muy lentamente en soluciones alcalinas acuosas calientes, mientras que el SiO2 amorfo se disolverá fácilmente a temperatura ambiente:
La reacción es relevante para el colector, ya que a veces se usan soluciones alcalinas y detergentes para eliminar musgo y líquenes de muestras minerales. Los cristales de cuarzo generalmente no son un problema, pero tendría mucho cuidado al limpiar variedades criptocristalinas.
Una reacción similar conduce a la formación de geles de sílice en el concreto, cuando los compuestos alcalinos del concreto, típicamente Ca(OH)2, reaccionan con sílice amorfa y cuarzo criptocristalino (es decir, ópalo y calcedonia). El gel de sílice atrae el agua, hincha y agrieta el hormigón en unas pocas décadas.
Todas las formas de sílice se disuelven en natrón fundido (Na2CO3) o potasa (K2CO3) para formar silicatos:
A altas temperaturas de muchos entornos geológicos, el cuarzo actúa como ácido y reacciona con muchos minerales alcalinos. Un ejemplo bien conocido es la formación del mineral wollastonita Ca3Si3O9 a partir de cuarzo y calcita en procesos metamórficos de contacto a temperaturas de aproximadamente 600 ° C hacia arriba:
La reacción opuesta tiene lugar en la erosión de rocas de silicato, aquí el ácido carbónico H2CO3 presente, por ejemplo, en aguas meteóricas libera ácido silícico y forma carbonatos.
el Cuarzo es el «mineral» de silicio. El silicio se recupera a una temperatura de aproximadamente 2000°C en la siguiente reacción endotérmica (consumidora de energía):
El enlace Si-O es mucho más fuerte que el enlace C-O, y la reacción solo funciona porque el monóxido de carbono CO escapa del sistema como gas, por lo que el equilibrio del sistema se empuja hacia el lado derecho. La formación de monóxido de carbono en lugar de dióxido de carbono CO2 es típica de las reacciones reductoras con carbono a altas temperaturas. El silicio formado en este proceso no es lo suficientemente puro para la producción de chips y necesita purificarse en un procedimiento bastante complejo. Así que a pesar de la abundancia de su mineral, el silicio puro es relativamente caro.
Solubilidad en agua
La solubilidad del dióxido de silicio en el agua depende de la temperatura, la presión, su estructura superficial y su modificación estructural. La siguiente tabla ofrece una visión general de la solubilidad a temperatura ambiente y presión normal.
Datos de:
– Holl Hollemann & Wiberg, 1985
– Ry Rykart, 1995
A temperatura ambiente, el cuarzo es prácticamente insoluble en agua. El agua del grifo generalmente está casi saturada con sílice disuelta (con respecto al cuarzo), y el proceso de disolución es muy lento, por lo que no hay necesidad de preocuparse por que los cristales de cuarzo se dañen por la limpieza repetida.
Sin embargo, la disolución de sílice en lecho de roca y suelos juega un papel importante en climas cálidos y húmedos. La formación de suelos de laterita está relacionada con el lavado gradual de sílice de las capas superficiales y un enriquecimiento de compuestos que, al menos en esas condiciones climáticas, son menos solubles en agua, como los óxidos de hierro y aluminio.
A temperaturas superiores a 100°C y altas presiones, la solubilidad del cuarzo aumenta rápidamente. A 300°C está entre 700 y 1200 mg / l, dependiendo de la presión.
El SiO2 se disuelve en agua formando ácido ortosilícico, H4SiO4:
El ácido ortosilícico es un ácido muy débil, más débil que el ácido carbónico, por ejemplo. Se disocia con un pK1 de 9.51 de acuerdo con
No hay moléculas de SiO2 o agregados de tetraedros de SiO4 presentes en una solución acuosa. La reacción inversa es la forma en que crecen los cristales de cuarzo, pero una molécula de H4SiO4 no puede simplemente deshacerse de 2 moléculas de agua, necesita otra molécula de H4SiO4 o una molécula de sílice ya presente con una terminación hidroxil (-OH):
El ácido ortosilícico solo es estable en una solución acuosa diluida, no se puede extraer el ácido puro. La propiedad más interesante del ácido ortosilícico es su tendencia a polimerizarse en soluciones acuosas para formar primero un sol y luego un gel de ácidos polisilícicos: las moléculas de ácido ortosilícico se condensan en moléculas grandes de acuerdo con las reacciones y . Tan pronto como comience a concentrar una solución de H4SiO4, las moléculas se polimerizarán. A temperatura ambiente en condiciones de laboratorio, el punto final de este proceso es la formación de sílice amorfa. Los geles de ácido silícico polimerizado son probablemente también los predecesores de las variedades de ópalo y cuarzo criptocristalino (calcedonia en un sentido más amplio) en la naturaleza.
Estructura básica de sílice
El SiO2 se produce en no menos de 13 modificaciones estructurales diferentes. Sus estructuras cristalinas (si están presentes) pueden diferir, pero todas comparten algunas propiedades básicas. Lo siguiente se aplica a todas las modificaciones de sílice, excepto donde se indique. La estructura molecular específica del cuarzo se cubre en la Estructura del capítulo.
Los enlaces químicos en sílice son covalentes: se basan en orbitales moleculares en los que se comparten 2 electrones entre los átomos (a diferencia de los enlaces iónicos que se encuentran en sales como fluorita o sal de mesa; aquí los electrones se transfieren de un elemento a otro para formar iones de carga eléctrica opuesta, y en un cristal estos iones se mantienen unidos por atracción electrostática).
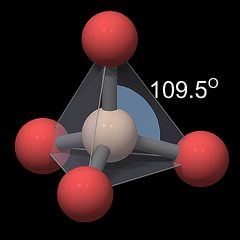
Fig.1: SiO4-Tetraedro
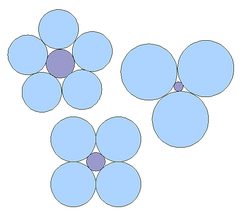
Fig.2

Fig.3: Modelo de Enlace SiO4-Iónico
El bloque de construcción básico en casi todas las modificaciones de sílice (las excepciones son modificaciones de muy alta presión) es la unidad SiO4, en la que un átomo de silicio central está rodeado por cuatro átomos de oxígeno.
. |O| - | - .O-Si-O. - | - |O| .
La geometría de esta unidad se muestra en una representación de bola y palo en la Fig.1, con silicio simbolizado por un color marfil, oxígeno por una esfera roja y enlaces químicos por tubos grises entre ellos. Los tamaños de los átomos no son a escala. Los átomos de oxígeno ocupan posiciones alrededor del átomo de silicio que los mantienen a la mayor distancia posible entre sí, por lo que forman las cuatro esquinas de un tetraedro, simbolizado por la pirámide gris translúcida. Tenga en cuenta que los átomos de oxígeno no están conectados entre sí, las líneas grises entre ellos solo se han dibujado para visualizar la geometría tetraédrica. El ángulo de los enlaces centrales O-Si-O es muy cercano al valor de un tetraedro ideal (109,5°, arco gris-azul en la Fig.1), con una distancia de oxígeno de silicio de aproximadamente 0.161 nm para todos los átomos de oxígeno, por lo que el tetraedro individual tiene una simetría casi cúbica.
El enlace Si-O es altamente polar, con electrones más atraídos por el oxígeno, lo que lleva a una distribución desigual de las cargas eléctricas en el tetraedro: las esquinas son más negativas, el centro está más cargado positivamente.
Moléculas individuales construidas como O = Si = O (con una estructura lineal como la del dióxido de carbono CO2) solo se pueden encontrar en un gas SiO2 a temperaturas superiores a 2500°C.
Muchos libros de texto explican la geometría del SiO4-tetraedro y otras estructuras minerales determinadas por los tamaños relativos de los diferentes iones, como se muestra en la Fig.2: Cuanto mayor es el tamaño relativo del ion central, más iones de carga opuesta son necesarios para encerrarlo. En consecuencia, el tetraedro SiO4 a menudo se dibuja como un pequeño catión Si4 + encerrado por cuatro aniones O2 grandes (Fig.3). Se puede argumentar que esto es inexacto: El silicio y el oxígeno están conectados por enlaces covalentes polares de orbitales de electrones unidos, por lo que forman una unidad, y no están separados de la misma manera y libremente movibles que los iones en una sal. De hecho, no existen compuestos con iones Si4+. Hay cierta variación en la interpretación de los hallazgos experimentales, y mientras algunos autores ven el enlace Si-O como principalmente covalente, otros enfatizan las características iónicas del enlace. Para una revisión, véase Gibbs et al., 1994 y Cohen, 1994.,
| | O O | | -O-Si-O-Si-O- | | | | O O O O | | | |-O-Si-O-Si-O-Si-O-Si-O- | | | | O O O O | | | | -O-Si-O- | O |
Fig.4: Red de sílice
El oxígeno es bivalente, y los átomos de oxígeno en las esquinas del tetraedro están vinculados a otro átomo de silicio en un tetraedro vecino. Por lo tanto, el cuarzo, y la sílice en general, se pueden describir como una red tridimensional de tetraedros SiO4 interconectados. Una vista esquemática de su estructura en símbolos químicos se muestra en la Fig.4. Las figuras más elaboradas de la estructura molecular del cuarzo se pueden encontrar en la Estructura del capítulo.
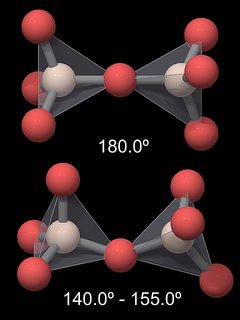
Fig.6
|
El enlace Si-O-Si que une dos tetraedros no es recto (180°), sino que forma un ángulo de 144° en cuarzo (Fig.5). Como resultado, la estructura cristalina general del cuarzo es bastante compleja. En otras modificaciones de sílice, este ángulo es diferente, mientras que los ángulos dentro del tetraedro SiO4 (definido por el enlace O-Si-O) permanecen básicamente iguales. La siguiente tabla enumera ángulos y distancias para algunas modificaciones de sílice.
Datos de:
Holl Hollemann & Wiberg, 1985
Ry Rykart,1995
Medición con JMol basada en coordenadas de celda unitaria.
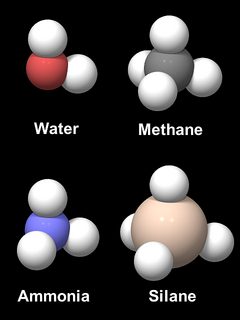
El oxígeno tiene una tendencia inherente a formar un enlace angular X-O-X, al igual que sus vecinos en el sistema periódico de elementos. La Figura 6 muestra modelos de cuatro compuestos de hidrógeno, agua (H2O), metano (CH4),amoníaco (NH3) y silano (SiH4). Las distancias interatómicas y los tamaños relativos de C, N, O y Si son a escala, pero los átomos de hidrógeno están sobredimensionados para su legibilidad. Las moléculas CH4 y SiH4 son obviamente tetraédricas. El NH3 y el H2O tienen casi la forma de una molécula de metano con 1 o 2 átomos de hidrógeno eliminados, con un ángulo H-O-H de 104,5° y un ángulo H-N-H de 106,8°. La razón de esta similitud es la geometría de los orbitales de electrones de unión, los cuatro llamados orbitales híbridos sp3, que forman un tetraedro. Una disposición tetraédrica de cuatro orbitales híbridos sp3 también se encuentra en el silicio y es la razón principal de la forma tetraédrica y la rigidez de la unidad SiO4 en sílice y silicatos.
De este se esperaría que el ángulo Si-O-Si fuera más pequeño, así que ¿por qué es más abierto? Por un lado, debido a que el enlace Si-O es altamente polarizado y los átomos de oxígeno están polarizados negativamente, hay fuerzas repulsivas entre los grupos SiO4, y un Si-O-Si recto mantendría los átomos de oxígeno a una mayor distancia. Además, la longitud del enlace Si-O es más corta que la calculada para un enlace simple: el valor debe ser de 0,181 nm, pero de hecho es de alrededor de 0,161 nm en cuarzo y tiene valores similares en otras modificaciones de sílice. Esto es una indicación de un carácter de doble enlace parcial de este enlace (Hollemann & Wiberg, 1985), lo que también explicaría su gran fuerza . Este doble enlace está de acuerdo con el ángulo Si-O-Si mayor de lo esperado (144° en lugar de 109,5°). Tenga en cuenta que la distancia Si-O es más corta en β-tridimita, y esta modificación tiene un ángulo Si-O-Si de 180°. La teoría detrás del carácter de doble encuadernación parcial es bastante compleja y no profundizaré en ella.
Sílice y silicatos
Aunque la sílice químicamente hablada es un óxido, en la literatura mineralógica angloamericana el cuarzo y todas las demás modificaciones de sílice generalmente se clasifican como silicatos (según un esquema de clasificación establecido por Dana). El razonamiento detrás de llamar al cuarzo silicato es que está construido por una red de tetraedros de SiO4. Los silicatos se clasifican de acuerdo con la forma en que los tetraedros de SiO4 se integran en la estructura cristalina y si y cómo los tetraedros están vinculados entre sí, y de acuerdo con ese cuarzo se llama tectosilicato («silicato de red» o «silicato de marco»).
Un silicato es una sal de ácidos silícicos y uno o varios metales. El ácido ortosilícico, H4SiO4, es solo la forma más simple, otros ácidos silícicos están hechos de varias unidades de SiO4 unidas con hidrógeno unido.
Se podría pensar que los silicatos se forman cuando un hidróxido metálico y ácido ortosilícico reaccionan, como
pero esta no es la forma en que los silicatos se forman normalmente en la naturaleza. Los silicatos se pueden formar cuando un óxido metálico o carbonato reacciona con sílice, como
Reacciones similares de hecho ocurren en la naturaleza, la formación de wollastonita durante los procesos metamórficos ya se ha mencionado (reacción ). Pero la forma normal de formación de silicatos es la de una transformación: los silicatos reaccionan entre sí para formar nuevos silicatos. Una vez que el tetraedro SiO4 se ha formado, no se rompe fácilmente, y solo se puede usar en reacciones para formar nuevos anillos, cadenas, láminas o redes de tetraedros. Solo muy raramente y en ambientes muy especiales se puede encontrar silicio en minerales no silicatos.
Pureza de los cristales de cuarzo
A diferencia de la mayoría de los minerales, un cristal de cuarzo transparente siempre es químicamente puro, con un contenido de SiO2 cercano al 99,5%, a menudo más. Básicamente, hay dos razones para ello.
En primer lugar, el cuarzo tiene una estructura macromolecular. No contiene iones aislados de algún elemento que podría ser fácilmente reemplazado por otro elemento. Si, por ejemplo, una sal (un compuesto hecho de iones aislados unidos por fuerzas electrostáticas) crece en una solución acuosa, sus iones podrían reemplazarse casi arbitrariamente siempre que el tamaño y la carga de los iones de reemplazo tengan un valor idéntico. Cuando el cuarzo crece de una solución acuosa, no hay literalmente nada «atractivo» en la superficie de crecimiento para otros iones en la solución. Solo si, por ejemplo, se incorpora una unidad de grupo en lugar de una unidad SiO4, la estructura se desbalancea eléctricamente y permite incluir un pequeño catión monovalente adicional (principalmente H+, pero también Na+ o Li+). Solo unos pocos elementos cumplen los criterios para actuar como reemplazo del silicio en la unidad SiO4, como aluminio en -, fósforo en + o hierro en – y activan la inclusión de iones adicionales. Curiosamente, el mineral berlinite, AlPO4, que podría ser interpretado como la fórmula O2 es un estructurales isomorph de cuarzo, mostrando casi idénticos estructurales y las propiedades de simetría, y muy similares propiedades físicas:
| Fórmula | Sistema de Cristal | Densidad | Dureza | Índices de Refracción | |
|---|---|---|---|---|---|
| Berlinite | AlPO4 | trigonal | 2.64 g/cm3 | 7 | 1.524-1.530 |
| α-Cuarzo | SiO2 | trigonal | 2.65 g/cm3 | 7 | 1.544-1. 553 |
En segundo lugar, la red tridimensional de tetraedros SiO4 es bastante rígida. Muchos minerales pueden tolerar cantidades relativamente grandes de ciertos otros átomos y / o iones en su red cristalina sin mostrar grandes desviaciones en sus propiedades físicas. El color puede cambiar por completo, pero los cristales parecen claros y uniformes, ya que la celosía de cristal es algo flexible o espaciosa y mantiene su estructura original en su conjunto. La celosía cristalina del cuarzo, sin embargo, es apretada y muy inflexible (por lo que es dura pero frágil), y solo se pueden incorporar cantidades muy pequeñas de un número de otros elementos con pequeños cationes (generalmente Li, Na, H) durante el crecimiento sin distorsionar la estructura de la celosía. Y de hecho, la cantidad de cationes monovalentes que se encuentran en el cuarzo es aproximadamente proporcional a la cantidad de aluminio. El cuarzo que contiene mayores cantidades de otras sustancias es de translúcido a opaco, y a menudo opaco, porque el cristal «crece alrededor» de los minerales encerrados, y la luz se dispersa en los bordes de los diferentes materiales.
Esto no es generalmente cierto para las otras modificaciones de sílice, y parece que para algunos de ellos la presencia de oligoelementos tiene de hecho un efecto estabilizador en su estructura.
Pero si bien la composición general de los cristales de cuarzo transparente es notablemente pura (al menos en comparación con la mayoría de los otros minerales), las impurezas generalmente no se distribuyen uniformemente dentro del cristal. Las concentraciones de elementos individuales pueden variar en un orden de magnitud dentro de una distancia de unos pocos micrómetros. Por ejemplo, la concentración de aluminio puede variar entre menos de 5 ppma (partes por millón de átomos)y 10000 ppma dentro de un solo cristal (Per Perny et al. 1992). El patrón de distribución de los oligoelementos se puede hacer visible con una técnica llamada catodoluminiscencia: los haces de electrones de alta energía («rayos catódicos») inducen efectos de luminiscencia de corta duración que pueden capturarse en una película ordinaria. Las fotografías resultantes de finas rodajas de cristales muestran un fino patrón laminar. Todas las capas se encuentran paralelas a las caras de cristal, similares a los fantasmas, por lo que este patrón de distribución de oligoelementos es causado por cambios rápidos en el entorno de crecimiento.
Químicamente puro a menudo todavía no es lo suficientemente puro para fines técnicos. Un cristal perfecto y homogéneo es tan transparente como un vacío, pero los oligoelementos causan distorsiones y defectos en la red cristalina, y esto a su vez afecta las propiedades ópticas. La mayoría de los elementos incorporados en el cuarzo (H, Li, Al, Na, Ti, Fe) son ubicuos y, por lo tanto, la purificación adicional de sílice es complicada y costosa. Por esa razón, los depósitos de cuarzo con un bajo contenido de oligoelementos siguen siendo muy buscados (ver, por ejemplo, Lar Larsen et al. 2000).
Más información, Literatura, Enlaces
Se puede encontrar una tabla de propiedades de cuarzo en mindat.org:
Otra tabla en www.webmineral.com:
Notas al pie de página
1 La IUPAC es una organización que tiene como objetivo eliminar ambigüedades y nombres divertidos, pero familiares, como Knallsäure (en alemán, ácido fulmínico) de la nomenclatura química. Los nombres antiguos siguen siendo válidos siempre que no sean ambiguos.
2 Algunos de ustedes pueden encontrar tentador hacer algunos experimentos con fluoruro de hidrógeno. El fluoruro de hidrógeno es una sustancia muy peligrosa. Simplemente busque un caso en un buen libro de texto sobre toxicología; después de la conferencia no querrá tocarlo ni siquiera con un poste. La solución acuosa no es un ácido fuerte (es de HF puro), y las pequeñas moléculas de HF no disociadas penetran fácilmente en la piel y se unen al calcio en las células para formar fluorita insoluble, CaF2. El calcio es esencial para las funciones vivas de todas las células del cuerpo. Una pequeña gota en un dedo que pasa desapercibida, ya que no duele de inmediato, puede, después de un cierto retraso, causar daños sustanciales y un gran dolor.Hagamos los cálculos rápidamente: 1 Mol HF = 20g. Una gota (aproximadamente 50 µl) de una solución al 20% contiene 0.00005 l x (200g/l) = 0.01 g. 10 mg, eso no suena como mucho.
1 Mol Ca = 40g y 1 Mol F = 19g.1 Ca unirá 2 F, por lo que 40g Ca unirá 38g F de 40g HF. 1 ml de tejido corporal contiene aproximadamente 0,1 mg de Ca, y 0,1 mg de HF permitirá que se precipite casi por completo. En teoría, el HF de 10 mg en la pequeña gota podría precipitar la mayor parte del Ac en el tejido de 100 ml, matando todas las células en él.Y no, no me opongo a la fluoración del agua (aquí no hay ironía).
3El término «agua meteórica» se refiere a su origen de la atmósfera, no de los meteoritos. Los griegos pensaban que las estrellas fugaces provenían de la misma esfera que las nubes: Las estrellas y los planetas eran considerados seres eternos, algo que las nubes y las estrellas fugaces obviamente no son. Piensa en «meteorología».
4 Es por eso que el cuarzo en las rocas volcánicas a menudo se acompaña de calcita.
5 Esto es algo contrario a la intuición, pero una solución saturada está en equilibrio termodinámico con el cristal. Cuando una molécula se incorpora a una estructura cristalina, se forman nuevos enlaces y, dependiendo de la geometría de la estructura cristalina, se libera o consume más o menos energía. Para disolver una sustancia, se necesita energía para romper los enlaces, pero la energía también se libera cuando las moléculas de agua se orientan hacia la molécula disuelta y forman nuevos enlaces electrostáticos (energía de hidratación). Una modificación más estable de un compuesto es generalmente menos soluble, ya que se requiere más energía para romper los enlaces.
Esto no tiene nada que ver con la velocidad de la reacción. Bajo ciertas condiciones, una modificación más inestable se formará primero a partir de una solución y solo más tarde será reemplazada por la modificación estable: El cuarzo criptocristalino se forma típicamente a partir de una solución acuosa, pero con pasos intermedios de cristobalita y ópalo, porque la cinética de las reacciones está a favor de la formación de ópalo. Y cuando pones un cristal de cuarzo en 1 litro de agua pura a temperatura ambiente, puedes estar bastante seguro de que cuando lo sacas al día siguiente no pesará 2,9 mg menos. Probablemente será muy difícil medir la diferencia. Tal vez después de un mes, o después de un año.
6Los tetraedros en cuarzo no son de hecho perfectamente isométricos como un tetraedro ideal, sino ligeramente distorsionados, porque la distancia al átomo de silicio central es de 0,16101 nm para 2 átomos de oxígeno, y de 0,16145 nm para los otros 2 átomos de oxígeno. Sin embargo, esta desviación de la forma ideal es insignificante para la mayoría de los propósitos prácticos, ya que es inferior al 0,3%.
7Los números de oxidación de Si y O son de hecho +4 y -2, respectivamente. La energía necesaria para eliminar 4 electrones del Si es demasiado alta para permitir un enlace iónico puro estable. Incluso SiF4 es un compuesto con enlaces polares, pero covalentes, a pesar de la alta electronegatividad del flúor. Pero existen compuestos de aniones Si4 (como el Ca2Si).
8Rykart (1995) da los valores de 152,8° y 143,5° para cuarzo α y β, respectivamente. Esto parece ser un error tipográfico, los valores deben cambiarse.
9Pero no es cierto que «todo vale». Cuando un mineral se forma, elementos e iones se construyen en su red cristalina cuando cumplen con ciertos criterios, como una carga, tamaño o electronegatividad específicos, y por lo tanto son similares a los que ya forman la red.
 Versión para imprimir
Versión para imprimir