Un número creciente de observaciones clínicas indica que los hongos se están convirtiendo en una causa más común de enfermedades alérgicas de las vías respiratorias superiores, como el asma, así como otras afecciones como la sepsis, una enfermedad potencialmente mortal causada por la respuesta del cuerpo a una infección. Lo más importante, explica el Dr. David B. Corry, es que las infecciones por hongos que causan enfermedades alérgicas en las vías respiratorias y sepsis se han asociado con un mayor riesgo de demencia en el futuro.
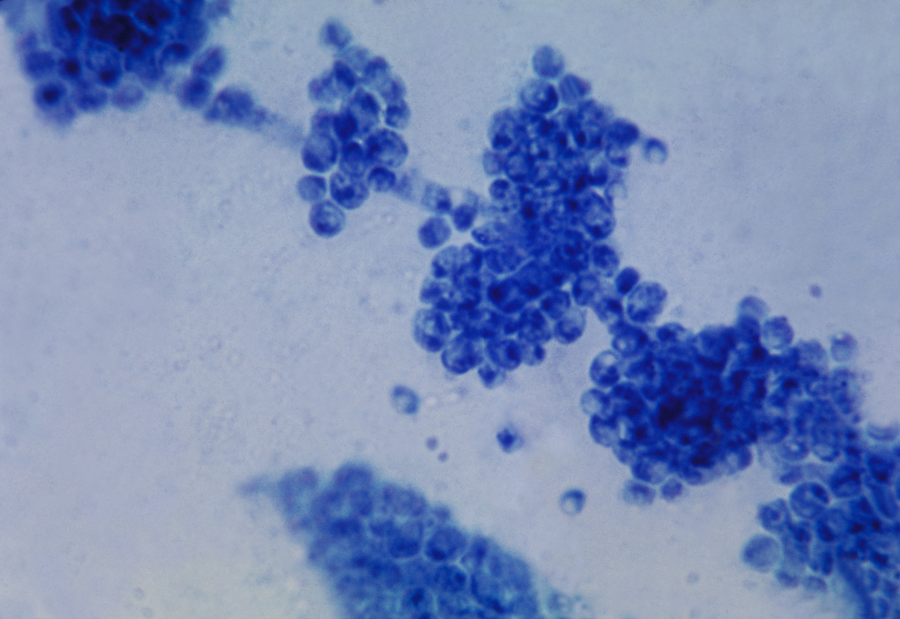
«Estas observaciones que vinculan las infecciones fúngicas con deficiencias neurológicas nos llevaron a investigar la posibilidad de que los hongos pudieran producir una infección cerebral y, de ser así, las consecuencias de tener ese tipo de infección», dijo Corry, profesor de medicina-inmunología, alergia y reumatología y Catedrático de Patología Fulbright en la Facultad de Medicina de Baylor.

Los investigadores comenzaron su investigación desarrollando un modelo de ratón de una infección por hongos de bajo grado con la levadura común C. albicans que no causaría una enfermedad grave, pero podría tener implicaciones para la función cerebral. Probaron varias dosis y finalmente se establecieron en una dosis de 25,000 levaduras.
Inyectaron C. albicans en el torrente sanguíneo de los ratones y se sorprendieron al descubrir que la levadura puede cruzar la barrera hematoencefálica, un mecanismo de protección robusto que el cerebro emplea para excluir todo tipo de moléculas grandes y pequeñas, así como una serie de microorganismos que pueden dañar potencialmente el cerebro.
«Pensamos que la levadura no entraría al cerebro, pero lo hace», dijo Corry, quien también es miembro del Centro Oncológico Integral Dan L Duncan. «En el cerebro, la levadura desencadenó la actividad de la microglía, un tipo de célula inmune residente. Las células se volvieron muy activas «comiendo y digiriendo» la levadura. También produjeron una serie de moléculas que mediaron una respuesta inflamatoria que llevó a la captura de las levaduras dentro de una estructura de tipo gránulo dentro del cerebro. Lo llamamos granuloma glial inducido por hongos, o FIGG.»
C. albicans y la enfermedad de Alzheimer
Corry y sus colegas también probaron la memoria de los animales en ratones infectados y no infectados por levaduras. Encontraron que los ratones infectados tenían una memoria espacial dañada, que se revirtió cuando la infección se despejó.
Los ratones eliminaron la infección por levaduras en aproximadamente 10 días; sin embargo, la microglía permaneció activa y los FIGG persistieron mucho más allá de este punto, hasta al menos el día 21. Curiosamente, a medida que se formaron los FIGGs, las proteínas precursoras amiloides se acumularon dentro de la periferia y las moléculas beta amiloides se acumularon alrededor de las células de levadura capturadas en el centro de los FIGGs. Estas moléculas de amiloide se encuentran típicamente en placas que son la marca registrada de la enfermedad de Alzheimer.
«Estos hallazgos sugieren que el papel que desempeñan los hongos en la enfermedad humana potencialmente va mucho más allá de la enfermedad alérgica de las vías respiratorias o la sepsis», dijo Corry.
Los resultados nos llevaron a considerar la posibilidad de que, en algunos casos, los hongos también pudieran estar involucrados en el desarrollo de trastornos neurodegenerativos crónicos, como el Alzheimer, el Parkinson y la esclerosis múltiple. Actualmente estamos explorando esta posibilidad.»
«Por estas razones, si comprendemos mejor cómo nuestro sistema inmunológico lidia con este tipo de amenaza constante y cuáles son las debilidades en nuestra armadura inmunológica que ocurren con el envejecimiento, lo que permite que la enfermedad fúngica arraigue, probablemente aumentaríamos la posibilidad de encontrar formas de defenderse», dijo Corry.
Interesados en leer todos los detalles de este trabajo? Encuéntralo en Nature Communications.
Otros autores que contribuyeron a este trabajo incluyen a Yifan Wu, Shuqi Du, Jennifer L. Johnson, Hui-Ying Tung, Cameron T Landers, Yuwei Liu, Brittany G. Seman, Robert T. Wheeler, Mauro Costa-Mattioli, Farrah Kheradmand y Hui Zheng. Los autores están afiliados a una o más de las siguientes instituciones: Baylor College of Medicine, Michael E. DeBakey VA Center for Translational Research on Inflammatory Diseases y la Universidad de Maine.
Este trabajo fue apoyado por los Institutos Nacionales de Salud de los Estados Unidos (subvenciones P30684 AI036211, P30 CA125123, S10 RR024574, T32AI053831, R01HL117181, R01 AI135803 y R41AI124997) y la Oficina de Investigación y Desarrollo del VA (subvención 5I01BX002221).
