La ionización química (CI) es una técnica de ionización suave, que es la aplicación directa de los resultados de la investigación de reacciones moleculares e iónicas en química analítica. La primera técnica de ionización fue la ionización por bombardeo electrónico (EI). El producto obtenido por EI tiene muchos fragmentos, lo cual es difícil de analizar. El CI, que produjo muy pocos fragmentos, comenzó en la década de 1950 y tiene un gran potencial en química analítica.
En el proceso de CI, los electrones bombardean primero el gas reactivo para generar iones reactivos. Las moléculas de la muestra son ionizadas por iones reactivos a través de la vía de reacción molecular e iónica. La década de 1970 fue considerada un hito en el desarrollo de la IC. En ese momento, los investigadores resolvieron las deficiencias del trabajo de CI en un entorno de vacío, lo que permitió que CI trabajara en condiciones atmosféricas. La ionización química atmosférica proporciona energía a partir de la descarga de corona y no requiere un entorno de vacío, lo que aumenta en gran medida la gama de aplicaciones de CI. Actualmente, el CI se ha utilizado ampliamente en la técnica de espectrometría de masas.
El Principio de Ionización química
El principio de CI es usar el ion reactivo X+ para reaccionar con la molécula de analito A para lograr la ionización del analito:
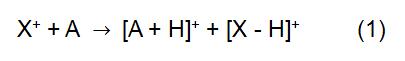
En la reacción anterior, X+ se deriva del gas de reacción ionizado. Algunos gases reactivos comunes incluyen metano, amoníaco, agua e isobutano. El tiempo de reacción y la constante de velocidad (k) en la fórmula se pueden obtener mediante literatura o medición. Cuando el ion reactivo X + es H3O+, la fórmula (2) es:
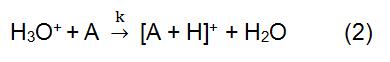
El ion reactivo es producido por una fuente de iones. Las fuentes de iones de uso común incluyen principalmente la fuente de radiación, la fuente de alimentación de descarga de cátodo hueco y la fuente de alimentación de descarga luminosa ordinaria. 210Po y 241Am son las fuentes de radiación más comunes. El proceso de ionización comienza con las partículas alfa emitidas por 210Po y 241Am. Tiene una alta energía y puede chocar con el gas reactivo para generar iones reactivos y electrones. Si los electrones generados son lo suficientemente altos, pueden chocar con el gas reactivo para formar nuevos iones reactivos y componentes electrónicos. En el CI que utiliza H3O+ como ion reactivo, se usa comúnmente una fuente de alimentación de descarga de cátodo hueco, que puede producir el 99,5% de H3O+.
De acuerdo con las condiciones de ionización química, el CI se clasifica en ionización química a baja presión (
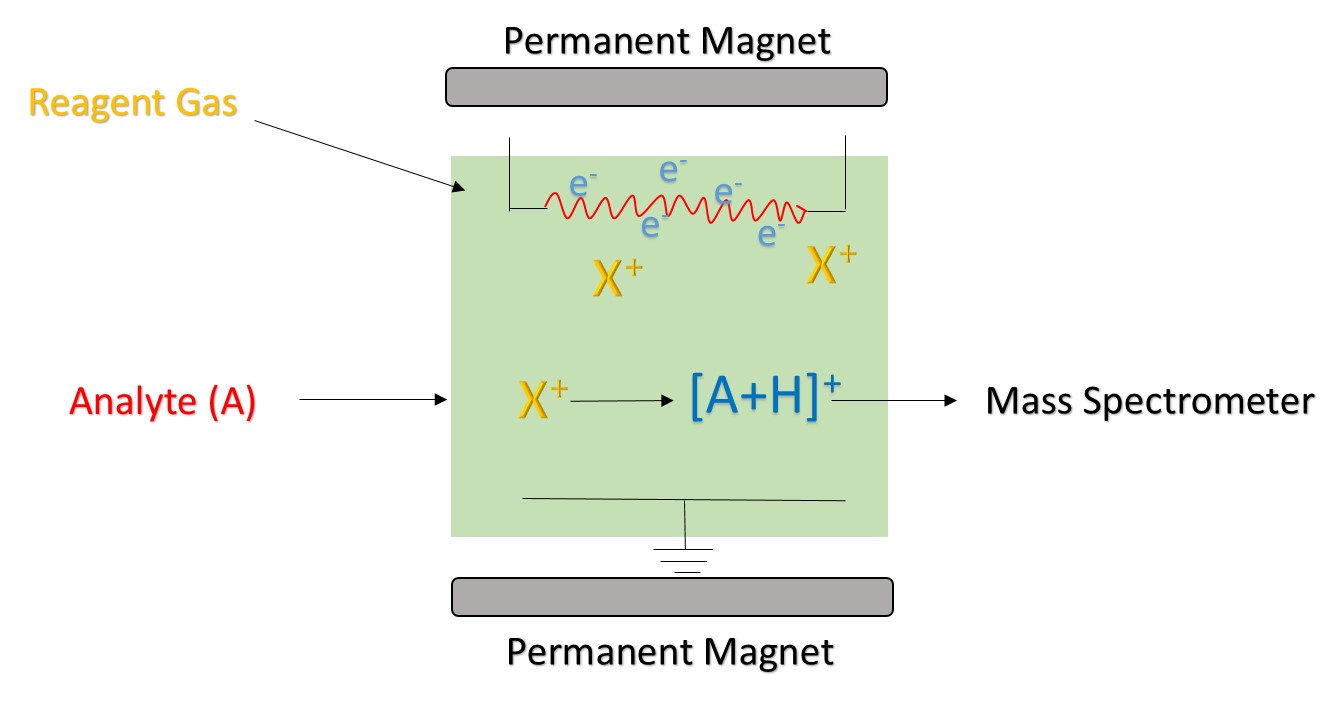 Figura 1. El principio de ionización química
Figura 1. El principio de ionización química
Ventajas y desventajas de CI
La resolución del espectro de CI es simple y se puede obtener el peso molecular exacto del analito. El producto obtenido por CI tiene pocos fragmentos, y sus productos son principalmente moléculas e iones del analito. La selectividad del CI se puede aumentar fácilmente seleccionando un ion reactivo apropiado. Por ejemplo, el ion reactivo H3O+ reacciona solo con una sustancia orgánica que tiene una afinidad de protones mayor que H3O+. Además, el CI tiene alta sensibilidad y respuesta rápida (15s). Sin embargo, si los iones reactivos son impuros y una variedad de reacciones de ionización química ocurrirán al mismo tiempo, la espectrometría de masas se vuelve difícil.
Ejemplos de aplicaciones de CI
En la actualidad, el CI se utiliza ampliamente como fuente de iones en sistemas de espectrometría de masas para detectar diversas sustancias traza. El CI se puede utilizar para la detección de sustancias como gases traza en la atmósfera, residuos de pesticidas en verduras y frutas, melamina en leche en polvo, plastificantes y herbicidas en el suelo. Además, el CI también se puede utilizar para la identificación de materiales, como la identificación de la calidad del té.
- Medición de compuestos orgánicos volátiles (COV)
En la medición de COV por CI, el H3O+ se utiliza generalmente como ion reactivo. H3O+ no reacciona con la mayoría de las sustancias en el aire, como O2, N2, CO2, etc. Por otro lado, la mayoría de las reacciones de transferencia de protones no están disociadas, por lo que los iones del producto son únicos, lo que hace que el análisis de los resultados sea simple. El principio de medición de COV utilizando H3O+ como ion reactivo se muestra en la ecuación (3). El producto final se resolvió mediante espectrometría de masas de reacción de transferencia de protones.
- Determinación de melamina en leche en polvo
En la medición de melamina por CI, se utiliza N2 como gas reactivo. Bajo la acción de alto voltaje, el N2 y el H2O experimentan complejas reacciones fisicoquímicas para generar iones reactivos H3O+. El proceso de reacción se muestra en la fórmula (3-6). H3O + reacciona con melamina en la leche en polvo, y el principio de reacción se muestra en la fórmula (2).
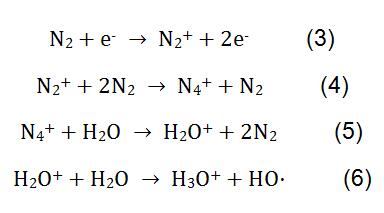
- Identificación de la calidad del té
Se pueden identificar diferentes tipos de té midiendo las sustancias químicas en la superficie de las hojas de té con CI. H3O + reacciona con la superficie del té con butanol, geraniol, cafeína y otras sustancias, y los productos de reacción forman diferentes espectros de masa en el espectrómetro de masas. El contenido de la misma sustancia en diferentes variedades de té es diferente, por lo que el espectro de masa formado por la detección de CI es diferente. El espectro de masa puede reflejar las características químicas de las huellas dactilares del té en cierta medida. Por lo tanto, CI tiene un importante valor de aplicación práctica para la identificación rápida y el análisis de calidad del té.
La ionización química es ampliamente utilizada en espectrometría de masas debido a su fuerte selectividad y alta sensibilidad. La espectrometría de masas de ionización química (CIMS) no solo permite la identificación por espectrometría de masas en tándem de sustancias en muestras complejas, sino que también obtiene datos de huellas dactilares químicas para muestras para análisis quimiométricos. La aplicación de CIMS tiene un efecto positivo en la promoción del desarrollo de la alimentación, la medicina, la protección del medio ambiente, la agricultura y otras industrias.
Hemos introducido brevemente el CI, un tipo de método de ionización, que puede ayudarlo a comprender más sobre la espectrometría de masas. En Creative Proteomics, hemos desarrollado la plataforma profesional de espectrometría de masas, que contiene instrumentos de última generación. Mediante el uso de espectrometría de masas, Creative Proteomics puede proporcionar diferentes servicios para cumplir con diversos requisitos, incluidos:
- Servicio de Proteómica
- la Metabolómica Servicio
- Glicómica Servicio
- Fales H M; et al. Comparación de espectros de masa de algunos compuestos biológicamente importantes obtenidos mediante diversas técnicas de ionización. Química Analítica, 1975, 47(2):207-219.
- Lindinger W; et al. Monitoreo en línea de compuestos orgánicos volátiles a niveles de pptv por medio de espectrometría de masas de reacción de transferencia de protones (PTR-MS), aplicaciones médicas, control de alimentos e investigación ambiental. Revista Internacional de Espectrometría de Masas & Procesos de iones, 1998, 173(3):191-241.
- Chen H; et al. Espectrometría de masas de ionización química a presión atmosférica de desorción superficial para el análisis directo de muestras ambientales sin contaminación química tóxica. Revista de Espectrometría de Masas, 2010, 42(8):1045-1056.
- Yang S; et al. Detección de Melamina en Productos Lácteos por Espectrometría de Masas de Ionización Química a Presión Atmosférica de Desorción Superficial. Química Analítica, 2009, 81(7):2426.
