El primer enfoque para desarrollar antagonistas cannabinoides a finales de la década de 1980 fue modificar la estructura del THC, pero los resultados fueron decepcionantes. A principios de la década de 1990 se descubrió una nueva familia de agonistas cannabinoides a partir del fármaco AINE (antiinflamatorio no esteroideo) pravadolina, lo que llevó al descubrimiento de antagonistas aminoalquilindol con un éxito limitado. Como la búsqueda basada en la estructura de los agonistas fue decepcionante, no fue sorprendente que el primer antagonista cannabinoide potente y selectivo perteneciera a una familia química completamente nueva. En 1994, el primer antagonista cannabinoide selectivo, SR141716 (rimonabant), fue introducido por Sanofi, perteneciente a una familia de 1,5-diarilpirazoles.
RimonabantEdit
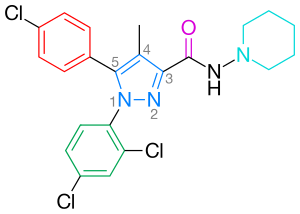
Rimonabant, también conocido por el nombre sistemático, es un antagonista de los receptores CB1 de 1,5 diarilpirazol (Figura 2). El Rimonabant no solo es un ligando potente y altamente selectivo del receptor CB1, sino que también es activo por vía oral y antagoniza la mayoría de los efectos de los agonistas cannabinoides, como el THC, tanto in vitro como in vivo. Rimonabant ha demostrado una eficacia clínica clara para el tratamiento de la obesidad.
Bindingeditar
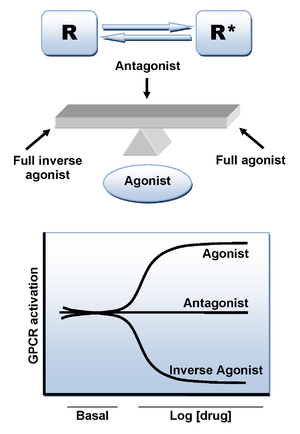
La unión de un ligando agonista al receptor CB1 provoca un cambio conformacional y conduce al estado activo del receptor que es responsable de la transducción de señales. Sin embargo, hay un mecanismo adicional que puede conducir al estado activo en ausencia de ligando. Como muchos otros GPCR, el receptor CB1 muestra un alto nivel de actividad constitutiva y, por lo tanto, puede adoptar espontáneamente un estado conformacional activo en ausencia de unión agonista, manteniendo niveles basales elevados de señalización intracelular. Esto puede explicarse por el modelo de dos estados de activación de receptores en el que los receptores están en equilibrio entre dos estados, activo e inactivo (R* y R). Un agonista estabilizará el estado activo que conduce a la activación, un antagonista neutro se une por igual a los estados activo e inactivo, mientras que un agonista inverso estabilizará preferentemente el estado inactivo (Figura 3).
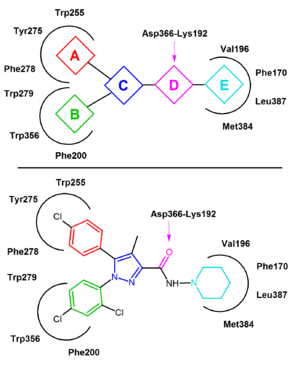
Rimonabant se ha reportado en muchos casos que se comporta como un agonista inverso en lugar de como un antagonista neutro y es probable que se una preferentemente al estado inactivo del CB1, disminuyendo así la activación de la vía de señalización. La interacción clave de unión es un enlace de hidrógeno formado entre el grupo carbonilo de rimonabant y el residuo Lys192 del receptor CB1. Este enlace estabiliza el puente salino Lys192-Asp366 del extremo intracelular de las hélices transmembranarias 3 y 6 (Figura 4). Este puente salino específico está presente en el estado inactivo del receptor, pero ausente en el estado activo.
En el estado inactivo de los enlaces de rimonabant CB1 dentro de la transmembrana-3-4-5-6 microdominio aromático. La unión del rimonabant implica interacciones de apilamiento aromático directo entre su anillo de 2,4-diclorofenilo y los residuos Trp279/Phe200/Trp356 por un lado y el anillo para-clorofenilo y los residuos Tyr275/Trp255/Phe278 por el otro lado. La fracción lipofílica de piperidinilo encaja perfectamente en una cavidad formada por los residuos de aminoácidos Val196/Phe170/Leu387 y Met384 (Figura 4).
FarmacoforeedItar
La mayoría de los antagonistas CB1 notificados hasta ahora son análogos cercanos o isosteros de rimonabant. Se puede extraer un modelo general de farmacóforo agonista inverso CB1 de las características comunes de estos análogos, los diarilpirazoles (Figura 4). Este farmacóforo contiene un núcleo cíclico, C, (por ejemplo, pirazol en rimonabant) sustituido por dos mitades aromáticas, A y B. Una unidad aceptora de enlace de hidrógeno, D, conecta C con una parte lipofílica cíclica, E. En algunos casos, la unidad E se conecta directamente a C. En la Figura 4, el rimonabant se usa como ejemplo. La unidad A representa un grupo 4-clorofenilo y la unidad B un anillo 2,4-diclorofenilo. La unidad C es el anillo pirazol central y la unidad D representa el grupo carbonilo que sirve como receptor de enlace de hidrógeno. La unidad E representa una fracción aminopiperidinil lipofílica.
Relaciones estructura-actividadeditar
La unión óptima en el receptor CB1 requiere un anillo fenilo para-sustituido en la posición 5 del pirazol. El sustituyente 5 del pirazol está implicado en el reconocimiento y antagonismo de los receptores. El para-sustituyente del anillo fenilo podría ser cloro, bromo o yodo, pero se ha demostrado que una cadena alquilo también podría ser tolerada. La numeración del anillo central de pirazol se muestra en la Figura 2.
Se prefiere un anillo fenilo 2,4-dicloro sustituido en la posición 1 del pirazol para la afinidad, así como para la actividad. Se ha demostrado que los halógenos adicionales en este anillo fenílico disminuyen la afinidad.
También es favorable tener una sustitución de anillo en el grupo 3-carboxamida, como el grupo 1-piperidinilo en rimonabant. La sustitución del sustituyente amino piperidinilo por alquil amidas, éteres, cetonas, alcoholes o alcanos resultó principalmente en una disminución de la afinidad. La sustitución de la cadena piperidinil por pentilo o heptilo dio a los compuestos propiedades agonistas. Con base en estos resultados, se concluyó que la posición 3 del pirazol parece estar involucrada en el agonismo,mientras que las posiciones 1,4 y 5 parecen estar involucradas en el antagonismo.
La investigación ha demostrado que la ausencia de oxígeno carboxamida resulta en una disminución de la afinidad. Además, la presencia de oxígeno carboxamida contribuye a conferir las propiedades agonistas inversas, mientras que los análogos que carecen de este oxígeno se encuentran como antagonistas neutros. Estos resultados apoyan la hipótesis de que el oxígeno carboxamida forma un enlace de hidrógeno con el residuo Lys192 en el receptor CB1.
Derivados de diarilpirazoleditar
Los análogos SR141716 (rimonabant) han sido descritos recientemente por varios grupos, lo que lleva a una buena comprensión de la relación estructura-actividad (SAR) dentro de este grupo químico. Aunque la mayoría de los compuestos descritos son menos potentes que el SR141716, vale la pena mencionar dos de ellos, el SR147778 y el AM251, aunque ambos también pueden tener acción en los receptores opioides mu.
SR147778 (surinabant), un antagonista de segunda generación, tiene una duración de acción más larga que el rimonabant y una mayor actividad oral. Esta mayor duración de la acción se debe probablemente a la presencia del grupo etílico metabólicamente más estable en la posición 4 de su anillo pirazol. Otro cambio es la sustitución del sustituyente de cloro 5-fenilo por bromo.
El derivado de diarilpirazol, AM251, se ha descrito donde el sustituyente de cloro ha sido reemplazado por yodo en la posición para del anillo 5-fenilo. Este derivado parecía ser más potente y selectivo que el rimonabant.
se sintetizaron 21 análogos que poseían una amida alquilo o una hidracida alquilo de longitudes variables en la posición 3. Se observó que la afinidad aumenta con el aumento de la longitud de la cadena de carbono hasta cinco carbonos. También los análogos de la amida exhibieron una afinidad más alta que los análogos de la hidrazida. Sin embargo, ninguno de estos análogos poseía una afinidad significativamente mayor que el rimonabant, pero sin embargo, eran ligeramente más selectivos que el rimonabant para el receptor CB1 sobre el receptor CB2.
Se han realizado varios intentos para aumentar la afinidad de los derivados del diarilpirazol rigidizando la estructura de rimonabant. En términos del modelo farmacóforo general, las unidades A, B y / o C están conectadas por enlaces adicionales que conducen a moléculas rígidas. Por ejemplo, el pirazol policíclico condensado NESS-0327 mostró 5000 veces más afinidad por el receptor CB1 que el rimonabant. Sin embargo, este compuesto posee una biodisponibilidad central pobre.
Otro compuesto, el derivado indazólico O-1248, puede considerarse como un análogo del rimonabant en el que su grupo 5-arilo se fusiona con la fracción pirazólica. Sin embargo, esta modificación estructural resultó en una disminución de 67 veces en la afinidad de los receptores CB1.
Estos derivados de diarilpirazol de rimonabant se resumen en la Tabla 1.
 |

|
| SR147778 | AM251 |
 |
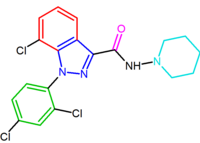 |
| NESS-0327 | O-1248 |
Other derivativesEdit
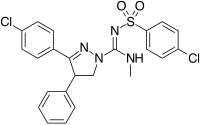
Structurally different from the 1,5-diarylpyrazoles are the chemical series of the 3,4-diarylpyrazolines. Dentro de esta serie se encuentra el SLV-319 (ibipinabant), un potente antagonista CB1 que es aproximadamente 1000 veces más selectivo para CB1 en comparación con CB2 y muestra actividad in vivo similar a rimonabant.
Otro enfoque utilizado para desarrollar análogos de rimonabant fue reemplazar el anillo central de pirazol por otro heterociclo. Un ejemplo de este enfoque son los 4,5-diarilimidazoles y las 1,5-diarilpirrol-3-carboxamidas.
Se ha notificado un gran número de derivados bicíclicos fusionados de diaril pirazol e imidazoles. Un ejemplo de esto es un derivado de purina donde un anillo de pirimidina se fusiona con un anillo de imidazol. Otenabant (CP-945,598) es un ejemplo de derivado bicíclico fusionado desarrollado por Pfizer.
Varios grupos de investigación han estudiado bioisosteros de pirazol anular de seis miembros. Por ejemplo, se demostró que un derivado de 2,3-diarilpiridina era un agonista inverso CB1 potente y selectivo. La estructura de este compuesto demuestra la posibilidad de que la fracción amida de rimonabant pueda dividirse en una funcionalidad lipofílica (benciloxi) y una funcionalidad polar (nitrilo). Otros análogos de anillo de seis miembros son, por ejemplo, pirimidinas y pirazinas.
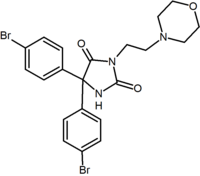
Además de los análogos de anillo de cinco y seis miembros, hay otros derivados cíclicos como las azetidinas. Un ejemplo es el derivado de metilsulfonamida azetidina, que tiene un grupo 1,1-diarilo que imita la fracción 1,5-diarilo de los diarilpirazoles. El grupo sulfonilo sirve como aceptor de enlaces de hidrógeno. El grupo 1,1-diarilo también está presente en derivados como los benzodioxoles y las hidantoinas.
También se han notificado análogos acíclicos. Estos análogos contienen un motivo de 1,2-diarilo que corresponde a los sustituyentes de 1,5-diarilo del rimonabant. Un ejemplo de análogo acíclico es taranabant (MK-0364) desarrollado por Merck.
Los representantes de estos análogos se resumen en la Tabla 2.
 |
 |
 |
|
| Type of derivative |
3,4-Diarylpyrazoline (Ibipinabant) | 4,5-Diarylimidazole | 1,5-Diarylpyrrole-3-carboxamides |
 |
 |
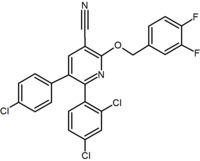 |
|
| Type of derivative |
Purine (pyrimidine ring fused to an imidazole ring) |
Purine derivative (Otenabant) | 2,3-Diarylpyridine |
 |
 |
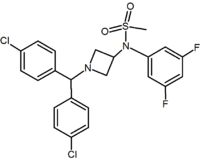 |
|
| Type of derivative |
Pyrimidine | Pyrazine | Methylsulfonamide azetidine |
 |
 |
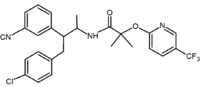 |
|
| Tipo de derivado | Benzodioxol | Hidantoína | Derivado acíclico (Taranabant) |
