

kulsyre (CO2) er en kemisk forbindelse. Det er en gas ved stuetemperatur. Det er lavet af et kulstof og to iltatomer. Mennesker og dyr frigiver kulsyre, når de trækker vejret ud. Også hver gang noget organisk brændes (eller en ild er lavet), gør det kulsyre. Planter bruger kulsyre til at lave mad. Denne proces kaldes fotosyntese. Egenskaberne af kulsyre blev undersøgt af den skotske videnskabsmand Joseph Black i 1750 ‘ erne.
kulsyre er en drivhusgas. Drivhusgasser fælder varmeenergi. Drivhusgasser ændrer klimaet og vejret på vores planet, Jorden. Dette kaldes klimaændringer. Drivhusgasser er en årsag til global opvarmning, stigningen i Jordens overfladetemperatur.
biologisk rolle
kulsyre er et slutprodukt i organismer, der får energi ved at nedbryde sukker, fedt og aminosyrer med ilt som en del af deres stofskifte. Dette er en proces kendt som cellulær respiration. Dette omfatter alle planter, dyr, mange svampe og nogle bakterier. Hos højere dyr bevæger kulsyre sig i blodet fra kroppens væv til lungerne, hvor det indåndes. Planter indtager kulsyre fra atmosfæren til brug i fotosyntese.
tøris
tøris, eller fast kulsyre, er den faste tilstand af CO2-gas under -109,3 liter F (-78,5 liter C). Tøris forekommer ikke naturligt på jorden, men er menneskeskabt. Det er farveløst. Folk bruger tøris til at gøre tingene kolde og til at gøre drikkevarer brusende, dræbe gophers og fryse vorter. Dampen af tøris forårsager kvælning og til sidst død. Forsigtighed og professionel assistance anbefales, når tøris er i brug.

Ved normalt tryk smelter den ikke fra et fast stof til en væske, men skifter i stedet direkte fra et fast stof til en gas. Dette kaldes sublimering. Det vil ændre sig direkte fra et fast stof til en gas ved enhver temperatur højere end ekstremt kolde temperaturer. Tøris sublimerer ved normal lufttemperatur. Tøris udsat for normal luft afgiver kulsyre, der ikke har nogen farve. Kulsyre kan flydende ved tryk over 5,1 atmosfærer.gas, der kommer ud af tøris, er så kold, at når den blandes med luft, afkøles vanddampen i luften til tåge, der ligner en tyk hvid røg. Det bruges ofte i teatret for at skabe udseende af tåge eller røg.
isolering og produktion
kemikere kan få kulsyre fra køleluft. De kalder denne luftdestillation. Denne metode er ineffektiv, fordi en stor mængde luft skal køles for at udvinde en lille mængde CO2. Kemikere kan også bruge flere forskellige kemiske reaktioner til at adskille kulsyre. Kulsyre fremstilles i reaktionerne mellem de fleste syrer og de fleste metalcarbonater. For eksempel gør reaktionen mellem saltsyre og calciumcarbonat (kalksten eller kridt) kulsyre:
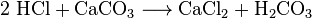
kulsyren (H2CO3) nedbrydes derefter til vand og CO2. Sådanne reaktioner forårsager skumdannelse eller bobling eller begge dele. I industrien anvendes sådanne reaktioner mange gange til at neutralisere affaldssyrestrømme.
Hurtigkalk (CaO), et kemikalie, der har udbredt anvendelse, kan laves opvarmning af kalksten til omkring 850 liter C. Denne reaktion gør også CO2:
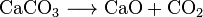
kulsyre fremstilles også ved forbrænding af alle kulstofholdige brændstoffer, såsom methan (naturgas), petroleumsdestillater (bensin, diesel, petroleum, propan), kul eller træ. I de fleste tilfælde frigives vand også. Som et eksempel er den kemiske reaktion mellem metan og ilt:
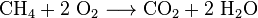
kulsyre fremstilles i stålværker.

gær metaboliserer sukker til fremstilling af kulsyre og ethanol, også kendt som alkohol, i produktionen af vin, øl og anden spiritus, men også i produktionen af bioethanol:
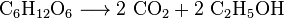
alle aerobe organismer producerer co2, når de ilter kulhydrater, fedtsyrer og proteiner i mitokondrier af celler. Det store antal involverede reaktioner er meget komplekse og beskrives ikke let. (De omfatter cellulær respiration, anaerob respiration og fotosyntese). Photoautotrophs (dvs.planter, cyanobakterier) bruger en anden reaktion: planter absorberer CO2 fra luften og reagerer sammen med vand for at danne kulhydrater:
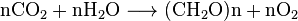
kulsyre er opløseligt i vand, hvor det spontant interkonverterer mellem CO2 og H2CO3 (kulsyre). De relative koncentrationer af CO2, H2CO3 og de deprotonerede former HCO−
3 (bicarbonat) og CO2−
3(carbonat) afhænger af surheden (pH). I neutralt eller svagt alkalisk vand (pH > 6.5) dominerer bikarbonatformen (>50%) og bliver den mest udbredte (>95%) ved havvandets pH, mens den er i meget alkalisk vand (pH > 10.4) den dominerende (>50%) form er carbonat. Bicarbonat – og carbonatformerne er meget opløselige. Så, luft-ækvilibreret havvand (mildt alkalisk med typisk pH = 8,2–8,5) indeholder omkring 120 mg bicarbonat pr.
industriel produktion
industriel kulsyre fremstilles hovedsageligt fra seks processer:
- ved at opfange naturlige kulsyre kilder, hvor det produceres ved virkningen af syrnet vand på kalksten eller dolomit.
- som biprodukt fra brintproduktionsanlæg, hvor metan omdannes til CO2;
- fra forbrænding af fossile brændstoffer eller træ;
- som et biprodukt af fermentering af sukker ved brygning af øl, øl og andre alkoholholdige drikkevarer;
- fra termisk nedbrydning af kalksten, CaCO3, ved fremstilling af kalk (Calciumoksid, CaO);
kemisk reaktion
kulsyre kan skabes med en simpel kemisk reaktion:
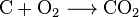 carbon + oxygen → carbon dioxide
carbon + oxygen → carbon dioxide
Images for kids
-

Crystal structure of dry ice
-

Pellets of “dry ice”, a common form of solid carbon dioxide
-

Carbon dioxide bubbles in a soft drink.
-

Dry ice used to preserve grapes after harvest.
-

Use of a CO2 fire extinguisher.
-

A carbon dioxide laser.
-

CO2 in Earth’s atmosphere if half of global-warming emissions are not absorbed.(NASA computer simulation).
-

pterapodskal opløst i havvand justeret til en havkemi projiceret for året 2100.
-

oversigt over fotosyntese og respiration. Kulsyre (til højre) danner sammen med vand ilt og organiske forbindelser (til venstre) ved fotosyntese, som kan respireres til vand og (CO2).
-

stigende niveauer af CO2 truede Apollo 13-astronauterne, der måtte tilpasse patroner fra kommandomodulet for at levere kulsyre-skrubberen i månemodulet, som de brugte som redningsbåd.
-

CO2 concentration meter using a nondispersive infrared sensor
