Sidst ændret: søndag, 08-Nov-2009 04: 44: 32 cet
Dokumentstatus: komplet
kvarts er en forbindelse af en del silicium og to dele ilt, siliciumdiokse, SiO2. Dens kemiske sammensætning (og grundstoffet silicium, Si) blev opdaget af den svenske kemiker J. J. Larts Jakob Berselius i 1823. Silica kaldes almindeligvis silica.
ifølge IUPAC er følgende to navne korrekte: silica og dioksosilan.
![]()
10mm![]()
1040h800 193kb – 2080h1600 684kb
Dette er et lille stykke industrielt produceret rent silicium. Det er et lys (densitet 2.328 g/cm3), gråt krystallinsk stof med stærk metallisk glans. Det er meget hårdt (omtrent lige så hårdt som kvarts og meget hårdere end de fleste metaller), men skørt og ikke formbart som metaller. Silicium er grundlaget for halvlederindustrien: rent silicium er kun en svag leder af elektricitet, men når der tilsættes spormængder af passende elementer (siliciumet er doteret), nærmer dets ledningsevne sig et metal, og ved at vælge typen og mængden af sporstoffer kan de elektriske egenskaber af det doterede silicium styres.
reaktioner
ved stuetemperatur er SiO2 i alle modifikationer næsten inert og reagerer ikke med de fleste andre stoffer. Selv ved moderat høje temperaturer silica er kemisk meget stabil. Af den grund anvendes smeltet kvarts (silicaglas) i vid udstrækning til kemiske apparater, især når katalytiske reaktioner af metalkationerne i almindeligt glas skal undgås. Årsagen til silicas lave reaktivitet er den meget stærke Si-o-binding, men også dens makromolekylære struktur.
at være anhydrit af en syre selv (orthosilicinsyre, H4SiO4), vil kvarts generelt ikke blive angrebet af syrer. Den fremtrædende undtagelse er flussyre, HF, som nedbrydes kvarts til dannelse af først siliciumfluorid SiF4, derefter hydrofluorosilicinsyre:
SiO2 er også angrebet af alkaliske stoffer (som kaliumhydroksid, KOH). Reaktionshastigheden afhænger af modifikationen og krystalstørrelsen: krystallinsk kvarts opløses kun meget langsomt i varme vandige alkaliske opløsninger, mens amorf SiO2 let opløses ved stuetemperatur:
reaktionen er relevant for opsamleren, da alkaliske opløsninger og vaskemidler undertiden bruges til at fjerne mos og lav fra mineralprøven. Kvartskrystaller er normalt ikke et problem, men jeg ville være meget forsigtig, når jeg rengør kryptokrystallinske Sorter.
en lignende reaktion fører til dannelsen af silicageler i beton, når de alkaliske forbindelser af betonen, typisk Ca(OH)2, reagerer med Amorf silica og kryptokrystallinsk kvarts (det vil sige opal og Chalcedon). Silicagelen tiltrækker vand, svulmer og revner betonen inden for få årtier.
alle former for silica opløses i smeltet natron (Na2CO3) eller kaliumchlorid (K2CO3) til dannelse af silicater:
Ved de høje temperaturer i mange geologiske miljøer fungerer kvarts som en syre og reagerer med mange alkaliske mineraler. Et velkendt eksempel er dannelsen af mineralvollastonit Ca3Si3O9 fra kvarts og calcit i kontakt metamorfe processer ved temperaturer fra omkring 600 liter C opad:
den modsatte reaktion finder sted ved forvitring af silikatsten, her frigiver kulsyre H2CO3 til stede, for eksempel i meteoriske farvande kiselsyre og danner carbonater.
kvarts er” malm ” af silicium. Silicium hentes ved en temperatur på omkring 2000 liter C i den følgende endotermiske (energiforbrugende) reaktion:
Si-O-bindingen er meget stærkere end C-O-bindingen, og reaktionen fungerer kun, fordi kulilte Co slipper ud af systemet som en gas, så systemets ligevægt skubbes til højre side. Dannelsen af kulilte i stedet for CO2 er typisk for reduktive reaktioner med kulstof ved høje temperaturer. Siliciumet dannet i denne proces er ikke rent nok til chipproduktion og skal renses i en ret kompleks procedure. Så på trods af overflod af sin malm er rent silicium relativt dyrt.
opløselighed i vand
opløseligheden af silicium i vand afhænger af temperaturen, trykket, overfladestrukturen og dens strukturelle modifikation. Følgende tabel giver et overblik over opløseligheden ved stuetemperatur og normalt tryk.
Data fra:
– Kristian Hollemann& Viberg, 1985
– Kristian Rykart, 1995
ved stuetemperatur er kvarts praktisk talt uopløseligt i vand. Ledningsvand er normalt næsten mættet med opløst silica (med hensyn til kvarts), og opløsningsprocessen er meget langsom, så der er ingen grund til at bekymre sig om, at kvartskrystaller beskadiges ved gentagen rengøring.
ikke desto mindre spiller opløsningen af silica i grundfjeld og jord en vigtig rolle i varme fugtige klimaer. Dannelsen af lateritjord er forbundet med, at silica gradvist vaskes ud af overfladelagene og en berigelse af forbindelser, der – i det mindste under disse klimaforhold – er mindre opløselige i vand, som f.eks.
Ved temperaturer over 100 liter C og højt tryk øges opløseligheden af kvarts hurtigt. Ved 300 liter C er det mellem 700 og 1200 mg/l afhængigt af trykket.
SiO2 opløses i vand ved dannelse af orthosilicic acid, H4SiO4:
Orthosilicic acid er en meget svag syre, svagere end kulsyre, for eksempel. Det adskiller sig med en pK1 af 9.51 i henhold til
Der er ingen SiO2-molekyler eller aggregater af SiO4-tetraeder til stede i en vandig opløsning. Den omvendte reaktion er den måde, kvartskrystaller vokser på, men et h4sio4-molekyle kan ikke blot bortskaffe 2 molekyler vand, det har brug for et andet h4sio4-molekyle eller et allerede til stede silica-molekyle med en hydroksyl (- OH) slutning:
Orthosilicinsyre er kun stabil i en fortyndet vandig opløsning, man kan ikke ekstrahere den rene syre. Den mest interessante egenskab ved orthosilicinsyre er dens tendens til at polymerisere i vandige opløsninger til først at danne en sol og senere en gel af polysiliciske syrer: orthosilicinsyremolekyler kondenserer til store molekyler i henhold til reaktioner og . Så snart du begynder at koncentrere en h4sio4-opløsning, polymeriserer molekylerne. Ved stuetemperatur under laboratoriebetingelser er slutpunktet for denne proces dannelsen af Amorf silica. Geler af polymeriseret kiselsyre er sandsynligvis også forgængerne for opal-og kryptokrystallinske kvartsvarianter (Chalcedon i bredere forstand) i naturen.
basisstruktur af Silica
SiO2 forekommer i ikke mindre end 13 forskellige strukturelle modifikationer. Deres krystalstrukturer (hvis de er til stede) kan variere, men de deler alle nogle grundlæggende egenskaber. Følgende gælder for alle silica-modifikationer, medmindre andet er angivet. Den molekylære struktur, der er specifik for kvarts, er dækket af kapitelstrukturen.
de kemiske bindinger i silica er kovalente: de er baseret på molekylære orbitaler, hvor 2 elektroner deles mellem atomerne (i modsætning til ioniske bindinger, der findes i salte som fluorit eller bordsalt; her overføres elektroner fra et element til et andet for at danne ioner med modsat elektrisk ladning, og i en krystal holdes disse ioner sammen ved elektrostatisk tiltrækning).
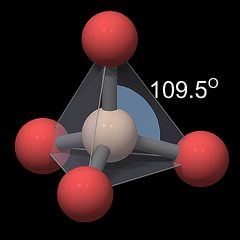
Fig.1: SiO4-tetraeder
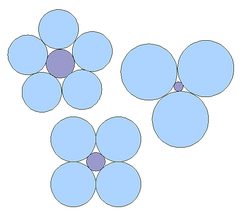
Fig.2

Fig.3: SiO4-Ionbindingsmodel
den grundlæggende byggesten i næsten alle modifikationer af silica (undtagelserne er meget højtryksændringer) er SiO4-enheden, hvor et centralt siliciumatom er omgivet af fire iltatomer.
. |O| - | - .O-Si-O. - | - |O| .
denne enheds geometri er vist i en kugle-og-pind-gengivelse i Fig.1, med silicium symboliseret ved en elfenben farvet, ilt ved en rød kugle, og kemiske bindinger af grå rør mellem dem. Atomernes størrelse skaleres ikke. Iltatomerne indtager positioner omkring siliciumatomet, der holder dem i størst mulig afstand fra hinanden, så de danner de fire hjørner af en tetraeder, symboliseret af den gennemskinnelige grå pyramide. Bemærk, at iltatomerne ikke er forbundet med hinanden, de grå linjer mellem dem er kun trukket for at visualisere den tetraedriske geometri. Vinklen på de centrale o-Si-o-bindinger er meget tæt på værdien i en ideel tetraeder (109,5 liter, gråblå bue i Fig.1), med en siliciumiltafstand på ca.0.161 nm for alle iltatomer, så den enkelte tetraeder har en næsten kubisk symmetri.
Si-O-bindingen er meget polær, hvor elektroner tiltrækkes mere af iltet, hvilket fører til en ujævn fordeling af elektriske ladninger i tetrahedronen: hjørnerne er mere negativt, midten er mere positivt ladet.
individuelle molekyler bygget som O=Si=O (med en lineær struktur som den af CO2) kan kun findes i en SiO2-gas ved temperaturer over 2500 liter C.
mange lærebøger forklarer geometrien af SiO4-tetraeder og andre mineralstrukturer som bestemt af de relative størrelser af de forskellige ioner, som vist i Fig.2: jo større den relative størrelse af den centrale ion er, jo flere ioner med modsat ladning er nødvendige for at omslutte den. Følgelig tegnes SiO4-tetrahedronen ofte som en lille Si4+ kation omgivet af fire store O2 – anioner (Fig.3). Man kan argumentere for, at dette er unøjagtigt: Silicium og ilt er forbundet med polære kovalente bindinger af sammenføjede elektronorbitaler, så de danner en enhed og er ikke på samme måde adskilt og frit bevægelig som ionerne i et salt. Forbindelser med Si4 + ioner eksisterer faktisk ikke. Der er en vis variation i fortolkningen af de eksperimentelle fund, og mens nogle forfattere betragter Si-O-bindingen som primært kovalent, understreger andre bindingens Ioniske egenskaber. For en gennemgang, se Gibbs et al. 1994 og Cohen 1994.,
| | O O | | -O-Si-O-Si-O- | | | | O O O O | | | |-O-Si-O-Si-O-Si-O-Si-O- | | | | O O O O | | | | -O-Si-O- | O |
Fig.4: Silica-netværk
ilt er bivalent, og iltatomerne i hjørnerne af tetrahedronen er hver forbundet med et andet siliciumatom i en nærliggende tetrahedron. Så kvarts og silica generelt kan beskrives som et tredimensionelt netværk af sammenkoblet SiO4 tetraeder. Et skematisk billede af dets struktur i kemiske symboler er vist i Fig.4. Mere detaljerede figurer af kvartsmolekylær struktur kan findes i kapitlet struktur.
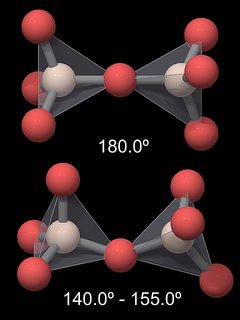
Fig.6
|
si-O-Si-bindingen, der forbinder to tetraeder, er ikke lige (180 liter), men danner en vinkel på 144 liter i kvarts (Fig.5). Som følge heraf er den samlede krystalstruktur af kvarts ret kompleks. I andre silica-modifikationer er denne vinkel forskellig, mens vinklerne inde i SiO4 tetraeder (defineret af O-Si-O-bindingen) forbliver stort set de samme. Følgende tabel viser vinkler og afstande for et par silica modifikationer.
Data fra:
Kristian Hollemann& Viberg, 1985
Kristian Rykart, 1995
måling med JMol baseret på enhedscellekoordinater.
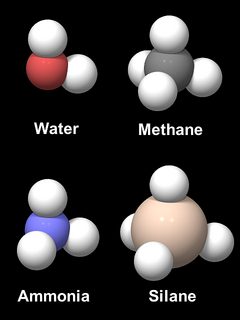
ilt har en iboende tendens til at danne en vinkelbinding, ligesom dets naboer i det periodiske system af elementer. Figur 6 viser modeller af fire hydrogenforbindelser, vand (H2O), methan (CH4), ammoniak (NH3) og Silan (SiH4). De interatomiske afstande og de relative størrelser af C, N, O og Si skaleres, men hydrogenatomerne er overdimensionerede for læsbarhed. CH4-og SiH4-molekylerne er naturligvis tetraedriske. NH3 og H2O er næsten formet som et metanmolekyle med 1 eller 2 hydrogenatomer fjernet med en H-O-H-vinkel på 104,5 liter og en h-N-H-vinkel på 106,8 liter. Årsagen til denne lighed er geometrien af de bindende elektronorbitaler, de fire såkaldte sp3 hybridorbitaler, der danner en tetraeder. Et tetraedrisk arrangement af fire SP3 hybridorbitaler findes også i silicium og er hovedårsagen til den tetraedriske form og stivheden af SiO4-enheden i silica og silicater.
fra denne ville man forvente, at si-O-Si-vinklen er mindre, så hvorfor er den mere åben? For en, fordi Si-O-bindingen er meget polær, og iltatomerne er negativt polariserede, er der frastødende kræfter mellem SiO4-grupperne, og en lige Si-O-Si ville holde iltatomerne i større afstand. Derudover er længden af Si-O-bindingen kortere end beregnet for en enkelt binding: værdien skal være 0, 181 nm, men er faktisk omkring 0, 161 nm i kvarts og har lignende værdier i andre silica-modifikationer. Dette er en indikation for en delvis dobbeltbindende karakter af denne binding (Hollemann & Viberg, 1985), som også ville forklare dens store styrke . Denne dobbeltbinding er i overensstemmelse med den større end forventet si-O-Si-vinkel (144 liter i stedet for 109,5 liter). Bemærk, at si-o-afstanden er kortest i prisT-tridymit, og denne ændring har en si-O-si-vinkel på 180 liter. Teorien bag den delvise dobbeltbindende karakter er ret kompleks, og jeg vil ikke gå længere ind i den.
Silica og silicater
selvom kemisk talt silica er et ilt, klassificeres kvarts og alle andre silica-modifikationer i Angloamerikansk mineralogisk litteratur normalt som silicater (baseret på et klassificeringsskema oprettet af Dana). Ræsonnementet bag at kalde kvarts et silikat er, at det er opbygget af et netværk af SiO4 tetraeder. Silikater klassificeres efter den måde, SiO4 tetraeder er integreret i krystalstrukturen, og hvis og hvordan tetraeder er knyttet til hinanden, og ifølge det kaldes kvarts et tektosilikat (“netværkssilicat” eller “rammesilicat”).
et silikat er et salt af kiselsyrer og et eller flere metaller. Orthosilicinsyre, H4SiO4, er bare den enkleste form, andre kiselsyrer er lavet af flere forbundne SiO4-enheder med fastgjort hydrogen.
man kunne tro, at silikater dannes, når et metalhydroksid og orthosilicinsyre reagerer, som
men det er ikke den måde, silikater normalt dannes i naturen. Silicater kan dannes, når et metaloksid eller carbonat reagerer med silica, som
lignende reaktioner forekommer faktisk i naturen, dannelsen af ullastonit under metamorfe processer er allerede nævnt (reaktion ). Men den normale måde at danne silikat på er en transformation: silikater reagerer med hinanden for at danne nye silikater. Når SiO4 tetraeder er dannet, brydes den ikke let fra hinanden og kan kun bruges i reaktioner til at danne nye ringe, kæder, ark eller netværk af tetraeder. Kun meget sjældent og i meget specielle miljøer kan man finde silicium i ikke-silikatmineraler.
renhed af kvartskrystaller
I modsætning til de fleste mineraler er en klar kvartskrystal altid kemisk ren, med et SiO2-indhold, der nærmer sig 99,5%, ofte mere. Der er grundlæggende to grunde til dette.for det første har kvarts en makromolekylær struktur. Det indeholder ikke isolerede ioner af noget element, der let kunne erstattes af et andet element. Hvis for eksempel et salt (en forbindelse lavet af isolerede ioner, der holdes sammen af elektrostatiske kræfter) vokser i en vandig opløsning, kan dets ioner næsten vilkårligt erstattes, så længe størrelsen og ladningen af de erstattende ioner har en identisk værdi. Når kvarts vokser fra en vandig opløsning, er der bogstaveligt talt intet “attraktivt” på den voksende overflade til andre ioner i opløsningen. Er indbygget i stedet for en SiO4-enhed, bliver strukturen elektrisk ubalanceret og tillader en yderligere lille monovalent kation (for det meste H+, men også Na+ eller Li+), der skal medtages. Kun få elementer opfylder kriterierne for at fungere som erstatning for silicium i SiO4-enheden, som aluminium i -, fosfor i + eller jern i-og udløser inkludering af yderligere ioner. Interessant nok er mineralet berlinit, AlPO4, som kunne fortolkes som formlen O2, en strukturel isomorf af kvarts, der viser næsten identiske strukturelle og symmetriegenskaber og meget lignende fysiske egenskaber:
| formel | krystal System | densitet | hårdhed | brydningsindeks | |||
|---|---|---|---|---|---|---|---|
| berlinite | alpo4 | trigonal | 2.64 g/cm3 | 7 | 1.524-1.530 | ||
| kristilkvarts | SiO2 | trigonal | 2, 65 g/cm3 | 7 | 1.544-1.553 |
for det andet er det tredimensionelle netværk af SiO4 tetraeder ret stift. Mange mineraler kan tolerere relativt store mængder af visse andre atomer og / eller ioner i deres krystalgitter uden at vise store afvigelser i deres fysiske egenskaber. Farven kan ændre sig fuldstændigt, men krystallerne ser klare og ensartede ud, da krystalgitteret er noget fleksibelt eller rummeligt og opretholder sin oprindelige struktur som helhed. Krystalgitteret af kvarts er imidlertid stramt og meget ufleksibelt (hvilket gør det hårdt, men sprødt), og kun meget små mængder af et antal andre elementer med små kationer (normalt Li, Na, H) kan indbygges under vækst uden at fordreje gitterets struktur. Og faktisk er mængden af monovalente kationer, der findes i kvarts, omtrent proportional med mængden af aluminium. Kvarts, der indeholder større mængder af andre stoffer, er gennemskinnelig til uigennemsigtig og ofte kedelig, fordi krystallen “vokser omkring” de lukkede mineraler, og lys er spredt ved grænserne af de forskellige materialer.
dette gælder generelt ikke for de andre modifikationer af silica, og det ser ud til, at tilstedeværelsen af sporstoffer for nogle af dem faktisk har en stabiliserende virkning på deres struktur.
men mens den samlede sammensætning af klare kvartskrystaller er bemærkelsesværdigt ren (i det mindste sammenlignet med de fleste andre mineraler), er urenhederne typisk ikke jævnt fordelt i krystallen. Koncentrationerne af individuelle elementer kan variere med en størrelsesorden inden for få mikrometer afstand. For eksempel kan koncentrationen af aluminium variere mellem mindre end 5 ppma (dele pr. 1992). Mønsteret for sporelementfordelingen kan synliggøres med en teknik kaldet katodoluminescens: højenergielektronstråler (“katodestråler”) inducerer kortvarige luminescenseffekter, der kan fanges på almindelig film. De resulterende fotografier af tynde skiver krystaller viser et fint laminært mønster. Lagene ligger alle parallelt med krystalfladerne, svarende til fantomer, så dette mønster af sporelementfordeling skyldes hurtige ændringer i vækstmiljøet.
kemisk ren er stadig ofte ikke ren nok til tekniske formål. En perfekt, homogen krystal er så gennemsigtig som et vakuum, men sporstoffer forårsager forvrængninger og defekter i krystalgitteret, hvilket igen påvirker de optiske egenskaber. De fleste af de elementer, der er indbygget i kvarts (H, Li, Al, Na, Ti, Fe) er allestedsnærværende, og derfor er yderligere oprensning af silica kompliceret og dyr. Af den grund er forekomster af kvarts med et lavt sporstofindhold stadig meget efterspurgte (se f.eks. 2000).
yderligere Information, litteratur, Links
en tabel over kvartsegenskaber findes på mindat.org:
en anden tabel på www.webmineral.com:
fodnoter
1 IUPAC er en organisation, der sigter mod at fjerne uklarheder og sjove, men velkendte navne som Knalls Risure (tysk for “banging acid”, fulminic acid) fra kemisk nomenklatur. Gamle navne er stadig gyldige, så længe de er entydige.
2 nogle af jer kan finde det fristende at lave nogle eksperimenter med hydrogenfluorid. Hydrogenfluorid er et meget farligt stof. Bare slå en sag op i en god lærebog om toksikologi; efter foredraget vil du ikke røre det selv med en pol. Den vandige opløsning er ikke en stærk syre (ren HF er), og de udissocierede små HF-molekyler trænger let ind i huden og binder calcium i cellerne til dannelse af uopløselig fluorit, CaF2. Calcium er afgørende for de levende funktioner i alle kropsceller. En lille dråbe på en finger, der går ubemærket, da den ikke straks gør ondt, kan – efter en vis forsinkelse – forårsage betydelig skade og stor smerte.
Lad os hurtigt gøre matematikken: 1 Mol HF = 20g. en dråbe (ca.50 liter) af en 20% opløsning indeholder 0,00005 l (200 g/l) = 0,01 g. 10 mg, det lyder ikke meget.
1 Mol Ca = 40G og 1 Mol F = 19g. 1 Ca vil binde 2 F, således 40g Ca vil binde 38g F fra 40g HF. 1 ml af dit kropsvæv indeholder ca. 0,1 mg Ca, og 0,1 mg HF vil lade det udfælde næsten fuldstændigt. I teorien kunne 10 mg HF i det lille dråbe udfælde det meste af Ca i 100 ml væv og dræbe alle celler i det.
og nej, jeg er ikke imod vandfluoridering (ingen ironi her).
3udtrykket” meteorisk vand ” refererer til dets oprindelse fra atmosfæren, ikke fra meteoritter. Grækerne troede, at stjerneskud kom fra den samme sfære som skyerne: Stjerner og planeter blev betragtet som evige væsener, noget skyer og stjerneskud er naturligvis ikke. Tænk på “meteorologi”.
4derfor er kvarts i vulkanske klipper ofte ledsaget af calcit.
5dette er noget modintuitivt, men en mættet opløsning er i en termodynamisk ligevægt med krystallen. Når et molekyle inkorporeres i en krystalstruktur, dannes nye bindinger, og afhængigt af krystalstrukturens geometri frigives eller forbruges mere eller mindre energi. For at opløse et stof er der brug for energi til at nedbryde bindingerne, men energi frigives også, når vandmolekyler orienterer sig mod det opløste molekyle og danner nye elektrostatiske bindinger (hydratiseringsenergi). En mere stabil modifikation af en forbindelse er generelt mindre opløselig, da der kræves mere energi for at bryde bindingerne.
dette har intet at gøre med reaktionshastigheden. Under visse betingelser dannes en mere ustabil modifikation først fra en løsning, og først senere erstattes den af den stabile modifikation: Kryptokrystallinsk kvarts dannes typisk fra en vandig opløsning, men med cristobalit og opal som mellemliggende trin, fordi reaktionernes kinetik er til fordel for opaldannelse. Og når du lægger en kvartskrystal i 1 liter rent vand ved stuetemperatur, kan du være ret sikker på, at når du tager den ud næste dag, vil den ikke veje 2,9 mg mindre. Sandsynligvis vil det være meget svært at måle forskellen. Måske efter en måned eller efter et år.
6tetraeder i kvarts er faktisk ikke perfekt isometrisk som en ideel tetraeder, men lidt forvrænget, fordi afstanden til det centrale siliciumatom er 0,16101 nm for 2 iltatomer og 0,16145 nm for de 2 andre iltatomer. Denne afvigelse fra den ideelle form er ubetydelig til de fleste praktiske formål, da den er mindre end 0,3%.
7 oksidationstallene for Si og O er faktisk henholdsvis +4 og -2. Den energi, der er nødvendig for faktisk at fjerne 4 elektroner fra Si, er for høj til at muliggøre en stabil rent ionbinding. Selv SiF4 er en forbindelse med polære, men kovalente bindinger på trods af fluorens høje elektronegativitet. Men Si4-anionforbindelser findes (som Ca2Si).
8Rykart (1995) giver værdierne 152,8 liter og 143,5 liter for hhv. Dette ser ud til at være en typografisk fejl, værdierne skal skiftes.
9men det er ikke sandt, at “noget går”. Når et mineral dannes, er elementer og ioner indbygget i dets krystalgitter, når de opfylder visse kriterier, som en bestemt ladning, størrelse eller elektronegativitet, og svarer således til dem, der allerede danner gitteret.
 Printervenlig Version
Printervenlig Version