introduktion
celle-eller vævsfornyelse og regenerering er de to vigtigsteudviklingskrav hos voksne organismer. Begge processer har som udgangspunkt en population af stamceller, der normalt er placeret i et specifikt miljø kaldet “niche” , som giver dem de nødvendige signaler for at opretholde stammenes egenskaber ellerat differentiere til de krævede forskellige celletyper (Figur 1). Stamcelleproliferation og differentiering skal koordineres meddøden af de celler, der skal udskiftes. Derudover processersåsom cellemigration, epigenetik og cellulær kommunikation er også nødvendige for korrekt cellefornyelse . Hurtig fornyelsevæv kan genkendes ved en højere mitotisk aktivitet. Omvendt indeholder langsomt fornyelsesvæv mindre mitose og kan muligvis ikke let anerkendes fra ikke-fornyende områder, som også kan udgøre somemitose . Skæbne beslutninger af stamceller under proliferationdirekte indflydelse på vævsfornyelse og homeostase. Derfor er det kritisk at forstå de reguleringsmekanismer, der opretholder en afbalanceret celledeling og differentiering. Ekstracellulære signaler (f.eks. vævsmikromiljø, intracellulær ROS og cytokiner) såvel som intracellulære faktorer (f. eks. epigenetiske maskiner, transkriptionsfaktorer og DNA-skaderespons) er ansvarlige for regulering af stamcelledeling.
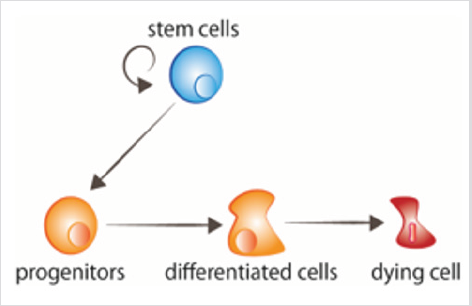
figur 1: celleomsætning stamceller prolifererer, giverstigning til forfædre, der derefter modtager signalerne tildifferentiere. Ældre celler modtager signaler om at dø.
stamceller viser tre mulige opdelingsmuligheder: asymmetrisk opdeling, hvor en stamcelle og en forpligtet dattercelle stammer fra; symmetrisk engagement, somhar to engagerede datterceller; og symmetrisk opdeling,der giver to datterceller, der opretholder stamcelleegenskaber figur 2. Selvom det kunne forudsiges, at asymmetrisk opdeling er den eneste mekanisme, der muliggør opretholdelsen af en stabil population af stamceller, viste de nuværende data fra lineagetracingeksperimenter, at balancen mellem stamcelleproliferation og generering af differentieretafkom i de fleste væv opnås på niveauet for hele stamcellepopulationen.Tabet af stamceller på grund af differentiering eller celleskader inducerersymmetrisk opdeling for at udfylde dette hul . Efter stamcelledeling passerer de celler, der følger differentieringsprocessen, gennem forskelligestadier, der er defineret af en kombination af transkriptionsfaktorerder styrer aktiviteten af det passende repertoire af gener ogtillade deres engagement og terminal differentiering. For hver cellelinie er slutproduktet af rækkefølgen af beslutninger en specifikdifferentieret celletype figur 3a. under de fleste omstændigheder er cellulær identitet – produktet af normal differentiering – stabilinden for væv,og vedligeholdelsen er afgørende for normalt vævfunktion. En sådan stabilitet opnås gennem epigenetisk regulering-f .eks. histondemethylering og acetylering – der resulterer i arveligemønstre af vævsspecifik genekspression.
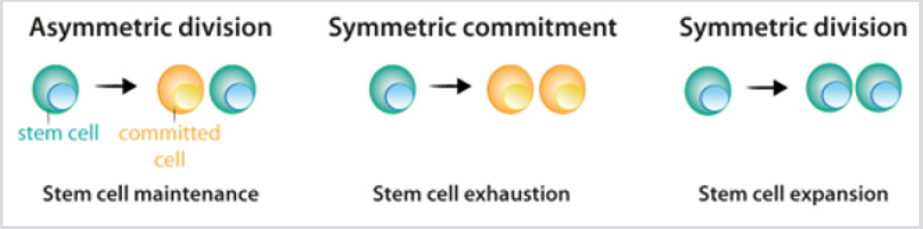
figur 2: Opdelingsmønster af stamceller.
a) under asymmetrisk opdeling giver stamceller anledning til en stamcelle, som opretholder stamcellepopulationen, og en celleder bliver forpligtet til differentiering.
b) under symmetrisk engagement giver stamcelledeling anledning til to datterceller, der blev forpligtet tildifferentiering.
c) under symmetrisk opdeling giver stamcelledeling anledning til to stamceller. Som forklaret i teksten, nuværende eksperimentelledata indikerer, at de tre opdelingsmetoder kan forekomme, mens stamcellepopulationen opretholdes.
dog kan tab af celleidentitet forekomme. Faktisk celler fradrosophila imaginal disc er i stand til at transdeterminere og erhverveen ny voksen skæbne efter transplantation . I denne situation synes ekstracellulære signaler at omprogrammere nogle forstadier ellerdifferentierede celler for at erhverve karakteristika for enten en mere stamstat eller en ny differentieret tilstand. Der er to mekanismerhvorved en celle kan ændre sin identitet: dedifferentiering ogtransdifferentiering. Dedifferentiering refererer til processen vedsom en differentieret eller engageret celle erhverver karakteristikaf en mindre moden celle figur 3b. Det mest dramatiske eksempel på dedifferentiering er in vitro omdannelse af terminaltdifferentierede celler til pluripotente celler (inducerede pluripotentstemceller, iPSC ‘ er) ved overekspression af et begrænset antal transkriptionsfaktorer . Transdifferentiering forekommer derimod, når en differentieret celle ændrer det transkriptionsprogram ogkonverterer til en anden differentieret celletype. Processen kanforekomme gennem et formidlet trin af dedifferentiering mod aless modent stadium før omdannelsen til den nye differentierede celle eller direkte uden det formidlede trin figur 3c-d.den direkte omdannelse af fibroblaster til myoblaster ved den ektopiske ekspression af MyoD er et eksempel på den anden proces .
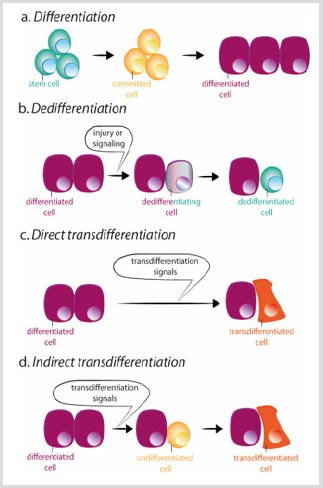
figur 3: ordninger for differentiering, dedifferentiering og transdifferentiering.
a) under normal differentiering giver stamceller anledning til engagerede celler, som igen adskiller sig i forskellige celletyper.
b) Dedifferentiering består af erhvervelse af stamcelleegenskaber af en differentieret celle. Transdifferentiering kan forekommepå en direkte eller indirekte måde.
c) under direkte transdifferentiering erhverver en differentieret celle transkriptionsprogrammet af en anden celletype, normalttæt relateret, som for eksempel eksokrin til endokrine bugspytkirtelceller, bliver en anden differentieret celle.
d) under indirekte transdifferentiering, en differentieret celle dedifferentierer inden vedtagelsen af det nye transkriptionalprogram af den anden celletype.
Dedifferentiering og transdifferentiering forekommer også ien naturlig måde som reaktion på en skade eller vævstab .Dedifferentiering forekommer for eksempel naturligt under lemmergeneration i urodele amfibier. Efter amputation af lemmer, celler ved siden af såret dedifferentiere, der danner et blastema, derbestår af udifferentierede celler,der prolifererer og til sidst redifferentierer i samme celletype for at skabe alle komponenterneaf det tabte lem. Naturlig transdifferentiering forekommer indirekte: først dedifferentierer cellen; og derefter aktiveres det naturlige udviklingsprogram, hvilket gør det muligt for cellen at differentiere til den nye afstamning. Tsonis og samarbejdspartnere beskrev en naturligmekanisme for transdifferentiering i en ny. De fandt det hvornårlinser fjernes, pigmenterede epitelceller fra dorsal iristransdifferentiere og regenerere det manglende væv. For at opnådette skal pigmenterede epitelceller først dedifferentiere ogproliferere for at skabe nye linseceller og derefter differentiere ind imodne celler i linsen . I begge situationer-dedifferentieringog redifferentiering i samme celletype eller transdifferentierettil en ny celletype – kan et komplekst netværk af signalveje kontrollere det transkriptionsprogram, der er erhvervet af hver celle iperfekt tidspunkt.
hus, den spatiotemporale kontrol af genekspression erkontinuerligt påkrævet under dyrehomeostase og under aregenerativ proces. Under regenerering skal cellerne imidlertid tilpasse sig den nye situation, hvilket kræver, at der træffes flere fundne beslutninger på celleniveau, ofte inklusive processer afdifferentiering og transdifferentiering, som under homeostasiser knappe.Clevers H, Loh KM, Nusse R (2014) Stamcellesignalering. Et integreret program til vævsfornyelse og-regenerering med signalering og stemcell-kontrol. Videnskab 346 (6205): 1-9.
