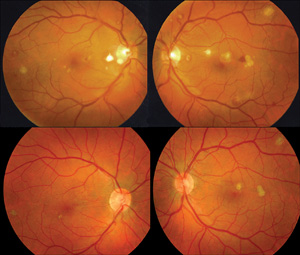
Figur 1. Farve fundus fotografi af begge øjne i en IV stofmisbruger før sekventiel bilateral vitrektomi (øverste række) og efter vitrektomi (nederste række). Før vitrektomi var der mild vitritis og nogle få glasagtige opaciteter bilateralt. Områder af hæmoragisk retinochoroiditis er til stede. Efter vitrektomi og fem serielle amphotericin-B-injektioner i begge øjne givet to gange ugentligt, resterende retinochoroidale ar kan ses med opløsning af nethindeblødning og glasagtig opacitet. Denne patient modtog også en måned oral ketoconosol. endogen endophthalmitis er en usædvanlig, men potentielt ødelæggende intraokulær infektion, hvor patogener når øjet via blodstrømmen. Endogen endophthalmitis er mindre almindelig end eksogen endophthalmitis, der tegner sig for 2 til 8 procent af alle endophthalmitis tilfælde i forskellige undersøgelser.1,2 pædiatrisk endogen endophthalmitis er endnu sjældnere og udgør 0,1 til 4 procent af alle endogene endophthalmitis tilfælde.2,3
predisponerende tilstande er vigtige for at bestemme en patients risiko for endogen endophthalmitis. Hos patienter med akut eller kronisk panuveitis af uklar oprindelse kan invasive diagnostiske procedurer, oftest pars plana vitrektomi, være nødvendige for at stille diagnosen. Identificerede risikofaktorer for endogen endophthalmitis inkluderer: kroniske sygdomme (f. eks. diabetes mellitus, nyresvigt, maligniteter og erhvervet immundefektsyndrom); immunsuppressiv behandling; nylig invasiv kirurgi; intravenøst stofmisbrug; indbygget kateter; endokarditis; hepatobiliære infektioner; organtransplantation; graviditet eller fødsel; genitourinære operationer; eller tandprocedurer.4 fremkaldelse af en historie med intravenøst stofmisbrug er især vigtigt og ofte vanskeligt i betragtning af patienternes modvilje mod at diskutere dette spørgsmål. Positiv historie med underliggende medicinske tilstande som diabetes, hjertesygdom og malignitet blev rapporteret hos 90 procent af patienterne i en rapport af Annabelle A. Okada og kolleger i 1994.5 en større gennemgang af endogene endophthalmitis-patienter rapporterede underliggende medicinske tilstande, der disponerede for okulær infektion i 56 Til 68 procent af tilfældene.6 og kolleger rapporterede identifikation af allerede eksisterende prædisponerende tilstand hos 90,9 procent af patienterne, og den mest almindelige systemiske tilstand, der blev fundet, var diabetes mellitus (50 procent).7
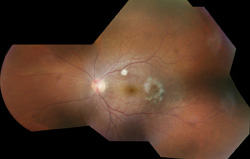
figur 2. Farvefundusfotografi af venstre øje hos en patient med Candida endophthalmitis post-vitrektomi og behandling med fem intravitreale injektioner af amphotericin-B givet to gange ugentligt, der viser hvide retinochoroidale læsioner i makulaen såvel som et ekscentrisk makulært hul som følgevirkninger af svampeendophthalmitis. Synsstyrken var 20/30. Denne patient modtog også en måned oral ketoconosol.
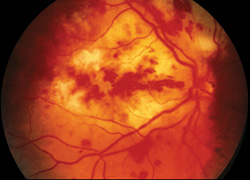
figur 3. Farve fundus fotografi af højre øje af en patient med endogen endophthalmitis forårsaget af Aspergillus. Patienten havde en historie med intravenøst stofmisbrug og blev behandlet med intravitreal og systemisk amphotericin B, men havde et dårligt visuelt resultat.
endogen endopthalmitis er oftest forårsaget af bakterier eller svampe. Forårsagende organismer varierer geografisk. En undersøgelse fra Bascom Palmer Eye Institute rapporterede svampe som en mere almindelig årsag end bakterier (62 procent svampe vs. 38 procent bakteriel),8 mens en Hong Kong-undersøgelse rapporterede bakterier som den mere almindelige årsag til endogen endophthalmitis (72,7 procent bakteriel vs. 27,3 procent svampe).7 litteratur fra Østasien rapporterede, at gramnegative organismer var den mere almindelige årsag (70 procent), og Klebsiella var den mest almindelige årsagsorganisme (60 procent).9 Data fra Nordamerika og Europa viste en stigende procentdel af gramnegative organismer fra 32 procent i 1986 til 52 procent i 2003.6 gær er en mere almindelig årsag og forbundet med bedre visuelle resultater sammenlignet med forme i svampe endogen endophthalmitis.10,11 Candida er den mest almindelige organisme, der er ansvarlig for svampe endogen endophthalmitis.8,11,12 hos immunsuprimerede patienter, såsom AIDS-patienter, skal atypiske organismer såsom Cryptococcus, Mycobacterium avium, Nocardia og Pneumocystis jiroveci overvejes.
det involverede øje kan have smerter, rødme, flydere eller nedsat syn. Diagnosen er forsinket i den pædiatriske befolkning ved manglende evne til at rapportere symptomer tidligt. Bilateral præsentation er rapporteret i 14 til 25 procent af tilfældene og mere almindeligt med svampe og bakterier som Meningococcus, Escherichia coli og Klebsiella.6 endogen endophthalmitis kan være ensidig til at begynde med og derefter udvikle sig i medøjet. Bakterielle eller svampeinfektioner kan udvise irismikroabscess, hypopyon, forskellige grader af glasagtig tåge, diskrete nethindeknuder, perivaskulær nethindeblødning, arteriolær emboli eller nekrotisk nethinde. Alvorlige tilfælde kan udvikle sig til panophthalmitis. Tilstedeværelse af chokoladebrunt ekssudat i det forreste kammer antyder Bacillus som den ansvarlige organisme, mens Listeria er kendetegnet ved brun hypopyon og Serratia af en rød hypopyon.
svampe endophthalmitis med Candida kan have fluffy bolde i glaslegemet, chorioretinitis, hypopyon, perivasculitis, optisk neuritis eller chorioretinal læsioner (cremet, dybt og godt omskrevet). Infektion med forme som Aspergillus er mere fulminant, typisk begrænset til det subretinale rum og kan have chorioretinale læsioner (sammenflydende med utydelige margener), intraretinale blødninger, vaskulær okklusion eller nethindenekrose i fuld tykkelse. Positive glasagtige aspiratkulturer er vanskeligere at opnå fra forme end gær, måske fordi forme ikke involverer glaslegemet så almindeligt som gær.13
endogen endophthalmitis kan efterligne konjunktivitis, ikke-infektiøs anterior uveitis, iritis, akut glaukom, cellulitis, grå stær og især retinoblastom hos børn. Fejldiagnose ved den første præsentation er rapporteret i 16 til 63 procent af tilfældene, hvilket forsinker diagnosen og korrekt styring.6,12
diagnosen endogen endophthalmitis stilles typisk efter mikrobiologisk bevis for infektion fra en intraokulær prøve (vandig eller glasagtig). Positive kulturer fra blod, cerebrospinalvæske eller ethvert ekstraokulært sted kan være meget suggestive. Blodkulturens positivitetsrate varierer meget, fra 33 procent til 94 procent af tilfældene.6,8 i fravær af lokaliseringssymptomer rapporteres det diagnostiske udbytte fra blod i endogen Aspergillus endophthalmitis at være meget lavt.14 kulturer bør opstilles med både aerob og anaerob medium (chokoladeagar, fåreblodagar og Sabouraud agar) og inkuberes i op til to uger. Gram-plet bruges ofte til at vurdere for bakterier. Svampevækst kan bekræftes af Geimsa eller Calcorfluor hvide pletter. Polymerasekædereaktionsundersøgelse af vævsprøven er en hurtig metode til at identificere ansvarlige organismer, men har en ulempe, at den ikke kunne bruges til at vurdere antibiotisk eller antifungal følsomhed.
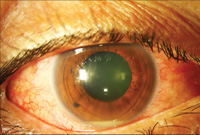
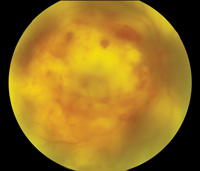
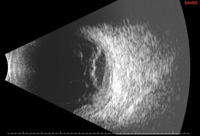
figur 4. Nocardia endogen endophthalmitis. Den indledende glasagtige biopsi var negativ, og kun subretinal biopsi gav positive kulturer. Topbillede (4a) viser hypopyon til stede ved præsentationen. Mellembillede (4b) viser fundusfund, inklusive en stor submakulær abscess. B-scan ultrasonografi (4c) viser neurosensorisk frigørelse og en submakulær masse.
ultralyd B-scanning af øjet er vigtigt for at bestemme omfanget og typen af glasagtige ekssudater, skleraltykkelse, choroidal abcess og tilstedeværelse af nethindeløsning. Computeriserede tomografiscanninger af kredsløbet hjælper med at identificere orbitalinddragelse. Andre undersøgelser såsom røntgenbillede af brystet, ultralyd mave, CT mave, ekkokardiografi og Gallium-67 scanninger kan hjælpe med at identificere et systemisk infektionsfokus.
Behandling
• bakteriel endogen endophthalmitis. Soon-Phaik Chee og kolleger rapporterede, at systemiske antibiotika kan opnå terapeutiske niveauer i øjet på grund af den forstyrrede blod okulære barriere.1 ikke desto mindre suppleres systemiske midler oftest med intravitreale antimikrobielle stoffer og vitrektomi, især i indstillingen af fremtrædende glasagtig involvering. Vancomycin (1 mg/0, 1 mL) og ceftasidim (2, 25 mg/0, 1 mL) forbliver de valgte intravitreale antibiotika. Ifølge en gennemgangsundersøgelse er øjne, der gennemgår pars plana vitrektomi, tre gange mere tilbøjelige til at bevare nyttigt syn end dem, der ikke gennemgik vitrektomi.6 også disse øjne er tre gange mindre tilbøjelige til at kræve udtagning eller enukleation. Bredspektret systemisk antibiotika som vancomycin, aminoglycosider eller tredje generation cephalosporiner udgjorde grundpillerne i behandlingen tidligere, men bruges nu supplerende til lokal terapi. Anbefalede antibiotika er bredspektret antibiotika, der dækker de fleste gram-positive og negative organismer. Systemiske antibiotika fortsættes typisk i mindst tre til fire uger eller som den ekstraokulære infektion hos patienten dikterer.
• svampe endogen endophthalmitis. Behandlingen afhænger af omfanget af okulær involvering. Systemisk terapi alene er tilstrækkelig, når infektionen er isoleret til nethinden og choroid. Vitrektomi og intravitreal svampedræbende injektioner sammen med systemisk terapi anbefales i tilfælde, hvor glasagtig er involveret.15
intravenøs amphotericin-B har klassisk været det valgte lægemiddel, men har brug for omhyggelig overvågning i betragtning af dets systemiske toksicitet. Oral voriconosol eller fluconasol i forbindelse med lokal terapi anvendes i stigende grad. Intravitreal injektion af enten voriconasol (100 liter/0.1 ml) eller amphotericin-B (5 til 10 liter/0,1 ml) sikrer øjeblikkelige, passende niveauer af antisvampemiddel i det bageste segment. C. glabrata og C. krusei), hvor fluconasol eller amphotericin-B er ineffektive. Nyere antifungale midler som echinocandiner, micafungin, caspofungin og anidulafungin har dårlig okulær penetration og anbefales ikke til brug ved endophthalmitis.16 vitrektomi hjælper med at reducere infektionsbelastningen og bedre tilgængelighed af antifungale midler til intraokulære strukturer. Behovet for gentagne intravitreale injektioner bør baseres på klinisk forbedring, øjets status (vitrektomiseret vs ikke-vitrektomiseret) og farmakokinetikken af antifungal medicin.
lokale eller systemiske kortikosteroider undgås generelt ved svampeendophthalmitis,10 selvom deres anvendelse forbliver kontroversiel.14,15
resultat
endogene endophthalmitis tilfælde har normalt et dårligt visuelt resultat. Visuel skarphed for at tælle fingre eller mere er rapporteret i 22.2 til 41 procent tilfælde.17,18 tab af syn på grund af blindhed, udtagning eller enukleation rapporteres i 55 Til 69 procent af tilfældene.6 visuelle resultater efter behandling er værre for endogen Aspergillus endophthalmitis sammenlignet med Candida-tilfælde, og det kan skyldes tidligere påvisning af Candida-infektion, hvilket fører til mere rettidig indledning af behandlingen.15
patienter, der har ekstraokulære foci af bakteriel infektion, har en rapporteret dødelighed på 5 procent6 til 32 procent.19 faktorer såsom infektion med virulente organismer, Dårligt værtsforsvar, fejldiagnose, der fører til forsinket behandling, utilstrækkelig behandling, brug af upassende antibiotika, panophthalmitis anses for at være forbundet med dårlig prognose. Svampeinfektion har høj dødelighed med en 7 procent rapporteret dødelighed ved systemisk Candida-infektion.20
endogen endophthalmitis er en potentielt ødelæggende øjeninfektion og skal diagnosticeres og håndteres hurtigt. Anvendelse af kombinerede okulære og systemiske antibiotika er almindelig. Systemisk coinfektion er almindelig og er forbundet med en høj dødelighed. Dr. Relhan er forsker i vireoretinale sygdomme og uveitis ved Bascom Palmer Eye Institute. Hun var tidligere juniorkonsulent i vitreoretinal kirurgi ved LV Prasad Eye Institute i Hyderabad, Indien. Dr. Albini er lektor i klinisk oftalmologi med speciale i vitreoretinale sygdomme og uveitis ved Bascom Palmer Eye Institute. Dr. Flynn er professor i oftalmologi med speciale i vitreoretinal kirurgi hos Bascom Palmer. Henvendelser skal rettes til Dr. Albini på [email protected].
1.Chee SP, Jap A. endogen endophthalmitis. Curr Opin Ophthalmol 2001; 12 (6):464-70.
2 . Rasmus Jørgensen, Jørgen Jørgensen, Jørgen Jørgensen. Endogen endophthalmitis forårsaget af salmonella serotype B i et immunokompetent 12-årigt barn. Arch Ophthalmol 2012; 130(6):802-4. doi: 10.1001 / archophthalmol.2011.1862.
3. Chaudhry IA, Shamsi FA, al-Dhibi H, Khan AO. Pædiatrisk endogen bakteriel endophthalmitis: Case rapport og gennemgang af litteraturen. J AAPOS 2006;10 (5): 491-3. Epub 2006 7.September.
4. Den kliniske udfordring af endogen endophthalmitis. Nethinden 2001; 21 (6):572-4.
5. Okada AA, Johnson RP, Liles toilet, D ‘ Amico DJ, Bager som. Endogen bakteriel endophthalmitis-rapport om en tiårig retrospektiv undersøgelse. Oftalmologi 1994; 101:832-8.
6. Jackson TL, Eykyn SJ, Graham EM, Stanford MR (2003). Endogen bakteriel endophthalmitis: en 17-årig prospektiv serie og gennemgang af 267 rapporterede tilfælde. Surv Ophthalmol 2003; 48(4):403-23.
7. Det er et spørgsmål om, hvordan man gør det, og hvordan man gør det. Gennemgang af kliniske træk, mikrobiologisk spektrum og behandlingsresultater af endogen Endophthalmitis over en 8-årig periode. J Ophthalmol 2012: 265078. doi: 10.1155/2012/265078. Epub 2012 Februar 23.
8. Schiedler V, Scott IU, Flynn Jr, Davis JL, bens MS, Miller D. Kultur-bevist endogen endophthalmitis: kliniske træk og synsskarphedsresultater. Am J Ophthalmol 2004; 137:725-31.
9. JS, Chan TK, Lee HM, Chee SP. Endogen bakteriel endophthalmitis: en østasiatisk oplevelse og en revurdering af en alvorlig okulær lidelse. Oftalmologi 2000; 107:1483-91.
10. Endogen fungal endophthalmitis: Årsagssygdomme, ledelsesstrategier og synsskarphedsresultater. Am J Ophthalmol 2012; 153:162-6.e1. doi: 10.1016 / j. ajo.2011.06.020. Epub 2011 September 13.
11. Sridhar J, Flynn Jr, Kuriyan Ae, Miller D, Albini T. endogen svampe endophthalmitis: risikofaktorer, kliniske træk og behandlingsresultater i skimmel-og gærinfektioner. J Oftalmisk Inflamm Inficere 2013;September 20; 3(1):60. doi: 10.1186 / 1869-5760-3-60.
12. Bindemiddel MI, Chua J, Kaiser PK, Procop GV, Isada CM. Endogen endophthalmitis: en 18-årig gennemgang af kulturpositive tilfælde på et tertiært plejecenter. Medicin (Baltimore) 2003;82(2):97-105.
13. Rao NA, Hidayat AA. Endogen mykotisk endophthalmitis: variationer i kliniske og histopatologiske ændringer i candidiasis sammenlignet med aspergillose. Am J Ophthalmol 2001; 132(2):244-51.
14. PD1, Flynn Jr, Murray TG, Davis JL, Barr CC, Gross JG, Mein CE, McLean toilet Jr, Killian JH. Endogen Aspergillus endophthalmitis. Kliniske træk og behandlingsresultater. Oftalmologi 1998; 105:57-65.
15. Brod RD, Flynn HV, Miller D. endogen svampe endophthalmitis. I: Duanes kliniske oftalmologi. Harper og række; 2004. CD-ROM. ch 11
16. En potentiel søgning efter okulære læsioner hos indlagte patienter med signifikant bakteriæmi. Clin Inficere Dis 2000; 30(2):306-12.
17. Riddell J 4th1, comer GM, Kauffman CA. Behandling af endogen svampendophthalmitis: fokus på nye antifungale midler. Clin Inficere Dis 2011; 52(5):648-53. doi: 10.1093 / cid / Cik 204. Epub 2011 Jan 16.
18. MJ, LG, sælge CH. Metastatisk bakteriel endophthalmitis: en moderne revurdering. Surv Ophthalmol 1986; 31(2):81-101.
19. Chen YJ1, Kuo HK, PC, Kuo ML, Tsai HH, Liu CC, Chen CH. En 10-årig sammenligning af endogene endophthalmitis-resultater: en østasiatisk oplevelse med Klebsiella pneumoniae-infektion. Nethinden 2004; 24 (3): 383-90.
20. Menes AV1, Sigesmund DA, Demajo, Devenyi RG. Dødelighed hos indlagte patienter med Candida endophthalmitis. Arch Praktikant Med 1994; 154 (18): 2093-7.
